乙腈中黄曲霉毒素B1 溶液标准物质的研制及不确定度评估
2023-09-19王兴龙刘少颖诸寅倪晓峰蔡强
王兴龙,刘少颖,诸寅,倪晓峰,蔡强*
(1.浙江清华长三角研究院,浙江嘉兴 314000;2.杭州市疾病预防控制中心,浙江杭州 310000)
黄曲霉毒素B1(Aflatoxin B1,AFTB1)主要是由黄曲霉菌(Aspergillus flavus)和寄生曲霉菌(A. parasiticus)等多种真菌产生的次生代谢产物,是二氢呋喃氧杂萘邻酮的衍生物,含有一个双呋喃环和一个氧杂萘邻酮(香豆素)。从国内外部分地区AFTB1污染状况及膳食暴露风险评估中发现,虽然总体污染水平不高[1-3],但是黄曲霉毒素有显著的慢性毒性,摄入大剂量AFTB1后会对氧化、遗传、肝脏系统造成一定程度的损伤[4-5]。目前不同国家和地区对黄曲霉毒素检测种类和限值要求均不同,例如我国《食品安全国家标准 食品中真菌毒素含量》(GB 2761—2017)中对AFTB1有限量要求,欧盟除规定了AFTB1的限量外,还规定了4 种黄曲霉毒素总和的限量要求。真菌毒素标准物质,无论从品种上还是从数量上都无法满足国际互认和量值比对的溯源需要,因此有必要开展系统的AFTB1标准物质的研制工作,对于保证食品中AFTB1监测检测及风险评估数据一致性评价具有重要意义。
根据标准物质量值的溯源性、准确度、精密度等技术指标,本研究采用高效液相色谱串联高分辨质谱法、紫外-可见光谱法对AFTB1进行表征与鉴定。通过使用满足计量学特性要求的测量方法和计量器具,采用了8家实验室联合定值,同时考察了其均匀性、稳定性,并系统地评估了在研制过程引入的不确定度。
1 材料与方法
1.1 仪器与试剂
1260 高效液相色谱仪,美国Agilent 公司;QE高分辨液质联用仪,美国Thermo Scientific 公司;Lambda 35 紫外-可见分光光度计,美国PerkinElmer公司;XSE105DU 电子天平,美国Mettler Toledo 公司;Milli-Q 超纯水仪,美国Millipore 公司。
黄曲霉毒素B1标准溶液(GBW 10174),中国计量科学研究院;黄曲霉毒素B1固体粉末(纯度99%以上),以色列Fermentek 公司;乙腈,色谱纯,德国默克公司。
1.2 实验方法
1.2.1 标准物质候选物选择
为了进一步确认原料(黄曲霉毒素B1固体粉末)的准确可靠,分别采用高分辨质谱法、紫外分光光度法对购买的原料进行了主成分定性分析。将经过主成分定性分析的标准物质原料,采用重量-容量法配制标准物质溶液[6]。黄曲霉毒素B1在乙腈中相对稳定[7],因此选择适量乙腈,将9.97 mg AFTB1固体充分溶解,将冷却后的溶液沿玻璃棒小心转入2 000 mL 的容量瓶中,定容至刻度。分装至5 mL 洁净干燥器的棕色安瓿瓶中,每个包装量为4 mL,将安瓿瓶快速熔封,共分装474 个包装单元,置于-18 ℃冰箱内保存。AFTB1原料充足,满足复制的要求。
1.2.2 定性分析
(1)高效液相色谱条件
色谱柱:Thermo Hypersil GOLD(100 mm×2.1 mm,1.9 μm);流动相:A 为超纯水,B 为乙腈-甲醇溶液(体积比1 ∶1);柱温:35 ℃;进样量:2 μL;等度洗脱。
(2)高分辨质谱条件
NCE:30/50/70;模式:Full MS/ddMS2,Full MS分辨率为70 000,dd MS2分辨率为17 500;离子源模式为ESI+。
(3)紫外-可见光谱分析
采用紫外-可见光谱分析法测定配制好的AFTB1溶液标准物质,波长扫描范围为200 ~450 nm,分析化合物紫外可见光吸收光谱。
1.2.3 高效液相色谱-紫外检测法定量分析
色谱柱:XTerra RP18(150 mm×4.6 mm,5 μm);流动相:乙腈-甲醇溶液(50+50);柱温35 ℃;进样体积:10 μL;紫外检测器:检测波长为359 nm;标准溶液及待测溶液直接进样,外标法单点定值。梯度洗脱0 ~1 min,B 相30%;1 ~7 min,B 相变化至90%;7 ~9 min,B 相保持100%;9 ~13 min,B 相保持30%。
1.2.4均匀性检验
根据《标准物质的定值及均匀性、稳定性评估》(JJF 1343—2022)[8],对标准物质进行均匀性研究。采用简单随机抽取方式,抽取15 瓶样品,按照1.2.3 确定的分析方法,每一瓶抽取3 份子样进行测定,最小取样量为10 μL。采用单因素方差分析法(F检验法)对检测数据进行统计分析[9],判断标准物质的均匀性。
1.2.5稳定性考察
稳定性是所有标准物质的关键特征之一,通常评估样品短期稳定性和长期稳定性。短期稳定性评估采用同步稳定性评估方法,将制备好的溶液标准物质统一保存在60 ℃条件下,分别在第0 天、第1 天、第3 天、第5 天、第7 天取2 份样品于-18 ℃下保存,所有取出的样品平行测定2 次。长期稳定性评估,在-18 ℃条件下,分别于第0 个月、第1 个月、第3 个月、第6 个月每个时间点取2 个样品,每个样品平行测定3 次。以监测时间和监测结果拟合直线,采用趋势分析法对结果进行统计分析[10]。
1.2.6标准物质的定值
本溶液标准物质采用8 家实验室间联合定值。为确保定值过程中的可溯源性与质量控制,在定值过程中将标准物质溶液直接与一级有证标准物质溶液GBW 10174 比对,单点外标法定值。向每家定值单位发放2 个包装的AFTB1溶液标准物质(包装1、包装2),每个包装平行测定6 次,提供12 个测定结果。数据经过正态分布检验、组内可疑值检验、组间数据精度检验后,将有效数据汇总,计算总平均值和标准偏差。
2 结果与分析
2.1 高分辨质谱定性分析
将AFTB1溶液标准物质用20%乙腈水溶液逐级稀释至100 ng/mL,按照1.2.2 项方法进行测试,测定结果见图1。得出的AFTB1质荷比为313.069 64,AFTB1理论质荷比为313.070 66[11]。按照高分辨质谱的判定原则,两者基本符合。AFTB1主要碎片离子285.1、241.0,与国家标准GB 5009.22—2016[12]相一致。由此可以判定,溶液中的主成分为AFTB1。
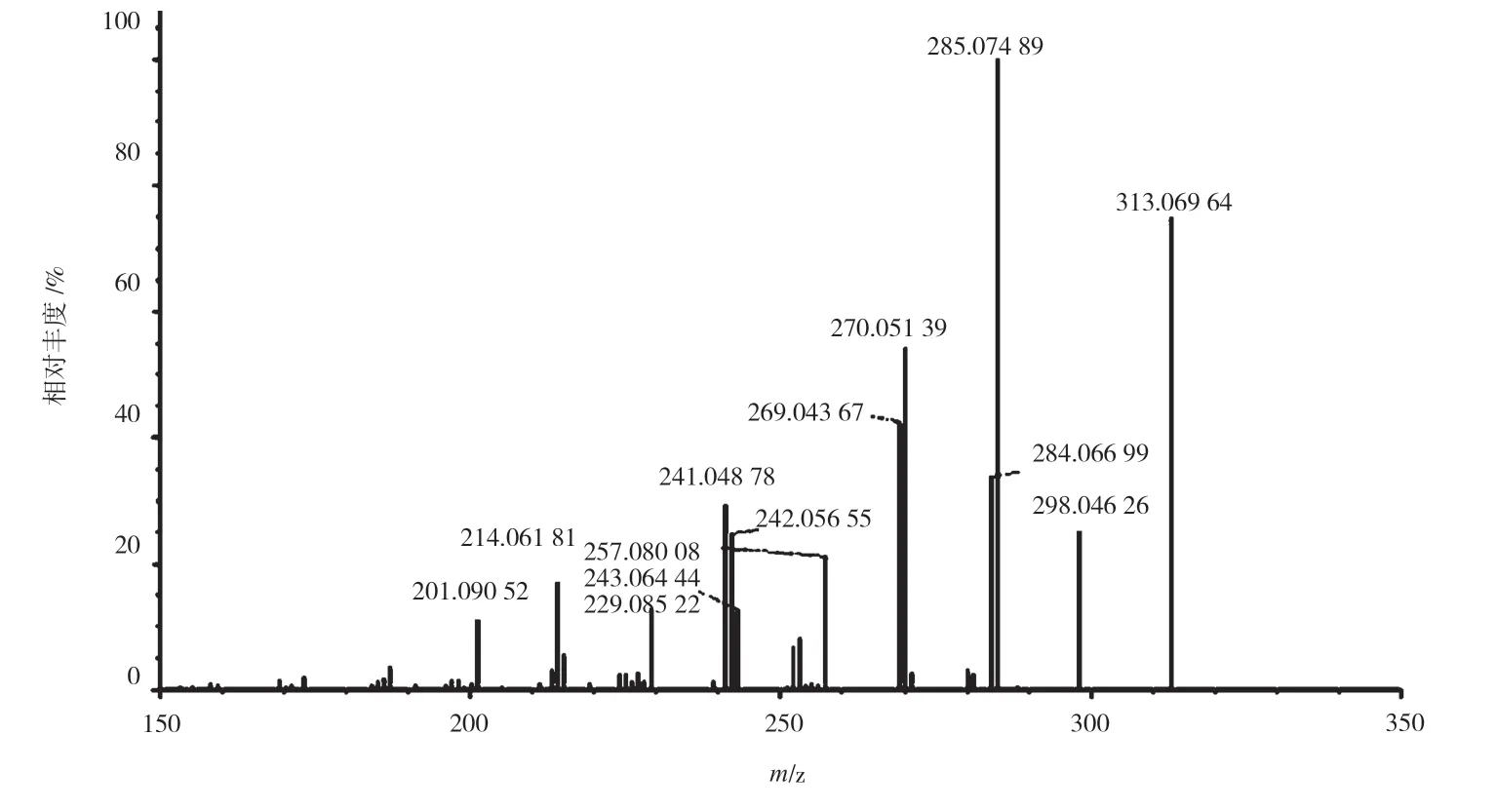
图1 黄曲霉毒素B1 的高分辨质谱图
2.2 紫外光谱分析定性研究
AFTB1化合物在乙腈中的紫外-可见光谱如图2所示,在223 nm,264 nm 和359 nm 波段左右处,存在最大吸收,与RODRICKS[13]报道的AFTB1在甲醇中的最大吸收波段(223 nm、265 nm 和361 nm)基本一致,初步鉴定化合物为AFTB1。

图2 乙腈中黄曲霉毒素B1 的紫外光谱
2.3 均匀性检验及最小取样量的确定
对随机抽取的15 个样本中黄曲霉毒素B1实测数据采用F检验进行统计分析,通过组间方差和组内方差的比较判断各组测量值之间有无系统误差。查表得F(0.05,14,30)=2.037,乙腈溶液中黄曲霉毒素B1成分分析标准物质均匀性数据的F计算值为1.145,小于F(0.05,14,30)=2.037,说明在95%的置信区间内,乙腈中黄曲霉毒素B1分布均匀,同时确定最小取样量为10 μL。
2.4 稳定性检验
短期稳定性是评估运输过程对标准物质量值的影响。在95%置信水平下进行短期稳定性评估,发现乙腈中黄曲霉毒素B1测定值随时间变化的拟合直线斜率为|β1|=0.000 244,斜率标准偏差S(β1)=0.001 141,t0.95,3=3.18,|β1|<t0.095,3·S(β1)。说明60 ℃条件下,乙腈中黄曲霉毒素在7 d 内是稳定的。
长期稳定性数据以平均值归一化后,其结果见图3。虚线内的两条黑实线代表乙腈中黄曲霉毒素B1随时间变化的不确定度。在95%置信水平下,乙腈中黄曲霉毒素B1测定值随月份变化的拟合直线斜率为|β1|=0.000 714 286,斜率标准偏差S(β1)=0.001 649 572,t0.95,3=4.30,|β1|<t0.095,3·S(β1)。乙腈中黄曲霉毒素B1溶液标准物质在-18 ℃条件下储存至少6个月内稳定。基于趋势分析,可将货架期延长至24 个月,以此来评估长期稳定性引入的不确定度[14]。
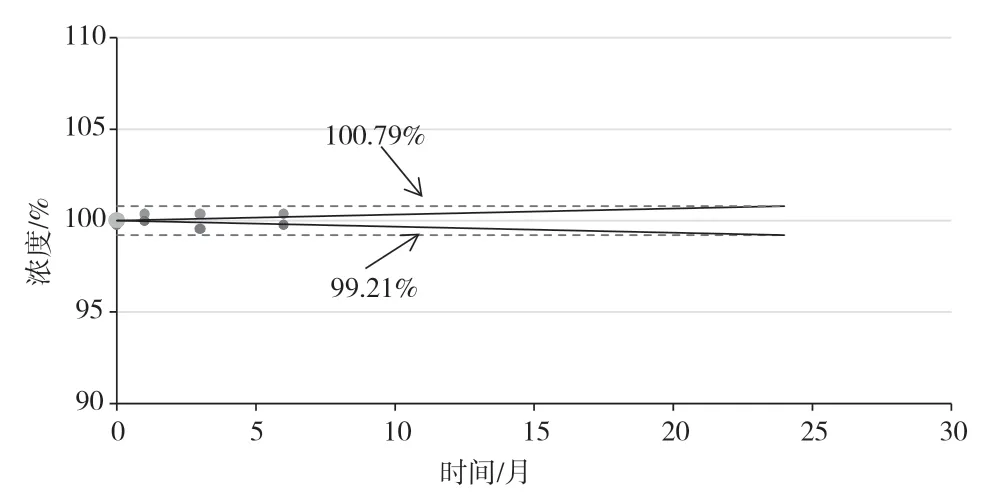
图3 乙腈中黄曲霉毒素B1 长期稳定性归一化结果
2.5 联合定值的结果
本次定值共有8 家单位(A、B、C、D、E、F、G、H)参与,均参考1.2.3 确定的方法进行测定,详见表1。根据达戈斯提诺(D’Agostioon)法检验数据的正态性。统计量Y=1.49,位于-3.61 ~1.59(p=0.99),故接受所有数据为正态分布;经格拉布斯(Grubbs)法检验,所有参与定值实验室的每组数据中|v1|均<λ(0.05,12)·s,无可疑值需要剔除;经科克伦(Cochran)法检验,科克伦检验结果C 为0.160,小于C(0.05,8,12)=0.275,说明各组间数据等精密度。
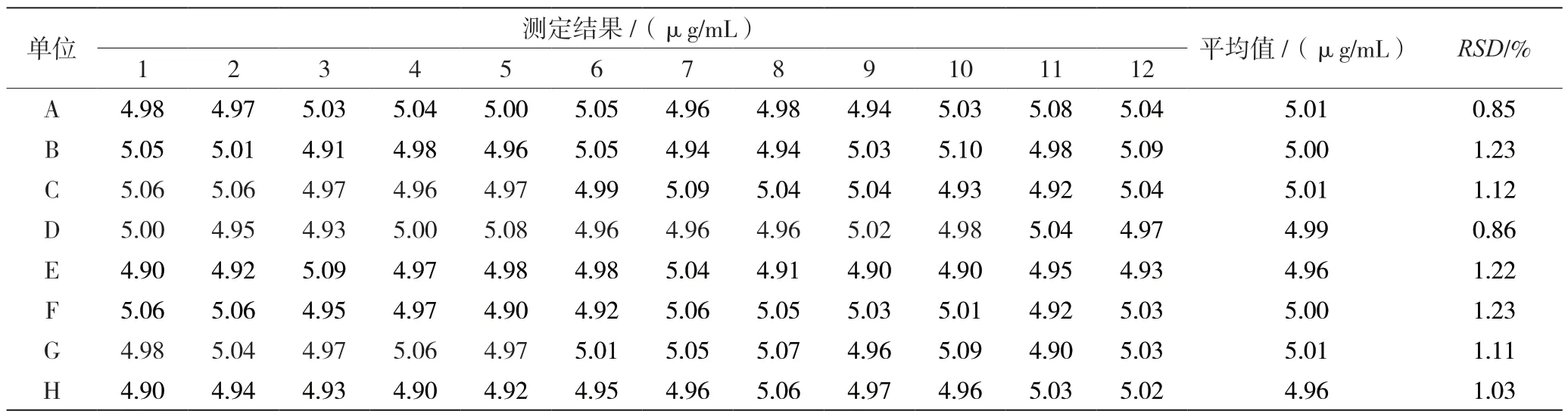
表1 联合实验室定值结果
因此,乙腈溶液中黄曲霉毒素B1定值结果为8家实验室测定结果的总平均值,即4.99 μg/mL。
2.6 不确定度评定
根据相关文献及技术规范[8],确定了影响乙腈中黄曲霉素毒素B1测定结果的各个不确定度分量,主要包括:标准物质的均匀性引起的不确定度u(bb);标准物质的稳定性引起的不确定度;标准物质的定值过程带来的A 类不确定度和B 类不确定度。
2.6.1 均匀性引入的不确定度
根据均匀性测定结果,由均匀性引入的不确定度可按式(1)表示[6]。
式中:S2为组内方差;n为组内测量次数,n=3;vs为组内自由度,Vs=30。
均匀性检验过程中,15 个样本,3 平行,45 个数据的均值为5.04。则由均匀性检验引入的相对不确定度为
2.6.2 稳定性引入的不确定度
由稳定性引入的不确定度可按式(2)表示[15]。
式中:s(β1)为回归分析斜率的标准偏差;X为稳定性评估的时间。
短期稳定性考察时,14 个样本的平均值为4.997 μg/mL;长期稳定性考察时,12 个样本的平均值为5.003 μg/mL。则由短期稳定性引入的相对不确定度为
由长期稳定性引入的相对不确定度为
2.6.3 定值过程引入的不确定度
定值过程引入的A 类不确定度按式(3)计算[16]。
式中:s为各实验室定值结果平均值的标准偏差;n为实验室个数。
则由定值过程引入的A 类相对不确定度为
定值过程引入的B 类不确定度由标准溶液不确定引入,根据GWB 10174 标准物质证书规定,标准溶液的相对扩展不确定为2%(k=2),则由定值过程引入的B 类相对不确定度为uBrel=2%/2=1%。
2.7 不确定度的合成
通过以上分析,将各分量合成总相对不确定度:
当k=2 时,相对扩展不确定度Urel=k×urel=2×1.302%=2.604%,则扩展不确定度。
因此,乙腈溶液中黄曲霉毒素B1成分分析标准物质特性值表示为(4.99±0.13)μg/mL(k=2)。
3 结论
本文制备的黄曲霉毒素溶液标准物质,经均匀性、稳定性考察,结果无显著性变化。对黄曲霉毒素B1的量值进行不确定度评定,发现影响不确定度的主要因素为均匀性、稳定性及定值过程相关的A 类不确定度与B 类不确定度。该溶液标准物质溯源至国家一级标准物质GBW 10174,符合相关国家标准物质技术规范要求,特性值表示为(4.99±0.13)μg/mL。该标准物质的研制,为实现量值可比性提供了物质保障与技术支撑。
