高效液相色谱法测定尿通卡克乃其片中吗啡含量*
2023-09-14马方圆单莲莲柴冰阳
周 钢,马方圆,单莲莲,柴冰阳,陶 虹△,严 华
(1. 新疆维吾尔自治区药品检验研究院,新疆 乌鲁木齐 830054; 2. 国家药品监督管理局中药<维药>质量控制重点实验室,新疆 乌鲁木齐 830054; 3. 中国药品生物制品检定研究院,北京 100050)
尿通卡克乃其片(国药准字Z20080304,规格为每片0.5 g)为维吾尔药制剂,由酸浆、黄瓜子、血竭、西黄蓍胶、阿拉伯胶、巴旦仁、甘草浸膏、乳香、芹菜子、阿片等组方,气微香,味甜、微苦涩,具有止痛、利尿功效,用于尿痛、尿不净、尿血、尿道流脓等症的治疗。阿片主要含有苄基异喹啉类和菲类生物碱[1-2],前者主要为罂粟碱,后者包括吗啡、可待因、蒂巴因等。阿片主要成分为吗啡[3],其为强效镇痛剂[4],但成瘾性较大[5]。现行尿通卡克乃其片现收载于《国家食品药品监督管理局 国家药品标准》YBZ00342008中,因干扰因素较多,无法准确对吗啡进行定量分析。为更好地控制尿通卡克乃其片的质量,本研究中采用高效液相色谱(HPLC)法[6]测定制剂中吗啡的含量。现报道如下。
1 仪器与试药
1.1 仪器
LC - 20A 型高效液相色谱仪(日本Shimadzu 公司),配有紫外检测器,Labsolution 工作站;Milli - Q 型超纯水仪[美国Millipore 公司,电阻率为18.2 MΩ·cm,总有机碳(TOC)不大于5 × 10-9 µg / L];XPR205 型电子分析天平(梅特勒- 托利多仪器<上海>有限公司,精度为0.1 mg);SK8210LHC 型超声波清洗器(上海科导超声仪器有限公司,功率为500 W,频率为35 / 53 kHz);Centrifuge5430R 型高速离心机(德国Eppendorf 公司,最大工作压力为29 bar,最大转速为17 500 r/min)。
1.2 试药
吗啡对照品(中国食品药品检定研究院,批号为171201-201123,纯度为97.9%);乙腈(批号为192552),甲醇(批号为211769),均为色谱纯,购自美国Fisher 公司,纯度为99.9%;冰醋酸(分析纯,国药集团化学试剂有限公司,批号为20210810,纯度不低于99.5%);磷酸氢二钾(分析纯,天津市致远化学试剂有限公司,批号为20140218,纯度不低于99.0%);庚烷磺酸钠(分析纯,成都市科龙化工试剂厂,批号为2017051101,纯度不低于99.0%);水为超纯水,实验室自制;尿通卡克乃其片(新疆银朵兰维药股份有限公司,批号分别为181197,180847,181196,190925,181034,191142,200103,200112,1904022,1902022,吗啡含量为0.065%)。
2 方法与结果
2.1 色谱条件与系统适用性试验
色谱柱:岛津Shim - pack GIST - C18柱(250 mm ×4.6 mm,5 µm);流动相:乙腈- 0.05 mol/ L 磷酸氢二钾溶液- 0.025 mol / L 庚烷磺酸钠溶液(15∶45∶40,V/V/V)[6];流速:1.0 mL/ min;检测波长:220 nm;柱温:35 ℃;进样量:10µL。供试品溶液色谱图中,吗啡色谱峰与相邻色谱峰分离度为1.85,理论板数为7 122,拖尾因子为1.20,表明吗啡和样品中其他组分色谱峰可达到基线分离。
2.2 溶液制备
对照品溶液:取吗啡对照品20.32 mg,精密称定,置50 mL容量瓶中,加5%冰醋酸溶液定容,摇匀,即得质量浓度为0.397 9 mg/mL对照品贮备液;精密吸取1 mL,置5 mL容量瓶中,加5%冰醋酸溶液定容,摇匀,即得。
供试品溶液:取样品20 片,研细,取5 g,精密称定,置锥形瓶中,加1%冰醋酸甲醇溶液25 mL,称定质量,超声处理30 min,放冷,再次称定质量,加1%冰醋酸甲醇溶液补足减失的质量,摇匀,离心(转速为5 000 r/min),取上清液,滤过,精密量取续滤液10 mL,置烧杯中蒸干,加1%冰醋酸甲醇溶液2 mL,振摇、超声,使残渣形成均匀混悬液,续加5%冰醋酸溶液10 mL,超声处理10 min,转移至20 mL容量瓶中,加少量5%冰醋酸溶液洗涤烧杯(重复2次),转移至20 mL容量瓶中,放冷,加5%冰醋酸溶液定容,摇匀,取5 mL,离心(转速为5 000 r/ min)10 min,取上清液,滤过,取续滤液,即得。
阴性对照品溶液:按处方工艺制备除阿片的阴性样品,按供试品溶液制备方法制备阴性对照品溶液。
2.3 方法学考察
专属性试验:取2.2 项下对照品溶液、供试品溶液(批号为200103)、阴性对照品溶液各适量,分别按2.1项下色谱条件进样测定。结果显示,供试品溶液色谱图中出现与吗啡对照品溶液保留时间一致的色谱峰,且阴性对照无干扰。色谱图见图1。
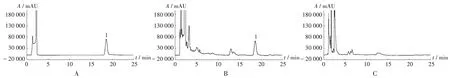
图1 高效液相色谱图Fig.1 HPLC chromatograms
线性关系考察:精密吸取2.2项下对照品贮备液1 mL,分别置2,5,10,25,50,100 mL 容量瓶中,加5%冰醋酸溶液定容,摇匀,即得质量浓度分别为3.979,7.958,15.916,39.790,79.580,198.950 µg/ mL 的系列对照品标准工作液,按2.1 项下色谱条件进样测定,以峰面积(Y)为纵坐标、吗啡的质量浓度(X,µg/mL)为横坐标进行线性回归,得回归方程Y= 3 578X- 43 665,r=0.999 9(n=6)。结果表明,吗啡的质量浓度在3.979~198.950µg/mL范围内与峰面积线性关系良好。
检测限与定量限确定:取线性关系考察项下供试品溶液,按2.1项下色谱条件进样测定,以信噪比(S/N)为3时的质量浓度为检测限,以S/N为10 时的质量浓度为定量限。结果检测限为1µg/mL,定量限为3µg/mL。
精密度试验:取2.2 项下对照品溶液适量,按2.1项下色谱条件连续进样测定6次,记录峰面积。结果吗啡峰面积的RSD为0.88%(n=6),表明仪器精密度良好。
稳定性试验:取2.2 项下供试品溶液,分别于0,2,4,8,12,24 h 时按2.1 项下色谱条件进样测定,记录峰面积。结果吗啡峰面积的RSD为0.32%(n=6),表明供试品溶液在24 h内稳定性良好。
重复性试验:取样品(批号为200103)适量,精密称定,按2.2项下方法制备供试品溶液6份,按2.1项下色谱条件进样测定,记录峰面积并计算含量。结果吗啡的平均含量为0.064%,RSD为2.09%(n=6),表明方法重复性良好。
加样回收试验:分别取已知含量的样品粉末(批号为200103)2.5 g,精密称定,共9 份,分别置三角瓶中;取吗啡对照品5.25,6.52,7.89 mg,精密称定,各3份,分别置100 mL 容量瓶中,即得质量浓度分别为0.051 40,0.063 83,0.077 24 mg/mL 的对照品溶液;精密吸取对照品溶液各25 mL,置三角瓶中,按2.2 项下方法从“称定质量”起制备供试品溶液,记录峰面积并计算加样回收率。结果见表1,符合要求[7]。
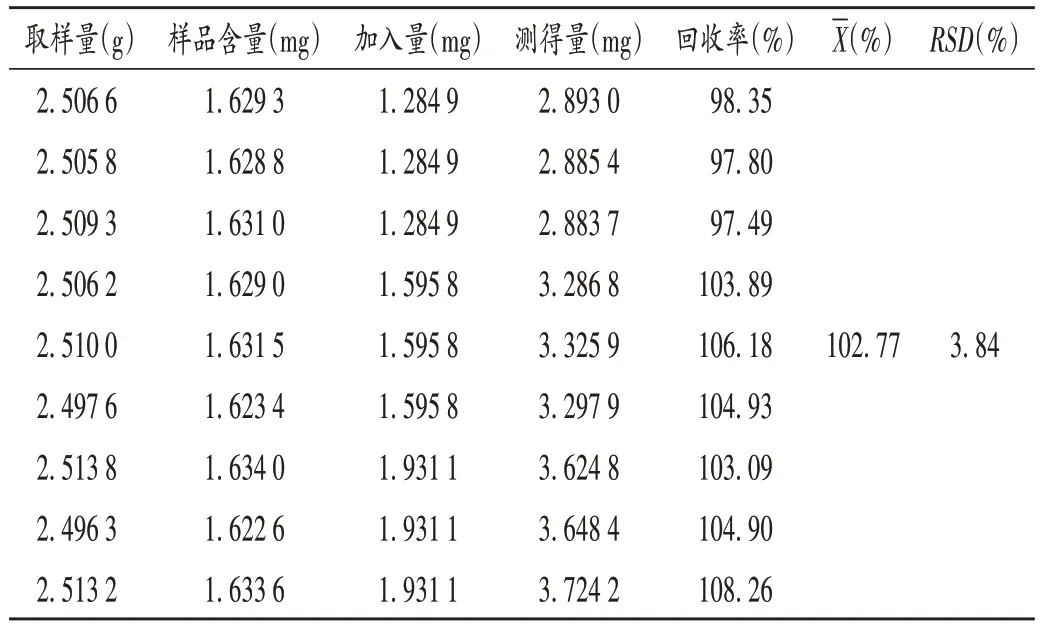
表1 加样回收试验测定结果(n=9)Tab.1 Results of the recovery test(n=9)
耐用性试验:取2.2 项下供试品溶液适量,分别使用不同色谱柱[岛津Shim-pack GIST-C18柱(250 mm×4.6 mm,5 µm)、Shiseido Capcellpak C18柱(250 mm ×4.6 mm,5µm)、Agilent Zobax SB C18柱(250 mm×4.6 mm,5 µm)]进样测定,结果每片分别含吗啡0.33,0.32,0.33 mg,表明色谱柱的耐用性良好。考察不同流动相系统[乙腈-0.05 mol/L磷酸氢二钾溶液-0.025 mol/L庚烷磺酸钠溶液(20∶40∶40,V/V/V),甲醇-0.05 mol/L磷酸氢二钾溶液-0.025 mol/L庚烷磺酸钠溶液(40∶30∶30,V/V/V)][8]和不同柱温(20~40 ℃)对样品中吗啡含量的影响,结果供试品溶液色谱峰保留时间与吗啡对照品溶液色谱峰保留时间一致,拖尾因子与分离度均符合要求。
2.4 样品含量测定
分别取10 批样品粉末5 g,各2 批次,精密称定,按2.2 项下方法制备供试品溶液,按2.1 项下色谱条件平行进样测定2次,记录色谱图,按外标法计算含量。结果10批样品中吗啡的平均含量为每片0.32 mg,详见表2。
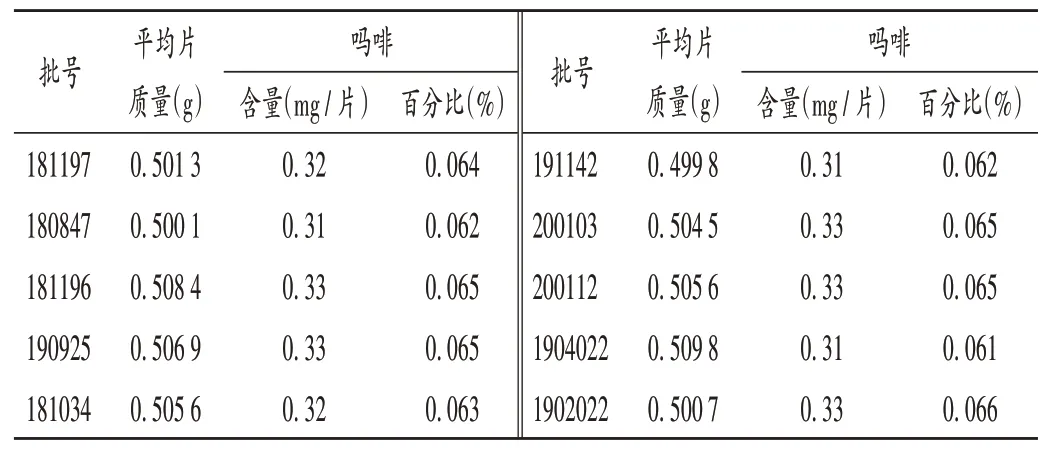
表2 10批样品中吗啡含量测定结果Tab.2 Results of the content determination of morphine in 10 batches of samples
3 讨论
3.1 提取方法考察
尿通卡克乃其片现行质量标准中阿片的含量测定项下存在以下问题:1)原标准中使用甲醇溶解吗啡对照品,稳定性较差,吗啡的峰面积随时间的延长而逐渐减小[9-10];2)使用高效液相色谱法分析供试品溶液,发现其他杂质峰对主峰干扰严重,使检测值严重失真。2020 年版《中国药典(二部)》阿片含量测定项下[11],经固相萃取柱提纯样品后使用高效液相色谱法测定,提取过程中杂质干扰较小,试验可顺利进行,但对尿通卡克乃其片中吗啡的提取无借鉴意义。
阿片在尿通卡克乃其片中占1%,吗啡在阿片中含量约为10%,在处方中约占0.1%。方中,树脂类药材总占比达40%以上,其中阿拉伯胶、西黄蓍胶为水溶性树脂[12],乳香、血竭为脂溶性树脂,导致样品成分复杂,用含水的溶剂提取会形成均匀的乳浊液,用滤头过滤后仍无法消除。吗啡在日光下和空气中放置会逐渐氧化变性,在常规溶液中不稳定,而在酸性溶液中较稳定且溶解度极好。故本研究中采用1%冰醋酸甲醇溶液提取样品,去除大多数阿拉伯胶和西黄蓍胶后,蒸干,先用少量1%冰醋酸甲醇溶液振摇、超声,使残渣形成均匀混悬液,续加5%冰醋酸溶液提取、定容。绝大部分乳香和血竭以沉淀形式析出,经离心、过滤后,得到供试品溶液[13-15]。
预试验中采用2 种方法考察提取过程中放置溶剂的蒸发皿对提取结果的影响。方法1:蒸干后残渣加1%冰醋酸甲醇3 mL,超声振荡形成均匀混悬液,再加5%冰醋酸溶液提取;方法2:蒸干后残渣直接加5%冰醋酸溶液提取。结果表明,方法1 所得吗啡含量高于方法2,原因为脂溶性成分和器具表面结合成一层疏水膜,冰醋酸溶液无法有效进入而提取吗啡。故最终确定2.2项下供试品溶液提取方法。
3.2 提取时间考察
取样品(批号为200103)研细,取粉末5 g,精密称定,共3 份,分别置三角瓶中,精密加入1%冰醋酸甲醇溶液25 mL,分别考察超声提取20,30,40 min 对提取结果的影响。结果显示,超声提取30 min 时吗啡含量最高,与提取40 min 的结果基本一致;提取20 min 的结果稍低,可能由于制剂中树脂占比大,影响吗啡的溶解速率。故最终确定提取时间为30 min。
3.3 检测结果偏高原因分析
制备供试品溶液时,溶液中存在较多血竭和乳香,影响定容,沉淀物占据容量瓶一定体积导致分析结果略偏高,可通过扩大稀释倍数减轻此影响。
3.3 制剂成瘾性分析
成人口服给药途径吗啡摄入量一般为每次5~15 mg,每天15~60 mg;极量为单次不得过30 mg,每日不得过100 mg。该制剂服用量为每次3~5片,每天2次,最大单次摄入量约为1.6 mg,每日最大摄入量约为3.2 mg,远低于吗啡的常规使用剂量,不会产生成瘾性。
3.4 方法评价
该方法操作简便、结果准确,可用于尿通卡克乃其片中吗啡的含量测定。
