锂离子电池富锂正极材料Li1.2 Mn0.54 Ni0.13 Co0.13 O2制备及其性能的实验研究
2023-09-13冯宁宁
冯宁宁, 任 杰
(常熟理工学院材料工程学院,江苏 常熟 215500)
0 引言
自20 世纪末以来,锂离子电池因具有较高的能量密度和良好的安全性能等优点[1-2],受到科研界的广泛关注和研究[3-5]。当前锂离子电池正极材料的电化学性能依然是制约其体系发展的主要瓶颈,因此开发和设计高性能的正极材料是促进锂离子电池发展的关键[6-8]。近年来,锂离子电池富锂三元正极材料Li1.2Mn0.54Ni0.13Co0.13O2具有较高的工作电压和比容量等优点,受到人们的高度关注[9]。富锂正极材料Li1.2Mn0.54Ni0.13Co0.13O2材料结构复杂,由等比例组分的Li2MnO3和LiMO2构成,属于α-NaFeO2层状结构。文献[10-12]中分别介绍了富锂正极材料Li1.2Mn0.54Ni0.13Co0.13O2的多种合成方法。化学共沉淀法制备Li1.2Mn0.54Ni0.13Co0.13O2正极材料是现在应用最多的方法,该方法工艺简单、煅烧温度低的优势,有良好的产业化前景。本文也多次使用化学共沉淀法制得Li1.2Mn0.54Ni0.13Co0.13O2正极材料[13],该法制备Li1.2Mn0.54Ni0.13Co0.13O2材料时,需在过渡金属Ni、Co、Mn盐溶液中加入适当的沉淀剂Na2CO3获得前驱体(Mn2/3Co1/6Ni1/6)CO3,再与锂源经过高温煅烧得到正极材料。为研究制备工艺中煅烧温度对材料电化学性能的影响,本实验用共沉淀法合成(Mn2/3Co1/6Ni1/6)CO3前驱体,再与锂源LiOH混合,分别在900 或950 ℃下高温烧结得到两种富锂三元正极Li1.2Mn0.54Ni0.13Co0.13O2材料,研究其电化学性能。该实验旨在利用“引研入教”思想来丰富新能源专业的课程实验内容,从而提升本科生实验操作能力。
1 实验内容
1.1 实验试剂和仪器
(1)实验试剂。实验所用的试剂主要有NiSO4·6H2O(AR),CoSO4·7H2O(AR),MnSO4·H2O(AR),氨水(AR),Na2CO3(AR),LiOH·H2O(AR),Super P,聚偏四氟乙烯(PVDF),N-甲基吡咯烷酮,所用试剂均为分析纯。锂离子电池选用商用电解液(国泰华荣化工新材料有限公司)。
(2)实验仪器。实验涉及的主要仪器设备有SmartLabSE X射线衍射仪XRD(Rigaku 公司),采用Cu-Kα射线,铜钯波长为0.154 nm,连续扫描模式:扫描范围10° ~80°,扫描速度为0. 5°/min,步长为0.02°;CT2001A电池测试系统(LAND 武汉金诺电子公司),进行恒电流充放电测试。
1.2 富锂正极材料的制备
(1)共沉淀合成前驱体(Mn2/3Co1/6Ni1/6)CO3。将MnSO4·H2O、NiSO4·6H2O、CoSO4·7H2O 3 种盐按照Mn∶Ni∶Co =4∶1∶1 mol比配成2 mol/L的金属盐溶液,再配制0. 5 mol/L 氨水溶液作为络合剂,并以2 mol/L的Na2CO3溶液作为沉淀剂。利用蠕动泵将上述3 种溶液缓慢加到反应釜中,在750 r/min 下搅拌,调节水浴温度至50 ℃,混合溶液体系始终维持pH =8.0 左右。整个反应体系在持续搅拌12 h,再静置陈化12 h,用去离子水不断清洗和离心所得到的前驱体混合物,直到取上层清液加入氯化钡溶液,不再出现白色硫酸钡沉淀为止。最后经过干燥、碾磨、过筛等流程后,得到碳酸盐前驱体。
(2)高温烧结得到产物Li1.2Mn0.54Ni0.13Co0.13O2。按照化学计量比称量一定量的(Mn2/3Co1/6Ni1/6)CO3前驱体和LiOH·H2O于玛瑙研钵中研磨混合均匀,锂盐过量5%,将粉末刮入坩埚,移至马弗炉中,以5 ℃/min速率升温至500 ℃,预烧结5 h,在900 ℃(或者950 ℃)下12 h,即可得到黑色Li1.2Mn0.54Ni0.13Co0.13O2三元富锂正极粉末,分别命名为S-900,S-950。具体制备流程如图1 所示。
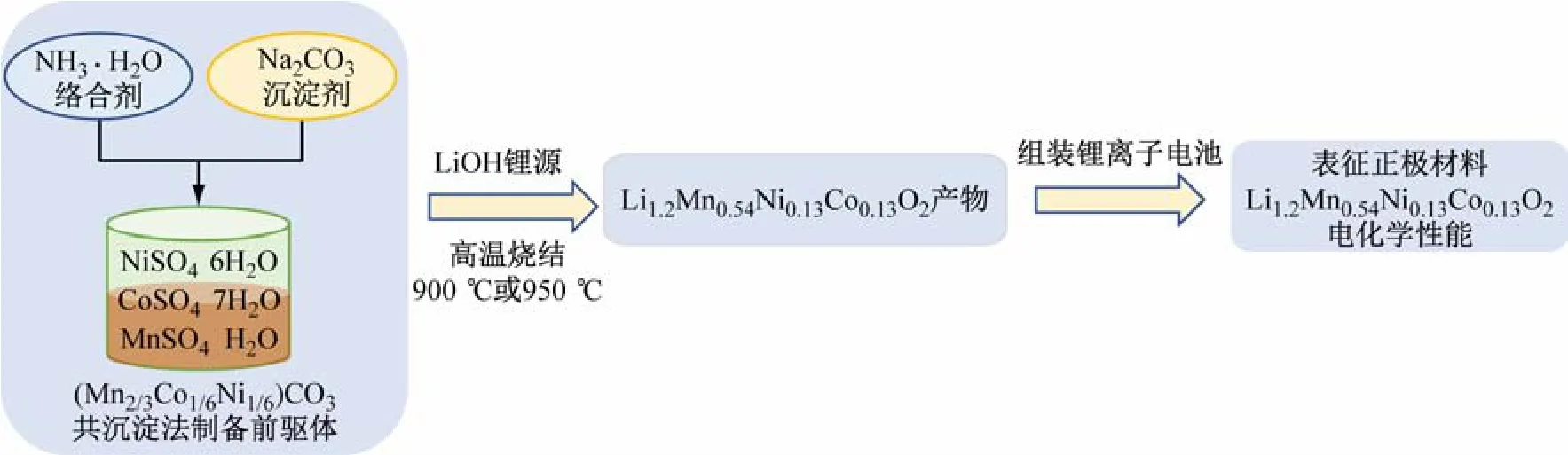
图1 Li1.2Mn0.54Ni0.13Co0.13O2 材料的制备及性能测试流程
1.3 电极的制备和电池的组装/测试
称取富锂正极粉末样品、Super P 和聚偏氟乙烯(PVDF)并混合均匀,质量比为85∶10∶5,用N-甲基吡咯烷酮为溶剂,搅拌均匀后将浆料均匀地涂覆在铝箔上,并放入真空烘箱中120 °C保温10 h。然后用直径φ12 mm的圆形冲子刻电极片,电极片中含有的活性样品质量一般为3.0 mg左右。
以电极片为正极,金属Li 为负极,1. 15 mol/L LiPF6的混合碳酸酯溶液(碳酸乙烯酯、碳酸丙烯酯和碳酸二甲酯,三者体积比为1∶1∶1)为电解液,组装扣式电池CR2032。组装顺序为负极壳、金属锂负极、隔膜Celgard 2300、正极电极片、不锈钢垫片、不锈钢弹片,然后滴加电解液,扣上正极电池壳。在手动扣式电池封口机上对电池进行封装,即完成电池组装。电池组装在水氧体积分数值均小于10-5%的氩气手套箱中进行。电池组装测试之前静置8 h 后在武汉金诺电子公司型号为CT2001A 的LAND 电池测试系统进行恒电流充放电测试。电压窗口为2. 0 ~4. 8 V(vs.Li+/Li),测试电流为0.1 C(其中1C =250 mA/g)。所有电池测试均在室温下进行。
2 实验结果与分析
2.1 Li1.2Mn0.54Ni0.13Co0.13O2 材料结构表征
图2 所示为900 和950 ℃下所得样品S-900 和S-950,在10° ~80°范围内的XRD 图谱。通过分析可得S-900 和S-950 的物相中主要含有2 种组分:①Li2MnO3,位于20° ~25°的一组宽衍射峰(020)/(110),属于C2/m空间群的单斜层状晶体结构[14];②LiMO2(M =Ni、Co 和Mn),图中主要的衍射峰与α-NaFeO2层状结构的特征峰一致,属于R -3m空间群的α-NaFeO2的六方层状晶体结构。此外,清晰分裂的双衍射峰(006)/(102)和(108)/(110)可知S-900和S-950 材料具有高度有序的层状结构[15]。

图2 2种温度下烧结所得S-900和S-950材料的XRD
2.2 Li1.2 Mn0.54 Ni0.13 Co0.13 O2 三元富锂材料的电化学性能测试
分别将S-900 和S-950 组装成扣式电池后进行0.1 C的恒电流充放电测试,结果如图3 所示。由图可知,S-900 和S-950 的首次充电曲线均存在2 个电压平台,当S-900 和S-950 首次充电至4.5 V 左右时,出现第1 个斜向右上角的电压平台,此时材料中LiMO2(M=Ni、Co和Mn)结构中过渡金属离子被氧化,同时脱出Li+;当继续充电至4.8 V的过程中,出现第2 个电压平台,此时体相中脱出O2-和Li+,并留下大量的氧空位和锂空位,但此电压平台会在后续循环中消失。富锂正极材料放电时比容量损失大、库伦效率低,主要原因是充电时过渡金属离子迁移出Li+和O2-后留下的空位,造成较大的不可逆比容量损失。图中S-900和S-950 的首圈放电比容量分别为238. 8 和196. 9 mAh/g,首圈库仑效率分别为55.75%和66.68%。同时,比较900 和950 ℃下制得的Li1.2Mn0.54Ni0.13Co0.13O2,900 ℃的S-900 样品具有较大的放电比容量,这可能是因为煅烧温度越高,造成的锂损失越多,样品中含有更多的Li+,充电过程中就有更多的Li+脱出,形成更多的锂空位和氧空位;在放电过程中就会出现较多的Li+难以重新嵌入正极材料中,故S-900 存在较大的比容量损失。
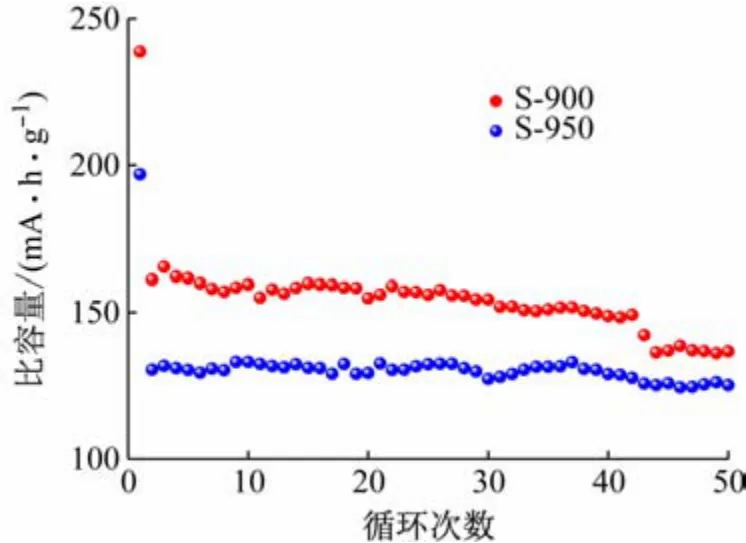
图3 在0.1 C电流下2 种温度烧结所得S-900 和S-950 首次充放电曲线
研究制备的正极材料循环性能是体现其电化学性能的重要因素。为了研究其循环性能,分别将S-900和S-950 组装成扣式电池在0.1 C 下循环50 次,结果如图4 所示。50 次循环后的放电比容量分别为136.7和125.2 mAh/g,容量保持率分别为57.2%和63.6%。S-900 循环性能比S-950 差的原因可能在于,材料表面过多的Li+形成Li2O,在循环中会在正极表面沉积Li2CO3,导致电池阻抗增大,循环性能随之变差。
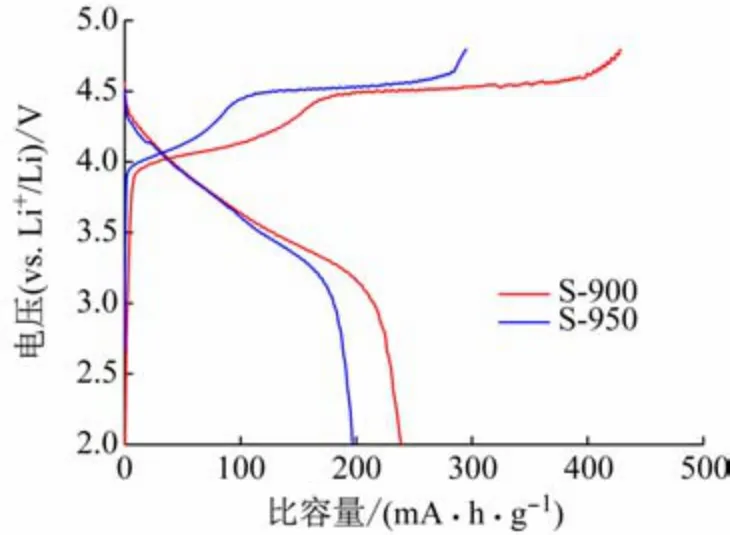
图4 在0.1 C电流下2 种温度烧结所得S-900 和S-950 循环性能
3 结语
本实验采用共沉淀-高温煅烧法成功制得两种烧结温度下的三元富锂正极材料Li1.2Mn0.54Ni0.13Co0.13O2,并进一步对材料进行了结构和电化学性能表征。XRD分析结果表明,S-900 和S-950 材料均具有高度有序的层状结构;电化学测试结果表明,比较900 ℃和950 ℃所得样品,后者具有较高的首圈库仑效率(66.68%)和良好的容量保持率(循环50 圈后63.6%)。这主要归因于900 ℃较低温度烧结所得样品中含有更多的Li+,充电过程中就有更多的Li+脱出,在材料表面形成过多的Li2O,造成放电时Li+无法嵌回正极材料中,导致容量不可逆损失。此外循环过程中出现Li2CO3沉积电极表面,严重降低电池循环性能。据此可知,高温有利于提高富锂正极材料的电化学性能。
此外,本实验可作为新能源专业本科生教学实验之一,将科研与教学相结合,不仅丰富新能源专业实验内容,还可以提升学生的实验操作能力,如管式炉高温烧结操作、正极电极片的制作和锂离子电池的正确组装等等。
科学技术是第一生产力,是先进生产力的集中体现和主要标志,也是人类文明进步的基石。在刚刚过去的二十世纪,科学技术突飞猛进,科学理论充分发展,极大地推动了生产力的发展和社会进步,人类创造了空前丰富的物质文化财富。在二十一世纪,科学技术将会继续取得重大突破,给人类社会的发展带来新的巨大推动。当今世界,科学发现、技术发明与商品化产业化之间的关系越来越紧密,科技成果转化为现实生产力的周期越来越短,科技进步和创新越来越成为经济社会发展的重要决定性因素。
摘自《江泽民在中国科协第六次全国代表大会上的讲话》
