食源性多糖缓解脂质代谢异常的研究进展
2023-09-13刘英语吴酉芝张冠亚
刘英语,吴酉芝,张冠亚
(1.上海中侨职业技术大学 食品药品学院,上海 201500;2.南昌大学食品科学与技术国家重点实验室,江西 南昌 330047)
脂质代谢异常指先天因素或获得因素导致体内脂质及其代谢物的紊乱,糖脂代谢异常的相关疾病,近年来已成为全球性慢性疾病[1]。饮食引起的肥胖会导致机体脂质代谢紊乱,从而产生一系列疾病,包括代谢综合征(metabolic syndrome,MS)、非酒精性脂肪肝(nonalcoholic fatty liver disease,NAFLD)、酒精性脂肪性肝炎(non-alcoholic steatohepatitis,NASH)、高脂血症以及糖尿病等。这些慢性代谢疾病的患病率和发病率逐年上升,已严重地威胁了人们的身体健康和影响了人们正常生活[2]。
目前,许多策略包括饮食干预、体重控制、加强运动和药物治疗已经被提出用来缓解或治疗肥胖、NAFLD 等脂质代谢异常的慢性疾病。多糖因其无毒副作用也被广泛作为膳食补充剂和功能食品,用于减轻和防治脂质代谢紊乱相关的疾病[3]。不同来源的多糖(植物多糖、真菌多糖、细菌多糖等)已经成为具有生物活性的重要天然产品类型[4-5],同时从基本药理活性到作用机制,多糖改善脂质代谢异常的研究已经取得了巨大进展[6]。因此,本文从抑制脂质的合成和促进脂质氧化分解、维持能量平衡、减少脂质的易位堆积、缓解氧化应激损伤和减少促炎因子释放5 个方面总结多糖调控机体脂质代谢平衡的作用及机理,同时还对多糖调控脂质代谢的体内靶点进行讨论,以期为未来功能食品的开发和应用提供理论基础。
1 多糖概述
多糖通常是指由20 个以上单糖分子,通过糖苷键连接而成的长链聚合物,包括由同一种单糖组成的同多糖,以及由两种及以上的单糖组成的杂多糖。杂多糖通常指由高等植物、动物、微生物细胞等提取出的一类非常重要的大分子物质[7],通常不能被人体的消化系统完全消化,其对人体健康的益处主要体现在减缓胃排空、改善肠道功能以及调节肠道微生物结构并作为微生物发酵底物[8]。食源性多糖的生理功能众多,包括免疫调节、抗肿瘤、抗糖尿病、降血脂、缓解溃疡性肠炎和代谢综合征以及肠道微生态调节作用。植物多糖(如猪苓多糖、菊苣多糖[9])、真菌多糖(如粒毛盘菌多糖、桦褐孔菌多糖[10])以及细菌多糖(如乳酸菌多糖)目前已被证明具有改善饮食引起的脂质代谢紊乱的功能[11],且受到了研究者的广泛关注。
2 多糖缓解脂质代谢异常的机制
多糖调控脂质代谢异常的途径,通常包括抑制脂质的合成、促进脂质的氧化分解,以及维持机体能量代谢平衡3 个方面。抑制脂质合成和促进脂质氧化分解通常是同时存在的,因此本文主要从抑制脂质合成和促进脂质氧化分解、维持机体能量平衡、减少脂质的易位积累以及缓解氧化应激和炎症损伤等方面,来陈述并总结多糖维持脂质代谢稳态的机制。
2.1 抑制脂质的合成和促进脂质氧化分解
脂肪代谢的关键调节因子过氧化物酶体增殖物激活受体-α(peroxisome proliferator activated receptorα,PPAR-α),在过氧化物酶体及线粒体的脂肪酸氧化等途径中扮演着重要的角色,是调节脂质分解的关键基因[12]。据研究,米糠多糖以及黄精多糖可以通过上调小鼠PPAR-α、PPAR-β、PPAR-γ、PPAR-δ 基因的mRNA 表达量,进而降低高脂血症小鼠的体重、总胆固醇(total cholesterol,TC)、甘油三酯(triglyceride,TG)和低密度脂蛋白(low density lipoprotein-cholesterin,LDLC)含量[13-14]。浒苔多糖通过下调与脂质合成相关蛋白固醇调节元件结合蛋白-2(regulatory element binding protein-2,SREBP-2)的表达以及抑制SREBP-2 基因的表达,从而下调了胆固醇从头合成限速酶3-羟基-3-甲基戊二酸单酰辅酶A 还原酶(3-hydroxy-3-methylglutaryl coenzyme A reductase,HMGCR),维持肝脏胆固醇的代谢平衡[15]。脂肪酸甘油三酯脂酶(adipose triglyceride lipase,ATGL)在机体中发挥分解脂质的作用,而脂肪酸合酶(fatty acid synthase,FAS)和羟甲基戊二酰辅酶A 还原酶(hydroxymethylglutaryl-coenzyme A reductase,HMG-CoA)在机体中的作用是调控脂质的合成。研究表明青钱柳多糖通过上调ATGL 蛋白以及下调FAS 和HMG-CoA 蛋白水平,降低了血脂含量,有效地改善了脂质代谢紊乱[16]。姬松茸多糖干预明显下调了胆固醇生物合成相关的清道夫受体B 类成员1F(scavenger receptor class B member-1F,SCARB-1F)和SREBP-1C 的基因表达量以及上调了与脂质分解相关的胆固醇7α-羟化酶(cholesterol 7α-hydroxylase,CYP7a-1)和PPAR-α 的基因表达量,展现出了很好的降脂功效[17]。贻贝多糖改善脂质代谢异常主要与其阻碍FXR/SREBP-1C/FAS 信号通路的激活有关[18]。秋葵多糖通过抑制小鼠肝脏和脂肪组织中肝X 受体α 和β(liver X receptor α/β,LXRα/β)的基因mRNA 的表达、下调LXR 靶基因的表达及ATP 结合盒转运蛋白G1(ATP binding cassette transporter G1,ABCG1)、载脂蛋白E(apolipoprotein E,ApoE)、CYP7a-1 的蛋白水平,可改善高胆固醇血症[11]。去乙酰化蛋白类型1(sirtuin type1,Sirt1)可以调控能量代谢等过程,进而抑制脂肪酸合成和促进脂肪酸氧化,从而发挥改善脂质代谢紊乱的作用。慈姑多糖是通过刺激Sirt1 蛋白表达以及调控B 淋巴细胞瘤-2(B-cell lymphoma-2,Bcl-2)、Sirt1、Bcl-2 相关x 蛋白(Bcl-2 associated x protein,Bax)的基因表达量来改善肝功能和维持脂质代谢平衡的[19]。灵芝多糖通过上调肝组织PPAR-γ 的基因、下调环氧合酶(cyclooxygenase-2,COX-2)的基因表达量发挥防治NAFLD 的作用[20]。Li 等[21]研究发现菊苣多糖可调节脂质代谢相关X 框结合蛋白1(X-box binding protein 1,Xbp1)、胰岛素诱导基因2(insulin induction gene 2,nsig2)和胱硫醚酶(cystathionase,Cth)的基因表达,抑制脂肪合成,同时通过增加L-氯化棕榈酰和棕榈酰辅酶A 活性,促进了脂肪酸β-氧化,最终实现了缓解脂肪肝和脂质代谢紊乱的目的。Zhu 等[3]基于银耳多糖的研究,发现多糖可促进NAFLD 大鼠超长链脂肪酸β氧化并改善谷氨酸和酪氨酸代谢,最终改善NAFLD 引起的大鼠脂质代谢异常症状。拟鹿角灵芝多糖通过调节磷脂酰胆碱(phosphatidylcholine,PC)代谢促进肝脏脂肪运输[22],同时快速分解脂质为小鼠维持正常体重和血脂状态提供了保障。研究还证实了通过抑制脂肪合成调节因子乙酰辅酶A 羧化酶(acetyl-coa carboxylase,ACC)的基因表达,抑制CYP4a-1 和CYP7a-1 信号分子的基因表达,灰树花多糖也可以使高脂饮食(high fat diet,HFD)模型大鼠的脂质合成减少以及脂质分解增加,从而有效地改善脂代谢紊乱[23]。多糖缓解脂质代谢异常的作用机理如图1 所示。
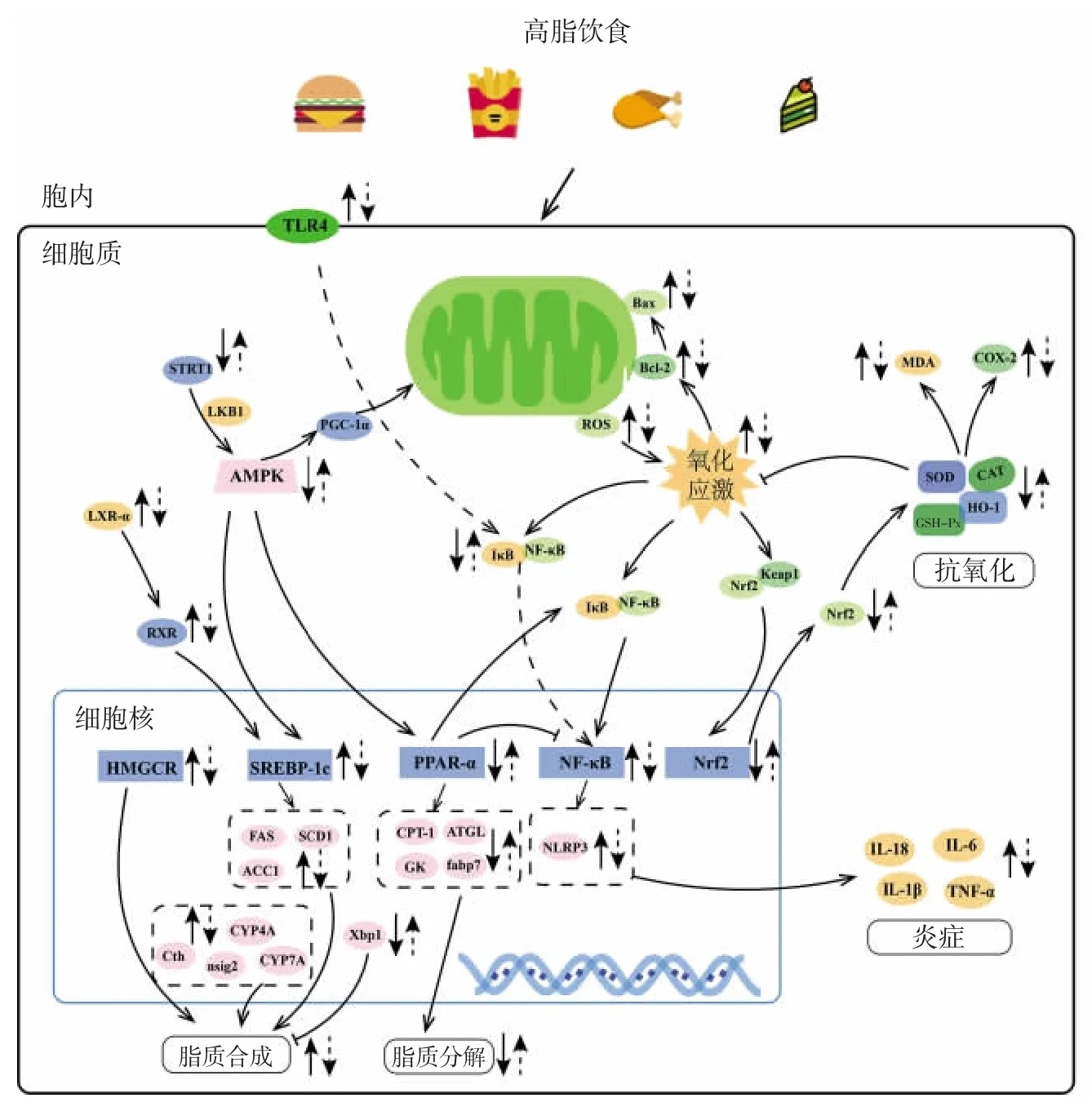
图1 多糖缓解脂质代谢异常的作用机理Fig.1 Mechanism of polysaccharides in alleviating lipid metabolism disorders
2.2 维持能量平衡
糖代谢和脂质代谢是能量代谢平衡的关键,而维持能量代谢的平衡也是改善机体脂质代谢的策略之一。AMP 活化蛋白激酶(AMP-activated protein kinase,AMPK)是机体维持能量代谢稳态的关键蛋白,通过上调AMPK 基因和蛋白的表达并激活AMPK 信号通路,多糖可以降低血清中TC 和TG 含量,维持糖脂代谢平衡并发挥了间接降脂作用[9]。通过对桦褐孔菌多糖的研究发现,激活的AMPK 信号通路是SREBP-1C、FAS和ACC 蛋白水平下调的原因,且多糖在维持能量平衡的同时缓解了脂质代谢紊乱[10]。枸杞多糖、金线兰多糖通过调控AMPK/SIRT1/PGC-1α 信号通路表现出了维持机体脂质代谢平衡的作用,这是多糖参与脂质代谢的重要途径[15]。Zhang 等[24]发现枸杞多糖在NAFLD 细胞模型中通过激活PGC-1α/NRF-1/TFAM 信号通路维持了细胞能量代谢平衡以及减少了胞内无法代谢的脂质。在多糖作用下AMPK/Nrf2/ARE 信号通路的激活可以改善脂质乳剂诱导的肝功能障碍和脂质代谢异常的症状[25]。灰树花多糖干预后明显下调的糖异生限速酶磷酸烯醇式丙酮酸羧激酶(phosphoenolpyruvate carboxykinase,PEPCK)的基因、SREBP-1C、FAS 和ACC基因表达量,AMPK-α、PPAR-α 和CYP7a-1 基因表达量的下调有助于维持能量代谢稳态以及缓解高脂血症大鼠体内的糖脂代谢紊乱[26]。
2.3 减少脂质的易位堆积
肝脏是脂类代谢的主要器官和重要场所,包括脂类的消化吸收、运输、分解代谢和合成代谢,都与肝脏有密切关系,因此,维持正常的肝功能也可以间接地改善脂质代谢紊乱,且肝-肠循环可能是肝脏发挥调节脂质代谢作用的主要途径[27]。脂肪代谢障碍导致的肝脏脂肪沉积是NAFLD 最本质的病理改变[28],而肝脏的异常脂质堆积是NAFLD 引起的脂质代谢紊乱的关键,上调肝细胞载脂蛋白B100 能够促进肝脏脂肪外排,缓解脂肪在肝脏的堆积。有研究发现麦冬多糖通过促进肠腔中胆汁酸吸收来阻碍肝-肠循环,从而减少肝脏总胆固醇含量以及缓解肝功能障碍[29]。五味子多糖与黄芪多糖联合干预可以通过上调与肝脏胆固醇代谢相关的LXRα、ATP 结合盒转运体A1(ATP-binding cassette transporter A1,ABCA1)和ABCG1 蛋白水平来促进脂质由肝脏排出,从而缓解高脂血症引发的大鼠脂肪肝症状,进而间接地参与脂质代谢[30]。改变构象的载脂蛋白A1(apolipoprotein A1,ApoA1)可以与脂类更好地结合,进而刺激卵磷脂胆固醇酰基转移酶(lecithin-cholesterol acyltransferase,LCA),加速胆固醇酯化并转移至肝脏,最终加速胆固醇在肝脏的清除[23],从而保护肝功能。白术多糖通过降低脂肪酸转运蛋白CD36 含量和增加肝载脂蛋白B100 来缓解饮食引起的肝脏脂肪过度堆积[31]。蛹虫草多糖通过促进胆固醇的转化和外排、减少脂质在肝脏的堆积参与脂质代谢调节[32]。然而,具有更好的吸附脂肪和胆酸盐能力的水溶性壳聚糖微球、壳聚糖微球,可以在不影响食欲的情况下,抑制大鼠的体重和体内脂肪的沉积[33]。多糖通过肝-肠轴对脂质的调控见图2。
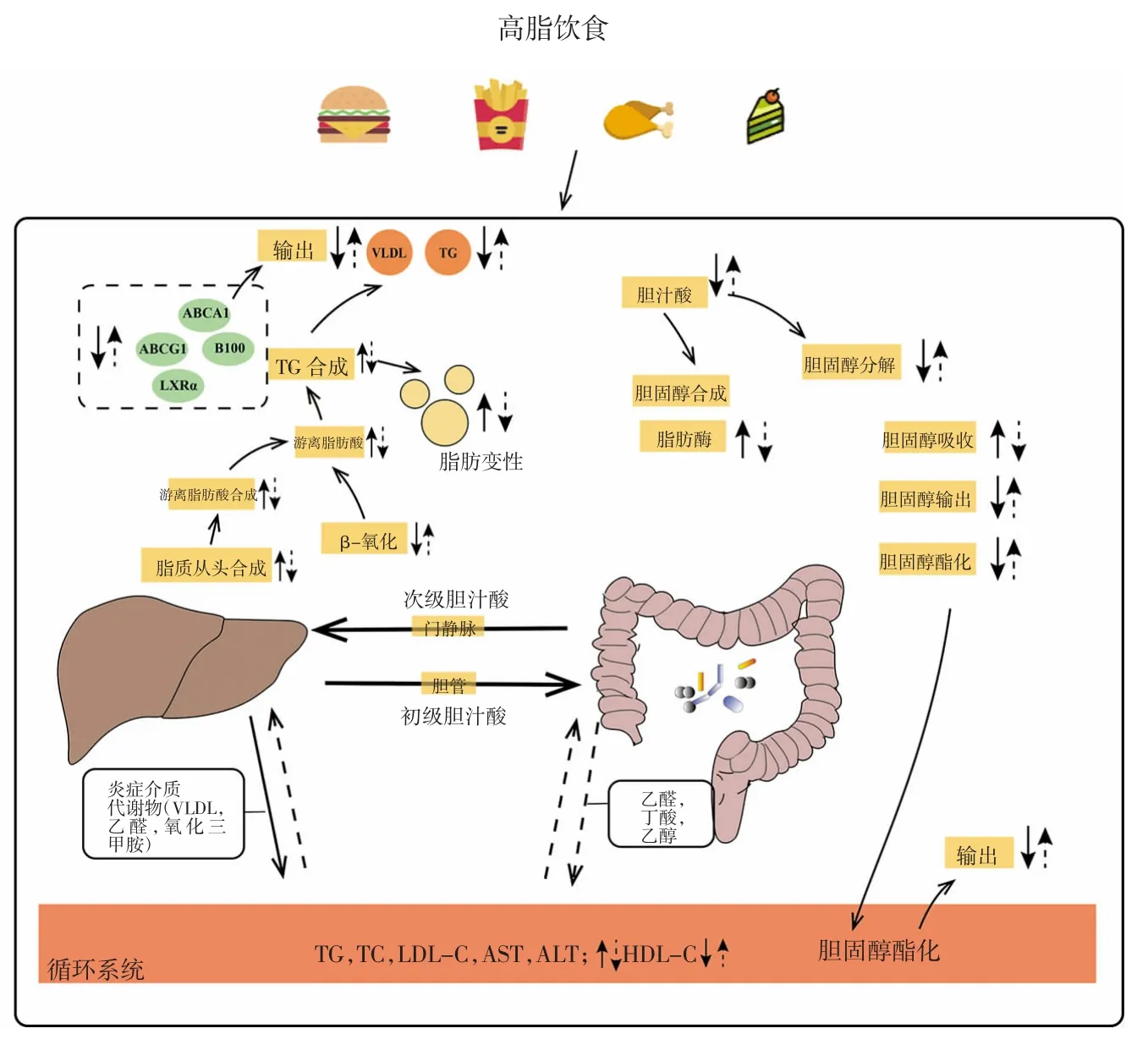
图2 多糖通过肝-肠轴对脂质的调控Fig.2 Polysaccharides regulate lipid metabolism through the liver-intestine axis
2.4 缓解氧化应激损伤
氧化应激是体内氧化作用与抗氧化作用稳态被打破的一种应激状态。过量的活性氧自由基(reactive oxygen species,ROS)积累,可以通过基因、信号传导、细胞和组织功能等途径损伤机体功能,导致机体抗氧化系统发生变化(氧化作用大于抗氧化作用),从而引发高脂血症及并发症的形成,如脂肪肝、肥胖、血管病变等疾病等[34],而减少氧化应激也被认为是多糖缓解脂质代谢紊乱的途径。肝细胞内堆积的游离胆固醇通过加速线粒体的谷胱甘肽消耗增加了肝细胞中的活性氧,进而加剧了氧化应激同时损伤了肝细胞,而增强抗氧化酶超氧化物歧化酶(superoxide dismutase,SOD)、谷胱甘肽过氧化物酶(glutathione peroxidase,GSH-Px)以及过氧化氢酶(catalase,CAT)活力,可降低肝脏中的过氧化产物丙二醛(malondialdehyde,MDA)含量。研究表明,黑皮鸡枞菌菌丝多糖[35]、黑木耳多糖[36]、硫磺菌多糖、毛头鬼伞多糖、灵芝多糖、北五味子多糖、黄芪多糖、铁皮石斛多糖[37]、蛹虫草多糖、粒毛盘菌(Lachnum YM281)[11,14,33]多糖可有效控制机体氧化和抗氧化作用的平衡同时维持脂质代谢稳态。金钗石斛多糖能够缓解NAFLD 引起的大鼠肝脏中CYP2E1 基因和蛋白的过度表达,并通过提高CAT 和SOD 活力修复机体氧化应激损伤,进而恢复肝代谢功能,同时维持机体脂质代谢稳态[38]。激活Nrf2/HO-1 信号通路来减少氧化应激损伤是慈姑多糖预防NAFLD 引起的脂质代谢紊乱的潜在机制[39]。天麻多糖调节脂质平衡的作用是通过上调Nrf2/GSH-Px 信号通路来增加SOD、GSH-Px 和CAT 活力和降低MDA 的含量并减少氧化应激损伤来实现的[40]。多糖可保护非酒精性脂肪肝病的小鼠肝功能,其可能与调节Keap1-Nrf2/ARE 信号通路、平衡抗氧化和氧化作用以及抑制氧化应激有关[41]。
2.5 减少促炎因子释放
炎症细胞因子除了介导炎症反应,还在胆固醇转运、脂质代谢中发挥重要作用。肿瘤坏死因子-α(tumor necrosis factor-α,TNF-α)能激发LDL-C 受体表达,阻碍胆固醇向肝脏外输送,导致肝脏胆固醇沉积,同时这也促进脂肪酸在脂肪组织中的释放以及脂肪分解,增加游离脂肪酸(free fatty acid,FFA)水平[27]。除了介导炎症反应,过量产生的白细胞介素-6(interleukin-6,IL-6)以及IL-1β 等促炎细胞因子还会抑制脂质的正常分解从而扰乱生物体正常的脂质代谢以及导致机体脂质代谢紊乱。据报道,慈姑多糖通过抑制NAFLD 小鼠IL-6 和TNF-α 基因的mRNA 表达,缓解脂代谢紊乱[42]。狗肝菜多糖通过抑制Toll 样受体-4(toll-like receptor 4,TLR-4)和NF-κB 信号通路的激活,抑制炎症细胞因子TNF-α、IL-6 和IL-1β 的释放,从而抑制肝脏炎症反应,同时缓解NAFLD 引发的脂质代谢异常[43]。抑制炎性小体NOD 样受体蛋白(nodlike receptor protein 3,NLRP3)和TLR4 通路的激活是金钗石斛多糖减少促炎因子IL-1β、IL-18、IL-6 以及TNF-α 释放的关键,进而抑制炎症反应同时间接地改善了高脂饮食诱发的肝脏脂质堆积和脂质代谢异常的症状[44]。菊粉和贻贝多糖缓解NAFLD 的作用与其抑制LPS/TLR4/NF-κB/NLRP3 炎症通路的激活有关[45]。
2.6 其他作用机制
多糖也被发现通过其他新的途径来发挥降脂作用。Myoung 等[46]发现芹菜素可以提高神经元细胞的厌食神经肽前阿皮黑素皮质激素(peptide preapirelanin corticosteroids,POMC)和可卡因-苯丙胺调节转录肽(cocaine-amphetamine regulatory transcription peptide,CARTP)的活性,减少小鼠的食物摄入量,从而使小鼠体重下降,血脂降低。胃排空延迟是粗纤维和壳聚糖降血脂的作用机理,同时壳聚糖分子中的氨基结构,在胃环境中易成盐溶解,而其在肠中可成溶胶从而阻碍机体胆固醇和脂肪的吸收。胃肠道与大脑有着密切的联系,多糖摄入后机体可以从胃肠道得到通过机械感应向大脑发出控制食物的信号,从而发挥抗肥胖作用[47]。
3 多糖调控脂质代谢的靶点
肠道菌群失调与多种疾病的发生息息相关,如肥胖、Ⅱ型糖尿病、非酒精性脂肪肝等脂质代谢异常的疾病[48]。肠道和肝脏通过胆道、门静脉和体循环的紧密双向连接,相互交流,肝脏通过释放胆汁酸等多种活性介质流入胆道和全身体循环来与肠道相通,这被称为肠-肝轴。在肠道内,通过门静脉宿主和微生物代谢的内源性(胆汁酸和氨基酸)和外源性(来自饮食和环境暴露)底物可以转运至肝脏并影响肝脏功能[49],这揭示了肠道菌群调节脂质代谢的肝-肠循环通道。而基于多糖的人体不可消化性,推测肠道可能是其作用靶点,且其主要作用为对肠道菌群结构以及菌群代谢物的调节。
据报道,多糖既可以促进肠道益生菌的生长直接发挥抗肠道炎症的作用,也可以经发酵产生的短链脂肪酸(short chain fatty acids,SCFAs)、乳酸、乙醇、琥珀酸和甲酸盐等发挥脂质调节的作用[50]。香菇多糖被证明可以作用于肠道同时通过促进双歧杆菌属(Bifidobacterium)的增殖,增加了小肠紧密连接蛋白,从而维护了机体肠道屏障完整性和氧化还原平衡并成功地改善了NAFLD[51]。麦冬根多糖通过增加SCFAs 产生菌,如丁酸弧菌属(Butyrivibrio)和罗氏菌属(Rothia),有效地抑制了肠道炎症反应同时缓解了NAFLD 引起的脂质代谢紊乱[52]。多糖对肠道菌群的调节作用[如增加拟杆菌属(Bacteroides)和放线菌门(Actinobacteria)的相对丰度] 可以改善肥胖引起的肠漏以及缓解代谢性内毒素血症、炎症和血脂异常,同时参与糖脂代谢稳态的调节[53]。增加肠道狄氏副拟杆菌(Parabacteroides distasonis)、粪厌氧棒状菌(Anaerofustis stercorihominis)和梭状杆菌(Fusobacterium)丰度,进而促进胆汁酸的分泌被证明是杏鲍菇多糖作用与肠道后发挥抗肥胖和降低胆固醇作用的关键[54]。增加拟杆菌属(Bacteroides)、普氏菌属(Prevotella)等肠道共生菌,减少沙门氏菌(Salmonella)、埃希氏菌(Escherichia)的丰度是膳食纤维作用于肠道并代谢葡萄糖生成乳酸、丁酸、琥珀酸的有力证据,同时改变的肠道菌群也维持了肠道微生态稳定和肠-肝循环系统,从而改善了NAFLD、高脂血症以及肥胖等疾病[14]。
4 总结与展望
高脂、高能量饮食会打破机体的脂质代谢平衡,增加肝脏负担,从而导致肝脏等多器官脂肪堆积,甚至引起全身代谢失调,如肥胖、NAFLD、Ⅱ型糖尿病和代谢综合征等的发生和发展。诸多的研究表明,饮食结构改变、适量的多糖干预能够显著改善机体的脂质代谢紊乱同时维持机体健康状态。多糖相关的脂质调节机制也被广泛地探索和研究,包括调控脂质的合成和分解、维护机体能量平衡、抑制脂质的易位堆积、减少氧化应激和炎症损伤以及多糖作用的靶点和通道等方面,但是目前仍没有清晰确切的机理被呈现。生物技术的进步以及宏基因组学、转录组学、蛋白质组学和代谢组学等组学技术的发展,丰富了解析多糖对脂质调控机制的手段,为研究者更全面地探索相关机制提供了技术支持。另外,本文为具有降脂以及调节脂质代谢紊乱作用的功能食品的开发和应用提供了理论依据。
多糖表现出了很好的降脂和促健康作用,但是对于其功能研究深度不够,仅停留在对其结构的解析和表型功效上,而没有明确的证据剖析多糖的结构与功能之间的确切关系,比如某一特殊的单糖组成或特定的连接键和空间构型与多糖的降脂作用存在的关联。分析多糖结构和功能以及挖掘其结构背后潜在的规律和联系是目前研究的难题,也是未来人们认识天然多糖结构和功能需要攻克的难关。此外基于多糖的精细结构,研究其作用的靶器官以及细胞信号通路,探究其发挥活性的分子机制并阐明多糖结构与功能之间的关系将会是未来的研究热点。
