pH 值对酪蛋白- 木糖醇复合物功能和结构特性的影响
2023-09-12安悦嘉曹雪妍陶冬冰岳喜庆
安悦嘉,曹雪妍,杨 梅,陶冬冰,张 旋,张 琦,潘 松,岳喜庆
(沈阳农业大学食品学院,辽宁 沈阳 110866)
酪蛋白是十分重要的优质蛋白,其必需氨基酸含量较高,且比例适中,种类齐全,在人体发育成长的过程中必不可少。木糖醇是糖尿病患者不可或缺的糖代品,其生物利用、医学辅助治疗预防方面都十分优质,大众需求不断提高。
酪蛋白的功能性质在食品加工中具有不可或缺的作用。酪蛋白较好的乳化性可提高脂肪乳化程度,常用于脂肪含量较高的蛋糕及咖啡伴侣中。较好的起泡性因可以形成稳定膜使酪蛋白被用作泡沫稳定剂,应用于人造奶油中。但酪蛋白的溶解性较差,难以在室温条件与其他缓冲液相融,导致其在食品加工行业的发展和利用中受到了阻碍[1]。pH 值是改变蛋白质溶解性较为重要的因素,尤其当pH 值接近酪蛋白等电点会对酪蛋白溶解性产生较大影响[2],且pH 值也会改变蛋白质的分子构象,结构的改变往往会带动其功能性质的变化。而木糖醇可以提高和改善酪蛋白的乳化稳定性、起泡能力、起泡稳定性及结构特性,尤其是可以改善酪蛋白较差的溶解性[3]。
以解决酪蛋白自身较差的溶解性为基础前提,利用圆二色光谱、荧光光谱、紫外分光光度等方法研究了不同pH 值对酪蛋白- 木糖醇复合物二级结构、三级结构及表面疏水性、乳化性、起泡性、溶解性的影响。以便选取最适宜的环境条件及加工技术,更好地对复合物进行加工及利用,对酪蛋白与木糖醇在乳制品、功能性食品的添加及研发提供理论指导。
1 材料与方法
1.1 材料与主要仪器
酪蛋白(蛋白质含量≥95.0 %,相对分子质量为50 000~375 000)、木糖醇(纯度>99%,相对分子质量为152.1),北京鼎国昌盛生物技术有限责任公司提供。
F-4600 型荧光光谱仪,日立公司产品;RH basic2 型磁力搅拌器,广州科仪公司产品;Cary 50 型紫外- 可见分光光度计,美国VARIAN 公司产品;DK-S26 型数显电子恒温水浴锅,上海精宏公司产品;T18 basic 型高速分散器,德国IKA 公司产品;pHS-25 型数显pH 计,上海精密科仪公司产品;J-810 型圆二色谱仪,日本Jasco 公司产品。
1.2 试验方法
1.2.1 预处理方法
将酪蛋白粉末与木糖醇颗粒按照浓度比为1∶1,1∶2,1∶3,1∶4,1∶5 称取并混合,再溶解于体积比为1∶1 的0.1 mol/L NaOH 溶液和0.05 mol/L 的Tris-HCl 溶液缓冲液中,置于50 ℃的水浴锅中待沉淀完全溶解后,置于磁力搅拌器中搅拌[4]。测定在中性pH 值室温25 ℃条件下,不同浓度配比对酪蛋白- 木糖醇复合物表面疏水性、起泡性、乳化性及溶解性的影响。选择复合物溶解性最好的浓度配比1∶1,并将接下来的试验设定酪蛋白与木糖醇浓度为1∶1,pH 值的范围设定为3,4,5,6,7,8,9,10,11。
1.2.2 表面疏水性的测定
将不同pH 值的酪蛋白- 木糖醇复合物溶液样品用缓冲溶液稀释适当倍数后分别加入25 μL 的ANS探针溶液,振荡均匀并放于室温下避光静置5 min。以样品缓冲溶液为对照,采用日立F-4600 型荧光分光光度计,激发波长为390 nm,发射波长为470 nm,激发和发射狭缝宽均为5 nm 条件下,测定样品的荧光强度[5]。
1.2.3 起泡性的测定
分别取适量酪蛋白- 木糖醇复合物于高速分散器以转速10 000 r/min 均质60 s,迅速记录泡沫体积即为初始泡沫体积。静置30 min 后再次计算泡沫体积,基于以下公式计算起泡性(FAI,%) 以及起泡稳定性(FSI,%)[6]:
式中:V——样品溶液的体积,mL;
V0——均质后即刻记录的样品初始泡沫体积,mL;
V30——静置30min 后记录的样品泡沫体积,mL。
1.2.4 溶解性的测定
采用考马斯亮蓝法,分别将酪蛋白- 木糖醇复合物溶液以转速8 000 r/min 离心20 min,取出1 mL的上清液稀释10 倍或100 倍,滴加5 mL 考马斯亮蓝溶液,避光10 min,于波长595 nm 处测定样品的吸光度,根据牛血清白蛋白标准曲线计算上清液中蛋白质含量,再根据以下公式计算溶解性(%):
1.2.5 乳化性的测定
将酪蛋白- 木糖醇复合物溶液与食用大豆油以3∶1 的比例混合,用高速分散器以转速10 000 r/min均质60 s,从乳化液即离心管底部吸取50 μL 的混浊液,立即用质量分数为0.1%的SDS 溶液稀释适当倍数后振荡均匀,分别在0 min 和10 min 时用紫外分光光度计测定样品在500 nm 波长处的吸光度,以SDS 为空白对照。根据下式计算乳化活性(EAI,m2/g) 和乳化稳定性(ESI,min)[7]:
式中:C——蛋白质质量,g;
φ——油相体积分数,%;
T=2.303;
DF——稀释因子;
θ——油相体积分数(0.25),%;
A0——0 min 时吸光度;
A10——10 min 时吸光度。
1.2.6 内源荧光光谱的测定
将处于不同pH 值的酪蛋白- 木糖醇复合物溶液样品稀释10 倍后加入ANS 荧光探针溶液,摇晃均匀,在避光的条件下反应5 min,以缓冲溶液(NaOH+Tris-HC)l 作为空白对照。激发波长为280 nm,激发和发射狭缝均为5 nm,扫描发射波长范围为300~450 nm 的荧光光谱。
1.2.7 圆二色谱(CD) 分析
用圆二色谱仪在25 ℃条件下测定样品在远紫外区域(190~250 nm) 的CD 光谱,以样品的缓冲溶液(NaOH+Tris-HCl) 为空白对照,比色皿的光径为0.1 cm,测定远紫外区的CD 光谱。扫描速率为100 nm/min,Data Fitch 为1.0 nm,Band Width 为2.0 nm,扫描3 次,取平均值得到最终的CD 光谱。使用带有selcon3 算法的CDpro 软件来计算蛋白质二级结构的组成和含量。
2 结果与分析
2.1 不同pH 值对酪蛋白- 木糖醇复合物表面疏水性的影响
不同pH 值对酪蛋白- 木糖醇复合物表面疏水性的影响见图1。
当pH 值在酪蛋白等电点附近时,其疏水性产生了明显的下降。可能是由于复合物溶液在等电点附近形成明显聚集沉降,疏水基团被沉降大多包在沉淀内部,使ANS 探针与位点的结合数量降低[8]。当pH 值逐渐增大,复合物疏水性也随之增大。由于木糖醇能够增加酪蛋白于等电点附近所带的电荷数,有效防止酪蛋白分子的相互作用及出现明显集聚,增强酪蛋白分子的结构稳定。
2.2 不同pH 值对酪蛋白- 木糖醇复合物起泡活性的影响
不同pH 值对酪蛋白- 木糖醇复合物起泡活性的影响见图2。
当pH 值处于等电点左右时,酪蛋白- 木糖醇复合物具有较差的起泡能力。由于此时酪蛋白的疏水性降低,影响了酪蛋白分子在水与空气两相的结合与吸收,溶液表面张力减小。当pH 值增大,酪蛋白- 木糖醇的起泡能力提高。由于酪蛋白分子结构变得松散,柔性增加,促进了酪蛋白分子在水与空气两相的快速吸收和结构展开[9]。
2.3 不同pH 值对酪蛋白- 木糖醇复合物起泡稳定性的影响
不同pH 值对酪蛋白- 木糖醇复合物起泡稳定性的影响见图3。
当pH 值为4 左右时,降低了复合物溶液的起泡稳定性。由于酪蛋白的疏水性因pH 值的影响降低,其柔性也因溶液中产生了絮状沉淀物而降低,使蛋白质分子在水和空气两相之间形成膜状结构的能力降低。当pH 值逐渐增大,复合物的起泡稳定性增强。由于逐渐递增的疏水性及疏松的分子内部结构使酪蛋白分子可以逐渐在水和空气两相形成绵密的泡沫,普拉长边界的数量增加[10]。
2.4 不同pH 值对酪蛋白- 木糖醇复合物溶解性的影响
不同pH 值对酪蛋白- 木糖醇复合物溶解性的影响见图4。
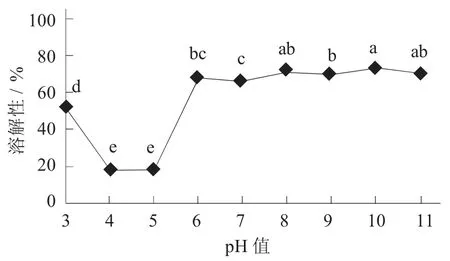
图4 不同pH 值对酪蛋白- 木糖醇复合物溶解性的影响
当pH 值为4 左右时,复合物的溶解性降低。由于酪蛋白分子所附的静电荷数可忽略不计,所以静电斥力也基本消失[11]。但当pH 值增加或降低时,复合物溶液的溶解度显著增加。酪蛋白分子之间的静电斥力因其正负电荷而提高,防止蛋白质发生沉降。
2.5 不同pH 值对酪蛋白- 木糖醇复合物乳化活性的影响
不同pH 值对酪蛋白- 木糖醇复合物乳化活性的影响见图5。

图5 不同pH 值对酪蛋白- 木糖醇复合物乳化活性的影响
当pH 值靠近等电点,复合物的乳化活性降低。由于酪蛋白自身的水合作用及静电斥力均受到不良影响,使酪蛋白表现为微溶的状态。同时,酪蛋白分子向油- 水界面的扩散,此时较低的溶解性受到影响,降低了其界面张力[12]。当pH 值增加或降低时,复合物的乳化活性增加。由于复合物的溶解性增加,酪蛋白分子与油和水两相之间的相互作用随之加大,使界面张力减小。
2.6 不同pH 值对酪蛋白- 木糖醇复合物乳化稳定性的影响
不同pH 值对酪蛋白- 木糖醇复合物乳化稳定性的影响见图6。

图6 不同pH 值对酪蛋白- 木糖醇复合物乳化稳定性的影响
当pH 值为5 时,降低了复合物的乳化稳定性。由于增加的复合物乳液分子相互作用表明其分子所带电荷数量可能偏低,使复合物溶液产生沉降。但当pH 值远离等电点,复合物溶液的乳化稳定性显著增加。可以说明酪蛋白的水合作用及静电斥力是由于所带电荷数量的变多而增加的。油—水界面的能量降低,避免溶液产生集聚[13]。
2.7 不同pH 值对酪蛋白- 木糖醇复合物内源荧光发射光谱的影响
不同pH 值条件下的酪蛋白- 木糖醇复合物内源荧光发射光谱见图7。
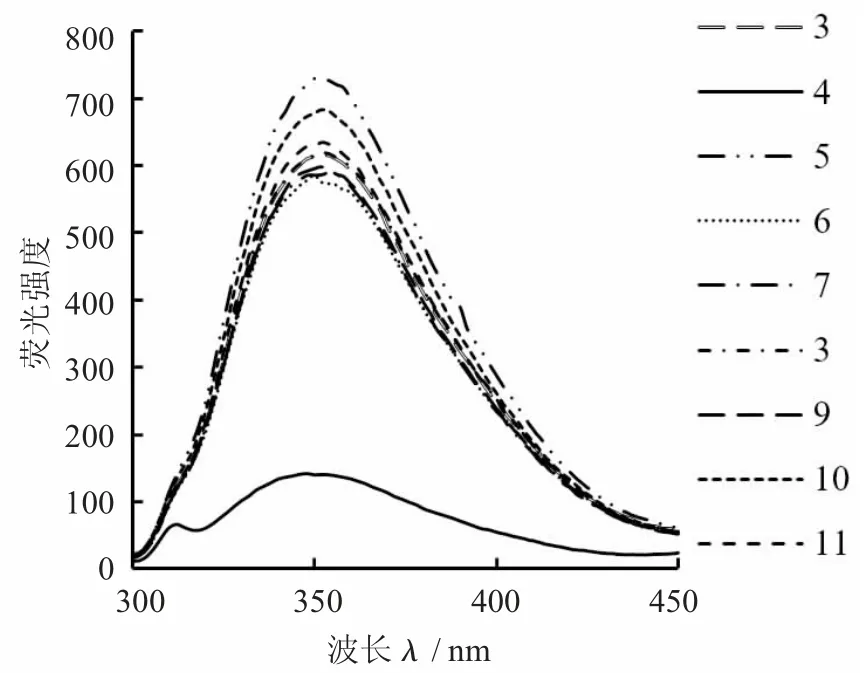
图7 不同pH 值条件下的酪蛋白- 木糖醇复合物内源荧光发射光谱
由图7 可知,当pH 值为4 时,样品的内源荧光光谱λmax与pH 值为3 时的样品相对比减小到348 nm,出现了少量的蓝移,与此同时,内源荧光值大幅度降低。可能是因为pH 值为4 左右时,酪蛋白分子之间的静电相互作用因其表面所带电荷数的增加而增大。溶液中形成明显的絮凝沉降,因其环境中的极性大幅度降低而减少了芳香族氨基酸残基的暴露数量[14]。当pH 值为7 时,样品的内源荧光光谱λmax值增加为354 nm,产生了红移,并且其内源荧光值也照样品pH 值为4 时大幅度增加。当pH 值继续逐渐增加至碱性条件下时,内源荧光值则没有较明显的变化。
2.8 不同pH 值对酪蛋白- 木糖醇复合物远紫外圆二色光谱的影响
不同pH 值条件下的酪蛋白- 木糖醇复合物远紫外圆二色光谱见图8。
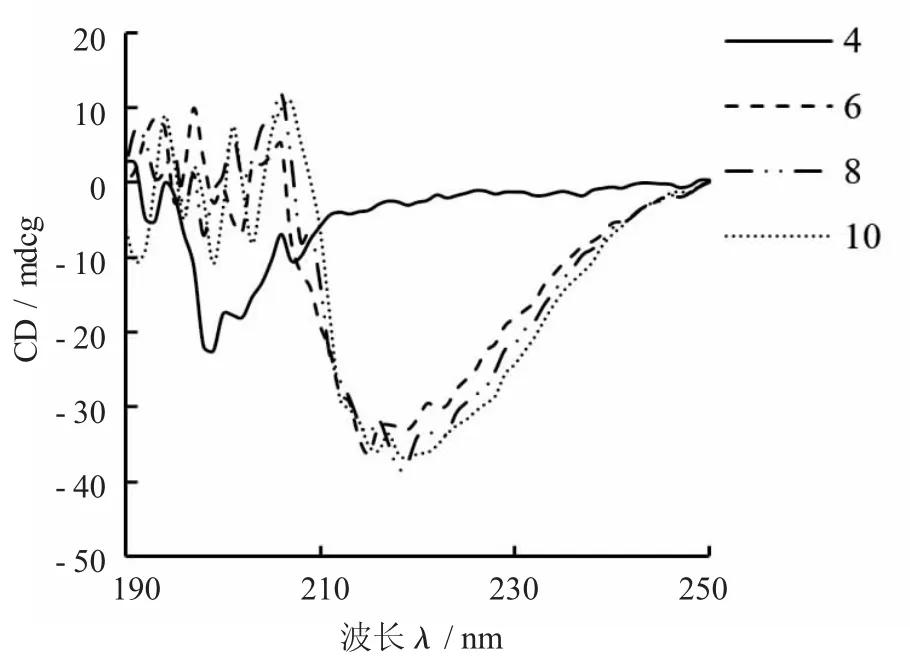
图8 不同pH 值条件下的酪蛋白- 木糖醇复合物远紫外圆二色光谱
由图8 可知,pH 值为6~10 时的样品圆二色谱的负吸收峰出现在210~230 nm,而pH 值为4 时,该样品的圆二色谱负吸收峰出现在190~210 nm 内。pH 值在6 附近时,酪蛋白具有紧密的分子结构,与碱性条件下的分子结构相差无异。当pH 值降低到酪蛋白等电点附近时,样品的圆二色谱负吸收峰的位置产生明显蓝移,说明此时酪蛋白分子中α- 螺旋结构的数量明显降低。当pH 值为10 时酪蛋白结构中α- 螺旋相对较多。
不同pH 值条件下的酪蛋白- 木糖醇复合物二级结构含量分析见表1。
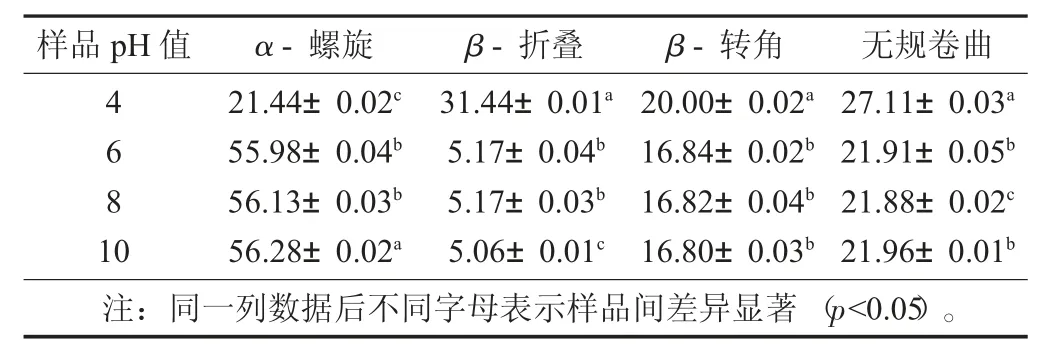
表1 不同pH 值条件下的酪蛋白- 木糖醇复合物二级结构含量分析/%
由表1 可知,pH 值由10 降低到4,酪蛋白分子的α- 螺旋结构从56.28%降低到21.44%,说明酪蛋白分子表面的氨基酸等质子化态会随着环境中的pH值的变化而发生改变,致使其结构中的α- 螺旋也随之明显改变[16]。与此同时,当pH 值为4 时的酪蛋白结构中β- 折叠、β- 转角及无规卷曲均出现相较于远离等电点条件而言明显增大。蛋白质分子的结构会由于结构中的无序转角及无规则卷曲结构数量的增多而变得松散,但因其表面所吸附的电荷量偏少,所以会在溶液中形成明显的絮凝沉淀物。
3 结论
当pH 值临近酪蛋白等电点4.6 时,酪蛋白与木糖醇复合物的功能特性(溶解性、乳化性、起泡性、疏水性) 均较差。复合物内源荧光值大幅度降低。分子结构稳定性较差。当pH 值远离等电点时,酪蛋白与木糖醇复合物的功能特性(溶解性、乳化性、起泡性、疏水性) 均显著提高。内源荧光值明显升高。分子结构稳定性较好。
在生产和加工含有酪蛋白- 木糖醇复合物的食品的过程中,应避免环境pH 值临近酪蛋白等电点,趋于中性或弱碱性的pH 值环境较好。
