直链淀粉-番茄红素复合物的光稳定性及降解动力学研究
2023-09-07孙世东赵文红任顺成
孙世东,赵文红,任顺成
河南工业大学 粮油食品学院, 河南 郑州 450001
番茄红素(lycopene)是一种天然色素,属于类胡萝卜素的一种[1],含有多不饱和的异戊二烯结构,具强抗氧化活性[2]。研究发现番茄红素具有清除过氧自由基[3]、高效猝灭单线态氧[4-5]、增强免疫力[6]、预防心血管疾病[7]和多种癌症[8]等生理功能。
由于番茄红素易受到光、pH 值、氧、热等因素的影响产生降解而造成损失[9-11],从而限制了其工业化的广泛应用。目前,常见的番茄红素制剂包括包合物[12]、微胶囊[13]、脂质体[14]和微乳[15]等。相比较而言,包合物制备作为一种包埋技术,不仅可以改善番茄红素的稳定性,还可以提高其在水基体系中的分散性[16]。Wang等[17]制备了番茄红素-β-环糊精包合物,发现在 50 ℃ 保持 210 min 后,包合物稳定性显著高于番茄红素。摆玉芬[18]研究建立了番茄红素-羟丙基环糊精包合片,在日光照射 6 h 后,番茄红素晶体几乎完全降解,而包合片中番茄红素保留率为65%。直链淀粉作为一种亲水胶体,在热处理过程中的特殊结构行为而被广泛用作封装功能性小分子的壁材[19-21]。
本课题组前期基于淀粉的回生特性制备得到了直链淀粉-番茄红素复合物(amylose-lycopene complexes,ALCs),并对其复合结构进行了初步分析[22],但该复合物的光稳定性尚不清楚。作者以番茄红素标准品为对照,通过测定ALCs 在不同光条件下番茄红素含量,分析比较对番茄红素保留率的影响,进而对其抗氧化活性变化规律及降解动力学行为进行研究,评价其光稳定性,研究淀粉基复合制剂对番茄红素的保护作用,以期为番茄红素稳定制剂的开发、番茄红素在食品领域的应用提供参考。
1 材料和方法
1.1 试验材料
直链淀粉(标准品,来源于马铃薯)、番茄红素(纯度为 90%):上海源叶生物科技有限公司;DPPH(纯度为 96%):上海麦克林生化科技有限公司;盐酸(纯度为 36.5%)、氢氧化钠、二甲基亚砜、丙酮、无水乙醇:天津科密欧仪器试剂有限公司;氮气(纯度为 98%):郑州新丰化学试剂有限公司;ALCs 和蒸馏水实验室自制。以上试剂均为分析纯。
1.2 仪器与设备
UV1800-BPC 型紫外分光光度计:上海美普达仪器设备有限公司;JXDC-10 型氮气吹扫仪:上海净信科技仪器有限公司;YM-120S 型超声波仪:广东洁盟电器有限公司;DZF-6050 型真空干燥箱:上海齐欣科学仪器有限公司;MS-H280-Pro 型磁力搅拌器:美国 SCI LOGEX 公司;紫外灯管:广东冠迪电器有限公司。
1.3 试验方法
1.3.1 ALCs 的制备
参照Lv 等[23]的制备方法,并稍做修改。称取番茄红素 15 mg 溶于 15 mL 二甲基亚砜中备用;取直链淀粉300 mg,用 0.4 mL 无水乙醇分散后加入 30 mL 蒸馏水溶解;将直链淀粉溶液置于 95 ℃ 水浴 5 min 后降温至 50 ℃;加入预制番茄红素溶液于500 r/min 搅拌 2 h,程序降温后放入冰箱冷藏 6 h;样品于 1 500 r/min 离心 30 min 后真空干燥沉淀,即得直链淀粉-番茄红素复合物。所有过程需避光、无氧氮气保护操作。
1.3.2 ALCs复合指数和复合率的测定
1.3.2.1 ALCs 复合指数的测定
复合指数是衡量直链淀粉与番茄红素发生复合程度的重要指标,通过碘与未复合的直链淀粉反应,间接体现出直链淀粉与番茄红素的复合程度。采用碘量法[24]测定 ALCs 的复合指数。称取0.1 g 样品分散于 1 mL 乙醇中,加入 9 mL NaOH(1 mol/L),于 100 ℃ 水浴锅热处理 10 min,定容至1 mg/mL,记为A。取 2 mL A,依次加入 3 mL NaOH(0.09 mol/L)、50 mL水、1 mL乙酸(1 mol/L)和 1 mL 试验用碘液,定容至 100 mL,放置 15 min 后在 680 nm 处测吸光度。

(1)
式中:A0为直链淀粉的吸光度;A1为 ALCs 的吸光度。
1.3.2.2 ALCs 的番茄红素复合率的测定
番茄红素复合率为 ALCs 中番茄红素的质量与初始制备中使用的番茄红素质量之比。为了测量番茄红素的质量,将真空干燥后的粉末状复合物(5 mg)分散在 10 mL H2O 中。将样品涡旋 10 min,然后添加 10 mL 丙酮,并将其放入超声仪中超声 20 min 以将番茄红素转移至有机相,直至水层无色。合并有机相,并用无水硫酸钠脱水。使用紫外分光光度计在 447 nm 处测定有机相的吸光度。

(2)
式中:w0是制备 ALCs 时加入的番茄红素质量,mg;w1是 ALCs 的质量,mg;w2是真空干燥后 ALCs 的质量,mg;c1是 ALCs 中番茄红素的含量,μg/mL;V是用于提取番茄红素的丙酮的体积,mL。
1.3.3 ALCs 中番茄红素含量和保留率测定
参照罗树伟等[25]使用的方法,并稍做修改。分别配制 0、2.5、5、7.5、10、15 μg/mL 的番茄红素丙酮溶液,采用紫外分光光度计测定其在 447 nm 处的吸光度,每个试验重复3次,对试验结果取平均值,绘制含量-吸光度图,并进行线性拟合,得到标准曲线方程。称取一定量复合物样品于若干试管中,分别置于避光、自然光、紫外光下,每隔一定时间取样 5 mg。将取出的样品置于试管中加入 10 mL丙酮,经超声萃取5 min 后以 1 500 r/min 离心 15 min,取上清液测定其在 447 nm 处的吸光度,根据标准曲线的回归方程计算得到其中的番茄红素含量后,依照公式(3)计算番茄红素保留率。

(3)
式中:C0是 ALCs 中番茄红素的初始含量,μg/mL;Ct是不同时间点测定的 ALCs 中番茄红素含量,μg/mL;V0是 ALCs 初始样品萃取番茄红素的丙酮体积,mL;Vt是不同时间点测定 ALCs 中番茄红素时萃取的丙酮体积,mL。
1.3.4 ALCs对DPPH的清除率测定
参考 Zhou等[26]的方法进行测定。将 ALCs 和番茄红素标准品分别置于避光、自然光、紫外光下,每隔一定时间取样 5 mg,经 10 mL 丙酮超声浸提得到其中的番茄红素;量取 1 mL 浸提液加入 3 mL 0.01 mmol/L的DPPH溶液中,避光反应 30 min 后在 517 nm 处测定吸光度。测定完成后计算复合物的 DPPH 清除率。计算公式如下:
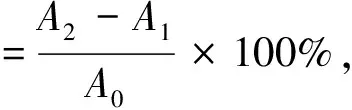
(4)
式中:A0为 DPPH 混合溶液(DPPH 无水乙醇溶液与丙酮的体积比为3∶1)的吸光度;A1为无水乙醇与 ALCs 丙酮溶液(体积比3∶1)的吸光度;A2为反应后 DPPH 溶液和 ALCs 溶液(体积比3∶1)的混合物的吸光度。
1.3.5 ALCs 中番茄红素降解动力学模型构建
参考 Aliyu等[27]使用的测定方法,依照阿伦尼乌斯方程进行降解动力学模型构建。依据 ALCs 中番茄红素的含量变化分别代入零级、一级和二级降解动力学方程式进行拟合,以探究直链淀粉-番茄红素复合物的降解动力学行为特征。零级、一级和二级反应动力学方程式分别见公式(5)、(6)和(7)。
y0=C0-Ct=kt+b,
(5)
(6)
(7)
式中:C0是 ALCs 中番茄红素的初始含量,μg/mL;Ct为不同时间点 ALCs 中番茄红素的相对含量,μg/mL;t为不同时间点,h;k为降解常数,μg/(mL·h)。
经降解动力学拟合后根据以上公式计算ALCs的速率常数k(μg/(mL·h))、半衰期(T1/2,h)和十分之一衰期(T9/10,h)等降解动力学参数。
1.3.6 数据处理
使用 SPSS 24.0 进行统计学处理,采用 Origin 2018 和 Microsoft Excel 2019 软件作图。各项指标以平均值±标准差表示;试验组与对照组计量资料采用配对t检验,定性数据比较采用χ2检验。
2 结果与分析
2.1 ALCs 的复合效果分析
直链淀粉-番茄红素复合物的复合效果用复合指数和复合率表示。将 447 nm 处的吸光度与不同番茄红素浓度作图,并进行线性拟合得标准曲线y=0.156 5x-0.011 3(R2= 0.999 9)。利用标准曲线和公式(1)和(2),计算可得 ALCs 的复合指数和复合率分别为 15.53%±1.01% 和 83.97%±0.16%。Jafari 等[28]使用改性淀粉封装番茄红素,发现复合指数介于 21.01%~29.73% 之间。Ranveer 等[29]利用蔗糖和明胶包合番茄红素,发现其复合率在 63.90%~82.20% 之间。
直链淀粉-配体复合物的包合效果取决于配体的碳链长短[30]。Chen等[31]制备了莲子直链淀粉-棕榈酸复合物,发现长脂肪酸链可能太长而无法被直链淀粉完全包埋。Zhou等[32]研究发现饱和脂肪酸与直链淀粉的复合效果明显优于不饱和脂肪酸,其原因是不饱键的存在导致了空间位阻的形成,抑制两者的复合。番茄红素是由8个异戊二烯单元组装而成的四萜,由于番茄红素的特殊结构,使其不能完全进入到直链淀粉的螺旋空腔中[33]。结果表明,番茄红素存在进入直链淀粉螺旋空腔中的行为,即直链淀粉包合番茄红素形成了复合物。
2.2 ALCs 含量变化分析
为了研究 ALCs 中番茄红素的光稳定性,课题组以番茄红素保留率为指标,观察 ALCs 在紫外光、自然光和避光条件下其番茄红素含量变化,结果见图 1。
由图 1(a)可知,在3种光条件下,随处理时间延长,ALCs 的番茄红素保留率呈逐渐降低趋势,光处理 24 h 后 ALCs 的番茄红素保留率为 61.23%±0.64%(紫外光)、73.43%±0.24%(自然光)、77.67%±0.34%(避光),紫外光处理下ALCs的番茄红素保留率最低;对照组的番茄红素保留率(图1(b))也表现出相同的降低趋势,光处理 24 h 后对照组的番茄红素保留率分别为36.59%±0.26%(紫外光)、57.88%±0.18%(自然光)、73.19%±0.18%(避光),紫外光处理下对照组的番茄红素保留率最低。综上可知,在3种光条件下,随处理时间的延长,复合物中的番茄红素逐渐损失,ALCs 的番茄红素光稳定性顺序为避光>自然光>紫外光。由此可见,紫外光对复合物中番茄红素的稳定性影响较大,因此,复合物在保存时应避免紫外光长时间照射,尽可能地避光保存。但复合物中番茄红素保留率显著优于对照,这可能与 ALCs 的包合型复合结构有关。与番茄红素标准品相比,ALCs 中的番茄红素可进入到直链淀粉的疏水螺旋空腔中,还可与直链淀粉分子链缠绕形成双螺旋结构[34-36],因此形成复合物可保护其中的番茄红素免受损失。以往的研究也表明包合番茄红素可有效延缓番茄红素的降解损失。袁翠英等[37]制备的番茄红素微乳在自然光条件下处理 100 h 后番茄红素保留率为 95%,优于未包埋的番茄红素;张倩倩[38]研究发现多孔淀粉-番茄红素微胶囊在低温避光环境下 25 d 后其保留率仍达 40%。

注:大写字母不同表示组间具有显著性差异,P<0.05;小写字母不同表示组内具有显著性差异,P<0.05。图1 不同光处理条件下ALCs的番茄红素保留率变化Fig.1 Change in lycopene retention of ALCs under different light treatment conditions
2.3 ALCs 的抗氧化活性变化分析
为研究ALCs的抗氧化活性的稳定性,测定了ALCs和番茄红素标准品在紫外光、自然光和避光条件下的抗氧化活性,结果见图2。
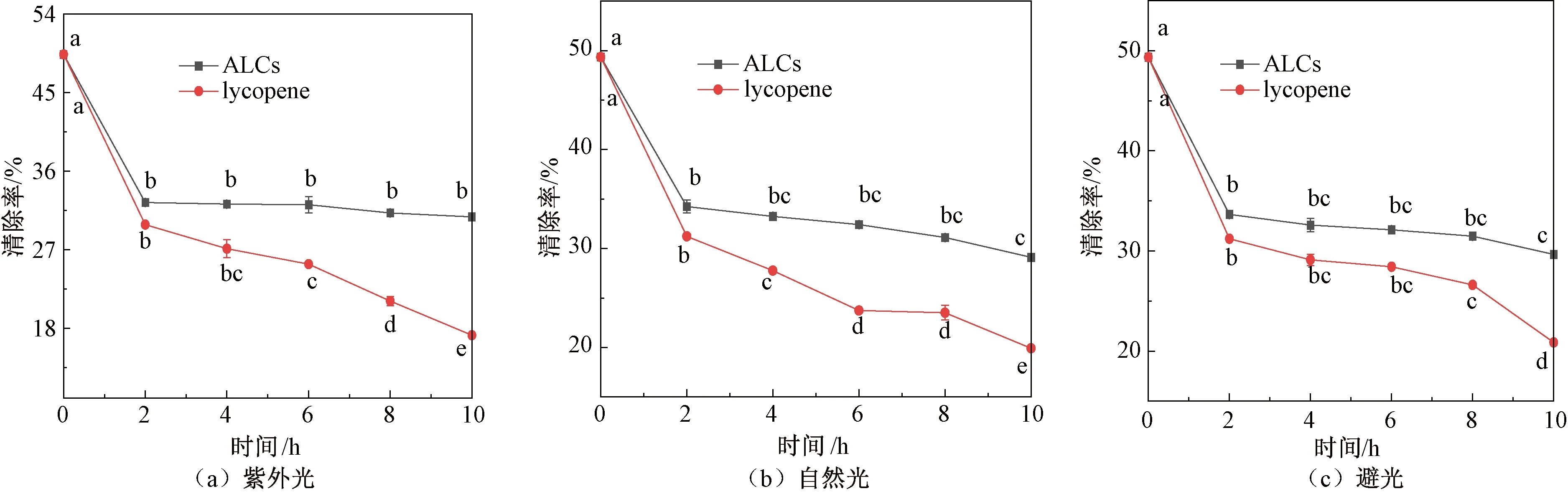
注:小写字母不同表示组内具有显著性差异,P<0.05。图2 不同光条件下ALCs的抗氧化活性Fig.2 Antioxidant properties of ALCs under different light conditions
由图2可知,在3种光条件下,ALCs 和番茄红素标准品的 DPPH 清除率均呈下降趋势,且表现出比对照组强的抗氧化活性。由图 2(a)可知,在紫外光条件下 ALCs 和对照组的 DPPH 清除率从最初的49.35%±0.00%(0 h)分别显著降至 32.75%±0.03% 和 13.92%±0.05%(10 h)(P<0.01)。结果表明,紫外光条件下 ALCs 能更好地保持抗氧化活性。Hajikhani 等[39]研究发现紫外光处理对聚乳酸纳米纤维包裹的番茄红素的抗氧化活性影响较小,与本研究结果相一致。由图 2(b)可知,在自然光条件下 ALCs 和番茄红素标准品的 DPPH 清除率从最初的49.35%±0.00%(0 h)分别显著降至 29.11%±0.32% 和 19.92%±0.09%(10 h)(P<0.01)。结果表明,自然光条件下ALCs能更好保持抗氧化活性。由图 2(c)可知,在避光条件下 ALCs 和番茄红素标准品的 DPPH 清除率从最初的 49.35%±0.00%(0 h)分别显著降至 34.65%±0.05% 和 20.86%±0.13%(10 h)(P<0.01)。结果表明,避光条件下 ALCs 能更好保持抗氧化活性。
综上,紫外光、自然光和避光条件下 ALCs 存在抗氧化活性降低现象,但降低比例不同。在不同光条件下,10 h ALCs的DPPH 清除率分别降低了 33.64%(紫外光)、41.01%(自然光)、29.79%(避光),避光条件下降幅最小。此外,ALCs 的抗氧化活性强于番茄红素标准品。结果表明,自然光对ALCs的抗氧化活性影响最大,直链淀粉与番茄红素复合后,能更好保持其抗氧化活性。制剂化后的 ALCs 可有效保持其抗氧化稳定性,这可能与储藏过程中复合物对番茄红素的保留有关。柴星星等[40]发现番茄红素纳米分散体的抗氧化活性与其番茄红素含量相关;Cefali等[41]比较分析不同品种番茄的抗氧化活性,发现不同品种番茄的番茄红素含量越高,其抗氧化能力越强。究其原因,直链淀粉是淀粉分子中的线性组分,具有特殊的螺旋结构,在施加的外力(热处理、溶剂处理、超高压等)作用下,其分子内氢键相互作用、链状结构旋转,形成了疏水性的左手螺旋空腔结构,这时番茄红素便可借助疏水作用力进入直链淀粉螺旋空腔与其复合[42],进而达到对番茄红素有效的保护作用。本研究发现 ALCs 在3种光条件下保留更高的番茄红素含量,因而具有良好的抗氧化活性。高丽[43]研究发现番茄红素在室内暗处 10 h 后吸光度无显著变化,而在室外日光下的样品吸光度下降为原始的 25%。
2.4 ALCs 中番茄红素的降解动力学分析
依据 1.3.3中方法,根据标准曲线回归方程计算 ALCs 中番茄红素的含量。在紫外光、自然光和避光条件下测定的番茄红素含量见表 1。
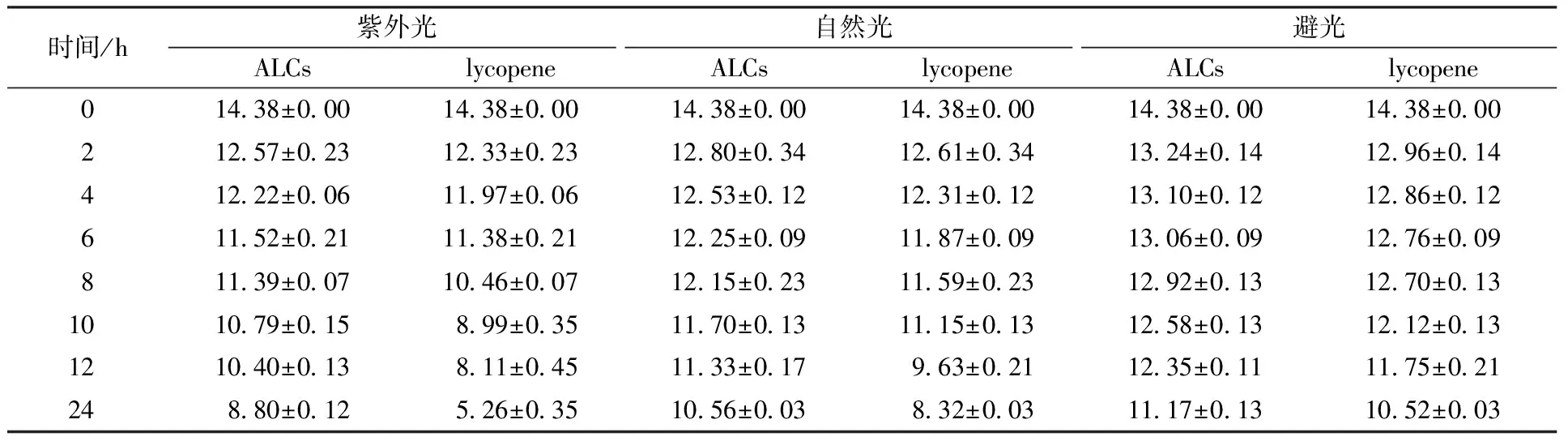
表1 ALCs和番茄红素标准品在紫外光、自然光和避光条件下其番茄红素的含量变化Table 1 Change in the lycopene content of ALCs and lycopene standards under different light treatment conditions μg/mL
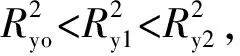
依据方程分别计算得到k、T1/2和T9/10等动力学参数,结果见表2。3种光条件下番茄红素标准品的番茄红素T1/2从小到大的顺序:紫外光(16.66 h)、自然光(33.14 h)、避光(69.55 h),T9/10从小到大的顺序:紫外光(2.53 h)、自然光(5.02 h)、避光(10.54 h),紫外光条件下番茄红素标准品的番茄红素降解更快。不同光处理条件下,与对照组的番茄红素半衰期相比,ALCs 显示出更长的T1/2和T9/10。结果表明,番茄红素与直链淀粉形成复合物后光稳定性增强,且 ALCs 光稳定性顺序:避光>自然光>紫外光。番茄红素的T1/2和T9/10短,是由于其在储藏过程中易分解而不残留[45];与之相比,ALCs 延缓其中番茄红素的降解损失,从而延长衰期。这与 ALCs 是番茄红素与直链淀粉形成的包合型复合物相关。与番茄红素标准品完全暴露在环境中不同,ALCs 中的番茄红素一部分进入了直链淀粉的疏水螺旋空腔,一部分与直链淀粉分子链缠绕形成双螺旋,这种复合结构对其中的番茄红素形成空间保护。光条件下需先降解复合物外的直链淀粉,才能降解番茄红素,因此ALCs 中番茄红素降解较缓慢,制剂化后的 ALCs 具有更良好的储藏稳定性。
3 结论
通过研究直链淀粉-番茄红素复合物的番茄红素含量、保留率、抗氧化活性及其降解动力学变化,发现ALCs 的光稳定性顺序为紫外光<自然光<避光。制剂 ALCs 能有效保护其中的番茄红素。处理 24 h 后3种光条件下 ALCs 中番茄红素保留率均显著高于标准品对照组。制剂 ALCs 能够保持其抗氧化活性。在不同光处理 10 h 后,ALCs 对 DPPH 清除率显著高于对照组。在3种光条件下,ALCs降解行为均符合二级反应动力学模型;相比于另外两种光条件,在避光条件下 ALCs 中番茄红素的半衰期T1/2和十分之一衰期T9/10最大,分别为 99.41 h 和 15.00 h,且显著优于对照组的 69.55 h 和 10.54 h。本研究旨在为番茄红素稳定制剂的开发与应用提供理论支持,拓展番茄红素在医药、食品和化妆品等方面的应用。
