煤炭地下气化制氢技术路径
2023-09-01刘淑琴纪雨彤
刘淑琴,戚 川,纪雨彤,刘 欢,曹 頔
(1.中国矿业大学(北京) 化学与环境工程学院,北京 100083;2.西安石油大学 化学化工学院,陕西 西安 710065)
0 引 言
氢气作为一种清洁绿色的二次零碳能源,是未来国家能源体系的重要组成部分,是用能终端实现绿色低碳转型的重要载体。随国家战略的高度重视及碳达峰、碳中和目标的助力驱动,到2060年,我国年氢气需求量将由当前的3.3×107t增至1.3×108t左右,因此提高氢气供给能力以满足未来能源体系需求极为迫切[1-2]。相对化石能源制氢,以太阳能、风能等作为电力来源电解水制氢为代表的可再生能源制氢路径更为清洁和绿色[3-5],但其在实际应用中仍面临一些挑战,其中最主要的是氢气生产的规模化问题[6-9]。目前,世界氢气产量以化石能源制氢为主,可再生能源来源的氢气产量仅占5%左右[10]。在我国,受资源禀赋条件影响,因地制宜发展煤制氢耦合碳捕集、利用与封存(Carbon Capture, Utilization and Storage,CCUS)技术将成为我国氢能市场发展中、长期的有效供氢主体与补充。煤炭地下气化技术可将地下煤炭原位高效转化为富含氢气的可燃气体,并将煤气中分离的二氧化碳回注气化空腔进行地质封存,该技术有望成为一种有潜力的低成本煤制氢路径。笔者重点解析煤炭地下气化过程富氢气体的生成机理,比较典型煤炭地下气化制氢工程案例,进行不同制氢技术的成本对比分析,分析耦合CCUS的深部煤炭地下气化制氢路径,推动煤炭地下气化制氢的产业化示范与应用。
1 煤炭地下气化富氢气体的生成途径
煤炭地下气化是将地下煤层进行有控制的热作用及化学作用,将其原位转化为以H2、CO、CH4为主要成分的一种特殊的化学工艺过程。现代煤炭地下气化基本单元由注入井和生产井构成,从地面分别向煤层钻进定向钻孔与垂直孔作为注入井与生产井,定向钻孔与垂直孔在煤层底部连通,形成气化通道[11]。根据氧气浓度的分布及化学反应的区别,将气化通道内的反应区域划分为干馏干燥区、还原区和氧化区[12-13]。此外,煤气化产生的可燃气体由气流通道向生产井流动的过程中也会发生部分氧化还原反应。
煤炭地下气化反应过程如图1所示,在气化通道固定区域点燃煤层后,从地面注入的含氧气化剂与通道两侧煤层发生燃烧反应放热,所放出的大量热一部分通过热对流作用沿气化通道轴向扩散,另一部分经热传导与辐射向煤层壁面内传递,该过程温度可达1 000 ℃以上,主要产生CO2和H2O(g)。远端湿润的煤壁受热干燥释放出水分并转化为水蒸气,汽化过程压力膨胀,水蒸气向通道方向扩散;在温度超过350 ℃的煤壁区域内,煤炭发生热解反应,主要产生包含H2、CO、CH4、CO2的热解气;热解气中的水蒸气、CO2与高温半焦发生水蒸气气化反应与二氧化碳气化反应,生成H2和CO[14-17]。热解煤气与气化煤气混后形成产品气体。煤炭地下气化过程中,除了定向钻孔构建的气化通道外,还存在由于热应力或其他压裂手段形成的裂隙通道,使反应面向两侧扩展,煤层得以气化开采。受煤层涌水影响,通道内常存在过量的水蒸气。在气流通道内,当温度超过400 ℃时,产品气中CO会与水蒸气发生水煤气变换反应,进一步生成H2[14-17]。因此,煤炭地下气化过程的氢气直接来源包括煤的热解反应、水蒸气还原反应及气流通道内的水煤气变换反应。
CH4作为煤炭地下气化的富氢气体产品,也是低成本制氢的重要来源。以目前成熟的CH4重整制氢技术路线计算,单位体积CH4可产出2.5倍氢气产品。一般来讲,煤炭地下气化的反应压力随煤层深度而增加,促进了CH4的原位生成,既可以成为低成本非常规天然气的重要补充,也可作为煤炭地下气化制氢的间接来源。
1.1 热解析氢过程
与地面气化不同,煤层内的中低温热解区范围较大,热解气是产品气的重要组成部分。在煤热解过程中,H2生成的温度范围较宽,热解温度达400 ℃左右即开始生成H2,温度升至700 ℃左右时热解析氢量达到最大,温度接近1 000 ℃时H2仍未析出完全[18-19]。低温条件下H2来源于氢化芳香结构脱氢作用[20],高温时则来自脂环族物质缩聚与脱氢作用[19]。
加压条件下的煤层原位热解特性研究表明,随热解压力升高,热解煤气中H2含量逐渐降低,热解压力对产品气组成影响[22]见表1,常压热解煤气中H2体积分数达42%以上,而3 MPa热解工况时,H2含量低于20%[21-22]。反之,CH4含量随热解压力的提高显著提升,热解压力由常压提高至3 MPa,CH4体积分数提升了100%以上。加压抑制了热解气体在煤焦孔道的释放,并阻碍了块煤的热破碎过程[22-23],导致包括H2等挥发分降低,但CH4除来源于煤中甲氧基、长脂肪链等裂解反应外,重要来源还包括半焦中脂肪族碳的加氢等二次反应,加压可促进加氢反应进行,显著提高了热解气中CH4含量。
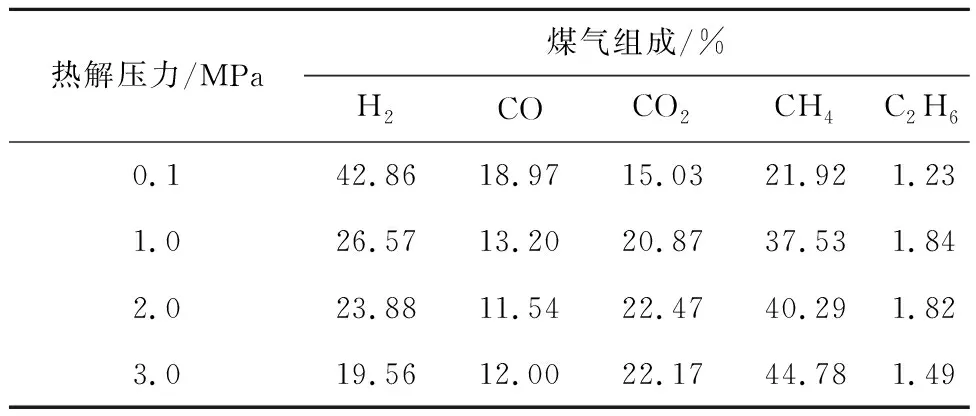
表1 热解压力对产品气组成影响[22]Table 1 Effect of pyrolysis pressure on gas composition[22]
引入催化剂可显著提高热解过程氢气产率。已有地面模拟研究通过引入钙基、铁基、钾基与钠基催化剂,考察煤炭地下气化过程催化热解效果,发现CaO、KNO3与Na2CO3对促进氢气产率提升作用明显,氢气产率可分别提高27%、25%和22%[22,24]。地下气化工艺中可将液态催化剂在煤层预压裂过程引入煤层,或随气化剂注入渗透至煤层内。
1.2 还原析氢过程
煤炭地下气化过程中,还原区主要发生H2O(g)和CO2与炽热煤焦的还原反应,产生大量H2和CO,是有效煤气组分的主要来源。还原区主要反应式如下:
H2O(g)+C→H2+CO-131.5 MJ/kmol,
(1)
2H2O(g)+C→2H2+CO2-90.0 MJ/kmol,
(2)
CO2+C→2CO-162.4 MJ/kmol。
(3)
氧交换机理常用于描述煤焦气化反应过程[25-26]:
H2O(g) + Cf→ H2+ C(O),
(4)
CO2+ Cf→ CO + C(O),
(5)
C(O) → Cf+ CO。
(6)
活性碳位Cf吸附含氧气体(H2O(g)、CO2)形成碳氧复合物C(O),而C(O)则进一步分解形成CO与Cf,如此循环,完成气化反应。对比H2O(g)和CO2反应机理可知,二者C(O)结构相同,合成速率一致,则H2O(g)和CO2的解离成为控制步骤。由于H2O(g)分子氢键弱于CO2分子[27],H2O(g)相对CO2更易解离氧。另一方面H2O(g)可进入孔径≥0.6 nm的半焦微孔发生还原反应,而CO2可进入微孔为1.5 nm以上。许多研究表明,H2O(g)气化活性高于CO2若干倍[27-30]。
对于还原反应来说,温度是导致煤气组分、热值变化的决定因素。地下气化反应过程中,地下水涌入量及注氧浓度决定了反应区的温度。
与地面气化不同的是,由于煤本身含水、煤层地下水涌入及干馏干燥带和氧化带反应产生的水,导致气化过程中水蒸气通常过量。从热力学平衡的角度分析,气化过程提高水蒸气含量进一步促进了水蒸气还原反应正向发生,产生更多氢气,但过量的水蒸气会降低反应区温度,破坏反应条件,同时导致H2与CO含量下降[31-32]。地下气化现场试验也表明,过量的地下水涌入会降低反应区温度,使氢气产量下降[22,32]。现场试验通常通过控制气化压力不大于煤层静水压力,控制涌入气化区及参与反应的水量。总体来看,H2O(g)较高的气化活性及煤层富水特征,导致煤层气化过程中,水蒸气还原反应占主导地位。
气化剂中氧气浓度提高可显著提高地下气化炉内反应区温度,如图2所示,气化剂中氧体积分数为40%~60%时,反应区内最高温度为1 100~1 200 ℃;当氧体积分数提高至80%时,反应区最高温度可达1 200~1 400 ℃。另外,富氧浓度的提高也显著扩展了反应区的边界,有利于生产煤气组成优化和产量的提高。
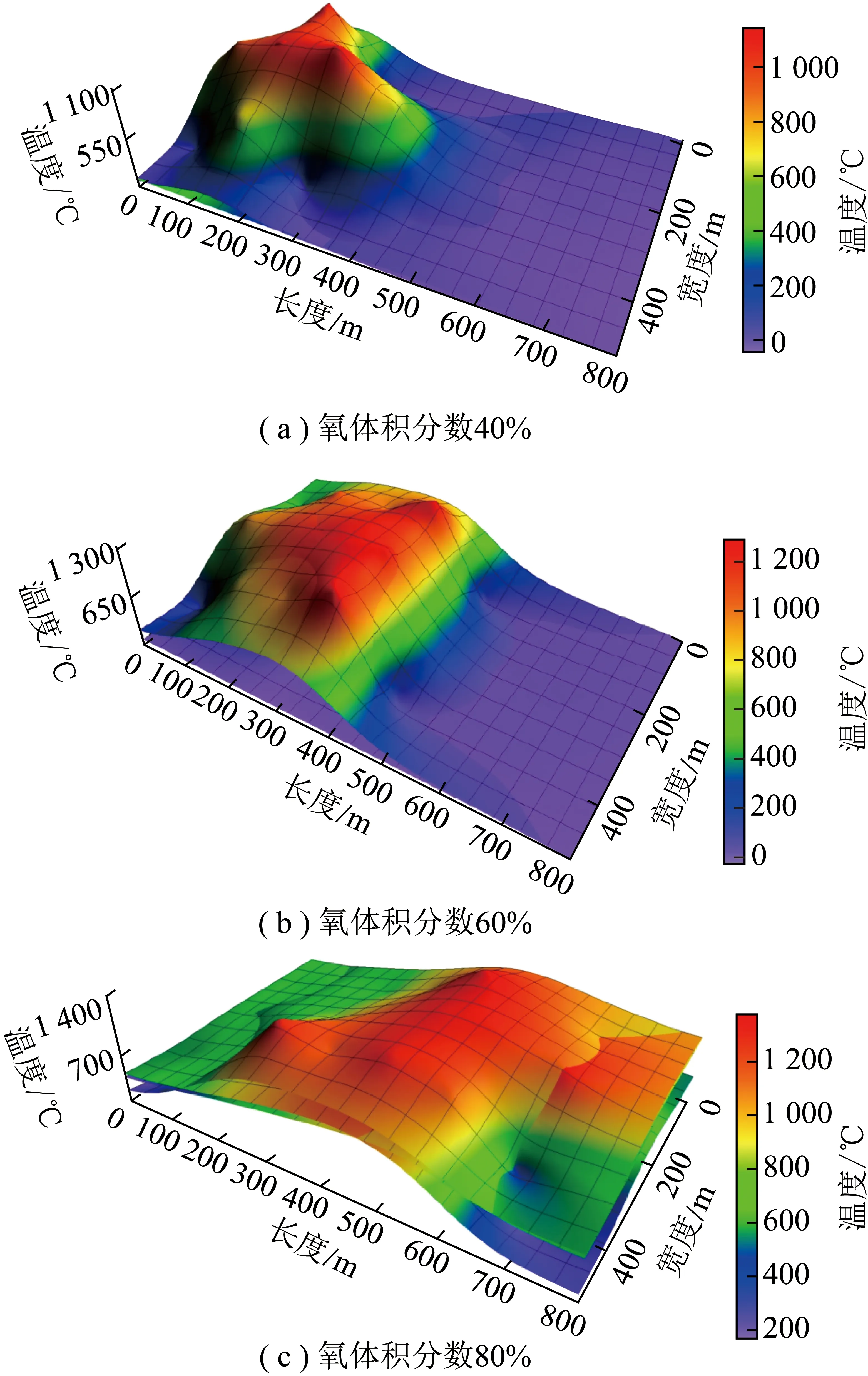
图2 不同富氧浓度条件下地下气化反应炉内温度分布[12]Fig.2 Temperature field distribution under different oxygen-enriched conditions[12]
富氧水蒸气地下气化模拟试验煤气组成随氧体积分数的变化,如图3所示。由图3可知,当富氧浓度由47%不断提高时,煤气中有效组分CO、H2、CH4含量均明显升高。氧气体积分数进一步提高时,有效组分含量有所降低,CO2含量显著提高。与地面气化不同,在一定富氧浓度范围内,通过适当提高氧气浓度来提升反应区温度以及扩展高温影响范围,强化了水蒸气分解反应和CO2还原反应,提高CO、H2含量,同时扩大煤的干馏干燥反应区范围,产生更多的H2、CH4等干馏组分。但过高的氧体积分数会加强煤的燃烧反应及通道中可燃组分的二次燃烧,产生更多CO2,导致局部温度过高,煤中矿物部分熔融而包覆煤焦,阻碍煤焦气化反应[12],煤气有效组分含量下降。
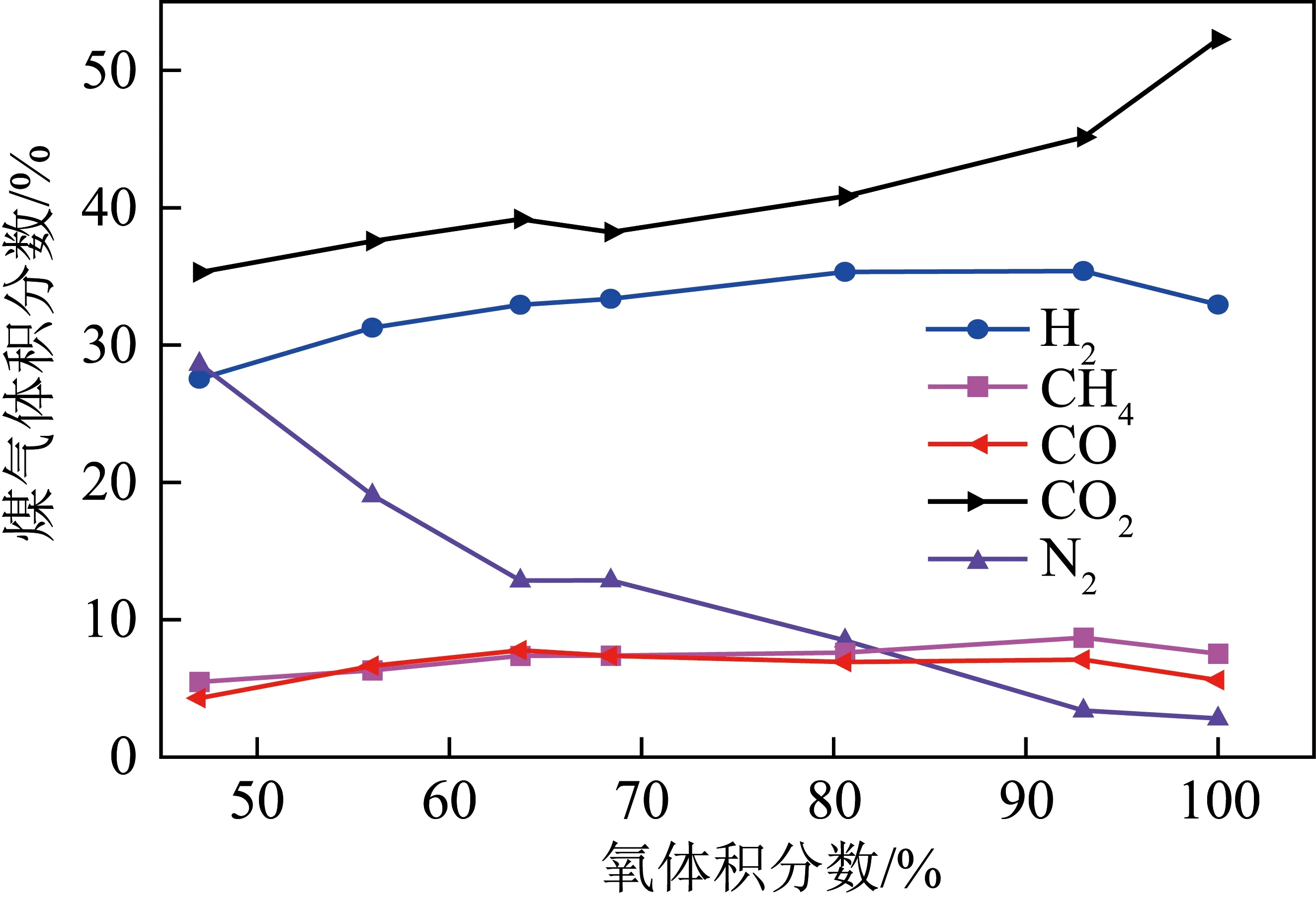
图3 富氧水蒸气地下气化模拟试验煤气组成随氧体积分数的变化Fig.3 Changes of gas composition with oxygen volumn fraction during O2-H2O(g) experiment
此外,半焦加压气化过程中,压力的提高也可以促进氢气与甲烷生成,提高煤气中富氢组分含量[22],见表2。常压气化过程水蒸气还原反应速率最快,CO2还原反应速率较慢,煤焦与H2的反应速率最慢,而加压气化过程中,水蒸气还原反应和CO2还原反应趋于零级反应[33],煤焦与H2的反应速率则显著提高,与前二者反应速率相当。此外,气化压力可促进水煤气变换反应进行,导致H2含量升高。
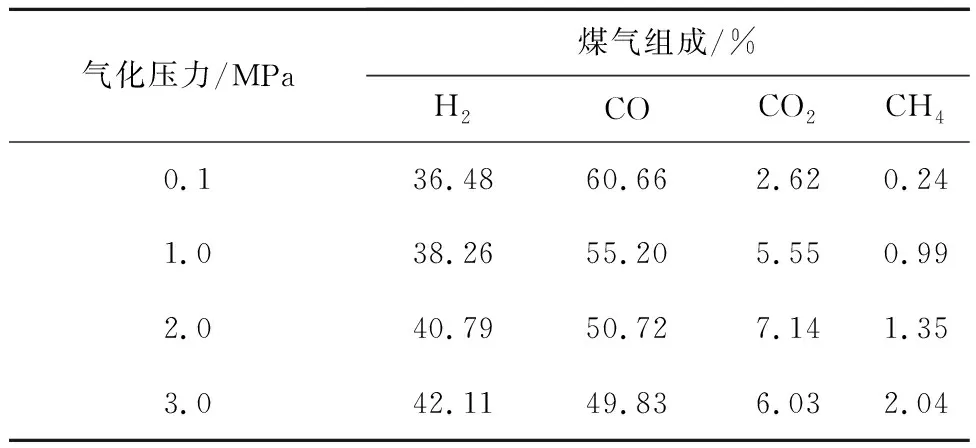
表2 压力对半焦气化煤气组成的影响[22]Table 2 Effect of pressure on gas composition during coal char gasification[22]
1.3 气化通道低温区的水煤气变换反应
热解与还原过程中生成的CO可与水蒸气进一步发生水煤气变换反应:
H2O(g)+CO→H2+CO2+42.3 MJ/kmol。
(7)
该反应在温度高于400 ℃时即可发生,当温度高于900 ℃时,其反应速率接近水蒸气分解反应速率[14]。由于水煤气变换为放热反应,较低的温度有利于提高氢气转化率,而较高的温度有利于提高反应速率。
此外,金属氧化物对水煤气变换反应具有催化作用,可使反应在更低温度发生并提高氢气转化率。地面蒸汽重整生产过程中,首先采用Fe2O3为主要成分的催化剂,操作温度在350~500 ℃,操作压力2~3 MPa条件下,将CO体积分数由10%~13%降至2%~3%;再采用Al2O3等催化剂,在操作温度200~250 ℃,操作压力1~3 MPa条件下,进一步将CO体积分数降至0.2%以下。
在煤炭地下气化过程中,气化完成后的煤灰渣存留于气化通道内。而气化灰渣富含Al2O3、CaO、MgO、Fe2O3、Fe3O4等氧化物[12,34]。500 ℃时金属氧化物对水煤气变换反应CO转化率的影响[32]见表3,煤气化灰渣中主要氧化物对水煤气变换反应具有较显著的催化效果。
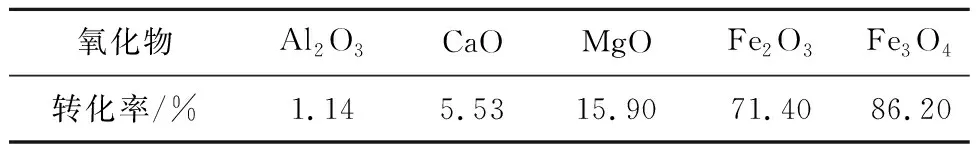
表3 温度500 ℃时金属氧化物对水煤气变换反应CO转化率的影响[32]Table 3 Effect of metal oxides on CO conversion rate during water-gas shift reaction at 500 ℃[32]
因此,在煤层气化过程,气化通道长度足够,且存留的气化灰渣具有显著催化效果,水煤气变换反应在气化通道内理论上具备达到热力学平衡的条件。
2 煤炭地下气化工程产氢数据分析
煤炭地下气化技术历经百余年的发展,理论与技术不断创新,控制手段及控制装备不断升级。以可控后退注气点工艺(Controlled Retracting Injection Point,以下简称CRIP)为基础,集成先进的煤层定向钻井/完井等技术及远程多介质注入装备的现代煤炭地下气化技术逐步形成[11]。受环境影响及碳排放制约,煤炭地下气化技术总体发展趋势呈现由矿井式向钻井式、由浅部煤层向深部煤层、由单一发电利用向综合利用的特征[35]。
基于矿井式气化的煤炭地下气化制氢早在20世纪90年代被提出[16-17,36]。在徐州新河2号井浅部煤炭地下气化试验中,采用2阶段工艺进行了富氢煤气生产试验。第1阶段鼓入空气生产空气煤气,同时在煤层中创造高温温度场,第2阶段鼓入水蒸气,进行水煤气反应,生产的富氢煤气中氢气体积分数高达70%(图4)[17,36]。通过煤气中H2及CO含量确定2阶段的切换时间。2阶段地下气化制氢的局限性在于水蒸气的输送距离过长,导致水蒸气温度低,还原率下降,最终富氢煤气产量比较低,不利用实现工业化应用。
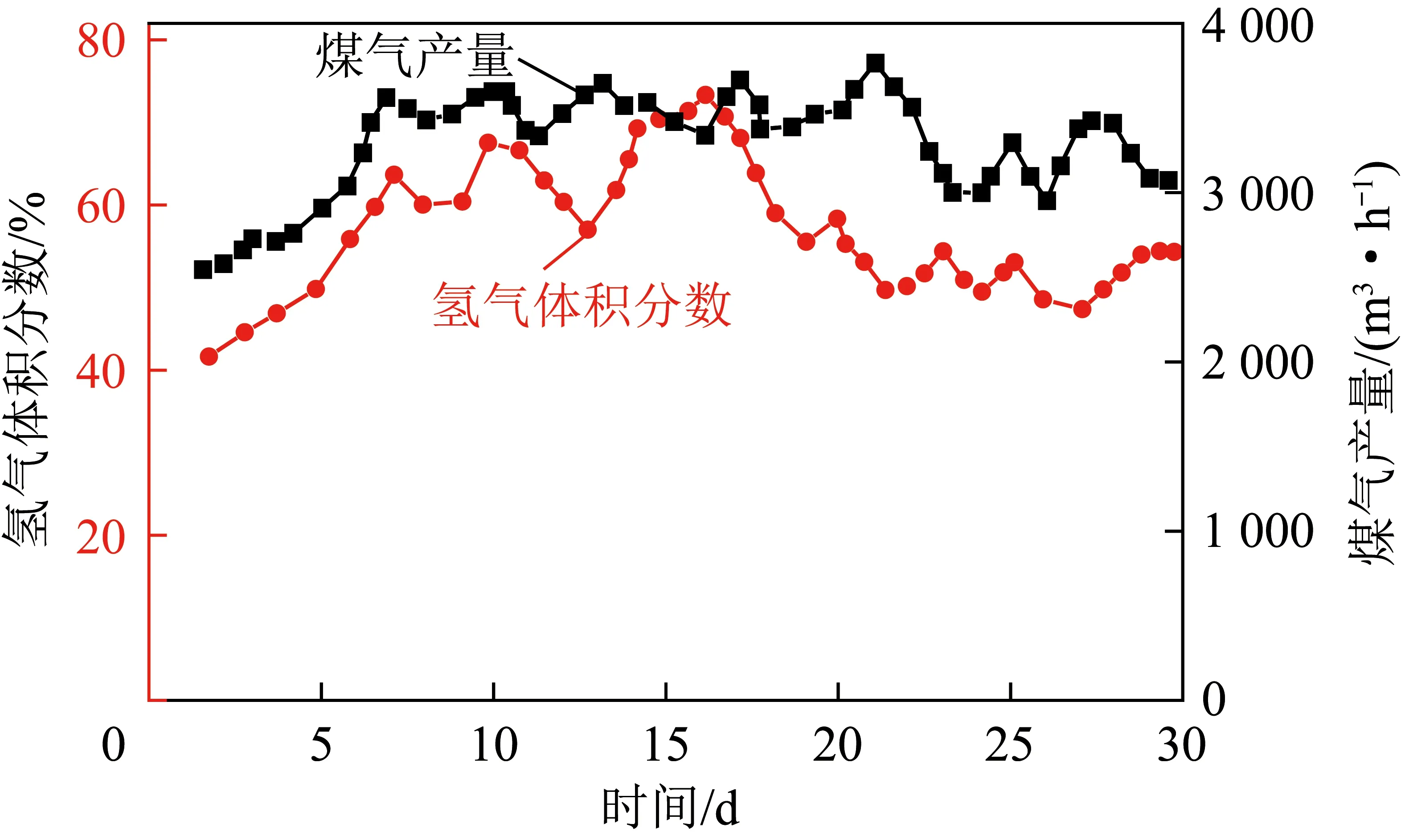
图4 徐州新河2号井煤炭地下气化现场试验煤气中氢气含量Fig.4 Hydrogen content in UCG gas at No. 2 well, Xinhe, Xuzhou
2006—2016年,中国矿业大学(北京)与新奥气化采煤有限公司联合开展了乌兰察布现代煤炭地下气化试验。煤层埋深285 m,厚度12 m左右,煤种为褐煤。以空气为气化剂的气化稳定运行时间达6个月以上,煤气产量达20万m3/d。采用氧气-二氧化碳为气化剂,气化压力1.5 MPa,连续稳定运行3个月,煤气产量达10万m3/d,有效气组分体积分数≥50%,煤气流量和组分波动范围低于20%。乌兰察布地下气化项目开创了我国现代煤炭地下气化技术的先河。
空气气化和富氧气化的平均煤气组成如图5所示,可知空气煤气中H2体积分数平均达36%,成本0.11元/m3,富氧煤气中H2体积分数平均达30%,CH4体积分数达10%,折合氢气体积分数达到65%,成本0.25元/m3,为低成本规模化煤炭地下气化制氢奠定了基础。
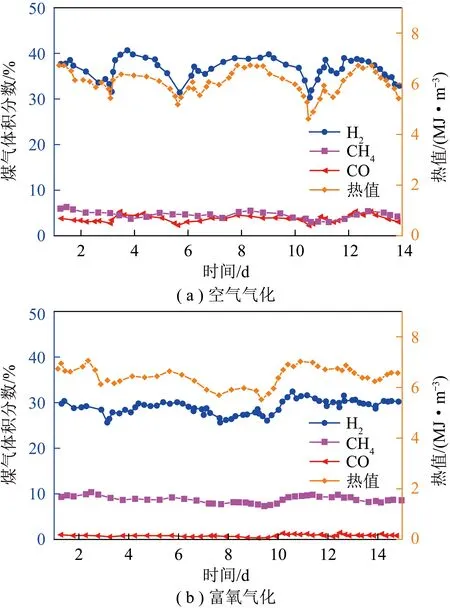
图5 空气气化和富氧气化UCG煤气组成Fig.5 Air gasification and oxggen eriched UCG gas composition
现场试验过程通过在气化通道一侧建立监测钻孔(图6),进行温度、压力与煤气组分采集,充分验证了在气化通道中存在显著的水煤气变换反应。监测数据显示,在注气点附近高温还原反应良好,CO体积分数可达30%以上,在气化通道中的水煤气变换反应导致最终出口煤气CO体积分数降至5%以下,CO变换率高达70%。变换反应的反应程度受到通道长度、温度、压力、煤中金属元素种类等多种因素的影响。
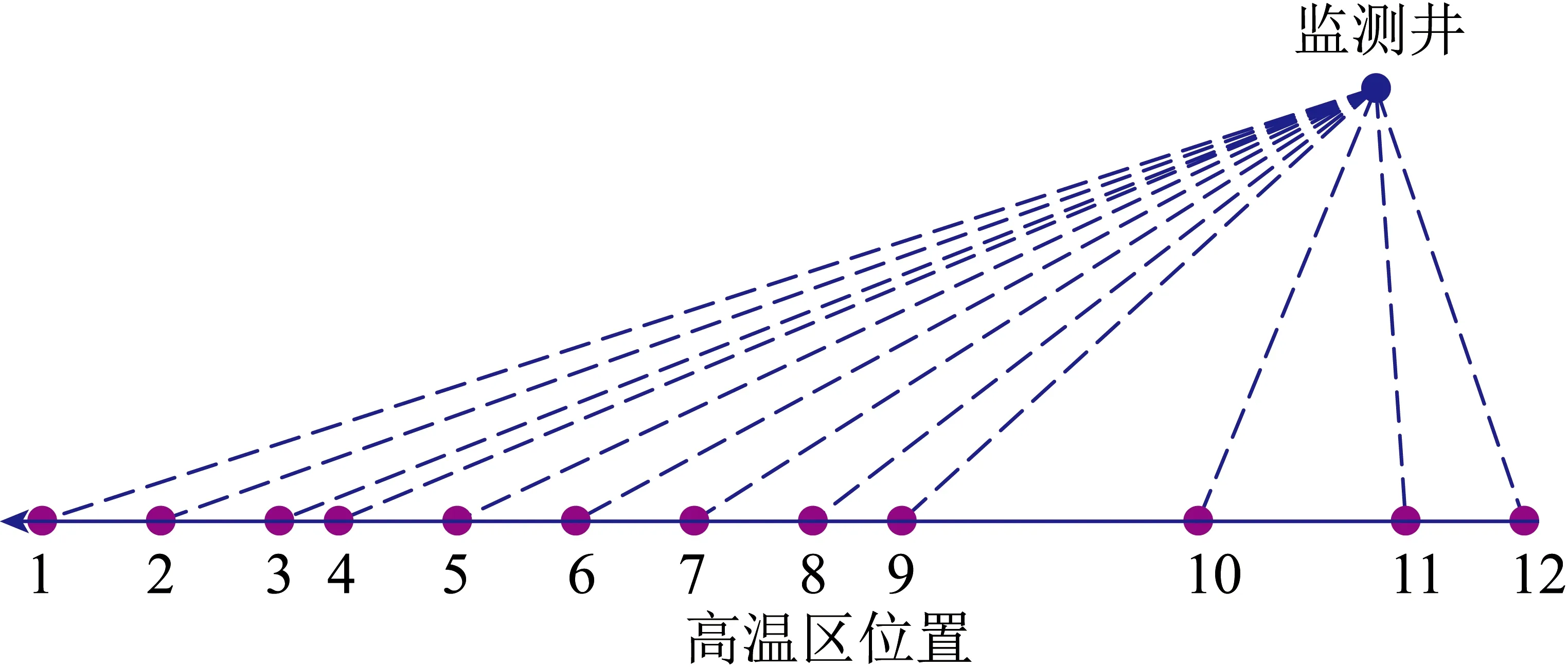
图6 煤炭地下气化试验监测示意Fig.6 Schematic diagram of monitoring during underground coal gasification experiment
国外的典型煤炭地下气化工程试验数据见表4。美国洛基山1号(Rocky Mountain 1)试验项目,煤层埋深110 m。试验过程中,开展了氧气-水蒸气气化试验,持续稳定气化时间93 d,煤气热值达9.5 MJ/m3。其中,产品煤气中H2体积分数平均达39%,CH4体积分数约10%,折合H2体积分数可达56%以上。澳大利亚钦奇拉(Chinchilla)项目,煤层埋深125~136 m,煤层厚度4~6 m,煤种为次烟煤。项目开展了12个后退周期试验,合计气化33 300 t煤,产出合成气4 800万m3,试验包括空气、富氧以及纯氧等不同气化剂。其中纯氧气化煤气中H2体积分数高达42.5%,CH4体积分数11.5%,折合H2体积分数63%以上。氧气浓度显著强化了水蒸气分解反应,提高了H2产量。20世纪80年代以来,欧洲致力于中深部煤炭地下气化技术研发,并将煤炭地下气化与制氢、氢燃料电池以及CCS等现代产业结合。西班牙埃尔特鲁埃尔(El Tremedal)试验项目,煤层埋深580 m左右,煤层厚度2~5 m,煤层水平通道长度100 m,气化压力5.3 MPa,气化剂为氧气。
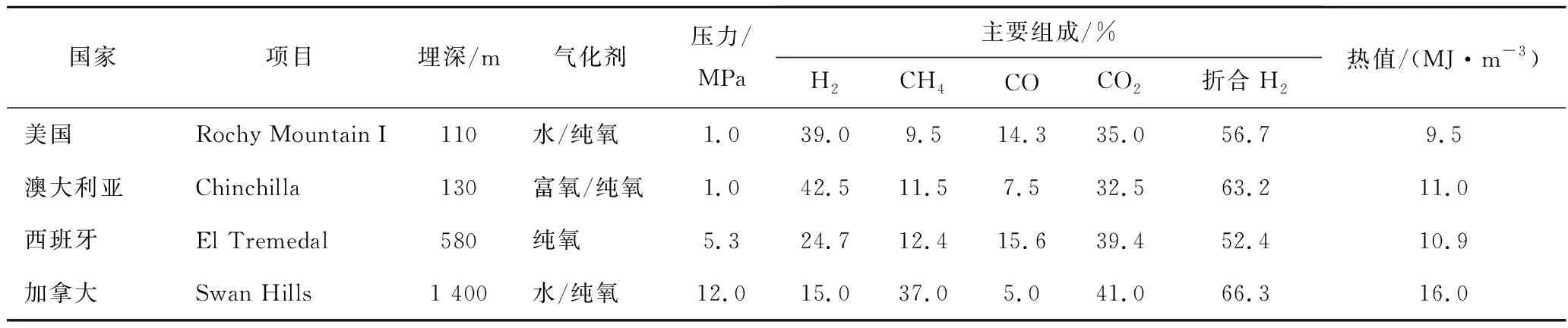
表4 国外典型煤炭地下气化工程案例产氢数据分析[35]Table 4 Enriched hydrogen gas production data from typical foreign UCG projects[35]
生产煤气中CH4体积分数平均为12.7%,H2体积分数接近25%,折合H2体积分数可达60%以上。加拿大天鹅山试验项目煤层埋深1 400 m,厚度7~8 m,煤层水平段长度1 400 m。气化压力达10~12.5 MPa,煤气中CH4体积分数高达37%,H2体积分数为15%,折合氢气体积分数达66%以上。气化压力的提高显著促进含氢气体CH4生成。
国内外典型煤炭地下气化运行数据表明,地下煤层的富水特征使煤炭地下气化天然具有生产富氢气体的优势,典型工程项目的实施,为低成本规模化煤炭地下气化制氢奠定了良好的工业基础。
3 不同制氢路径成本对比分析
目前,我国氢气的制取产业较为成熟的技术路线有煤炭、天然气等化石能源重整制氢,焦炉煤气、氯碱尾气、丙烷脱氢等工业副产制氢,以及电解水制氢[1]。我国较为成熟的制氢技术路线成本对比如图7所示。
地面煤气化制氢技术发展成熟,氢气制取成本较低。制氢成本主要受原料煤价格影响,原料煤消耗占地面煤制氢成本50%左右。以成本较低的煤气化技术为例,产能为54万m3/h合成气的装置,在原料煤(25 104 kJ(6 000 kcal),含碳量80%以上)价格800元/t情况下,制氢成本约0.85元/m3。
天然气制氢技术中,以蒸汽重整制氢较成熟,欧美等国主要采用该技术制氢。制氢成本重要因素是天然气价格,天然气原料消耗占制氢成本70%以上。以工业天然气成本3元/m3为例,天然气制氢成本约1.02元/m3。但受我国资源禀赋影响,不适宜大部分地区开展。
钢铁、化工等行业分布有大量工业副产氢气,结合提纯技术可制取满足燃料电池应用的氢气。焦炭生产过程中,每吨焦炭可产生190~265 m3氢气。我国烧碱生产过程中每年副产氢气75.0万~87.5万t。合成氨生产过程中每年可回收驰放气中氢气100万t/a。综合考虑副产气成本以及提纯成本,工业副产氢气制氢成本在0.89~1.43元/m3。
电解水制氢具有绿色环保、氢气纯度高等特点。制氢技术中以碱性电解槽技术最为成熟,生产成本相对较低,国内单台最大产氢量为1 000 m3/h。电解水制氢单位电耗4~5 kWh/m3,成本主要受电价影响,电价占总成本70%以上。如采用市售电价生产,制氢成本2.68~3.57元/m3。在国家及地方产业政策支持,采用“谷电”价格约0.3元/kWh,制氢成本约1.96元/m3。
以年产1 600万m3氢气煤炭地下气化制氢项目为例,结合地面CO变换以及甲烷裂解,吨煤可产氢气约900 m3,综合制氢成本约0.52元/m3。地下气化省去建井、采煤以及地面建炉气化等工艺,原料煤价格主要由煤矿资源价款影响,不受市场原料煤价格波动影响,因此制氢成本相对地面煤制氢以及天然气制氢等化石能源制氢技术更具有经济效益优势。
4 耦合CCUS技术的深部煤炭地下气化制氢路径
化石能源制氢具有成本低、技术成熟等优势,但面临制取环节的碳排放问题,耦合CCUS技术有望实现化石能源大规模低碳制氢,成为我国碳减排、能源安全保障以及可持续发展的重要手段。但当前我国CCUS技术仍处于探索阶段,能耗较高,二氧化碳的利用渠道较窄。国内目前CCUS成本350~400元/t,如结合CCUS,地面煤制氢成本提高0.63元/m3左右。耦合CCUS显著降低了地面煤制氢的成本优势。而深部煤炭地下气化工艺与CCUS技术天然地耦合,可形成低成本碳封存和资源化利用技术路线。
深部煤炭地下气化技术可采用纯氧-二氧化碳作为气化剂,循环利用二氧化碳,既可提高气化剂鼓入流量和流速,改善气化剂流动性,促进气化通道气固反应发生,又可强化CO2还原反应,有利于提高煤气有效组分产量。更重要地,研究表明适宜开展深部煤炭地下气化的选址区域通常也满足二氧化碳封存的地质条件,分离捕集的CO2可在气化后形成的地下空腔就地封存[37-39],天然具有与CCUS耦合的优势。特别是深部煤层气化空腔,不仅可在超临界状态下物理封存CO2,还可与气化灰渣发生矿化作用,研究表明,45 ℃、0.1~1.5 MPa条件下,每吨灰渣具备200 kg左右CO2封存能力[40],有效提升了地下空腔的封存能力;另一方面,在煤炭地下气化项目,地面空分单元在产出氧气作为气化剂外,产生大量高纯氮气,结合CO2合成化学品,实现CO2资源化利用;此外,CO2可用于临近油田CO2驱油提高原油采收率(Enhanced Oil Recovery,EOR)或用于驱替煤层气(Enhanced Coalbed Methane Recovery,ECBM),同时实现地质封存。煤炭地下气化的技术特点使其可结合多种碳减排方式,形成低成本的碳封存与利用技术路线。
以年产12亿m3氢气的深部煤炭地下气化项目为例(图8)[2],需以废气形式排放的CO2量约为90万t/a。项目实施过程所形成的气化空腔,CO2封存容量占项目全生命周期内总排放量的61.8%。气化过程中,以纯氧-二氧化碳作为气化剂,循环利用CO2,提高煤气有效组分收率,O2来源于空分装置制备,副产纯度≥99.9% N2。一部分N2用于酸性气体脱除外,剩余N2可与H2合成氨,再进一步与捕集分离的CO2反应生产尿素,将项目排放CO2全部消纳,形成零排放的深部煤炭地下气化制氢技术路线。
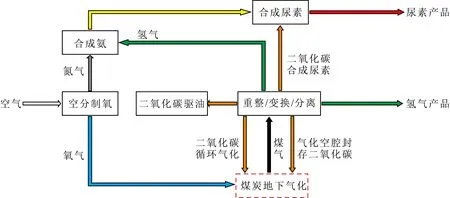
图8 深部煤炭地下气化制氢耦合CCUS与尿素联产技术路线Fig.8 Technological route for deep UCG hydrogen production coupled with CCUS and urea co-production
结合EOR为例,经核算,CO2捕集成本约50元/t,考虑200 km以内管道运输成本,CO2到达油气井口总成本低于100元/t[41]。国内CO2驱油项目中平均注入3 t CO2可增产1 t原油。年产12亿m3氢气深部煤炭地下气化制氢项目除气化空腔封存的CO2外,剩余CO2可支撑年产11万t的驱油项目。
深部煤炭地下气化制氢与气化空腔封存CO2结合,并联产化学品或协同驱油/驱替煤层气路线,既可规模化制取低成本氢气,又可实现二氧化碳零排放与资源化利用,对解决化石能源制氢碳排放难题以及发挥新型能源体系支柱作用具有重要意义,是符合中国国情、具有中国特色的化石能源清洁转型发展之路。因此,应加强煤炭企业与油气企业合作研发,加强技术攻关和示范项目建设,支撑新型能源体系发展。
5 结 语
1)解析了氢气析出途径。煤炭地下气化过程的富氢气体直接来源包括煤的热解反应、水蒸气还原反应以及气流通道内的水煤气变换反应。热解反应过程,主要产生富氢气体H2与CH4,特别是在深部煤层气化时,加压可显著提高富氢气体CH4含量;由于煤本身含水、地下水涌入及干馏干燥带和氧化带反应产生的水,导致地下煤层具有富水特征。H2O(g)相对CO2更易解离出氧及H2O(g)可进入更小煤焦微孔的优势使H2O(g)气化活性显著高于CO2。煤层富水特征和H2O(g)高气化活性使还原区以水蒸气还原反应为主导;而煤炭地下气化长气流通道以及气化灰渣催化作用进一步促进了水煤气变换反应。上述特征使煤炭地下气化天然具有产出富氢气体优势。
2)国内外典型煤炭地下气化试验运行数据表明,地下煤层的富水特征使煤炭地下气化天然具有生产富氢气体氢气和甲烷的优势,典型工程试验项目的实施为低成本规模化煤炭地下气化制氢奠定了良好的工业化放大基础。煤炭地下气化可产出折合氢气含量50%以上的煤气,而氢气含量与煤层条件、气化剂注入量、气化压力等密切相关。
3)地下气化省去建井、采煤以及地面建炉气化等工艺,原料煤价格主要由煤矿资源价款影响,不受市场原料煤价格波动影响,因此制氢成本具有显著得经济优势。煤炭地下气化制氢成本约0.52元/m3,远低于地面煤制氢和天然气制氢成本。
4)化石能源制氢面临制取环节的碳排放问题,深部煤炭地下气化工艺与CCUS技术天然耦合,可形成低成本碳封存和资源化利用技术路线。深部煤炭地下气化制氢与气化空腔封存CO2结合,并联产化学品或协同驱油/驱替煤层气路线,可规模化制取低成本氢气,又实现了二氧化碳近零排放与资源化利用,对解决化石能源制氢碳排放难题及发挥新型能源体系支柱作用具有重要意义,是符合中国国情、具有中国特色的化石能源清洁转型发展之路。
