牛大力提取物对小鼠的急性毒性与遗传毒性研究
2023-08-30赵羽洁陈美芬张紫虹黄金文黄俊明李冬利
赵羽洁,陈美芬,李 欣,张紫虹,黄金文,黄俊明,张 焜,李冬利*
(1. 五邑大学生物科技与大健康学院,广东 江门 529000;2. 广东省疾病预防控制中心, 广东 广州 510000)
牛大力为豆科崖豆藤属美丽崖豆藤Millettia specisoa的根,主要分布于广东、广西、海南等长江流域以南地区,可供药用,具有补虚润肺、强筋活络等功效[1]。此外,牛大力还具有广泛的药理活性,包括免疫调节[2]、抗疲劳[3]、抗氧化[4]等。近年来,牛大力深受大众追捧和热爱,可用作煲汤制药的原料,市场需求不断增加。根据《卫生部关于进一步规范保健食品原料管理的通知》(卫法监发[2002]51号)要求,牛大力并不在既是食品又是药品的物品名单及可用于保健食品的物品名单中。国家卫计委2018 年6 月对“牛大力粉”申报新食品原料给出的审查结论为“鉴于该产品具有地方传统食用习惯,建议按照《食品安全法》第29 条管理,终止审查”,即对牛大力有传统食用习惯的省份可通过制定食品安全地方标准进行管理。但目前对于牛大力毒性研究还不够系统[1,5]。因此,作者项目团队在对牛大力进行全面的食品安全性毒理学评价基础上牵头制定了《广东省食品安全地方标准——牛大力干制品》(DBS 44/016-2021),为广东省牛大力作为食品开发和应用奠定基础。本文主要报道基于食品安全国家标准[6—10],牛大力提取物的小鼠急性经口毒性试验、细菌回复突变试验、哺乳动物红细胞微核试验及体外哺乳类细胞染色体畸变试验结果。
1 材料与方法
1.1 试验药物
采集广东江门市恩平良西镇种植的牛大力植物新鲜根,洗净切成约1 cm 小段,晒干或烘干。按以下方法提取:①加入10 倍体积的50%乙醇煮沸回流提取2 h,过滤;②滤渣再以同样方法提取,过滤;③滤渣用10 倍体积水再次煮沸回流提取2 h,过滤得滤液和滤渣;④将三次滤液合并,浓缩至可流动的浸膏,尽量减小体积,得到牛大力提取物浓缩液样品。
700 kg 牛大力干品经提取浓缩得到提取物浓缩液57.0 L,重量72.0 kg,提取物得率10.3%,密度为1.26 g·mL–1,浓缩比例为12.3 g (药材) ·mL–1。
拟定牛大力干品的人体推荐每日服用量为15 g,以成人体重60 kg 计,推荐量为0.25 g·kg–1BW,按牛大力(提取物浓缩液)得率10.3%折算,则牛大力(提取物浓缩液)每日推荐量为0.02575 g·kg–1BW,以下各试验均采用牛大力(提取物浓缩液)进行。
1.2 供试动物
广东省医学实验动物中心提供的昆明种SPF 级健康小白鼠,生产许可证号:SCXK(粤)2018-0002;颗粒饲料由广东省医学实验动物中心提供,使用许可证号:SYXK(粤)2018-0011;动物实验室为屏障环境,室温20~26 ℃,相对湿度40%~70%。
1.3 方法
1.3.1 小鼠急性经口毒性试验
采用限量法[11],选用体重18~22 g 健康昆明种小白鼠20 只(质量合格证编号:44007200080668),雌雄各半,禁食不禁水4 h 后,空腹灌胃1 次,灌胃剂量为0.3 mL·10 g–1BW,观察14 d,记录小鼠的增重量及死亡情况。
1.3.2 细菌回复突变试验
采用符合要求的TA97a、TA98、TA100、TA102、TA1535等5种组氨酸营养缺陷型鼠伤寒沙门氏菌突变型菌株,在加及不加代谢活化系统S9 条件下采用平板掺入法进行试验[11]。设牛大力(提取物浓缩液)最高剂量为每皿5000 μg,按5 倍间隔,共设五个剂量组,分别为每皿5000、1000、200、40、8 μg,以上五组受试液经过20 min、121 ℃、0.103 MPa 高压灭菌后使用。另设各类阳性对照组、蒸馏水对照组、二甲亚砜对照组和未处理对照组。阳性对照物分别为NaN3、2-AF、丝裂霉素C、1,8-二羟蒽醌、2-AA和敌克松。在顶层培养基中加入0.10 mL 试验菌株增菌液,0.10 mL 受试物溶液和0.50 mL S9 混合液(当代谢活化时加入),混匀后倒入底层培养基平板上,每一剂量组均为3 个平皿。置于37 ℃下培养48 h,记录每个平皿回变菌落数,计算各试验组3个平皿回变菌落数的均数和标准差。如在背景生长良好的条件下,测试菌株TA98、TA1535 的回变菌落数等于或大于未处理对照组的2 倍,测试菌株TA97a、TA100、TA102 的回变菌落数等于或大于未处理对照组的2 倍,并具有以下a、b 两种情况之一的可判定为阳性结果:a 为有剂量-反应关系;b 为某一测试点有可重复的阳性结果。
1.3.3 小鼠骨髓嗜多染红细胞微核试验
选择昆明种小鼠 50 只(质量合格证编号:44007200082167),体重25~35 g,随机分为5 组,每组10 只,雌雄各半。设10.0、5.0、2.5 g·kg–1BW三个剂量组,另设阴性对照组(超纯水)和阳性对照组(40 mg·kg–1BW 环磷酰胺)。采用30 h 给受试物法进行试验,经口灌胃,灌胃剂量0.2 mL·10 g–1BW,第一次灌胃24 h 后以同样剂量进行第二次灌胃,6 h后处死小鼠,取胸骨骨髓材料制片、染色,每只小鼠观察2000 个嗜多染红细胞(PCE),计数含有微核的嗜多染红细胞数;若一个嗜多染红细胞中出现两个或两个以上微核,仍按一个有微核细胞计数,计算各组含微核细胞率(‰)。同时记录观察200 个红细胞(RBC)中嗜多染红细胞数(PCE),计算PCE/RBC比值。
1.3.4 体外哺乳类细胞染色体畸变试验
根据受试物对细胞的毒性及其溶解度,确定受试物最高剂量为2500 μg·mL–1,称取牛大力(提取物浓缩液) 2.5 g,加PBS 至100.0 mL,混合均匀,以此为基础用PBS 依次作2 倍稀释得一系列相应剂量的染毒液(2500、1250、625 μg·mL–1),于121 ℃,0.103 MPa 高压灭菌20 min 后使用,另设阴性对照组(PBS)、阳性对照组(15 μg·mL–1环磷酰胺、0.5 μg·mL–1丝裂霉素C)。将中国仓鼠肺细胞(CHL)接种于六孔培养板中,接种密度5×105个·孔–1,置于37℃、5% CO2培养箱中培养24 h 后,吸去培养板中的培养液,加入不同浓度受试物溶液、S9 混合液(不加S9 混合液时,需用培养液补足)以及一定量不含血清的培养液,置培养箱中染毒4 h 后用PBS 洗细胞,加入含10%胎牛血清培养液,继续培养24 h收获细胞,收获前4 h 加入秋水仙素(终浓度为1.0 μg·mL–1)。按常规方法消化、低渗、固定、制片、Giemsa 染色,在油镜下阅片观察。每处理分别选取100 个分散良好的中期分裂相细胞,分析染色体结构和数目改变情况,并计算染色体畸变细胞率。
1.4 数据统计
采用SPSS 16. 0 统计软件分析数据。微核发生率以含微核PCE 千分率计,均按泊松分布进行统计分析;计量数据以平均数±标准差表示,采用单因素方差分析对多个试验组与对照组之间均数进行比较;其余计数资料采用卡方检验。
2 结果与分析
2.1 急性毒性分析
受试样品牛大力(提取物浓缩液) 20.0 g·kg–1BW剂量组未观察到动物出现中毒反应和死亡,因此雌雄性小鼠LD50>20.0 g·kg–1BW,相当于受试物人体推荐每日服用量的777 倍(表1)。
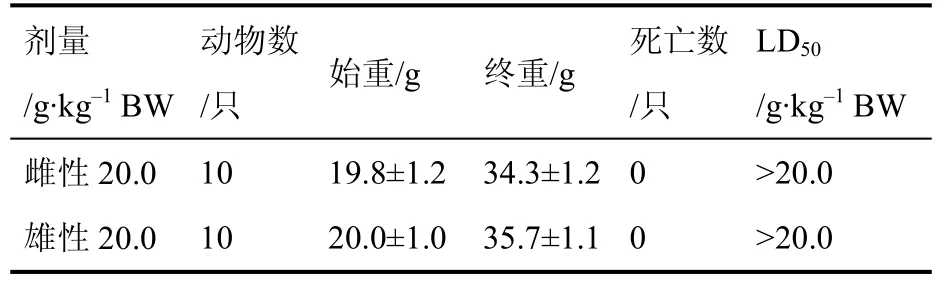
表1 小鼠急性经口毒性试验结果Table 1 Results of acute oral toxicity test in mice
按照《保健食品安全性毒理学评价程序和检验方法规范》中的剂量分级规定,受试样品牛大力(提取物浓缩液)属实际无毒级物质。
2.2 细菌回复突变结果
受试样品牛大力(提取物浓缩液)对鼠伤寒沙门氏菌TA97a、TA98、TA100、TA102、TA1535 等5种试验菌株的细菌回复突变结果显示,加或不加S9,五个剂量组处理的不同菌株回变菌落数均未超过未处理对照组的2 倍,亦无剂量-反应关系或可重复的并有统计学意义的阳性反应测试点(表2、表3)。因此,在该试验条件下,受试样品牛大力(提取物浓缩液)的细菌回复突变试验结果为阴性。
表2 第一次细菌回复突变试验结果( ± s)Table 2 Results of the first bacterial reverse mutation test ( ± s)

表2 第一次细菌回复突变试验结果( ± s)Table 2 Results of the first bacterial reverse mutation test ( ± s)
注:“–”表示未加S9,“+”表示加S9,表3、表6 同。
TA97a TA98 TA100 TA102 TA1535受试物 剂量/μg·皿–1 – + – + – + – + – +1 5000 137±5 145±4 45±3 47±3 167±5 175±7 399±14 467±12 21±2 23±2 2 1000 133±7 140±4 44±4 45±2 162±5 166±6 381±7 436±17 20±4 23±3 3 200 125±5 136±5 39±5 42±2 146±10 168±6 361±14 411±14 21±3 21±2 4 40 126±7 122±3 39±2 38±2 144±7 141±6 353±8 385±11 18±2 19±2样品组5 8 120±6 116±3 35±2 43±3 136±6 142±9 331±21 359±7 16±2 18±1未处理对照 108±5 110±6 36±4 39±3 127±5 138±7 278±13 297±14 15±3 17±5蒸馏水对照 112±7 115±6 38±3 41±2 127±7 140±6 282±11 301±12 13±3 18±4二甲基亚砜 96±5 117±3 40±2 40±3 128±7 130±5 291±20 296±15 14±2 13±3阳性物对照NaN3 1.5 1341±133 1815±123 2-AF 10.0 1646±79 1638±124 1733±106敌克松 50.0 2374±150 1245±100丝裂霉素 4.0 2083±166 1,8-二羟蒽醌 50.0 1235±151 2-AA 10.0 1231±95
表3 第二次细菌回复突变试验结果( ± s)Table 3 Results of the second bacterial reverse mutation test ( ± s)

表3 第二次细菌回复突变试验结果( ± s)Table 3 Results of the second bacterial reverse mutation test ( ± s)
TA97a TA98 TA100 TA102 TA1535受试物 剂量/μg·皿–1 – + – + – + – + – +1 5000 147±7 149±7 44±2 46±3 165±7 177±9 370±7 440±16 20±3 24±2 2 1000 137±3 145±5 37±4 42±4 160±8 171±5 373±8 435±10 21±3 19±1 3 200 140±5 140±3 39±2 38±1 145±8 160±5 354±14 413±11 17±1 19±2 4 40 127±4 131±3 38±4 40±3 151±11 146±5 339±8 381±9 17±3 21±3样品组5 8 125±5 125±6 37±2 39±3 136±2 147±7 301±10 336±11 16±2 17±2未处理对照 109±4 110±5 35±3 40±4 129±5 134±8 283±9 305±8 18±2 18±4蒸馏水对照 110±5 113±7 337±3 39±3 132±7 140±4 284±11 300±10 12±3 17±5二甲基亚砜 96±5 118±4 39±2 40±3 128±6 133±4 290±12 295±13 14±3 15±2阳性物对照NaN3 1.5 1347±83 1770±109 2-AF 10.0 1602±109 1662±102 1650±110敌克松 50.0 2297±114 1255±81丝裂霉素 4.0 2135±100 1,8-二羟蒽醌 50.0 1238±89 2-AA 10.0 1143±81
2.3 哺乳动物红细胞微核试验
与阴性对照组比较,受试样品牛大力(提取物浓缩液)各剂量组PCE/RBC 比值不小于阴性对照组的20%,说明受试样品未出现细胞毒性;受试样品牛大力(提取物浓缩液) 2.5~10.0 g·kg–1BW 剂量组的含微核细胞率与阴性对照组比较,均无显著差异(P>0.05),且雌性小鼠和雄性小鼠结果一致(表4、表5)。

表4 雌性小鼠红细胞微核试验结果Table 4 Results of erythrocyte micronucleus test in female mice

表5 雄性小鼠红细胞微核试验结果Table 5 Results of erythrocyte micronucleus test in male mice
以上结果显示,在该试验条件下受试样品牛大力(提取物浓缩液)的小鼠红细胞微核试验结果为阴性。
2.4 体外哺乳类细胞染色体畸变试验
经统计分析,受试样品牛大力(提取物浓缩液)处理CHL 细胞,不管加或者不加S9,各剂量组的染色体畸变细胞率与阴性对照组均无显著差异(P>0.05) (表6)。
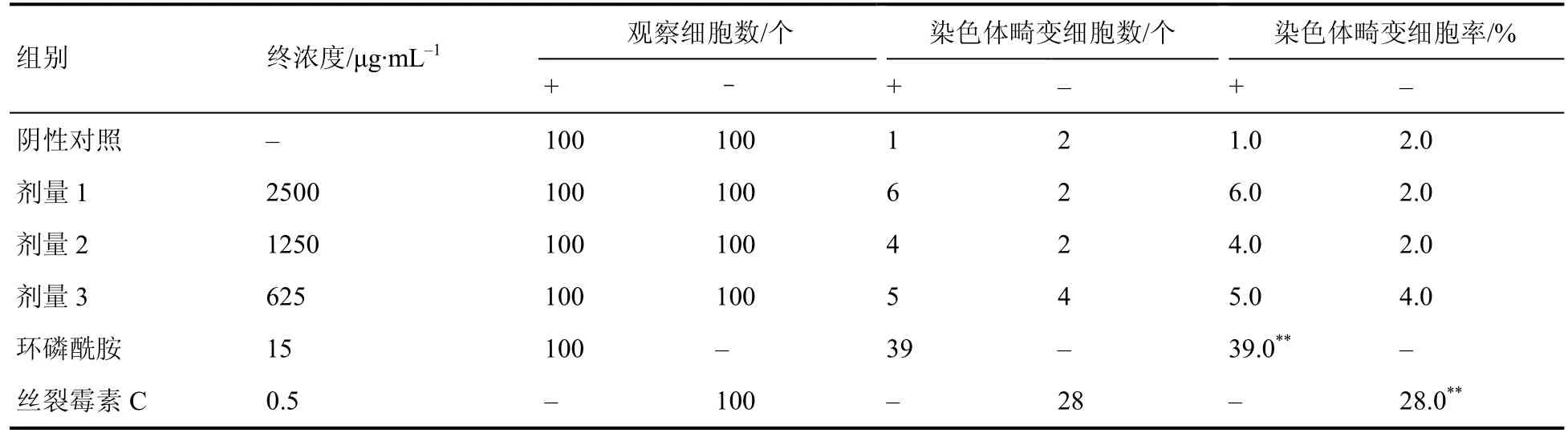
表6 体外哺乳类细胞染色体畸变试验结果Table 6 Test results of mammalian cell chromosome aberration in vitro
因此,在该试验条件下受试物牛大力(提取物浓缩液)的体外哺乳类细胞染色体畸变试验结果为阴性。
3 讨论
牛大力在《全国中草药汇编》《中华本草》《现代本草纲目》等药学专著中均有记载,其气味甘香、药性温和,具有壮阳、养肾补虚、强筋活络、平肝、润肺的功效,对腰酸腿痛、风湿病、慢性肝炎、慢性支气管炎、咳嗽、肺结核等有很好的疗效[12],还有一定的清热提神、抗疲劳等功效[13]。牛大力提取物具有广阔的市场前景,但作为食品原料开发利用还缺乏充分的毒理安全评价支撑。杨增艳等[14]对小鼠的最大耐受量(MTD)进行测定,发现牛大力的水、醇提物最大给药量均比成人日剂量的100 倍还要大,受试动物不仅均未出现任何中毒症状,而且饮食和活动都正常,无死亡病例,说明牛大力没有明显的毒副作用,但是牛大力醇提物致使小鼠体重减少的状况需结合长期的毒性试验进行分析和考量。急性毒性研究是了解外源化合物对机体产生急性毒性的根本依据,可快速直观反映受试物毒性[15]。本试验根据2014 年颁布的《食品安全国家标准 食品安全性毒理学评价程序》(GB 15193.1-2014)对牛大力提取物进行急性毒性和遗传毒性检测。小鼠经口急性毒性试验表明,牛大力(提取物浓缩液)的LD50>20.0 g·kg–1BW,属实际无毒级。
根据国家食品安全相关标准,食品遗传毒性研究必须遵循原核细胞与真核细胞、体内与体外试验相结合的方式进行。本研究选择细菌回复突变试验、小鼠骨髓细胞微核试验和体外哺乳动物染色体畸变试验进行测定。细菌回复突变试验检测牛大力提取物对微生物(细菌)的基因突变作用,预测其遗传毒性和潜在的致癌作用;哺乳动物红细胞微核试验通过分析动物骨髓红细胞,检测牛大力提取物是否引起成熟红细胞染色体损伤或有丝分裂装置损伤,预测其致突变性;哺乳类细胞染色体畸变试验通过CHL细胞进行体外染毒,检测牛大力提取物引起染色体畸变细胞率。细菌回复突变试验结果为阴性,表明当前试验体系下未检出受试物致突变性;小鼠骨髓红细胞微核试验结果为阴性,表明当前试验体系下未检出DNA 损伤风险;体外细胞染色体畸变试验结果为阴性,表明当前试验体系下未见染色体结构畸变风险。以上三项遗传毒性试验均表明牛大力提取物对哺乳类动物体细胞染色体无损伤作用。
牛大力提取物在本研究剂量范围内未检测到急性毒性和遗传毒性,为其进一步食品开发研究提供了理论依据。
