2D-UPLC-Q/TOF-MS法对替考拉宁未知杂质结构鉴定
2023-08-25邵伍军和燕玲袁红露周雪飞陈延安覃玉梅金美春杨荷友
邵伍军?和燕玲?袁红露?周雪飞?陈延安?覃玉梅?金美春?杨荷友
摘要:目的 建立一种在线二维超高效液相色谱-四极杆飞行时间质谱(2D-UPLC-Q/TOF-MS)分析方法对替考拉宁未知杂质进行结构分析。方法 采用在线二维超高效液相色谱-四极杆飞行时间质谱法,一维液相进行分离,二维液相脱盐后进行质谱分析,根据杂质精确分子量及其二级质谱碎片离子与已知主成分结构碎片离子对比,推导其结构。结果 该方法采用2D-UPLC-Q/TOF-MS法对替考拉宁未知杂质进行鉴定,鉴定杂质1为A3-1脱N-乙酰基葡萄糖降解物,杂质2为A2-2脱甘露糖降解物。结论 该方法可以快速地对替考拉宁未知杂质进行结构鉴定,很好地解决了杂质难以制备进行结构解析的难题。
关键词:在线二维超高效液相色谱-四极杆飞行时间质谱(2D-UPLC-Q/TOF-MS);替考拉宁;未知杂质;结构鉴定
中图分类号:R978文献标志码:A
Identify the unknow impurity structures in teicoplanin by 2D- UPLC-Q/TOF-MS
Shao Wu-jun, He Yan-ling, Yuan Hong-lu, Zhou Xue-fei, Chen Yan-an, Qin Yu-mei, Jin Mei-chun, and Yang He-you
(Zhejiang Hisun Pharmaceutical Co, Ltd., Taizhou 318000)
Abstract Objective To establish a two dimension-ultra high performance liquid chromatography-quadrupole/time-of-flight mass spectrometry(2D-UPLC-Q/TOF-MS) method for the structural analysis of unknown impurities in teicolanin. Methods The impurities were separated by 1D-UPLC, the salt was desalted by 2D-UPLC and the impurities were analyzed by Q/TOF-MS. The impurity structures were identified by accurate molecular weight of the impurities and the fragment ions of the mass spectrometry comparing with the fragment ions of the known principal component structure. Results The unknown impurities of teicolanin were identified by 2D-UPLC-Q/TOF-MS method. The impurity 1 was identified as the degradation product of A3-1 removing N-acetylglucosamine, and the impurity 2 was the degradation product of A2-2 removing mannose. Conclusion This method can be used to identify the structure of the unknown impurities in teicolanin, which solves the problem that it is difficult to prepare the impurities for structural analysis.
Key words Two dimension-ultro performance liquid chromatography-quadrupole time of flight mass spectrometer (2D-UPLC-Q/TOF-MS); Teicoplanin; Unknow impurity; Structure identification
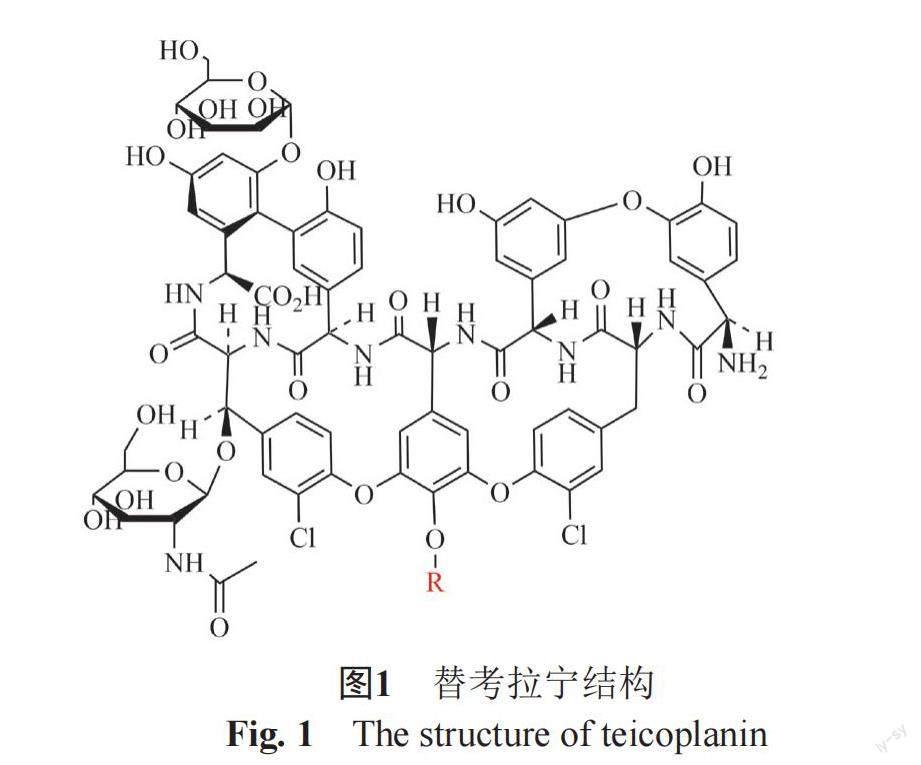
替考拉寧是一种糖肽类抗生素,用于严重的革兰阳性菌感染,主要由5个结构相似的化合物A2-1、A2-2、A2-3、A2-4、A2-5组成,其中A2-2为主要组分,占各组分相对含量的40%以上[1-2]。《中国药典》2020版或《欧洲药典》10.0中替考拉宁主组分结构见图1和表1[3-4]。
替考拉宁结构由七肽组成的苷元母核、甘露糖、N-乙酰氨基葡萄糖、氨基葡萄糖及其侧链组成[5]。目前替考拉宁主组分和杂质的分析方法有液相色谱法、液相色谱-质谱联用法、液相-核磁联用等。Baran等[6]通过核磁、质谱技术对替考拉宁的5个主成分结构进行了鉴定。Tengattin等[7]通过液相-质谱联用技术确定A3-1组分是A2-2水解脱去氨基葡萄糖及其侧链而形成。Cometti等[8]通过液相-核磁联用及气相质谱技术对替考拉宁两个杂质R'端的侧链进行了结构鉴定。Borghi等[9]等通过制备技术与核磁对替考拉宁的4个杂质进行了结构鉴定。张含智等[10]通过高效液相色谱-高分辨质谱推导了11个具有替考拉宁母核组分和4个脂肪酰基-氨基葡萄糖化合物。由于替考拉宁化学组成复杂,通过杂质制备进行结构鉴定费时费力,因此建立快速、简便、准确的杂质结构鉴定方法尤为重要。文献中的一维液相-质谱联用方法,由于质谱检测器的特殊性,流动相只能使用易挥发性盐或酸,所以一维液相-质谱联用需更换原液相方法中的流动相为易挥发盐或酸,这样很难确定液相质谱方法色谱峰与原液相方法色谱峰的一致性。本文通过在线二维超高效液相色谱-四极杆飞行时间质谱法对替考拉宁未知杂质进行结构鉴定,一维液相使用原液相方法,二维液相使用适合质谱检测器的流动相,检测结果既可以与原流动相方法色谱保留时间一一对应,也可以使用高分辨质谱结果对主组分和杂质一级、二级质谱对比研究,通过一级质谱确定其精确质荷比,推测其分子式,通过主组分裂解方式推测杂质的裂解方式并确定其结构。
1 试验部分
1.1 主要仪器与装置
在线二维超高效液相色谱-四级杆飞行时间质谱仪(美国Waters公司),配有Xevo G2-XS Q/TOF-MS四级杆飞行时间质谱仪、ACQUITIY UPLC 2D液相系统及Masslynx数据处理系统;Milli-Q Advantage A10 超纯水仪(德国Merck公司)。
1.2 主要材料与试剂
色谱级乙腈购自德国Merck公司;质谱级甲酸铵、甲酸购自德国Sigma公司;其余试剂均为分析纯;替考拉宁(浙江海正药业生产,批号2121-S200401)。
1.3 试验条件
1.3.1 一维色谱条件
色谱柱:ODS Hypersil(4.6 mm×250 mm, 5 ?m);波长:254 nm;流速2.0 mL/min;柱温:30 ℃;进样量:20.0 ?L;稀释剂:水;流动相A:3.0 g/L磷酸二氢钠溶液(用氢氧化钠试液调pH 6.0)/乙腈=9/1,流动相B:3.0 g/L磷酸二氢钠溶液(用氢氧化钠试液调pH 6.0)/乙腈=3/7;梯度洗脱,流动相B的梯度变化: 0~34.50 min:0%~50%;34.50~35.60 min:50%~90%;35.60~40.25 min:90%~90%;40.25~47.15 min:90%~0;47.15~51.00 min:0~0。
1.3.2 二维色谱条件
色谱柱:WATERS ACQUITY UPLC BEH C18(50 mm ×2.1 mm, 1.7 ?m);流速:0.5 mL/min;柱温:45℃;流动相A:0.01 moL/L甲酸铵pH 6.0),流动相B:乙腈;梯度洗脱,流动相B切缝脱盐后由2%到80%。
1.3.3 质谱条件
ESI源;正离子模式;离子源温度120℃;雾化气流速900 L/h;雾化气温度500℃;毛细管电压2500 V;锥孔气流速50 L/h;锥孔电压60 V;采集范围100~2500 u;采集模式MSE/MSMS,MSE碰撞能量20~50 eV。
1.3.4 操作步骤
取替考拉宁适量,用稀释剂制成2 mg/mL替考拉宁溶液,取20 ?L注入一维液相色谱仪,通过一维液相紫外色谱图确定各峰的出峰位置,分别对各峰进行中心切割,二维液相色谱方法中设置阀切换时间,将目标峰收集于定量环中,再通过阀切换将各目标峰从定量环中反冲至二维色谱柱上分离并脱盐,最后进入质谱进行分析。四极杆-飞行时间质谱仪采用MSE/MSMS采集模式,同时得到一级质谱和二级质谱。使用软件通过精确质荷比和同位素分布进行元素组成分析,确定分子式,结合替考拉宁各组分的二级质谱信息和未知杂质二级质谱碎片推导其结构。
2 结果与讨论
2.1 一维色谱结果
本实验采用在线二维超高效液相高分辨质谱方法建立了替考拉宁主成分及主要杂质结构的鉴定方法,一维液相中色谱方法为《中国药典》2020版或《欧洲药典》10.0[3-4]中替考拉宁有关物质测定方法,一维液相色谱图见图2,结合药典中替考拉宁相对保留时间,其中A3-1色谱峰保留时间为8.93 min,A2-1a色谱峰保留时间为17.77 min,A2-1b色谱峰保留时间为18.43 min,A2-1色谱峰保留时间为19.56 min,A2-2色谱峰保留时间为20.95 min,A2-3色谱峰保留时间为21.51 min,A2-4色谱峰保留时间为23.59 min,A2-5色谱峰保留时间为24.06 min,杂质1色谱峰保留时间为11.95 min,含量为1.61%,杂质2色谱峰保留时间为21.85 min,含量为0.65%。
2.2 二維色谱一级质谱结果
根据一维液相色谱图,分别对各目标峰进行中心切割,切换至二维液相中脱盐处理,再进行质谱分析。根据各峰精确质荷比及同位素分布,推测其分子式,替考拉宁主成分及2个杂质一级质谱结果分析见表2。
2.3 二维色谱二级质谱主成分裂解途径推导
替考拉宁主化学结构由七肽组成的苷元母核、甘露糖、N-乙酰基葡萄糖、氨基葡萄糖及其侧链组成,其主成分结构在质谱中容易脱甘露糖、N-乙酰基葡萄糖、氨基葡萄糖及其侧链、脱氨产生相应的m/z,同时脱去的糖基易在质谱中脱水产生相应的m/z。如 [MA2-2+H]+ m/z为1878.5643;[MA2-2-C5H6N2O4+H]+ m/z为1720.4591(推测结构如图5);[MA2-2-氨基葡萄糖及侧链+H]+ m/z为1563.3643;[MA2-2-氨基葡萄糖及侧链-甘露糖+H]+ m/z为1401.3124;[MA2-2-氨基葡萄糖及侧链-甘露糖- N-乙酰基葡萄糖+H]+ m/z为1198.2306;[MA2-2-氨基葡萄糖及侧链-甘露糖- N-乙酰基葡萄糖-氨基]+ m/z为1181.1993;[M氨基葡萄糖氨及侧链]+ m/z为316.2131;[M葡萄糖氨及侧链-H2O]+ m/z为298.2033;[M葡萄糖氨及侧链-2H2O]+ m/z为280.1939;298.2033离子烯醇式结构互变为酮式结构m/z为250.1809;[MN-乙酰基葡萄糖]+ m/z为204.0863;[MN-乙酰基葡萄糖- H2O]+ m/z为186.0754;[MN-乙酰基葡萄糖- 2H2O]+ m/z为168.0680;[MN-乙酰基葡萄糖-N-乙酰基-H2O]+ m/z为144.0658;[MN-乙酰基葡萄糖-N-乙酰基-2H2O]+ m/z为126.0570。 [MA3-1+H]+ m/z为1563.3555;[MA3-1-甘露糖+H]+ m/z为1401.3124;[MA3-1-甘露糖- N-乙酰基+H]+ m/z为1360.2847;[MA3-1-甘露糖- N-乙酰基葡萄糖+H]+ m/z为1198.2306;[MA3-1-甘露糖- N-乙酰基葡萄糖-氨基]+ m/z为1181.1993;[MN-乙酰氨基葡萄糖]+ m/z为204.0863;[MN-乙酰基葡萄糖- H2O]+ m/z为186.0754;[MN-乙酰基葡萄糖-2H2O]+ m/z为168.0680;[MN-乙酰基葡萄糖-N-乙酰基-H2O]+ m/z为144.0658;[MN-乙酰基葡萄糖-N-胰腺基-2H2O]+ m/z为126.0570。A2-2二级质谱图见图3,A3-1二级质谱图见图4,A2-2裂解方式见图5。
2.4 杂质1结构推导
杂质1[M+H]+ m/z为1360.2847,推测分子式为C64H55Cl2N7O23,杂质1二级质谱图见图6,从图中可知杂质1主要碎片离子包括m/z 1360.2847, m/z 1198.2306, m/z 1181.1993, m/z 1153.2052,未发现N-乙酰基葡萄糖、氨基葡萄糖及其侧链的质谱信号,其与主成分A3-1的主要碎片离子基本相同,推测为A3-1结构脱N-乙酰基葡萄糖所产生。其裂解方式为丢失甘露糖产生m/z 1198.2306 的子离子[M杂质1-甘露糖+H]+ ;丢失甘露糖和氨基产生 m/z 1181.1993的子离子[M杂质1-甘露糖-氨基]+;丢失甘露糖和乙酰基产生m/z 1153.2052的子离子 [M杂质1-甘露糖-乙酰基]+。推测杂质1结构如图7。
2.5 杂质2结构推导
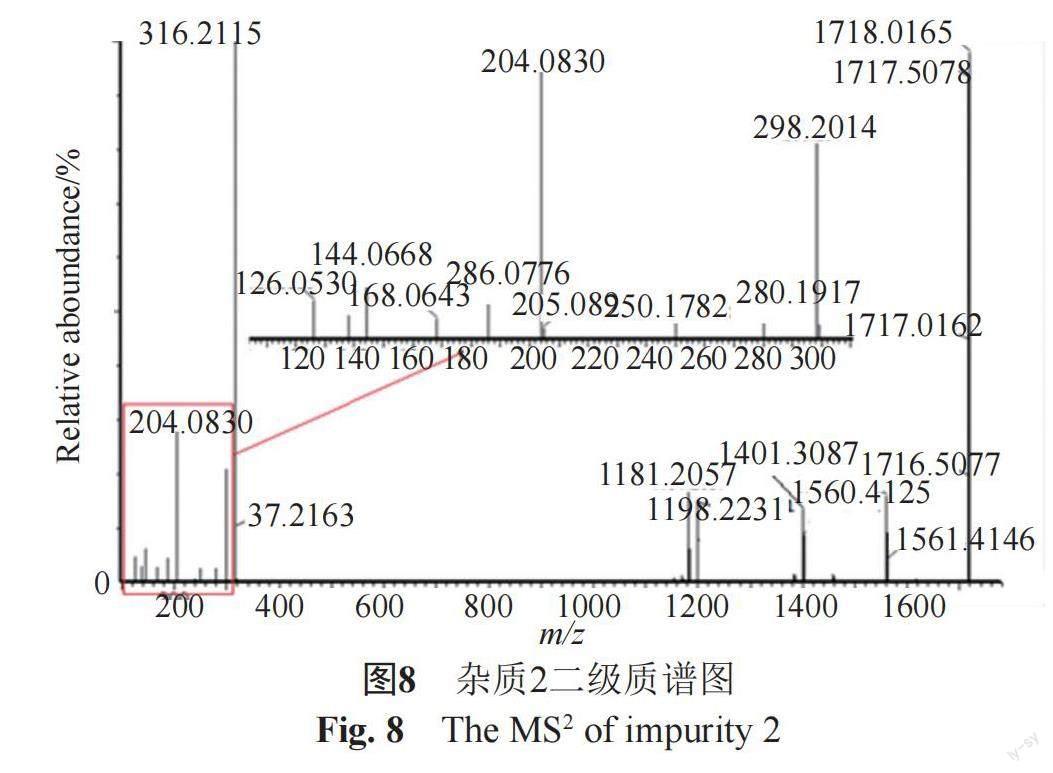
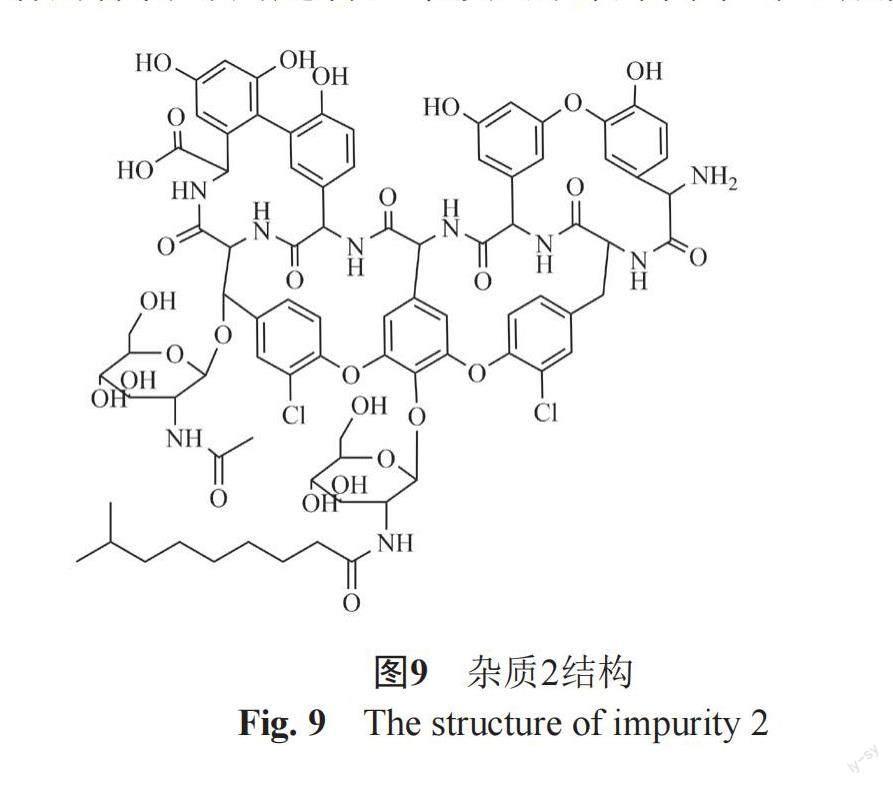
杂质2[M+H]+ m/z为1716.5077,推测分子式为C82H87Cl2N9O28,杂质2二级质谱图见图8,从图中可知杂质2主要碎片离子m/z有1716.5077, 1560.4125, 1401.3087, 1198.2231, 1181.2057, 316.2115, 298.2014, 280.1917, 250.1782, 204.0830, 186.0775, 168.0643, 144.0668, 126.0530,其与主成分A2-2或A2-3碎片离子m/z基本相同,推测可能是A2-2或A2-3脱甘露糖所产生。其裂解方式为丢失葡萄糖氨侧链产生m/z 1560.4125的子离子[M杂质2-葡萄糖氨侧链+H]+;丢失葡萄糖氨及侧链产生m/z 1401.3087的子离子 [M杂质2-葡萄糖氨及侧链+H]+;丢失葡萄糖氨及侧链和N-乙酰基葡萄糖产生m/z 1198.2231的子离子 [M杂质2-葡萄糖氨及侧链- N-乙酰基葡萄糖+H]+;丢失葡萄糖氨及侧链、N-乙酰基葡萄糖和氨基产生m/z 1181.2057的子离子 [M杂质2-葡萄糖氨及侧链- N-乙酰基葡萄糖-氨基]+;子离子[M氨基葡萄糖氨及侧链]+ m/z为316.2115;子离子[M葡萄糖氨及侧链-H2O]+ m/z为298.2014;子离子[M葡萄糖氨及侧链-2H2O]+ m/z为280.1917;298.2014离子烯醇式结构互变为酮式结构m/z为250.1782;子离子[MN-乙酰基葡萄糖]+ m/z为204.0830;子离子[MN-乙酰基葡萄糖- H2O]+ m/z为186.0775;子离子[MN-乙酰基葡萄糖- 2H2O]+ m/z为168.0643;子离子[MN-乙酰基葡萄糖-N-乙酰基-H2O]+ m/z为144.0668;子离子[MN-乙酰基葡萄糖-N-乙酰基-2H2O]+ m/z为126.0530。推测杂质2结构如图9。
2.6 讨论
本研究建立了一种二维在线超高效液相色谱-四级杆飞行时间质谱鉴定替考拉宁中未知杂质的方法,一维液相采用药典方法,根据相对保留时间对替考拉宁各组分进行了确认;二维液相与四级杆飞行时间质谱联用,一级质谱确认各组分及杂质的精确质荷比,推测其分子式;二级质谱采集各组分及杂质的碎片离子,对主成分A2-2及A3-1的二级碎片离子进行了归属,根据主成分裂解规律,推导了两个杂质的裂解方式,并推测了两个杂质的结构。Tengattin等[7]经研究,替考拉宁组分A2-2可以水解脱氨基葡萄糖及其侧链产生A3-1,则A3-1可以进一步水解脱N-乙酰氨基葡萄糖而产生杂质1;替考拉宁的葡萄糖胺发生脂肪酰基化,疏水酰基链改变了替考拉宁的活性,疏水酰基链的长短、支链的取代基及不饱和碳键造成了替考拉宁各组分之间的差异,疏水酰基链组成相同时,支链越多,该化合物在反相色谱的保留时间越弱。杂质2的碎片离子与主成分A2-2和A2-3脱去甘露糖后的碎片离子一致,根据替考拉宁支链越多,反相色谱保留时间保留越弱原理,杂质2为主成分A2-2脱甘露糖降解物。
3 结论
替考拉宁是发酵药物,主要结构组分有5个,杂质较多,杂质制备进行结构鉴定费时费力,采用液相色谱-质谱联用对其成分及杂质进行结构确认操作简单,省时省力,但一维液相色谱-质谱联用由于质谱检测器的特殊性,必须采用挥发性盐或酸作为流动相,流动相改变后原液相方法的色谱峰很难在质谱方法中进行定位,甚至色谱峰的出峰顺序会改变,而且由于易挥发性盐或酸种类有限,一维液相色谱-质谱联用的色谱方法分离度很难达到原液相方法的要求。本研究采用在线二维超高效液相色谱-四级杆飞行时间质谱联用技术,一维液相采用药典方法,二维液相采用适合质谱的流动相进行脱盐,脱盐后直接进行质谱分析。一维液相可以根据药典中色谱峰的相对保留时间确定主成分及杂质出峰时间,二维液相-飞行时间质谱联用进行一级二级质谱同时采集,一级质谱的精确质荷比可以推测主成分及杂质分子式;二级质谱碎片离子可以对裂解方式进行推导,推测未知杂质结构。此方法简便、灵敏,可以快速地对替考拉宁未知杂质进行结构鉴定,很好地解决了杂质难以制备进行结构解析,为难以制备的杂质进行结构鉴定提供了一种解决思路。
致谢:感谢沃特世科技(上海)有限公司应用工程师杨青老师在实验和解谱上的应用支持!
参 考 文 献
Bardine M R, Paternoster M, Coronelli C. Teichomycins, new antibiotics from Actinoplanes teichomyceticus nov. sp[J]. J Antibiot(Tokyo), 1978, 31(3): 170-177.
楊红, 秦川萍. HPLC法测定替考拉宁组分和有关物质[J]. 中国抗生素杂志, 2006, 31(3): 184-186.
国家药典委员会. 中华人民共和国药典(二部)[S]. 北京: 中国医药科技出版社, 2020: 1496-1498.
EDQM. European Pharmacopoeia[S]. 10.0. teicoplanin: 3967-3970.
Kahne D, Leimkuhler C, Lu W, et al. Glycopepide and lipoglycopepide antibiotics[J]. Chem Rev, 2005, 105(2): 425-448.
Barna J C J, Willarns D H, Stone D J M, et al. Structure elucidation of the teicoplanin antibiotics[J]. J Am Chem Soc,1984, 106(17): 4895-4902.
Tengattini S, Corana F, Blanchi D, et al. Application of an HPLC-MS /MS method for teicoplanin drug substance and related impurities, part 2: Identity assignment of related impurities[J]. J Pharm Biomed Anal, 2019,168: 38-43.
Cometti A, Gallo G G, Kettienring J, et al. Isolation and structure determination of the main related substances of teicoplanin, a glycopeptide antibiotic[J]. Farmaco Sci, 1988, 43(12): 1005-1018.
Borghi A, Antonin P, Zanol M, et al. Isolation and structure determination of two analogs of teicoplanin, a glycopeptide antibiotic[J]. J Antibiot(Tokyo), 1989, 42(3): 361-366.
張含智, 杨宝山, 罗文燕, 等. 基于高效液相色谱-飞行时间质谱的替考拉宁组分的结构解析研究[J]. 中国药学杂志, 2021, 56(23): 1941-1948.
