儿童伴胼胝体压部可逆性病变的轻度脑炎/脑病1例*
2023-08-15苏雯
苏 雯
天津市儿童医院神经内科 300134
伴胼胝体压部可逆性病变的轻度脑炎/脑病(MERS)在2004年由Tada等[1]学者提出。该疾病是多种病因累及胼胝体压部而引发的一种脑部疾病,其接受MRI检查后,头核磁共振成像表现为胼胝体压部(Splenium of corpus callosum,SCC)病灶且该病灶具有可逆性特点,在弥散加权成像(Diffusion weighted imaging,DWI)序列上最为典型,呈现高信号,该病以意识障碍、抽搐、头痛、呕吐等症状为主要临床表现,良性病程,一般于1周内消失,在1个月内痊愈,具有良好的预后效果[2]。本研究对1例MERS患儿的临床资料进行总结,探究其临床和影像学表现,为该疾病诊断治疗提供参考。
1 病例资料
患儿,男,主因“发热4d,抽搐3次”入院。入院前4d出现发热,体温最高39.9℃,间隔4~6h体温复升,耳后皮肤出现少许红色皮疹。入院前36h患儿清醒状态下出现抽搐,表现为全身强直发作,持续30s后缓解,抽后入睡,呼唤后偶可发“嗯嗯”音,家属自觉抽时无发热;入院前35h及33h,患儿又出现抽搐2次,表现大致同前,当地医院急诊予止惊治疗后入睡,抽时测体温37.4℃。否认既往抽搐史。母孕期体健,G1P1,足月剖宫产(自愿),否认生后缺氧窒息史,出生体重3.4kg,精神运动发育适龄。母亲婴儿期存在抽搐史(具体情况不详);父亲体健。否认智力低下、遗传代谢性疾病家族史。否认阳性新冠流行病学史。入院查体:神清,精神反应可,呼吸平稳、规则,无发绀,耳后皮肤可见散在红色皮疹,左侧为著,无出血点及牛奶咖啡斑,颈亢(-),双侧瞳孔等大等圆(d=3mm),对光反射灵敏,咽红,无渗出,双肺呼吸音粗,心音有力,律齐,心率120次/min,未闻及杂音,腹软不胀,未扪及包块,四肢肌力、肌张力正常,双侧膝腱反射(++),跟腱反射(++),双侧巴氏征(-),末梢暖,毛细血管再充盈时间小于2s,手足、臀部未见皮疹。辅助检查:头核磁(见图1):考虑可逆性胼胝体压部病变综合征,建议随诊复查,必要时增强MR检查;B超:肝脾肾未见异常,未见肠套叠征;血常规:HGB 111g/L,WBC 3.37×109/L,N 35.3%,L 46.30%,M 18.10%,PLT 255×109/L;CRP 19.70 mg/L;血电解质:Na 135.68mmol/L,K 4.10mmol/L,Cl 101.81mmol/L,CO218.80mmol/L,Ca 2.45mmol/L,P 1.36mmol/L,Glu 4.31mmol/L。入院后予更昔洛韦抗病毒、地塞米松抗炎、营养神经及对症支持治疗,患儿住院后未再抽搐,住院后发热1次,后体温正常,面部、躯干皮肤出现散在红色皮疹,入院5d,复查头核磁未见异常(见图2),共住院6d,皮疹消退,精神反应可,进食水可,病情好转,自动出院。
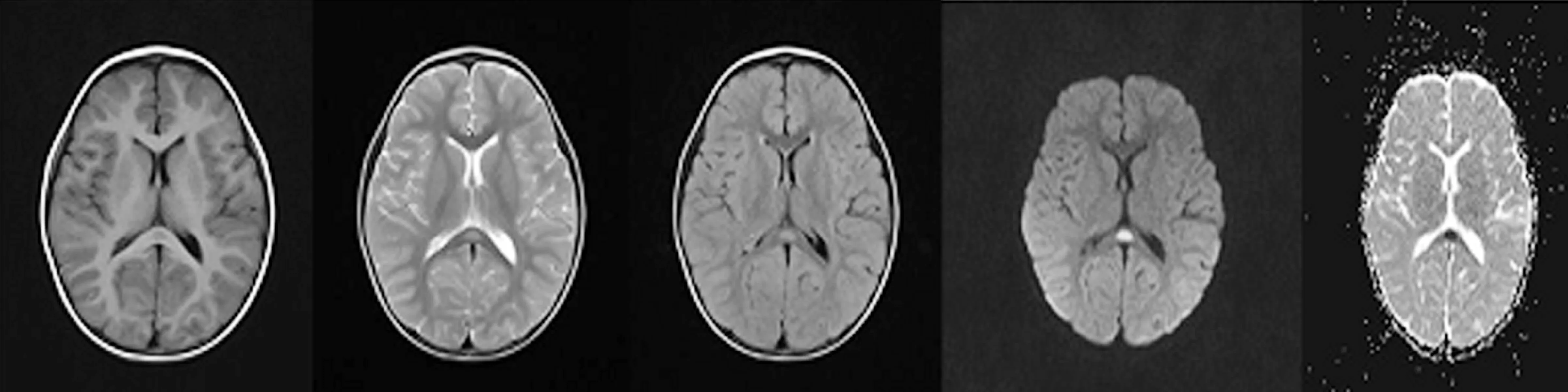
图1 患儿入院当天头核磁胼胝体压部小片状高信号影,病灶于T1WI呈低信号,于T2WI、FLAIR、DWI序列呈高信号,ADC降低
2 讨论
MERS最早于2004年由Tada等[1]提出,多发于儿童、青少年群体,属于临床影像综合征。Takanashi等[3]学者在2006年提出MERS谱系概念,根据头部核磁累及病灶部位的差异可以划分成Ⅰ型和Ⅱ型,前者病变只涉及胼胝体压部,后者除此之外还累及胼胝体膝部、体部、半卵圆中心或深部脑白质。近些年,该疾病研究和认识不断深入,并由Hoshino等[4]学者于2012提出了相应的诊断标准,该标准具体内容包括:(1)患者在发热7d内会出现神经精神症状,例如出现语言异常或是行为异常等表现,并出现意识障碍和惊厥等情况;(2)患者的神经精神症状一般在10d内可完全恢复,且不会产生任何后遗症;(3)急性期发病患者的MRI检查时,胼胝体压部信号升高,T1和T2信号会有轻微变化现象;(4)病变累及范围包括胼胝体整体以及对称性大脑白质;(5)病变反应消失时间一般为2周,不会出现残留信号和萎缩信号。Kashiwagi等[5]学者于2014年明确阐述了MERS概念,其认为临床表现有谵妄等意识状态改变、精神行为异常、抽搐、头痛、构音障碍、共济失调等症状。
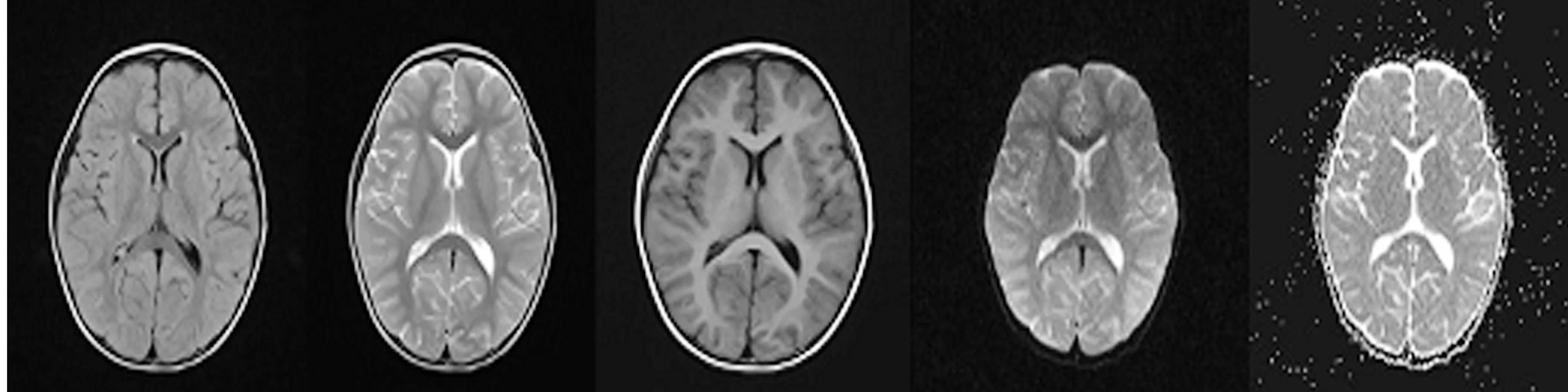
图2 入院后5d复查头核磁原T2WI、FLAIR及DWI序列胼胝体压部小片状高信号影基本吸收
MERS在成人和儿童均有报道,目前发病率尚缺乏确切报道。查阅关于MERS的国内外报道的文献,发病年龄在6个月~16岁。本研究的1例MERS患儿为1岁,与文献具有一致性,考虑与患儿年龄小、髓鞘化发育不完全有关。赵立荣等[6]于2014年首先报道了国内儿童病例。
大部分MERS患者在急性炎症发作期时会伴有发热表现。在感染性疾病中,常见感染为消化道感染,譬如轮状病毒、诺如病毒、腺病毒等病毒感染,本研究中患儿存在呼吸道感染,近期亦有报道[7]肺炎链球菌感染所致MERS。此外,有少数报道MERS发生于非感染性疾病过程中,譬如川崎病、高血糖、急性高原病等[8]。这一发现对于我们认识MERS提供了更坚实的理论基础。
MERS大多有前驱感染史,包括发热、呕吐、腹泻、咳嗽等,通常在炎症性疾病病程的第1~4天出现神经系统症状,较为常见的临床表现为抽搐、意识障碍(精神弱、嗜睡、昏睡)、精神行为异常等,此外,亦有头痛、眩晕、构音障碍、共济失调、吞咽困难、幻听、幻视等症状。有文献报道[9-10],肺炎支原体感染所致MERS易出现共济失调、构音障碍、吞咽困难,但是肺炎支原体感染相关的MERS较其他病原体所致MERS是否更易于出现以上的临床表现尚需要更多的样本研究。
MERS的临床症状轻重不一,预后转归亦有不同,大多预后好,仅有少数遗留中枢神经系统症状。大多数患儿临床症状在1个月内完全消失。病变局限在胼胝体压部的患儿临床症状通常轻于病变累及胼胝体外者。
头颅MRI是诊断MERS的重要手段[11-12]。MERS影像学特征表现局限在Ⅰ型和Ⅱ型可逆性异常信号表现中,病灶形状大部分为类圆形,在T1WI上表现为等信号或是低信号特征,在T2WI上表现为高信号特征,在FALIR上表现为高信号或是等信号特征,在DWI上表现为高信号且在ADC上表现为信号降低特征,由于细胞毒性水肿反应导致水分子运动扩散受到限制。一般在1~2周范围内的异常信号会被吸收甚至消失,最快6d内就会消失。本研究中,患儿病灶具有Ⅰ型特征,也就是胼胝体压部表现为孤立性类圆形信号特征,5d之后进行复查,可以发现异常信号已经基本被吸收。根据Takanashi等[3]报道可知,1例患儿在入院时接受头部MRI检测后发现,胼胝体整体和双侧侧脑室周、深部脑白质的DWI信号较高但是ADC信号会下降,次日接受复查扫描双侧侧脑室周和深部脑白质、胼胝体膝部的DWI序列呈现的高信号范围逐渐缩小,强度也会逐渐下降,这就表示波及双侧侧脑室周和深部脑白质所表现出来的异常信号相对于胼胝体压部所表现出来的异常信号更先消失。根据Takanashi等[3]学者报道了解到,有14例MERSⅡ型患者在发病4d之后接受头部MRI复查后发现,双侧侧脑室室周和深部脑白质所表现出来的异常信号已经彻底消失,这就表示Ⅱ型逐渐缓解,转归到Ⅰ型。
MERS发病机制并未明确,大部分学者认为胼胝体压部发生细胞毒性水肿是疾病发病主要机制。现阶段,针对该疾病发病机制假说包括以下几种:(1)胼胝体压部有着丰富的水量,但是其电解质调节机制不够完善,容易在髓鞘间或是髓鞘内部位发生一过性水肿,进而引发细胞毒性水肿现象。(2)炎性信号浸润或是血清炎症因子有明显上升表现。(3)低钠血症会使胼胝体压部细胞渗透压下降,进入更多的水分子。(4)癫痫患者由于长期服药或是突发性停药会导致阳离子通道受到影响,进而无法平衡细胞内外水分。(5)激活自体免疫系统。(6)受遗传因素的影响。
在临床中,因其影像学表现具有特征性,这就需要注意鉴别其与其他也具有涉及胼胝体压部或是其他白质脑病的疾病,例如急性播散性脑脊髓炎、多发性硬化、可逆性后部脑病综合征、遗传代谢性疾病累及白质、遗传性白质脑病以及伴可逆性脑白质病变的X连锁Charcot-Marie-Tooth病1型(CMTX1)等。
