6例万古霉素致药物热病例报道及分析
2023-08-05申庆荣莫广艳李刚
申庆荣 莫广艳 李刚
药物热是一种药物不良反应(adverse drug reaction,ADR),是在药物治疗过程中出现、停药后消失的发热[1]。药物热的诊断十分复杂,目前没有统一的诊断标准,且发热初期难以区分是感染性发热还是药物热[2]。因此,临床上常被误诊。万古霉素引起药物热的文献较少,多为个案报道。刘娟等[3]筛查了其他医院2014年1月1日—2020年12月31日使用万古霉素患者,并检索国内外主要的文献数据库1980年1月—2021年3月关于万古霉素致药物热的个例报道,仅收集32例患者,其发生率未见报道。近期,笔者遇到1例万古霉素所致药物热患者,观察其体温的变化与血药谷浓度值存在明显的时间相关性。为了解万古霉素与血药谷浓度之间的相关性,以及更深入地研究万古霉素所致的药物热,对广西壮族自治区人民医院出现万古霉素药物热的病例进行深入分析,为临床治疗提供宝贵的临床病例资料,并为安全合理用药提供一定的参考依据。
1 资料与方法
1.1 一般资料
查阅广西壮族自治区人民医院2017年1月—2021年12月使用万古霉素进行抗感染治疗患者的病历资料,筛选出现万古霉素相关药物热的患者。收集发生药物热的所有患者的基本信息,包括性别、年龄、身高、体质量、主要诊断、万古霉素血药谷浓度、万古霉素的用法用量及使用日期、血肌酐、白细胞计数、嗜酸性粒细胞计数、嗜酸性粒细胞比率、血小板计数、药物热发生时间、体温峰值、临床表现以及缓解时间等。本研究经医院医学伦理委员会批准(伦理-KY-ⅡT-2023-04)。
1.2 方法
对患者的一般资料进行研究和分析;计算万古霉素药物热的发生率;对患者药物热发生、发展的时间分布、体温变化、转归、再次用药的结果等进行分类整理和统计分析。
1.3 药物热的定义
药物热是一种药物不良反应,是在药物治疗过程中出现停药后消失的、临床医生仔细评估和实验室检查后无法明确原因的发热反应[1]。
1.4 纳入标准和排除标准
纳入标准:(1)使用万古霉素期间出现发热。(2)停用万古霉素后体温恢复正常。(3)再次给药后发热复发。至少满足(1)和(2)2个条件。
排除标准:(1)存在感染未控制的情况(感染症状加重、感染指标升高等)。(2)存在其他可引起发热的非感染性疾病(如肿瘤、血栓栓塞性疾病、脑血管意外、胶原血管疾病、急性痛风等)。(3)无法判断用药与发热之间关联性的病例。
1.5 药品信息
药品名称:注射用盐酸万古霉素(浙江医药股份有限公司新昌制药厂,国药准字 H20033366)和VIANEX S.A.(PLANT C)(批准文号:H20140174);规格:0.5 g/瓶,
1.6 统计学方法
采用SPSS 26.0统计学软件进行数据处理。计量资料采用(±s)和中位数表示,组间差异性分析采用t检验和秩和检验;计数资料用n(%)表示组间差异性分析采用χ2检验。
2 结果
2.1 出现万古霉素致药物热病例的相关情况
共筛选出6例使用万古霉素后发生药物热的患者,编号为1~6号,药物热发生率为0.3%(6/1976),见表1。
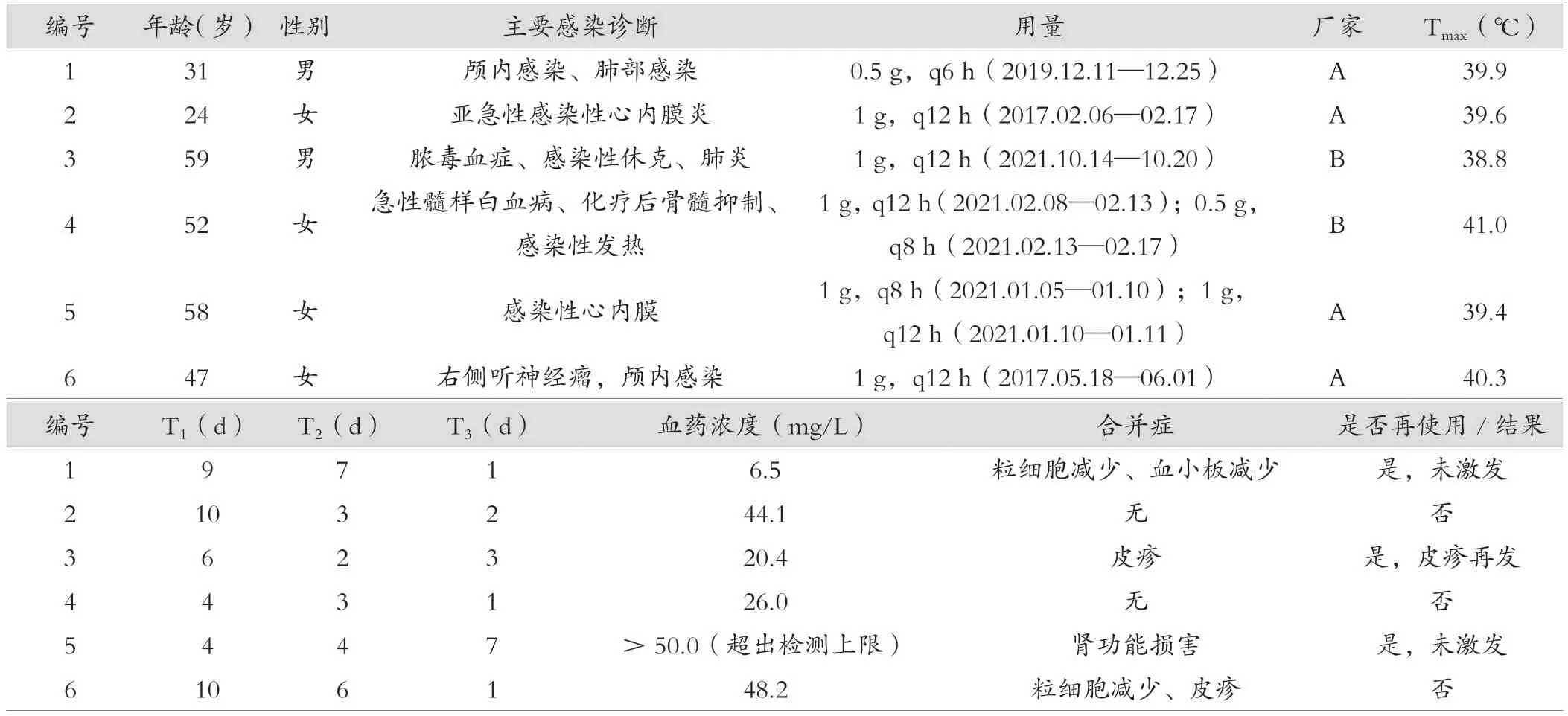
表1 万古霉素致药物热病例的相关情况
6例万古霉素致药物热的患者中,男性2例,女性4例,男女比例为1 : 2。年龄24~59岁,平均(45.2±14.5)岁,中位年龄49.5岁,患者年龄分布见表2。
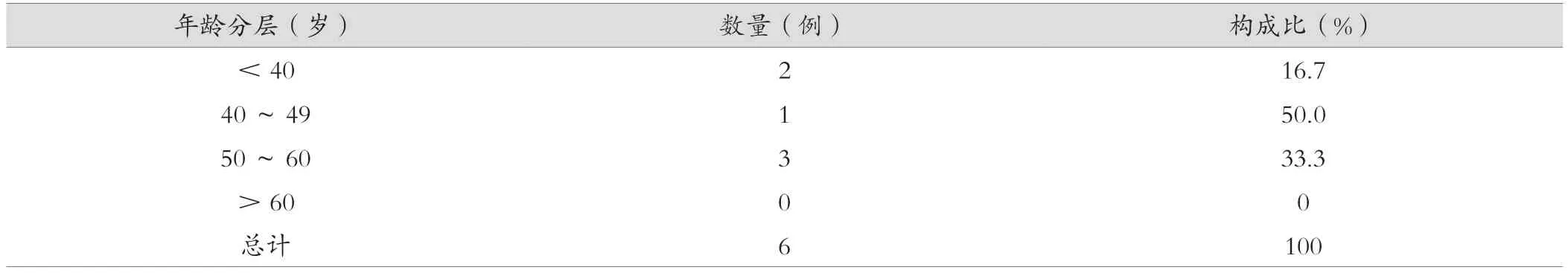
表2 发生药物热患者年龄情况
万古霉素致药物热最高体温38.8~41.0 ℃,平均(39.80±0.76)℃,83.3%(5/6)的患者体温高于39.0℃,患者体温分层见表3。
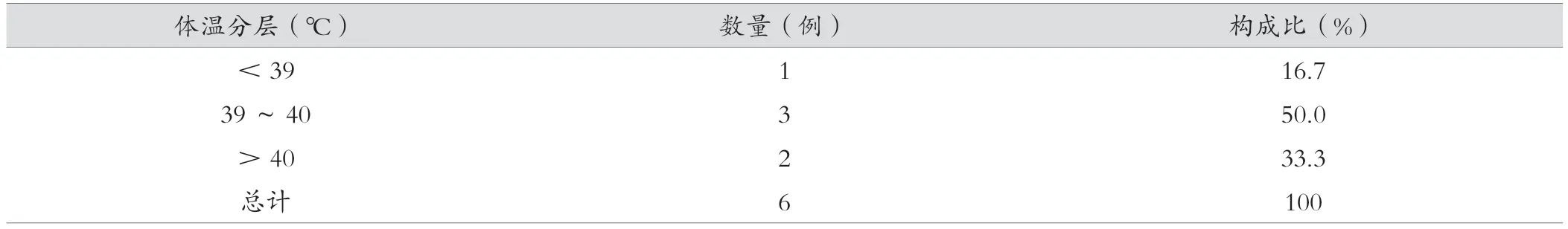
表3 发生药物热患者的体温峰值(Tmax)情况
2.2 药物热发生、发展的时间分布
6例万古霉素致药物热的患者中,药物热发生在用药第4~10天,平均(7.2±2.9)d,中位数为7.5 d。从出现药物热到停药的时间为2~7 d,平均(4.2±1.9)d,中位数3.5 d,83.3%(5/6)的患者从药物热发生到停药的时间超过3 d。见表4。
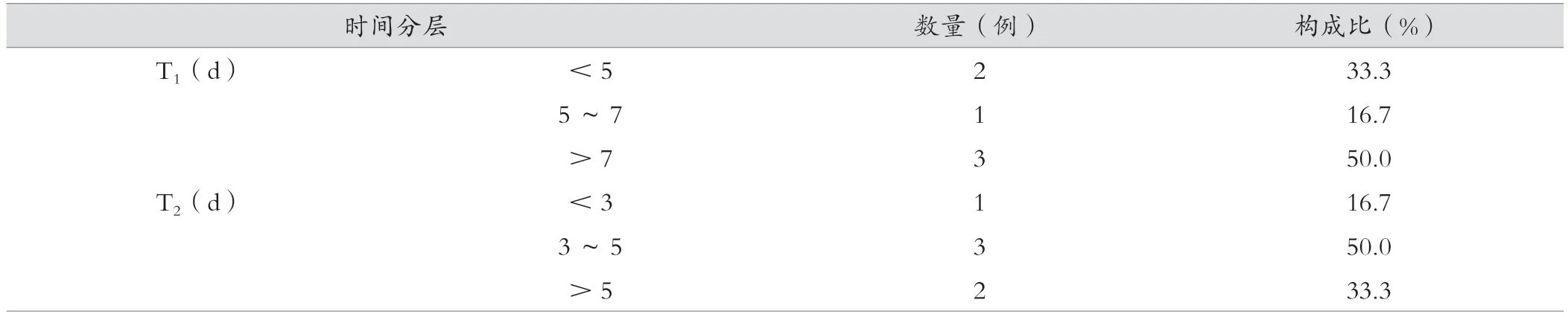
表4 患者药物热发生、发展时间分布
2.3 药物热转归及严重程度
停药后所有病例的体温均在1~7 d恢复正常,平均(2.5±2.4)d,中位数为1.5 d,66.7%(5/6)的患者体温会在停药后3 d内降至正常。见表1、表5。
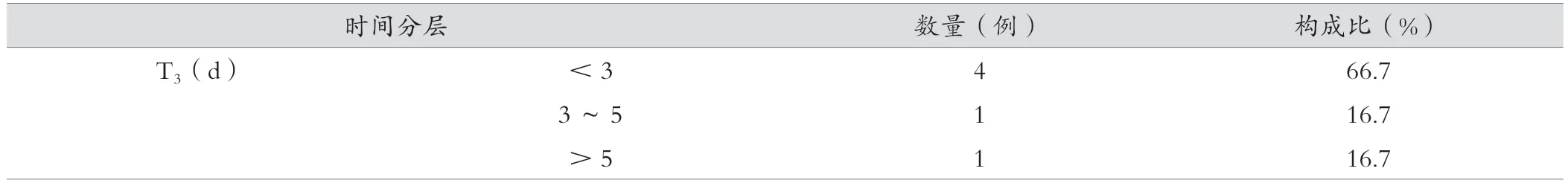
表5 药物热患者体温恢复的时间
多数患者在出现药物热的同时伴随有其他临床症状,2例患者仅发热未伴有其他不良反应;而其他4例不同程度地伴有1个以上系统或器官的损害,涉及血液系统、皮肤和肾脏;主要临床表现为血细胞减少、皮疹和肾功能损害。1例患者在出现药物热的同时伴发粒细胞减少和皮疹。停药后均能恢复到正常水平或基线水平,恢复的时间长短不一,见表6。
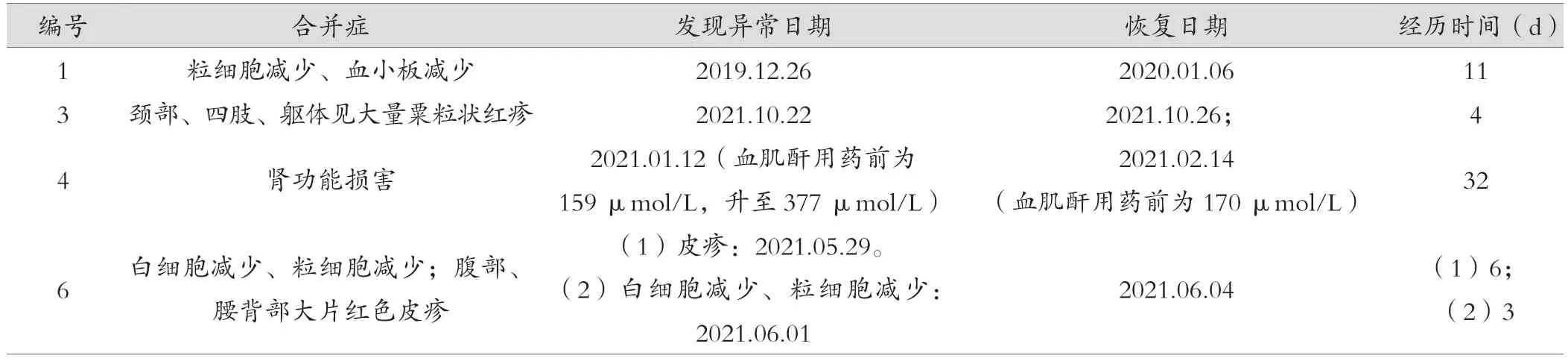
表6 药物热伴随的其他症状的转归情况
2.4 患者合并用药情况
6例万古霉素致药物热的患者中,万古霉素用法用量为“每8小时给药1次,每次给药1 g”1例(16.7%);“每12小时给药1次,每次给药1 g”4例(66.7%);“每6小时给药1次,每次给药0.5 g”1例(16.7%)。
用万古霉素的生产厂家来看,使用国产或进口药物均有可能出现药物热,但国产药物4例出现药物热,进口药物2例出现药物热。6例万古霉素致药物热的患者中,联合用药共计5例(83.3%),分别为头孢他啶、莫西沙星、哌拉西林他唑巴坦、头孢哌酮舒巴坦钠、头孢噻利等,均与药物热无明显相关性。
2.5 万古霉素药物热与血药浓度
本文中6例万古霉素致药物热的患者均对血药谷浓度进行了测定,并且5例(83.3%)患者的血药谷浓度均超过了20 mg/L,见表1。其中2例血药谷浓度在40~50 mg/L,1例血药谷浓度>50 mg/L;最低血药谷浓度为6.5 mg/L,最高血药谷浓度为>50 mg/L。血药谷浓度的平均值为(29.00±17.03)mg/L,中位数为26 mg/L(统计平均值和中位数时,由于1例患者血药浓度超出了检测高限,故统计软件进行了个案排除)。
5号病例,感染性心内膜炎,2021年1月5日给予万古霉素“每8小时给药1次,每次给药1 g”,2021年1月8日(用药第4天)出现了药物热,2021年1月11日查血药浓度>50.0 mg/L(超过检测上限),血肌酐377 μmol/L,即停用万古霉素,换用利奈唑胺“每12小时给药1次,每次给药0.6 g”。停药后持续监测血药浓度,2021年1月13日复查血药浓度仍>50.0 mg/L(超过检测上限),体温未见降低,且较前升高达到最高值39.4 ℃;1月14日体温峰值开始降低;1月15日血药浓度37.44 mg/L;1月18日血药浓度15.5 mg/L,体温降至正常。
2.6 再次用药的结果和转归
1、3、5号病例再次使用万古霉素,所有病例均未再出现药物热。3号患者再次用药,用药后的第4天再次出现颈部、四肢及躯干粟粒样红色斑丘疹,程度较前严重;给予异丙嗪注射液静脉注射,依巴斯汀、枸地氯雷他定口服,同时给予卤米松乳膏外涂;8 d后皮疹消退,恢复时间较前延长。
3 讨论
万古霉素所致的药物热可发生在各个年龄段。刘娟等[3]和岳小会等[4]报道,多数患者万古霉素所致药物热发生于用药后6~13 d,出现发热的平均时间为8.8 d,中位数为10 d;81.25%的患者体温会在3 d内恢复正常,但有18.75%退热时间会延迟到4~7 d。国外有文献报道,62% 的患者在用药后1周后出现发热,大多数患者停药3 d后体温恢复正常[5]。本文结果与文献报道相似。本研究显示女性患者略比男性患者更易产生药物热,中青年较老年患者相对容易产生药物热,本文所有案例年龄均在60岁以下。万古霉素所致的发热体温峰值多在39.0 ℃以上,体温最高达41.0 ℃;从出现药物热到停药的时间为2~7 d,平均(4.2±1.9)d,中位数3.5 d,83.3%的患者停药时间超过3 d;说明医务人员对药物热的了解还不够深刻,因而延误药物热的诊断和停药的时间。提示在用使用万古霉素抗感染的过程中需对患者进行密切的监护,笔者结合各类文献,总结万古霉素的监护要点[6-8]:(1)万古霉素治疗6~13 d出现高热,体温升高与临床症状不相符,常在原发感染控制后再次出现高热。(2)体温超过38.5 ℃,伴或不伴有皮疹、关节痛、嗜酸性粒细胞升高等。(3)不能用其他疾病或药物的原因解释。(4)停药体温峰值快速降低,一般在3 d内降至正常。
药物热的发生机制主要有:改变体温调节机制、给药相关反应、药物的药理作用、特异质反应和超敏反应,其中给药相关反应和超敏反应是万古霉素药物热相关的机制[9-10]。
当明确诊断为药物热时,停用致热药物是最有效地治疗方法。对于感染还没有得到控制的患者,可选用替代药物继续进行抗感染治疗。对于肺部感染和皮肤软组织感染可选用利奈唑胺,血流感染和感染性心内膜炎可选用达托霉素[3]。万古霉素和替考拉宁存在交叉过敏反应[11]。有学者对使用万古霉素后出现发热伴中性粒细胞减少或皮疹的患者对替考拉宁的耐受性进行过回顾性研究,研究表明有10.3%患者改成替考拉宁后出现替考拉宁引起的发热、中性粒细胞减少或皮疹等症状,且使用万古霉素出现中性粒细胞减少的患者仍有半数改用替考拉宁后出现中性粒细胞减少症[5]。因此,使用万古霉素后仅出现发热,可以改用替考拉宁;若出现中性粒细胞减少症患者则需谨慎使用替考拉宁。另外,还有研究发现,替考拉宁不良反应发生率在以前经历过万古霉素不良反应的患者中更高(23.1%比5.3%)[12]。因此在给有万古霉素过敏反应的患者开具处方前,医生需考虑交叉反应的危险因素。
血药浓度监测是保证万古霉素治疗有效性和安全性的有效措施之一,虽然2020年美国发布了《万古霉素治疗严重MRSA感染的治疗药物监测指南》,提倡严重MRSA感染的患者使用AUC/MIC作为万古霉素的治疗药物监测靶目标[13]。但这并不适用于所有人群,如肾脏替代治疗患者无法准确计算AUC,手术预防用药的患者疗程短没必要监测,脑膜炎的监测策略也有待考量[14]。2020年中国药理学会发布了《万古霉素治疗药物监测指南》指出,以下人群推荐监测血药谷浓度[15]:(1)危重患者、肥胖患者、服用伴有肾毒性药物的患者以及肾功能受损的患者(强烈推荐,证据质量较低)。(2)儿科患儿、新生儿和接受肾脏替代治疗的患者(强烈推荐,证据质量较低)。(3)肾功能不稳定的患者(强烈推荐,证据质量较低)。(4)老年患者(>65岁)(低推荐,证据质量较低)。(5)中度到重度心力衰竭患者、肾清除增强患者或体质量过轻患者(低推荐,证据质量较低)。从目前的文献来看,罕见报道过万古霉素药物热与血药浓度之间有关联,原因可能是大多数患者在怀疑发生药物热后只停药观察体温的变化,而没有监测血药浓度的变化。本文的5号案例首次观察到血药谷浓度与体温的下降、恢复之间存在着明显的时间相关性;且发生药物热的6个案例中,有5个案例血药浓度都超过了推荐范围。由此笔者大胆猜测,万古霉素药物热可能和血药谷浓度超限有一定的关系;如果将万古霉素血药谷浓度控制在正常范围,可能降低药物热的发生概率,但还需要进一步证实。
综上所述,万古霉素药物热缺乏统一的诊断标准,作为医护人员要加强学习药物热的发生机制、临床特征和发生机制等,及时诊断药物热,确保患者用药安全、有效、经济合理得到最大的保障。
