光标测技术在心脏电生理和心律失常研究中的应用
2023-08-04李阳鹏郑雨晴李剑鸿陈唐葶谭晓秋
李阳鹏,郑雨晴,李剑鸿,陈唐葶,谭晓秋,2
1.西南医科大学心血管医学研究所,医学电生理学教育部重点实验室,医学电生理四川省重点实验室(泸州646000);2.西南医科大学基础医学院(泸州 646000)
心律失常(cardiac arrhythmia)是一种临床上常见的心血管疾病,可单发也可与其他心血管疾病伴发,严重的心律失常可导致心源性猝死。因此,深入探究心脏电生理和心律失常机制尤为重要[1-2]。心律失常发生机制复杂[3-7],研究心律失常的方法也多种多样[8-9],包括从单细胞水平的膜片钳到组织层面的多通道电标测和整体水平的电生理记录。随着心脏电生理研究技术不断更新,越来越多心律失常的发病机制被揭示[10-11]。但是,作为一个功能合胞体,心脏在发生心律失常时其整体电活动表现、局部传导异常机制、以及心脏各区域之间的联系无法直观的研究和显示[12],这使得心脏电生理研究的发展在相当长一段时间都停滞不前。20 世纪末,随着荧光探针技术和高分辨率采集技术的出现,光标测技术应运而生并被用于神经系统的研究。由于心脏与神经系统的相似性,光标测技术被应用到心脏组织并逐渐成为研究心脏电生理功能的主要技术之一,对心脏电生理研究发挥了重要作用。此后,心脏电生理的研究不再局限于孤立的细胞或整体水平,器官水平的心律失常机制研究更为深入。通过心脏光标测技术,可以实现对心脏心肌细胞膜电位和胞内钙瞬变的同步记录[13],研究者可以直观地观察到心律失常发生前后心脏电信号和钙信号的整体变化,如异位激动、折返形成的位置和异常传导过程,从而加深对心律失常的认识,促进心脏电生理研究的深入[12]。本文就光标测技术及其在常见疾病模型下的应用进行了评述,并为抗心律失常药物的研究提供技术参考。
1 心脏光标测技术原理
电压敏感染料是一种双极性分子,可以稳定结合到细胞膜的磷脂双分子层,它们可以感受细胞膜内外的电场力变化而做出适应性的结构改变,在激发光的作用下,这种结构改变会导致其荧光强度发生改变,从而准确地反映膜电位的实时变化,因此,染料的荧光强度可以间接地反映膜电位的变化[12,14-16]。同样的,胞内钙活动与动作电位呈现类似的规律变化,因此,使用钙敏感染料可对胞内钙离子进行标记,钙染料荧光强度的变化可以反映胞内钙浓度或钙瞬变的变化[17-18]。具体的光学原理为:在染色结束后,荧光染料分子与细胞膜或胞内钙离子有效结合,使用530 nm 的激发光照射心脏,电压染料和钙染料的发射光(电压染料RH237发射光波峰为670 nm,钙染料Rhod-2AM 发射光波峰为580 nm)被相机镜头收集(图1A),通过几种滤光片将两种不同波长的荧光信号分离,采用EMCCD高速相机采集荧光信号,即可在采集系统上同时获得瞬时膜电位(动作电位)和钙瞬变的信号[19-20](图1B)。光标测技术是一种将荧光探针技术与高分辨率采集技术相结合的实验技术,实验数据丰富,运用特定的软件可完成对心脏整体或区域性电生理行为的分析和研究[21-22]。
光标测技术较其它电生理技术的优势:①高时空分辨率(时间分辨率——采样频率可达1 000 Hz,空间分辨率——最小像素点可达32 μm);②广阔的采样面积——可达10 000 个像素点以上[19-20],意味着可以标测哺乳动物心脏,如小鼠、大鼠、豚鼠等;③可以直接计算各个电生理参数在不同部位分布的差异;④可以从心脏整体层面观察心脏电信号和钙信号的传导,了解心律失常发生时的起点和传导路径;⑤对心脏损伤小,信号不会受电磁场的干扰[14]。
2 光标测技术各参数在电生理研究中的应用
光标测技术发展迅速,在20世纪末出现后已逐渐成为心脏电生理研究的主要技术之一,多用于心脏电生理和多种心血管疾病模型的电生理变化研究及药物的有效性评价。然而,要研究疾病模型下的心律失常机制,需对光标测的各个电生理参数有足够的了解,并将其有序整理、分析,从而明确该疾病模型下或药物干预后的电生理机制[22]。
2.1 动作电位
2.1.1 动作电位时程 动作电位时程(action potential duration,APD)不同时期的研究:工作心肌细胞动作电位分为0、1、2、3、4期,不同时期参与的离子通道不同,通过分析APD 的不同时间段,可以大致了解对应时段的离子通道的功能状态[23-25]。动作电位时程与心律失常密切相关,动作电位延长被认为是造成心律失常易感性增加的一种机制,可能与复极化延长导致的延迟后去极(delayed after depolarization,DAD)或早后去极(early after depolarization,EAD)的发生率增加有关;同时结合动作电位有效不应期(effective refractory period,ERP)的测量,我们可以分析ERP与APD的比值来大致评价心律失常风险[26]。
2.1.2 动作电位异质性 不同心肌细胞电生理特性不尽相同,各个细胞间除极和复极时间可能存在差异,这种差异被称为心肌动作电位异质性。在整体心脏中,光标测APD 热图可以直观地观察到,心房动作电位时程明显短于心室,这是由不同功能区域心肌细胞离子通道的种类和数量决定的[27],动作电位异质性的增加被认为是造成折返性心律失常的一种重要机制[25]。同样的,活体心肌切片心内膜与心外膜的APD差异[19],窦房结细胞与心房肌细胞APD的差异都是结构和功能的差异决定的。因此,可以将实验组与对照组进行对比分析,明确实验处理对于动作电位的影响,再分析具体影响的时段,从而更加深入的研究其中的分子机制,如某种离体通道是否存在数量和活性的改变[28],或某些药物通过影响离子通道活性影响动作电位时程。
2.1.3 动作电位的传导 心脏正常的传导方向为窦房结、左右心房、房室结、希氏束、左右束支及浦肯野纤维网[29]。通过对心脏的动作电位标记,可以研究在窦性节律下心脏电活动的起源和传导路径。因此,精准识别动作电位的传导在研究心律失常中非常重要[30-31]。窦房结细胞是心脏中自律性最高的起搏细胞,因而作为心脏整体电冲动发放的领导者。2010 年,华盛顿大学EFIMOV团队首次使用光标测技术解释人窦房结起搏点和传导路径,实验结果与经典理论相匹配,显示出光标测技术在组织器官水平电生理研究的优越性[32]。而部分实验需除去自身节律影响,采用额外刺激,此时心脏动作电位的传导则为刺激点向远处传播,后续的数据分析可以定量计算动作电位传导速度,而动作电位激活图可直观显示传导方向和传导时间(图1C)。通过对比传导速度可以明确实验组和对照组的传导功能是否存在差异,再结合相关的分子实验验证,如缝隙连接蛋白的丰度变化等,可以深入进行心脏电生理和心律失常机制研究[33-34]。此外,心律失常期间也存在动作电位传导的异常,可以分析激活图或相位图大致了解心律失常的起点和异常传导路径[34]。因此,光标测技术对于研究异位起搏点、折返、转子等异常传导方面体现出明显优势。
2.2 钙瞬变的研究
动作电位产生过程中,0期大量内流的钠离子导致细胞膜去极化,从而激活L型钙通道,钙离子进入胞内激活肌浆网的雷诺定受体(ryanodine receptor,RyR2),诱导钙促钙释放过程,造成大量钙离子从肌浆网进入胞浆,随后肌浆网钙离子ATP 酶(sarco/endoplasmic reticulum Ca2+ATPase,SERCA)将钙离子回收到肌浆网,整个过程即钙瞬变过程[35-36]。与动作电位一样,心脏不同区域或同区域不同类型组织的钙瞬变也存在差异(图1D);钙瞬变时程的延长或缩短一定程度说明肌浆网RyR2或SERCA活性的改变[37-38],这在病理状态下可能出现在整个心脏,也可能存在于局部病变部位及周边区域。而且,钙活动的紊乱与膜电位的异常密切相关,如舒张期异常的钙释放可能导致DAD 的形成,可能造成触发活动进而诱发快速室性心律失常[39]。
2.3 动作电位和钙瞬变耦联关系的研究
正常心脏电活动功能的实现依赖于膜电位和钙瞬变的协调配合,这是一个动态的、复杂的平衡关系。只有这样,心脏的兴奋才能正常传导,心脏舒缩活动才可能有效进行。一旦这种平衡被打破,心脏的兴奋传导可能加快、延迟或阻滞,严重时会造成快速室性心律失导致心源性猝死[40]。2019 年,牛津大学雷鸣教授在Cardiovascular Research期刊的一篇综述中指出膜钟和钙钟与心律失常的关系,膜钟和钙钟分别反映动作电位和钙瞬变过程。作者指出,膜钟激活产生钙钟,钙钟回馈膜钟,二者相互协调配合,稳定膜电位正常传导并维持胞内钙稳态。不论是信号转导异常还是离子通道功能改变,都会造成二者稳态的失衡引发心脏电活动的异常,即心律失常。二者的耦合关系被称为latency(图1E),即钙钟落后于膜钟的时间,对于功能正常的心脏来说,这个时间是基本固定的,但心脏心功能异常时,这种耦合关系可能出现改变[41]。光标测在整体心脏水平同时记录膜电位和钙离子浓度变化,可分析动作电位和钙瞬变之间的耦合关系并计算latency评价其心律失常易感性。本课题组利用光标测对老年鼠心脏检测后发现,其latency较青年鼠显著缩短,并且老年鼠心律失常发生率明显增加,这提示钙钟的提前激活可能是造成老年鼠心律失常易感性增加的机制之一[42]。研究者在儿茶酚胺敏感的多形性室性心动过速模型的研究中发现,钙异常释放导致的胞内钙超载引发钠钙交换体(sodium-calcium exchange,NCX)过度活化,引起DAD 诱发触发活动,导致膜电位异常引发快速室性心律失常,这便是钙钟异常引起膜钟异常的经典示例[39]。
3 光标测技术在心脏病理生理研究中的应用
心脏电生理研究的目的是为了深入了解疾病的电生理机制从而选择更好的治疗手段,通常的研究方法是用小鼠构建相关疾病动物模型。常见的心脏疾病动物模型有主动脉弓缩窄术诱导的左室肥厚伴心力衰竭(TAC)模型、心肌梗死模型(MI)、心脏缺血再灌注(IR)模型和遗传性心律失常或心脏病模型[43]。不同的疾病模型,其电生理功能及发病机制不尽相同,但也存在联系。通过分析这些模型的光标测实验结果后发现,在TAC模型中,动作电位的激活时间明显延迟,提示心脏电传导功能降低[44]。通过心脏光标测明确了表型后可以分析影响心肌细胞动作电位传导的相关因素,如心肌细胞缝隙连接蛋白含量或活性的下降,或者传导系统功能的异常都可能造成心脏整体传导功能的降低;同样的结果可以在IR模型和MI模型中重复发现[45-48],这可能与心肌细胞的损伤直接相关。总的来说,器质性心脏疾病的小鼠在基础状态下即出现钙处理明显异常(图2A)和动作电位时程延长与传导速度减慢(图2B),并且区域间分布差异明显,这可能是造成其心律失常易感性增加的原因。而非器质性病变的遗传性心律失常和心脏病模型中,在基础状态下,这些小鼠心脏的血流动力学和电生理功能是基本正常的,但在应激条件,如儿茶酚胺干预、活动或情绪激动等刺激下,其动作电位传导、钙处理等电生理功能则发生明显异常,常导致心律失常的发生[33-34]。
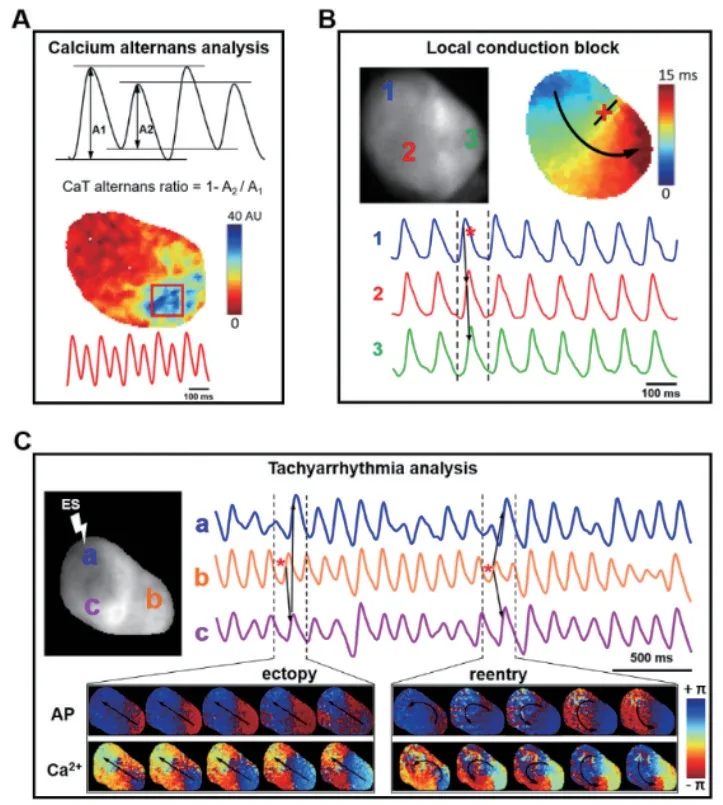
图2 心脏异常事件分析Figure 2 Analysis of abnormal cardiac events
4 光标测技术在心血管相关药物研究中的应用
目前心血管药物的研究越来越多,新型药物不断出现,许多经典药物的其它心血管作用不断被发现,非心血管药物在心血管疾病中的作用也逐渐被挖掘,光标测技术在评价这些药物的电生理功能中发挥了重要作用。比如恩格列净作为降糖药被广泛用于临床,近年来有研究表明其在心血管疾病中具有保护作用。离体心脏光标测实验发现,心梗小鼠使用了恩格列净后,其恶性心律失常和DAD 发生率明显降低,在发生快速室性心律失常时其主导频率也相应降低,提示药物干预后即使发生心律失常,其恶性程度也是明显降低的;在钙处理方面,恩格列净明显缩短了心梗小鼠的钙处理时间和钙衰减常数,提示恩格列净通过对电生理调控改善心脏功能[49]。另外,急性心肌梗死和PCI术后的缺血再灌注在临床中极为常见,二者通常出现心律失常易感性的增加,通过构建两种疾病小鼠模型,进行光标测实验发现,在缺血或梗死区,其传导速度明显减慢,且传导方向发生偏移(图2B),病变组织局部发生传导阻滞,通过雷诺嗪干预,传导速度有所恢复,传导阻滞现象明显减轻,且心律失常发生率明显降低,这提示药物通过改善心脏电传导功能降低了心律失常易感性,直接证明了药物的有效性。在大鼠无菌性心包炎模型中,作者使用白介素6(IL-6)抑制剂后发现,钙交替(图2A)程度明显减弱,空间不均一交替发生率显著降低,且雷诺定受体不应性明显恢复,心律失常发生率明显降低,提示药物通过改善钙处理减轻了大鼠心包炎致房颤的发作[50]。TAC术后小鼠心律失常易感性明显增加,在高频刺激后,其出现快速室性心律失常,光标测相位图分析发现,在快速室性心律失常时,异位激动和折返形成是介导室性心律失常的主要表现(图2C)。疾病状态下,心脏病理性改变势必导致心脏电生理重塑,光标测技术通过分析疾病状态下的高通量电生理数据,通过差异性分析,从各个层面评价药物对各电生理参数的影响,如动作电位时程的变化,动作电位传导的异常,钙处理的动力学改变等。因此,光标测技术逐渐在国内外心血管药物研究发挥了重要作用。
5 小结与展望
光标测技术作为目前研究心脏电生理的新兴技术,提供了高时空分辨率,同时获得高通量的跨膜电位和胞内钙处理的光学信号,在理解和研究心脏电生理及复杂心律失常时电传导和钙处理动力学中的作用尤为重要。然而,荧光染料和兴奋收缩解偶联剂对心脏的毒性作用,以及心脏离体后神经体液调节的缺失,难以获得完全生理状态下的电生理数据,且由于实验技术本身的限制,光标测技术目前无法直接应用于临床,仅在研究领域或临床前阶段使用,这是光标测技术目前的主要限制。随着药物研发技术的革新,不同靶分子的荧光探针被逐渐研发(如肌浆网钙指示剂Fluo-5N AM、线粒体膜电位指示剂TMRE[51-52]),高分辨率采集技术和荧光探针技术的改进,以及近几年全景光标测的提出[21,53],心脏光标测技术势必会取得日新月异的发展。相信在未来数十年,随着技术的改进,我们对心血管疾病的研究会进一步深入,对心律失常发生机制的理解和干预也会更加全面。
