肌肉参数和骨密度与髋部骨折后2年内再发髋部骨折风险的相关性分析*
2023-08-04周凤云苏永彬刘艳东黄朋举程晓光
张 薇,周凤云,苏永彬,刘艳东,黄朋举,闫 东,耿 健,尹 潞,程晓光,王 玲,3△
(1.首都医科大学附属北京积水潭医院放射科,北京 100035;2.国家心血管中心医学研究与生物信息中心,北京 102300;3.北京市创伤骨科研究所积水潭肌少症研究中心,北京 100035)
老年髋部骨折是最严重的骨质疏松性骨折,具有高致残率和死亡率,且治疗费用高昂[1-2]。而对于髋部骨折的患者,再次发生髋部骨折的风险较高,其发生率为2%~11%[3]。另外,也有研究报道髋部骨折可导致对侧再发骨折的风险增加2~4倍,并且再发骨折多发生在初次髋部骨折后2年内[4]。因此,对髋部骨折的患者进行再发髋部骨折风险评估和预防至关重要。目前很少有经证实的治疗方法来减少髋部骨折患者的再发骨折,因而再发事件的风险预测就更为重要[5]。双能X线测量仪(dual-energy X-ray absorptiometry,DXA)测量的面积骨密度(area bone mineral density,aBMD)是诊断骨质疏松和预测髋部骨折风险的重要指标,既往前瞻性研究表明低aBMD可以预测髋部骨折风险[6-7]。定量CT(quantitative CT,QCT)可测量近端体积骨密度(volumetric BMD,vBMD),它能反映骨矿物质三维分布及几何结构,可提高髋部骨折风险预测[8]。目前除了骨密度外,肌肉参数被认为是评估髋部骨折和预测再发骨折风险的重要指标[4],而基于CT测量的肌肉面积和密度与2年内髋部再发骨折风险的相关性目前尚不清楚。本研究探讨髋部骨折患者手术治疗后2年内再发髋部骨折风险与术前CT测量的肌肉参数及股骨近端骨密度间的相关性。
1 资料与方法
1.1 一般资料
所有髋部骨折的受试者都被招募参加中国第2次髋部骨折评估(CSHFE),美国临床试验注册库(NCT03461237),本研究为前瞻性纵向研究,旨在评估首次髋部骨折患者发生第2次髋部骨折的风险[9]。本研究共招募2015年5月至2016年6月北京积水潭医院收治的低能量髋部骨折患者共278例,将受试者分为2年内再发髋部骨折组(A组)、2年以上再发髋部骨折组(B组)、随访期内未再发骨折组(C组)。纳入标准:(1)发生髋关节骨折后48 h内就诊;(2)自主生活的社区成年居民;(3)髋部骨折均为低能量损伤骨折。排除标准:(1)不能独立坐立,不能独立行走(有或无辅助装置),或因为疼痛无法进行测试;(2)中风、神经系统疾病、代谢疾病、风湿病、心力衰竭、严重慢性阻塞性肺疾病和凝血功能障碍,以及其他限制功能的疾病;(3)手术后或者死亡前帕克活动能力评分(parker mobility score,PMS)<3分。采用PMS评分评估患者在第1次髋部骨折前的活动能力。2019-2020年(随访中位时间4.5年),通过电话对患者进行随访,以了解再发髋部骨折和/或死亡的发生率,并评估再发髋部骨折前或死亡前的PMS评分。如果患者既没有死亡也没有发生第2次髋部骨折,则评估电话访谈前3个月内患者的活动能力。本研究经北京积水潭医院伦理委员会批准(201512-2),患者及家属知情同意。
1.2 方法
1.2.1肌肉参数和骨密度评估
采用东芝Aquilion CT扫描仪(日本东芝公司)对所有患者进行髋关节扫描。患者呈仰卧位,扫描范围从髋臼顶部至小转子下3 cm,包括双腿。扫描参数:管电压120 kVp,管电流125 mAs,视野50 cm,矩阵512×512,层厚1 mm,标准重建算法。
肌肉测量的步骤和精度参照文献[10]。2018年9月采用OsiriX软件(Lite version 10.0.2,瑞士Pixmeo公司)测量非骨折侧股骨近端的大转子水平的臀大肌(gluteus maximus,G.Max)和第三骶椎(S3)水平的臀中小肌(gluteus medius and minimus,G.Med/Min)的肌肉横截面积(cross sectional area,CSA)和密度,见图1A、B。2017年5月采用计算机断层X射线吸收技术(version 4.2.3,美国Mindways公司)测量非骨折侧股骨近端的股骨颈(femoral neck,FN)、粗隆(trochanter,TR)、粗隆间(intertrochanter,IT)和全髋关节(total hip,TH)的aBMD,见图1C。采用医学图像分析组件软件中的股骨分析系统(MIAF,Femur Version 7.1.0,MRH,德国埃朗根纽伦堡大学)测量三维股骨颈皮质厚度(CortThick),见图1D。

A:臀大肌面积和密度;B:臀中小肌面积和密度;C:股骨近端各骨密度;D:股骨颈CortThick。
1.2.2评估活动能力
PMS评分是评估移动能力的有效可靠方法[11]。在第1次髋部骨折前(3个月内)、第2次髋部骨折前(3个月内)和未发生第2次髋部骨折的患者电话访谈前(3个月内)评估PMS评分。
1.2.3数据收集
人口统计学和人体测量学评估:年龄、性别和体重指数。健康相关:血压、高血压、既往骨折、骨关节炎、冠心病、糖尿病和抗骨质疏松治疗情况。骨质疏松症的治疗认定为服用双膦酸盐或特立帕肽。
1.3 统计学处理
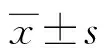
2 结 果
2.1 各组肌肉参数和骨密度比较
A组年龄高于C组(P<0.05),肌肉参数和骨密度均低于C组(P<0.05),但上述指标与B组比较无明显变化(P>0.05)。各组肌肉面积、密度及股骨近端各骨密度比较差异有统计学意义(P<0.01),见表1。
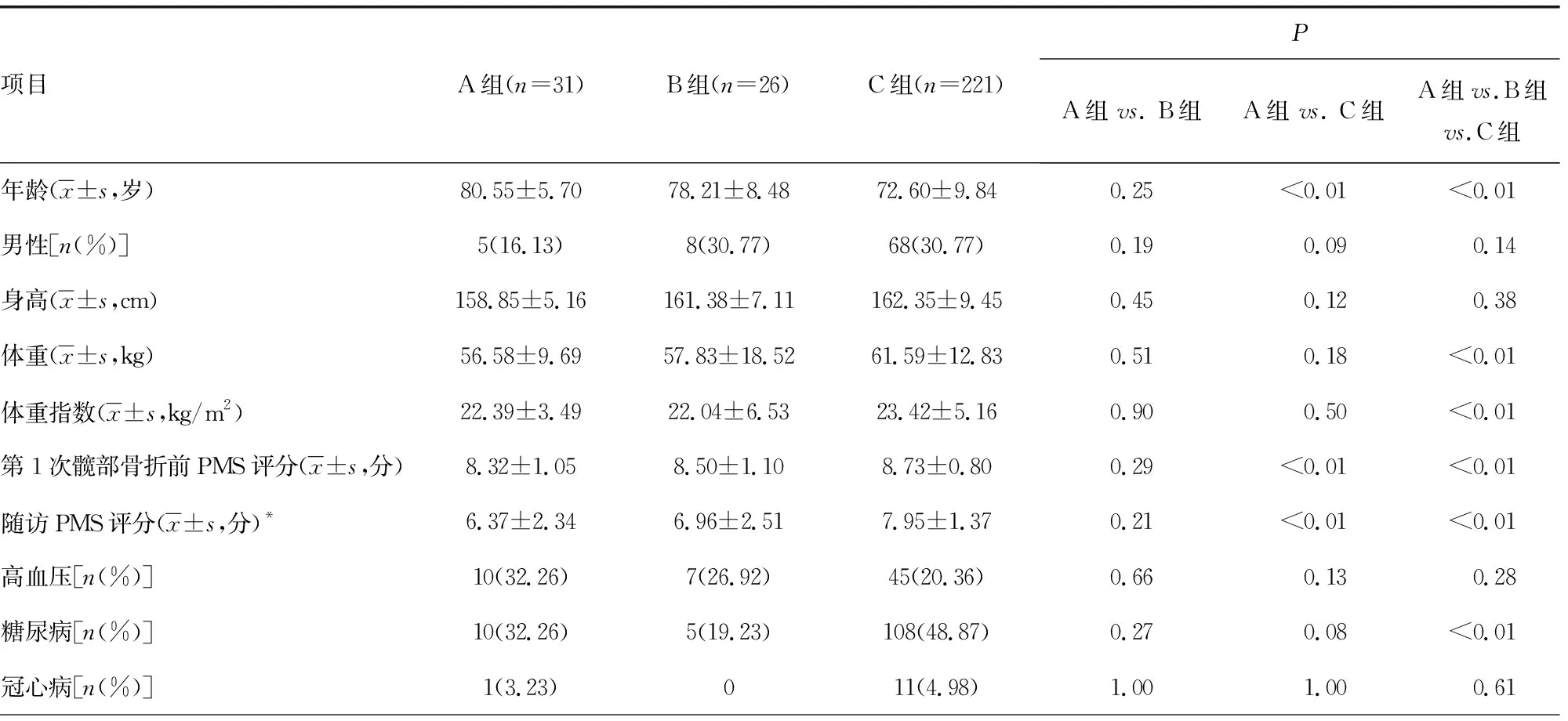
表1 各组一般资料、肌肉参数和骨密度比较
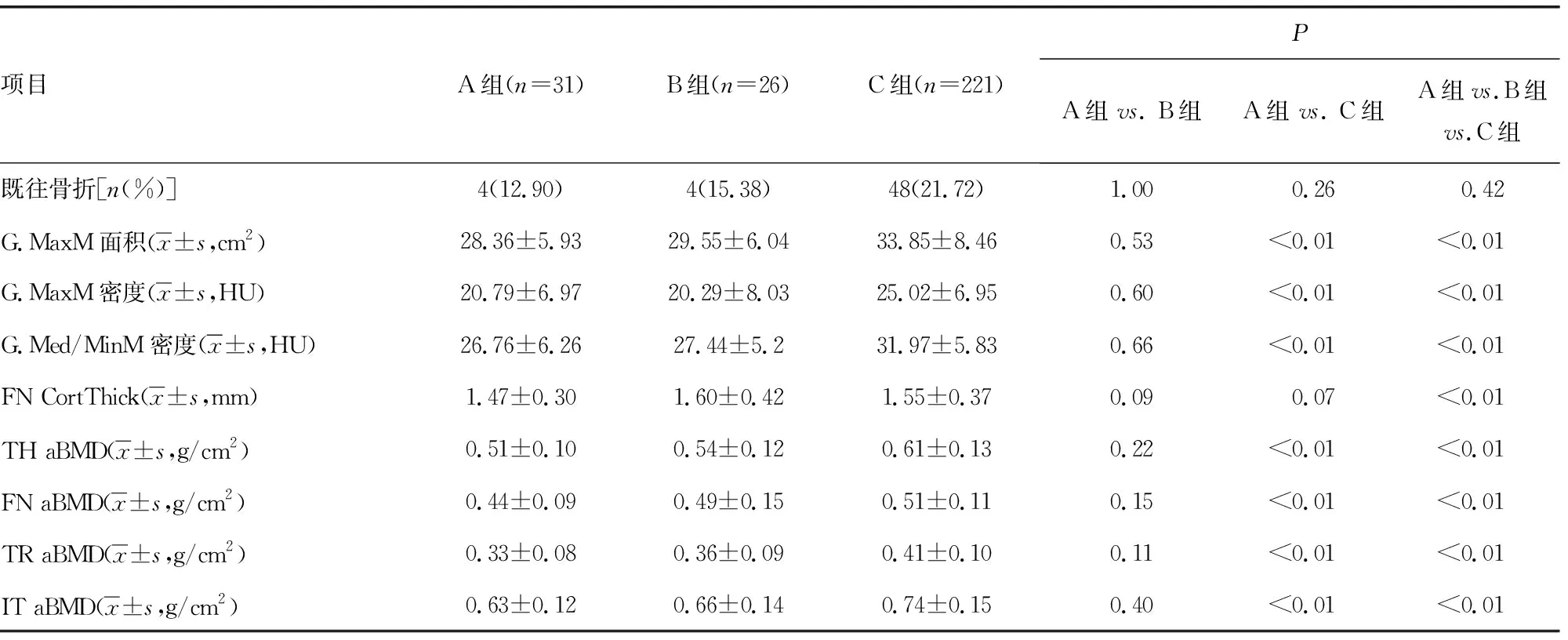
续表1 各组一般资料、肌肉参数和骨密度比较
2.2 相关性分析
G.Med/MinM密度在校正年龄、性别和第1次髋部骨折前PMS评分后仍与2年内再发髋部骨折风险相关(OR=1.88,95%CI:1.20~2.94,P=0.01),而其他肌肉参数在校正后与2年内再发髋部骨折风险无关(P>0.05)。所有骨密度参数均与2年内再发髋部骨折风险相关(P<0.05),而仅IT aBMD与2年以上再发髋部骨折风险相关(OR=1.70,95%CI:1.03~2.82,P=0.01),见表2。
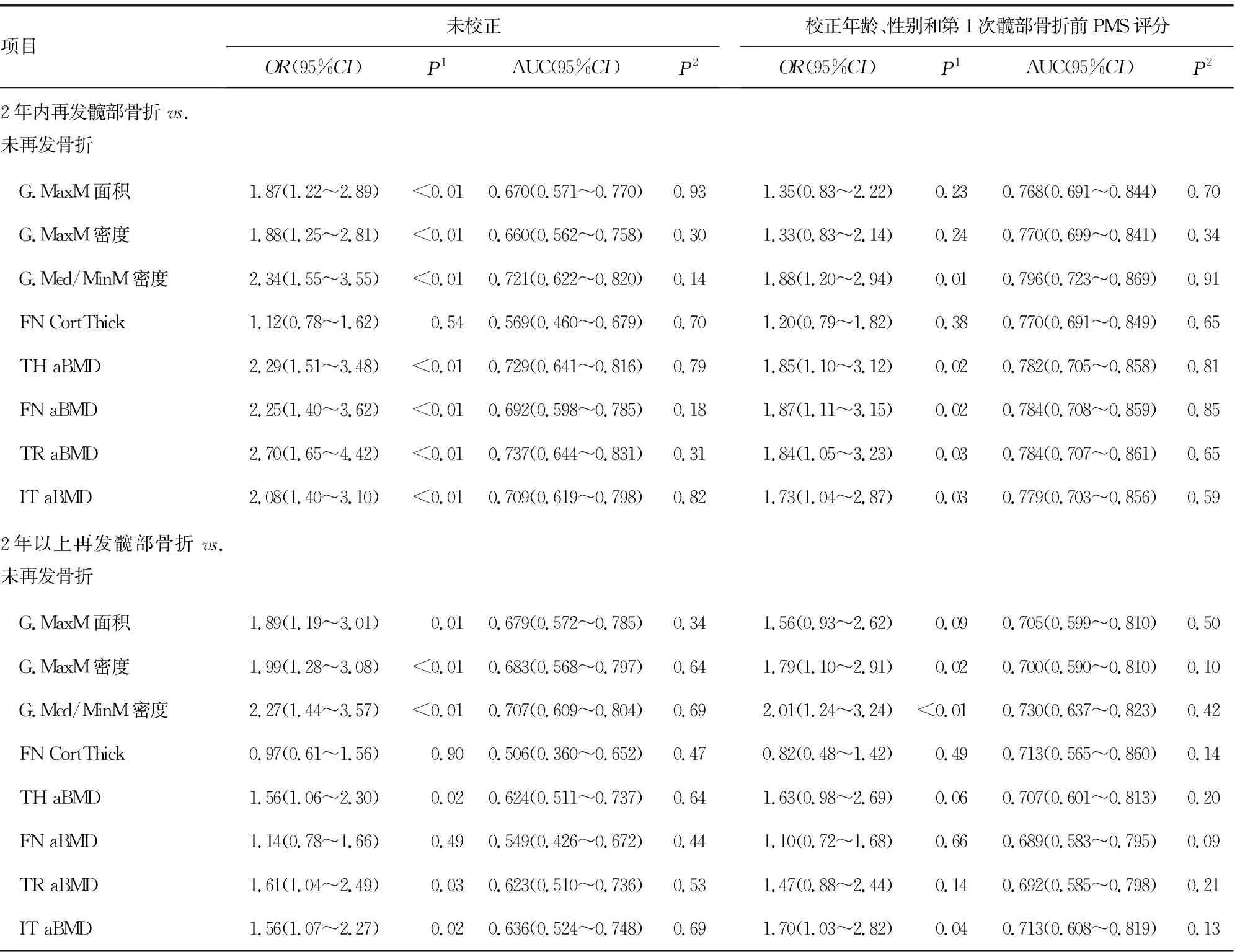
表2 肌肉参数和骨密度每降低一个标准差发生再骨折风险OR和AUC
2.3 再发髋部骨折风险模型选择
G.Med/MinM密度和TR aBMD结合的模型在校正年龄、性别和第1次髋部骨折前PMS评分后区分2年内再发髋部骨折风险效能最好,见表3。
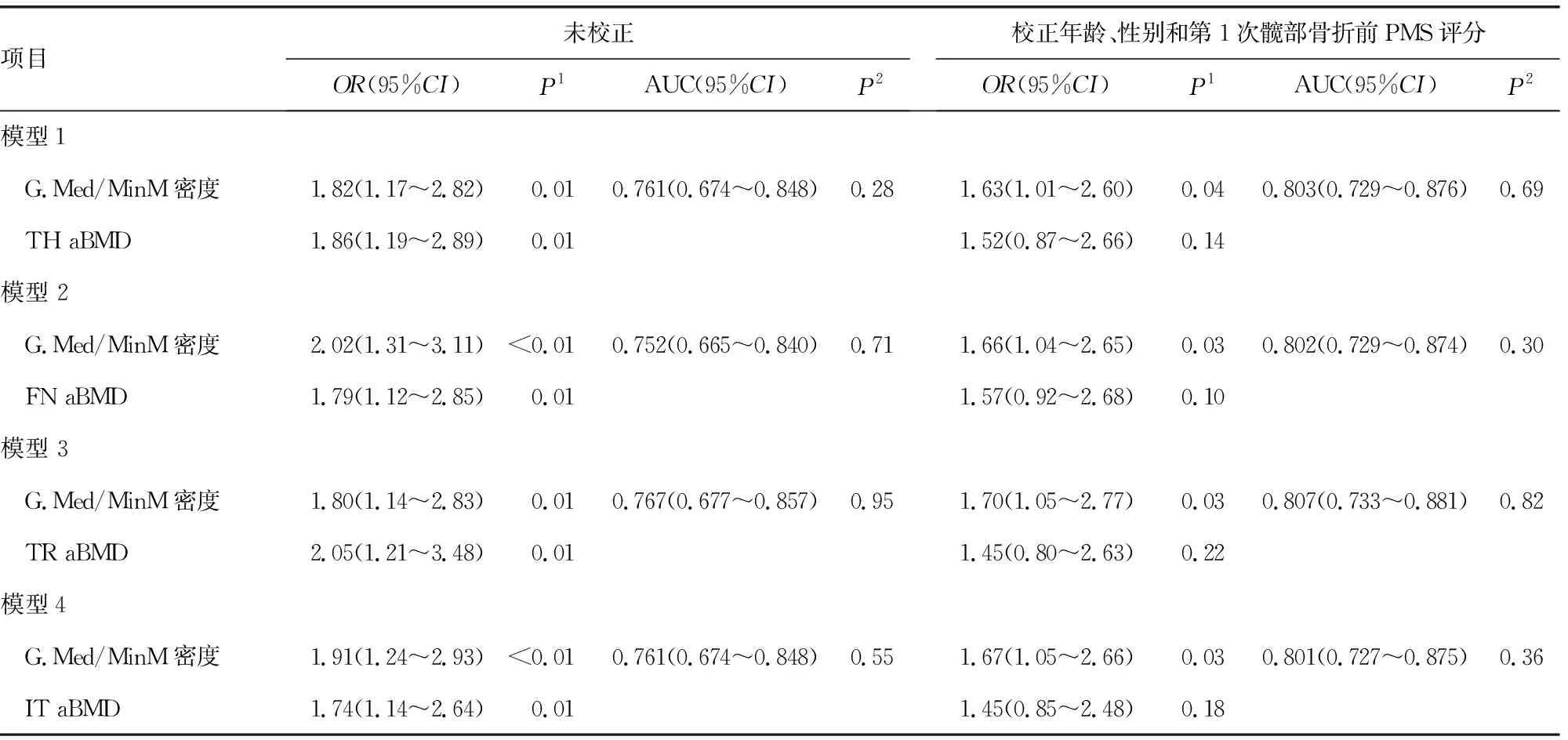
表3 肌肉参数和骨密度每降低一个标准差再发骨折风险模型选择
表中模型为2年内再发髋部骨折vs.未再发骨折;G.MaxM:臀大肌肌肉;G.Med/MinM:臀中小肌肌肉;P1:逻辑回归模型;P2:Hosmer-Lemeshow检验。
3 讨 论
老年髋部骨折患者再发髋部骨折风险较高,特别是2年内再发髋部骨折风险,这与髋部骨折患者术后的活动能力降低密切相关。老年髋部骨折患者发生再次髋部骨折后,其死亡和致残风险进一步增高,故研究老年髋部骨折患者的再发髋部骨折风险意义重大。目前文献报道中的相关风险因素,如年龄、性别、既往慢病史等[12-13],均无法进行干预,也就无从预防。而本研究中发现G.Med/MinM密度与2年内再发髋部骨折密切相关,提示加强肌肉锻炼、增强相关髋关节的肌肉质量和力量能够预防再次髋部骨折的发生,为进一步提高髋部骨折患者的诊疗效果提供了新的思路。
基于CT测量的肌肉参数包括横断面的肌肉面积和密度。肌肉密度是反映肌肉质量的重要指标,其与失能、骨折、预后等临床事件密切相关。然而肌肉密度的测量需要将肌肉间的脂肪组织剔除后计算,以消除密度很低的脂肪组织对于肌肉真实密度测量的影响。目前多采用第三方软件,如Osirix、Image J、Slice-O-matic等,或某些品牌CT的后处理工作站进行阈值分割,肌肉的阈值分割常定位-29~150 HU。但需要指出的是,该阈值范围不一定适用于所有肌肉组织。
既往有研究采用病例对照研究设计发现,髋部肌肉密度和面积或大腿肌肉间脂肪面积与髋部骨折风险相关[11,14-16],而最近一项研究[4]发现髋部肌肉密度和再发髋部骨折风险相关,但臀肌的肌肉面积和密度与2年内再发髋部骨折风险的关系则尚不清楚。因老年髋部骨折患者术后常需卧床且活动往往受限,故难以获得术后的CT或MRI等影像资料,而术前髋关节CT平扫检查是确诊髋部骨折的重要手段,并且不受骨折后体质成分变化影响,通过测量术前髋部的肌肉面积和密度,可探索性研究术前髋部CT评估骨折术后再发髋部骨折风险。本研究前瞻性地收集了术前髋关节CT平扫资料,建立了髋部骨折患者的术前肌肉测量值的基线资料,明确了低肌肉密度与老年髋部骨折患者2年内再发骨折风险相关。
骨密度在髋部骨折风险评估中占据重要地位,而目前国内外骨质疏松相关的指南中[17-18]均建议发生髋部脆性骨折后,无论患者的骨密度如何,均应积极抗骨质疏松治疗,以预防再次骨折的发生。本研究显示股骨近端的TH aBMD、FN aBMD、IT aBMD、TR aBMD均与再发髋部骨折风险相关,这符合指南中的临床实践。
本研究存在以下局限性:(1)2年内再发髋部骨折的样本量较小,今后尝试扩大样本量后进一步核实研究结果;(2)髋部骨折患者的日常活动能力和营养状况未评估;(3)基于CT测量的肌肉面积和密度均为单层面CT图像测量,而肌肉的功能应从整块肌肉的三维角度分析,这有待未来人工智能自动分割软件实现后进一步分析。
综上所述,G.Med/MinM密度与2年内再发髋部骨折风险密切相关,髋部肌肉质量评估可用于再发髋部骨折的风险预测。
