细胞外囊泡在泌尿系肿瘤诊断中的研究进展
2023-08-04金久凯庞百仞蒋军辉
金久凯,庞百仞,蒋军辉
作者单位: 315211 宁波,宁波大学医学部(金久凯);宁波大学附属第一医院(庞百仞、蒋军辉)
前列腺癌(PCa)、膀胱癌(BCa)和肾癌是最常见的三大泌尿系肿瘤,尽管目前早期发现肿瘤的比例越来越高,但仍需要新的生物标志物来提升泌尿系肿瘤的诊断效果。本文对细胞外囊泡(EV)不同亚型、表征方法、泌尿系肿瘤EVRNA标志物及临床应用前景进行综述,为未来泌尿系肿瘤诊断中应用新的生物标志物提供思路。
1 泌尿系肿瘤概况
1.1 PCa 近年来中国PCa患者显著增加,2022 年预计死亡人数达56239 例[1]。前列腺特异性抗原(PSA)已被广泛用于筛查PCa,但PSA敏感性特异性不强,早期检出率较低。MRI 等影像学方法无法做到早期诊断。前列腺穿刺活检即使采用多点活检仍可能有较高的假阴性率。
1.2 BCa BCa 发病率及死亡率高居前列。膀胱镜检查是BCa 初步诊断的首选。细胞学检查因其极高的特异性也是初始检查的重要方式。核基质蛋白(NMP22)、膀胱肿瘤抗原(BTA)等尿液标志物和增强成像目前并未十分成熟[2]。
1.3 肾癌 肾癌绝大多数为肾细胞癌(RCC),死亡率为30%~40%,而PCa 和BCa 的死亡率约为20%[3]。早期RCC大多无症状,发现主要依赖于影像学检查,目前暂无公认的用于RCC 早期诊断的肿瘤标志物。
1.4 其他 肾盂癌和输尿管癌等上尿路尿路上皮癌(UTUC)并不常见,无创诊断方法也并未满足临床需求。
早期诊断泌尿系肿瘤可以显著降低死亡率并挽救生命,然而现有的诊断策略并非令人满意。因此研发一种高灵敏度和高特异性的方法来补充诊断泌尿系肿瘤迫在眉睫。
2 EV 及不同亚型
EV 是由各种细胞类型分泌的纳米级细胞器样膜囊泡,由磷脂双分子层包裹,其含有核酸、蛋白质和脂质等,可动态参与细胞间通讯[4]。几乎所有细胞都会释放EV 到细胞外空间,它携带来自原始细胞的复杂生物信息,是以无创方式进行肿瘤诊断的重要来源[5]。近来发现细胞会释放多种EV 亚型并具有不同的生物特性和生物学功能。本文采用大小划分EV 并介绍了最新进展,见图1。
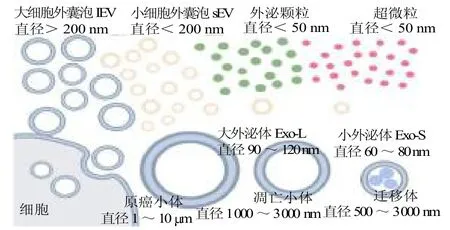
图1 EV 不同亚型
2.1 大细胞外囊泡(lEV,直径>200 nm) lEV 根据自身特征可分为迁移体(500 ~3 000 nm)、凋亡小体(1 000 ~5 000 nm)和原癌小体(1 ~10m)。
2.1.1 迁移体 迁移体是在迁移细胞收缩纤维上形成的囊泡,其中还包含直径50 ~100nm的小泡,因此也被称为石榴体(PLS)。除了参与细胞迁移,它在稳态维持、物质传递、信号整合等方面也起重要作用[6]。
2.1.2 凋亡小体 凋亡小体是相对较大尺寸的泡状小体,主要在细胞凋亡过程中产生。近年来发现它也参与细胞清除、组织稳态、免疫等诸多过程[7]。
2.1.3 原癌小体 原癌小体是另一类肿瘤衍生的EV,其有着非典型的大尺寸及丰富的致癌内容物,负责致癌信号的细胞间转移,并与PCa 密切相关[8]。
2.2 小细胞外囊泡(sEV,直径<200 nm) 外泌体是最具代表性的sEV,直径30~150nm,通过传递核酸、蛋白质和脂质等货物来调节细胞内通讯[9]。Zhang 等[10]鉴定出两个外泌体亚群:直径为90~120nm的大外泌体(Exo-L)和直径为60 ~80nm 的小外泌体(Exo-S),二者具有不同的分子特性,动物实验表现出不同的生物分布,表明它们在细胞间通讯中可能具有不同的功能。
2.2.1 外泌颗粒 Zhang 等[10]首先提取了一种直径35nm 的纳米颗粒,命名为“外泌颗粒”。它与sEV 相比,表现出不同的蛋白质、脂质、核酸谱,主要与肝脏中细胞融合,并可改变靶细胞的免疫功能。
2.2.2 超微粒 Zhang 等[11]鉴定了另一种细胞外纳米颗粒,其从前述“外泌颗粒”的上清液中提取出,并被命名为“超微粒”。它在形态和分子上与外泌颗粒不同,在体内显示出更高的富集,并且富含多种潜在的生物标志物,可能与癌症有着紧密联系。
3 细胞外囊泡的表征
3.1 表面等离子体共振(SPR) SPR传感器代表EV表征中的一种新方法,具有无标记实时检测和少样品处理的优点。Min 等[12]开发了一种名为“nPLEX-FL”的纳米等离子体传感平台,该平台通过使用金纳米孔提高灵敏度,对单个EV 上的目标表面和内部标记进行多重分析。Chen 等[13]报告了一种基于水凝胶-AuNP超分子球(H-Au)的SPR 生物传感器用于分析PCa 衍生的EV,并在人血清分析中表现出较好的实用性。
3.2 EV 成像的显微镜技术 近年来用于EV可视化的显微镜技术取得了巨大进步。Goughnour 等[14]通过实验证明了冷冻电镜与免疫金标记相结合,提供有关EV携带特定分子的证据。Bairamukov 等[15]应用AFM 技术来研究空气和液体中不同EV亚型的纳米力学特性,它们的显著差异为正确区分EV亚型提供了新的支持。
3.3 电阻脉冲传感(RPS) 可调RPS(TRPS)检测通过纳米孔颗粒的电阻来对EV 的尺寸和浓度进行测量。改进这项技术得到了微流控电阻脉冲传感(MRPS),二者不同之处在于MRPS 使用的滤芯是刚性预校准孔,而TRPS 使用的传感孔可以拉伸以调整孔径。Cimorelli等[16]开发了一种可重复的操作程序,应用MRPS 探索测量粒径分布的最佳稀释剂和样品稀释度。
3.4 纳米流式细胞术(nanoFC) nanoFC与传统FC相比,较小的通道减少背景信号,较低的系统压力增加颗粒的停留时间,从而增强信号的集成。Liu 等[17]通过nanoFC 同时实现单个EV(可低至40nm)的光散射和荧光检测,分析结直肠癌和鼻咽癌细胞系单囊泡水平的EV-DNA,同样该技术有望用于泌尿系肿瘤。
3.5 拉曼光谱(RS) RS是一种基于激光与分子振动相互作用的无标记光谱,能够在几乎没有预处理步骤的情况下分析样品。Qian等[18]使用表面增强RS(SERS)来快速准确地分析EV,发现血清衍生的EV诊断泌尿系肿瘤具有很高的准确性。
虽然EV 表征方法取得了巨大进步,但目前还无法做到精准鉴别EV 及其亚型。对于高异质性的EV 亚型及共分离的非EV 杂质,现有表征方法易将其归为一类,极大干扰后续EV 生物特性、所发挥的功能机制和工程化治疗的研究。高效、快速地检测和表征分析EV 的技术仍需探索。
4 泌尿系肿瘤诊断相关的EV RNA 标志物
LI 等[19]指出血浆miR-141-5p 有希望区分PCa,曲线下面积(AUC)为0.652;对于miR-125a-5p,AUC为0.691;而二者比值AUC值为0.793,比单一应用更合适。miR-217、miR-23b-3p、miR-30b-3p、miR-126-3p和circ_0044516 都有作为PCa潜在标志物的能力[20-22]。Li 等[23]发现miR-375、miR-451a、miR-486-3p 和miR-486-5p 可用于区分PCa 与健康对照者。Gan 等[24]得出PCA3 联合PSMA 是区分PCa 患者和健康者的最佳组合(AUC 为0.870)。ERG、PSMA、PCA3、CK19和EpCAM 在PCa 中也有诊断潜力。
研究发现lncLNMAT2、TERC、miR-19b1-5p、136-3p 及139-5p 可区分BCa 与健康对照组[25-27]。不同的RNA组合诊断性能优于尿液细胞学检查,可为诊断BCa 提供较高的敏感度和特异性[28-29]。Abbastabar 等[30]提出ANRIL 和PCAT-1 诊断BCa 时AUC为0.7229 和0.7292。El-Shal 等[31]指出miR-96-5p 和miR-183-5p 联合诊断BCa 的敏感度为88.2%,特异性为87.8%,均高于独自使用。Lin 等[32]验证了miR-93-5p、miR-516a-5p 的BCa 诊断性能,AUC 为0.838 和0.790,也显著高于尿液细胞学检查(0.630)。
Xiao等[33]对RCC和健康个体的血浆衍生EV进行高通量测序,揭示has-miR-92a-1-5p、has-miR-149-3p 和hasmiR-424-3p差异表达且具有诊断价值。miR-155和miR-224-5p作为尿RCC 诊断的EV 生物标志物也有潜在价值[34-35]。
5 临床应用难点及解决方案
5.1 分离过程 因EV不同的理化特性,样品预处理的标准化是EV 分离与检测中的一大挑战。临床样本中的EV 是一种目标和非目标EV 的混合物,不同分离技术得到的EV 不尽相同,也很难说哪种方法是最佳选择[36]。此外,很难从生物体液中分离出纯粹的EV,干扰物会影响样品纯度。因此,需要综合考虑产量、纯度和分离效率来选取最适合的EV 分离和表征方法。Tzaridis 等[37]建议将尺寸排阻色谱与超速离心相结合作为人血浆或血清生物标志物研究的首选EV分离方法。Van 等[38]报告了一种“双模式色谱”的新分离方法通过去除脂蛋白来提高EV 蛋白分析的准确性。5.2 EV 的高度异质性 从癌症中释放的EV 在大小、表面蛋白和其他成分方面都是异质的,即便是从同一细胞释放的EV 亚型也具有多样性[39]。应用单囊泡分析的单EV 研究是目前的最新研究方向,单囊泡检测可进一步明确单个EV 的特征。单EV 的功能及特性尚未完全明确,其较强的异质性可能源于EV 生物发生的随机机制[40]。Kim 等[41]使用基于“EV-Ident”的单囊泡分析方法来了解EV 异质性,并成功鉴定出PCa EV 的三种不同尺寸亚型。
6 总结与展望
早期诊断泌尿系肿瘤是提高患者生存率和预后的关键因素。目前以单囊泡分析为代表的新兴检测和分析方法在不断揭示EV 的内在特征,大量可能用于诊断泌尿系肿瘤的EV 生物标志物也在不断涌现,鉴于EV 在临床方面的巨大潜力,EV 用于诊断泌尿系肿瘤或许并不遥远。
利益冲突 所有作者声明无利益冲突
