埃索美拉唑诱导宫颈癌细胞增殖、迁移、侵袭和凋亡作用及机制
2023-08-01范佳杨蔡鑫熊蓉梁宵梁婷冯刚刘康罗岳西
范佳杨,蔡鑫,熊蓉,梁宵,梁婷,冯刚,刘康,罗岳西
(川北医学院第二临床学院南充市中心医院 1.妇产科,2.组织工程与干细胞研究所,3.肿瘤生物治疗南充市重点实验室,四川 南充 637000)
宫颈癌是女性最常见的恶性肿瘤之一,全球发病率仅次于乳腺癌,死亡率也位居第二[1]。据世界卫生组织国际癌症研究机构(IARC)发布的2020 年全球最新癌症数据,每年有近53万例新确诊宫颈癌患者,中国病例>13万例,且发病年龄逐渐呈年轻化趋势,严重危害女性健康[2-3]。当前对宫颈癌的治疗通常采用以手术、放疗、化疗或三者联合治疗为主的综合治疗模式,但由于放化疗及药物产生的不良反应和耐药等问题,患者的长期预后并未得到显著改善[4-5],且由于抗肿瘤药物价格昂贵,对患者家庭造成严重的经济负担。因此,筛选高效、不良反应较低且价格低廉的药物已成为抗肿瘤研究的热点方向。
肿瘤细胞与正常细胞的代谢途径存在很大差异,在恶性增殖过程中,肿瘤细胞的能量代谢途径由三羧酸循环为主转变为糖酵解为主,糖酵解产生大量酸性物质,即Warburg 效应。肿瘤微环境是影响细胞代谢的众多因素之一,也是肿瘤细胞赖以生存的综合内环境,在肿瘤的发生发展中起关键作用[6]。肿瘤细胞特殊的代谢途径通常导致微环境内大量H+积累且无法有效清除[7],引起肿瘤微环境酸中毒[8]。酸性外环境可为肿瘤的发生发展提供相对适宜的环境,增加肿瘤的侵袭力,促进肿瘤新生血管的形成[9]。由于酸性细胞外环境是几乎所有癌症的共同特征,因此抗酸治疗很可能是一种非常重要和有希望的新的癌症治疗方法。
质子泵抑制剂(proton pump inhibitor,PPI)是常用的上消化道疾病治疗药物,除抑制胃黏膜上皮H+-K+-ATP 泵外,还非特异性抑制其他质子泵,抑制肿瘤细胞内H+外排,从而诱发多种肿瘤细胞凋亡[10-12]。目前已有研究表明,PPI 对肿瘤细胞的增殖、侵袭和迁移能力具有一定抑制作用[13]。
埃索美拉唑(esomeprazole,ESO)是目前抑制效应最强的PPI质子泵抑制剂,具有肝首过效应低、血浆药物浓度高和血浆清除率低等优点,具有较高的生物利用度。近年来研究发现,ESO 对多种肿瘤细胞有抑制作用,如乳腺癌T41 和TS/A 细胞[14-15]、胶质母细胞瘤LN229 细胞[16]及胃癌AGS 细胞[17]等,然而其对宫颈癌细胞的作用及机制研究较少。本研究旨在探讨ESO对宫颈癌细胞增殖、迁移和侵袭等生物学行为的作用,并进一步探讨其潜在机制,以期为该药在宫颈癌治疗中的运用提供实验依据。
1 材料与方法
1.1 药物、试剂和主要仪器
ESO(每支40 mg,批号:K1911131),阿斯利康制药有限公司。胎牛血清、MEM、DMEM 培养基和胰蛋白酶消化液,美国Hyclone 公司;CCK-8 试剂盒,江苏凯基生物技术股份有限公司;MatrigelTM,美国BD 公司;Transwell 小室,美国Corning 公司;AnnexinⅤ-FITC/PI 细胞凋亡检测试剂盒,南京诺唯赞生物科技有限公司;BCA试剂盒,上海碧云天生物技术公司;结晶紫、PI和RIPA裂解液,美国Sigma公司;兔抗大鼠胱天蛋白酶3单克隆抗体,美国NEB公司;兔抗人磷脂酰肌醇3 激酶(phosphoinositide 3-kinase,PI3K)、磷酸化PI3K(phosphorylated-PI3K,p-PI3K)、兔抗人蛋白激酶B(protein kinase B,Akt)和p-Akt 多克隆抗体及小鼠抗人Bcl-2 单克隆抗体,英国Abcam 公司;辣根过氧化物酶标记的山羊抗小鼠IgG 抗体和山羊抗兔IgG 抗体,杭州联科生物技术有限公司。
3111 型CO2恒温细胞培养箱、Thermo ST40R离心机和Thermo 1300-A2超净工作台,美国Thermo公司;HH-S4 数显恒温水浴箱,江苏金城国胜实验仪器厂;TS100F 倒置荧光显微镜,日本Nikon 公司;ST-360 酶标仪,上海科华实验系统有限公司;BD FACSCaliburTM流式细胞仪,美国Becton Dickinson公司;电转仪及转膜系统,美国Bio-Rad公司。
1.2 细胞和细胞培养
人宫颈上皮永生化细胞株H8 细胞和人宫颈癌SiHa 细胞购自中国科学院干细胞库;人宫颈癌HeLa 细胞由川北医学院实验室提供。H8 和SiHa细胞用含10%胎牛血清的MEM 培养基培养,HeLa细胞用含10%胎牛血清的DMEM 培养基培养,3 种细胞均放置在5%CO2,37℃恒温细胞培养箱内培养。
1.3 CCK-8检测细胞存活率
取对数生长期的SiHa,HeLa 和H8 细胞,用胰酶消化、重悬,细胞计数后,以每孔4×103细胞分别接种在96孔板中。细胞培养24 h后,用ESO〔0(细胞对照组),60,80 和100 mg·L-1〕分别孵育24,48和72 h,每组设3复孔,放置于培养箱中。各孔分别加入100 μL CCK-8 工作液,37℃孵育1 h,用全自动酶标仪测定波长450 nm 处的吸光度(A450nm)值。细胞存活率(%)=(实验组A450nm-空白组A450nm)/(细胞对照组A450nm-空白组A450nm)×100%。
1.4 划痕实验检测细胞迁移率
选用对数生长期的SiHa 和HeLa 细胞,分别以每孔5×104接种在6 孔板中,待细胞完全贴壁融合后,用无菌枪头垂直于孔底均匀划线,用PBS 轻柔洗去悬浮细胞,用ESO(0,60,80 和100 mg·L-1)分别处理细胞24和48 h,于倒置显微镜下观察划痕愈合情况并拍照。细胞迁移率(%)=(初始划痕宽度-测量时划痕宽度)/初始划痕宽度×100%
1.5 Transwell 实验检测侵袭细胞数
用无血清培养基以4∶1 的比例稀释基质胶,取100 μL稀释后的基质胶铺于Transwell上室。SiHa和HeLa 细胞用无血清培养基调整细胞密度至1×109L-1,取100 μL细胞悬液接种在Transwell上室内,下室加入600 μL含10%血清的培养基,分别加ESO(0,60,80 和100 mg·L-1)置于37℃培养箱内孵育48 h,取出上室并吸出其内的培养基,擦去仍未穿透上室的细胞,浸泡于20%甲醇内固定15~20 min,用0.1%结晶紫染色30 min,PBS 清洗后在显微镜下观察并拍照,使用Image J 软件进行细胞计数。
1.6 流式细胞仪检测细胞凋亡率
SiHa 和HeLa 细胞同1.5 分组和处理,用胰酶消化后重悬细胞,根据凋亡试剂盒说明书操作,将Annexin Ⅴ-FITC试剂和PI染液各5 μL加入400 μL结合缓冲液中,混匀后避光室温孵育15~20 min,用流式细胞仪检测细胞凋亡率。
1.7 Western 印迹法检测Bcl-2 和胱天蛋白酶3 蛋白表达水平及Pl3K和Akt蛋白磷酸化水平
SiHa 和HeLa 细胞分组处理同1.5,收集细胞,提取蛋白质,根据BCA 法定量蛋白浓度。各组蛋白样品经SDS-PAGE 凝胶电泳和半干法转膜后,用5%脱脂牛奶室温封闭1 h,加入一抗〔稀释倍数:Bcl-2(1∶2000)、胱天蛋白酶3(1∶2000)、Akt(1∶2000)、p-Akt(1∶3000)、PI3K(1∶2000)、p-PI3K(1∶2000)、β 微管蛋白(1∶5000)〕,4℃孵育过夜,加入二抗(1∶2000)室温孵育1 h,漂洗3 次后滴加化学发光液显色,于凝胶成像系统下成像。采用Image J软件对蛋白条带进行积分吸光度(integrated absorbance,IA)值分析,以目标蛋白与内参蛋白条带IA值的比值表示目标蛋白相对表达水平;以磷酸化蛋白与总蛋白条带IA值的比值表示蛋白磷酸化水平。
1.8 统计学分析
实验结果数据用x±s表示,使用SPSS 26.0 和GraphPad Prism8 软件进行统计学分析和绘图。采用单因素方差分析,组间两两比较采用t检验。P<0.05表示差异具有统计学意义。
2 结果
2.1 ESO对SiHa,HeLa和H8细胞存活率的影响
CCK-8 结果(图1)显示,与细胞对照组相比,ESO 作用于宫颈癌SiHa 和HeLa 细胞48 h 后,ESO 80 和100 mg·L-1组细胞存活率均显著降低(P<0.01);72 h 后,ESO 60,80 和100 mg·L-1组细胞存活率显著降低(P<0.01)(图1A和1B),而不同浓度ESO 作用于正常宫颈细胞H8 24,48 和72 h 后,各给药组细胞存活率无显著差异(图1C)。表明ESO 可抑制SiHa 和HeLa 细胞的增殖,对正常宫颈细胞H8无抑制作用。

Fig.1 Effect of esomeprazole(ESO)on viability of SiHa(A),HeLa(B)and H8(C)cells by CCK-8 assay. SiHa,HeLa and H8 cells were treated with ESO 60,80 and 100 mg·L-1 for 24,48 and 72 h,respectively. Cell viability(%)=(A450 nm of ESO group-A450 nm of blank group)/(A450 nm of cell control group-A450 nm of blank group)×100%.±s,n=3. **P<0.01,compared with cell control group.
2.2 ESO对SiHa和HeLa细胞迁移能力的影响
划痕实验结果(图2)显示,与细胞对照组相比,ESO 分别处理SiHa 和HeLa 细胞24 或48 h 后,ESO 60,80 和100 mg·L-1组细胞迁移率均显著下降(P<0.01),表明ESO 可抑制SiHa 和HeLa 细胞的迁移能力。

Fig.2 Effect of ESO on migration of SiHa(A)and HeLa(B)cells. SiHa and HeLa cells were treated with ESO 60,80 and 100 mg·L-1 for 24 and 48 h. A2 and B2 were the quantitative results of A1 and B1,respectively. Cell migration rate(%)=(0 h scratch area-24 or 48 h scratch area)/0 h scratch area×100%.x±s,n=3.**P<0.01,compared with cell control group.
2.3 ESO对SiHa和HeLa细胞侵袭能力的影响
Transwell 侵袭实验结果(图3)显示,SiHa 和HeLa 细胞经ESO 处理48 h 后,与细胞对照组相比,ESO 60,80和100 mg·L-1组侵袭细胞数均显著减少(P<0.05,P<0.01)。表明ESO 可抑制SiHa 和HeLa细胞侵袭。

Fig.3 Effect of ESO on invasion of SiHa(A)and HeLa(B)cells by transwell assay. SiHa and HeLa cells were treated with ESO 0(cell control),60,80 and 100 mg·L-1 for 48 h.A2 and B2 were the quantitative results of A1 and B1,respectively.x±s,n=3.*P<0.05,**P<0.01,compared with cell control group.
2.4 ESO对SiHa和HeLa细胞凋亡的影响
流式细胞仪检测结果显示(图4),经ESO 处理48 h后,与细胞对照组相比,ESO 60,80和100 mg·L-1组细胞凋亡率显著升高(P<0.05,P<0.01),提示ESO可促进SiHa和HeLa细胞凋亡。

Fig.4 Effect of ESO on apoptosis of SiHa(A)and HeLa(B)cells by flow cytometry. See Fig.3 for the cell treatment. A2 and B2 were the quantitative results of A1 and B1,respectively.±s,n=3. *P<0.05,**P<0.01,compared with cell control group.
2.5 ESO 对SiHa 和HeLa 细胞胱天蛋白酶3 和Bcl-2蛋白表达的影响
Western 印迹结果(图5)显示,经ESO 处理48 h后,与细胞对照组相比,ESO 60,80,100 mg·L-1组SiHa和HeLa细胞胱天蛋白酶3表达水平明显上升(P<0.01),Bcl-2表达水平明显下降(P<0.01)。
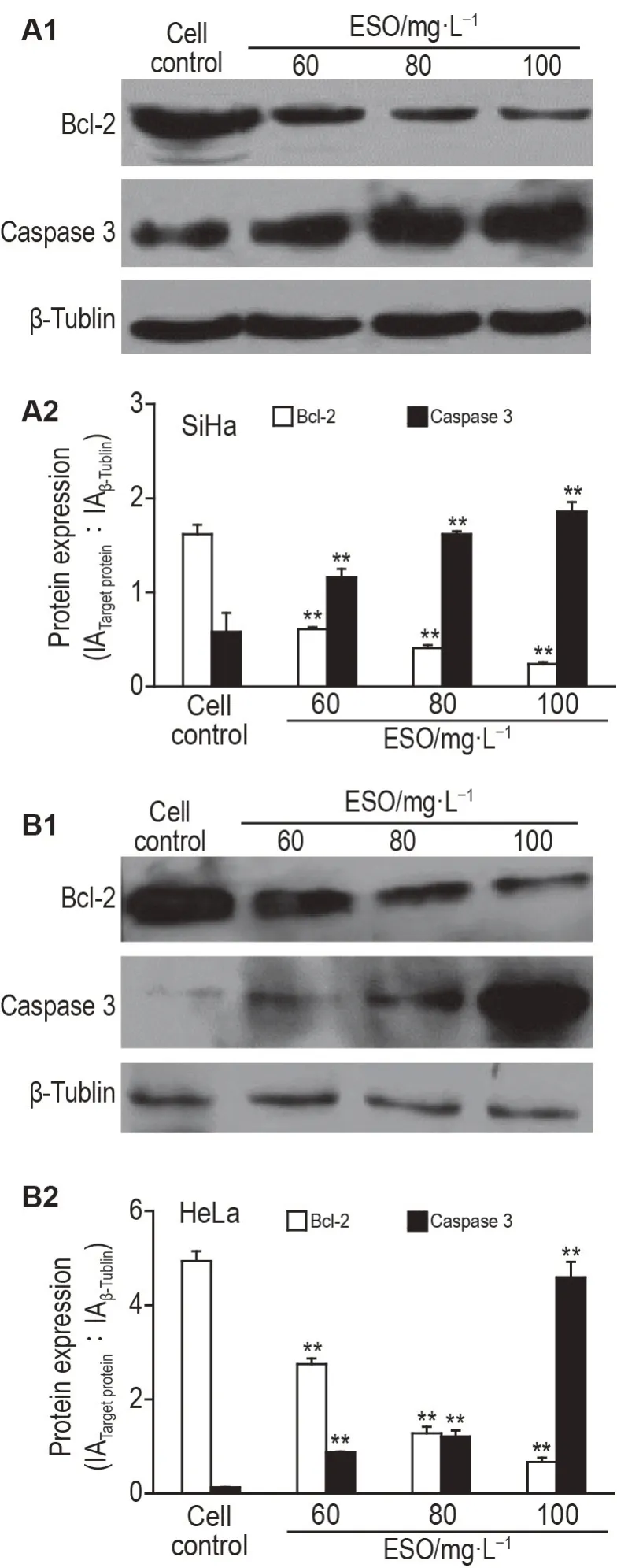
Fig.5 Effect of ESO on expression levels of caspase 3 and Bcl-2 in SiHa(A)and HeLa(B)cells by Western blotting. See Fig.3 for the cell treatment. A2 and B2 were the quantitative results of A1 and B1,respectively. IA:integrated absorbance.x±s,n=3.**P<0.01,compared with cell control group.
2.6 ESO 对SiHa 和HeLa 细胞Pl3K 和Akt 蛋白磷酸化的影响
Western印迹结果(图6)显示,经ESO处理48 h后,与细胞对照组相比,ESO 60,80 和100 mg·L-1组SiHa 和HeLa 细胞Akt 和PI3K 蛋白磷酸化水平明显降低(P<0.05,P<0.01)。

Fig.6 Effect of ESO on phosphorylation levels of protein kinase B(Akt)and phosphoinositide 3-kinase(Pl3K)in SiHa(A)and HeLa(B)cells by Western blotting.See Fig.3 for the cell treatment. A2 and B2 were the quantitative results of A1 and B1,respectively.±s,n=3. *P<0.05,**P<0.01,compared with cell control group.
3 讨论
本研究结果显示,正常宫颈细胞H8 细胞在长时间和高剂量ESO 作用下,细胞存活率并不随着药物浓度的升高而呈现明显下降,表明ESO对正常宫颈细胞无明显毒性作用。而经ESO 处理后,宫颈癌SiHa 和HeLa 细胞的增殖、迁移和侵袭能力均受到明显抑制,细胞凋亡率增加,PI3K/Akt 信号通路受到抑制。
细胞凋亡失衡是导致肿瘤无限增殖的重要因素之一,故调控细胞凋亡途径是抗肿瘤的重要策略[18]。细胞凋亡是一种程序性细胞死亡,通常存在线粒体[19-20]、内质网[21]和死亡受体[22]3 条通路。Bcl-2 蛋白家族在细胞线粒体凋亡中发挥着重要作用[23]。胱天蛋白酶家族是存在于细胞质中具有高度同源性的蛋白酶,其中胱天蛋白酶3 是细胞凋亡途径上的终末剪切酶,是细胞发生凋亡的标志性蛋白[24],同时也是Bcl-2 的下游蛋白。胱天蛋白酶3在内源性通路中的激活可以调控细胞凋亡的启动与执行[25]。本研究结果显示,经ESO 处理后,Bcl-2蛋白表达水平明显降低,胱天蛋白酶3 表达水平明显增加,表明ESO可能通过降低Bcl-2和增加胱天蛋白酶3的表达促进宫颈癌SiHa和HeLa细胞凋亡。
肿瘤的发生发展是由多种信号通路共同作用的复杂过程,其中PI3K/Akt 信号通路是人类癌症中最常被激活的信号通路之一[26]。既往研究表明,PI3K/Akt 信号通路能影响肿瘤细胞侵袭、迁移能力,在调控细胞的增殖和代谢等方面发挥着重要作用[27]。PI3K是存在于细胞质的一种脂类激酶,可被多种细胞外信号激活。Akt 是PI3K 的下游蛋白之一,参与细胞增殖、迁移、侵袭等多种生物过程[28]。Akt在多种肿瘤细胞中被异常激活,参与肿瘤的发生与发展[27]。Chen等[29]研究表明,胃癌细胞SGC7901经质子泵抑制剂预处理后,PI3K/Akt 信号通路被抑制。本研究结果显示,宫颈癌SiHa 和HeLa 细胞经ESO 处理后,PI3K 和Akt 磷酸化受到抑制,表明ESO 可能通过抑制PI3K/Akt 通路,从而诱导细胞凋亡。
综上所述,ESO可抑制人宫颈癌SiHa和HeLa细胞的增殖、迁移和侵袭,同时诱导细胞凋亡,该作用可能与抑制PI3K/Akt 信号通路有关。但本研究仅在细胞水平进行了探讨,存在局限性,后续还需在体内实验中进行进一步验证,为ESO 用于临床治疗宫颈癌提供新思路。
