新型褪黑素1型和2型受体激动及5-羟色胺2C受体拮抗剂GW117抗抑郁、抗焦虑作用及机制
2023-08-01杨雅琪杨秋实木热扎提提力瓦尔地高娜娜顾为李晓蓉金增亮
杨雅琪,杨秋实,木热扎提·提力瓦尔地,高娜娜,顾为,李晓蓉,金增亮
(1.首都医科大学基础医学院,北京 100069;2.首都医科大学附属北京朝阳医院药事部,北京 100020;3.首都医科大学附属北京世纪坛医院胃肠外科与临床营养科,北京 100038;4.北京广为医药科技有限公司,北京 100044)
抑郁症是以显著、持续的情绪低落和快感缺失为主要症状的一种精神障碍,是目前患病率最高的精神疾病。据统计,目前全球患病人数约3.4 亿,中国有超过9500万抑郁症患者,预计到2030年,抑郁症疾病负担将排全球第一[1-2]。抑郁症患者经常伴有焦虑和睡眠障碍,包括焦虑在内的多种精神疾病均与抑郁症高度相关[3]。抑郁症病理生理机制复杂,目前经典假说主要有单胺假说、下丘脑-垂体-肾上腺轴亢进假说、神经再生假说、突触可塑性假说和免疫炎症假说等[4-5]。
目前抑郁症治疗仍然以药物治疗为主,现有抗抑郁药主要包括单胺氧化酶抑制剂、三环类抗抑郁药、四环类抗抑郁药、选择性5-羟色胺再摄取抑制剂、选择性去甲肾上腺素再摄取抑制剂、选择性5-羟色胺和去甲肾上腺素再摄取抑制剂、以氯胺酮为代表的速效抗抑郁药和中草药等[6]。但以上抗抑郁药均存在明显不良反应,如导致性功能障碍、睡眠障碍、体重增加和心脏毒性等[7]。可见,新型抗抑郁药物研发存在很大改进和提升的空间,一直是神经精神类药物研发领域的热点之一。
褪黑素(melatonin,MT)受体激动剂具有抗抑郁、抗焦虑和调节睡眠等生物活性,与传统抗抑郁药物相比,该类药物可能具有起效快、不良反应少和促进睡眠等优势[8-9]。阿戈美拉汀(agomelatine,Ago)是唯一被批准用于临床治疗抑郁症的MT 受体激动剂,临床应用显示出良好的抗抑郁和抗焦虑效果,并且能够改善抑郁症患者的睡眠质量和增加睡眠持续性[10]。但Ago 吸收率和代谢率低、首过效应明显及具有显著肝毒性的特点限制了其临床应用[11]。本课题组以Ago 为先导化合物,设计合成了一系列新型化合物并进行抗抑郁活性筛选。结果显示,其中GW117(结构式见图1)表现出与Ago 同样的MT1/MT2受体激动作用和5-HT2C受体拮抗作用,且口服给药后,药物峰浓度和曲线下面积较Ago显著提高,生物利用度显著提高,引起的肝细胞和肝结构损伤作用较Ago 轻,有望成为一种新型高效的抗抑郁药[12]。

Fig.1 Structure of GW117.
本研究拟采用小鼠慢性不可预知性温和应激(chronic unpredictable mild stress,CUMS)造模5 周后,再给予不同剂量的GW117 和Ago 干预6 周后进行蔗糖偏嗜实验(sucrose preference test,SPT)、强迫游泳实验(forced-swimming test,FST)和悬尾实验(tail suspension test,TST)评价GW117的抗抑郁作用,并采用高架十字迷宫实验(elevated plus maze test,EPMT)和新奇抑制摄食实验(novelty-suppressed feeding test,NSFT)评价其抗焦虑作用;同时用免疫荧光染色技术,评价小鼠海马齿状回(dentate gyrus,DG)神经元再生;并用高效液相色谱-电化学检测(high performance liquid chromatography-electrochemical detection,HPLCECD)法检测小鼠海马组织中相关神经递质水平的变化,深入探究GW117 的作用机制,为其临床应用提供实验依据。
1 材料与方法
1.1 药品、试剂和主要仪器
GW117(批号:21041601,纯度99%)和Ago(批号:20201004,纯度99%),广为医药科技有限公司;5-羟色胺(5-hydroxytrypta-mine,5-HT),多巴胺(dopamine,DA)和去甲肾上腺素(norepinephrine,NE),德国默克公司。双皮质素(doublecortin,DCX)(货号:4604s)、Alexa Fluor 488 标记山羊抗兔荧光二抗(货号:8878)和含DAPI 封片剂,美国Cell Signaling Technology 公司;马血清,武汉三鹰生物技术有限公司;羧甲纤维素钠(Na-CMC)、Triton X-100、蔗糖、OCT、4%多聚甲醛、PBS缓冲液、KH2PO4、半胱氨酸、高氯酸、柠檬酸钾和EDTA-Na2,北京索莱宝公司。其他化学试剂均为国产分析纯。
LED频闪灯(白光,50~60 Hz),中山市驰联电子有限公司;小鼠开场敞箱(50 cm×50 cm×50 cm)、SuperMaze 自发活动分析系统和高架十字迷宫,上海欣软信息科技有限公司;悬尾箱(25 cm×25 cm×35 cm)、圆柱形玻璃游泳缸(高20 cm,直径10 cm),本实验室自制;HIMAC CR 20B2 离心机,日本HITACHI 公司;CM1950 冰冻切片机和TCS SP8 激光共聚焦显微镜和Leica LASX 图像处理软件,德国Leica公司;Waters2695高效液相色谱系统和Waters2465电化学检测器,美国Waters公司。
1.2 动物
104 只雄性ICR 小鼠,SPF 级,体重18~22 g,首都医科大学实验动物中心提供,动物许可证号:SCXK(京)2020-0001。饲养于恒温通风的清洁室内,每笼4~6 只。室温24~26℃,湿度40%~60%,12 h/12 h 明暗交替(8∶00-20∶00 灯光照明),自由摄食饮水。所有动物实验得到首都医科大学动物伦理委员会批准。
1.3 CUMS模型的建立[13-14]和实验分组
小鼠适应环境7 d 后,除正常对照组(10 只)常规饲养外,其余小鼠按照下述方案给予刺激,每天随机选择1~2 种,连续35 d,建立CUMS 模型。刺激方式包括:夹尾(用15 mm 夹子夹住小鼠尾根部距离身体1 cm 处,持续1 min);束缚(将小鼠置于直径4 cm,长9 cm 的圆筒束缚盒内,在黑暗环境中持续束缚3 h);冷水游泳〔将小鼠分别置于10℃冷水缸(10 cm×20 cm×12 cm)里游泳6 min〕;频闪照明(将频闪灯放置于鼠笼上方60 cm处,照射14 h);合笼饲养(将2 笼小鼠合并至1 笼内饲养14 h);夜照明(在夜间持续光照12 h);倾斜笼(鼠笼倾斜45 度放置18 h);潮湿饲养(向鼠笼中加入150 mL水,至垫料潮湿浑浊,饲养18 h)和禁食(14 h)。
CUMS 开始后第35~36 天,模型小鼠进行SPT,按照蔗糖偏嗜率均衡随机分为CUMS 模型组、模型+Ago(20 和40 mg·kg-1)组和模型+GW117(5,10,20 和40 mg·kg-1)组,从第36 天开始每天上午应激前1 h ig给药,持续给药49 d,给药容积为10 mL·kg-1,正常对照组和模型组给予等体积0.5% Na-CMC。从第78 天开始进行行为学检测。实验流程见图2。
1.4 蔗糖偏嗜实验[15]
CUMS 开始后第35~36 天(分组给药前)和第78~79 天(给药第43~44 天)分别进行SPT。实验首先进行适应性训练:在鼠笼中放置2瓶1%(W/V)蔗糖水,24 h 后将其中1 瓶更换为纯水,并在经过12 h后将2个水瓶交换位置,继续训练12 h,以排除水瓶位置对实验的干扰。正式测试前,小鼠禁食禁水24 h,然后鼠笼中对称放1%蔗糖水和纯水各1瓶,持续测试24 h,并同样在测试12 h时交换水瓶位置。测试24 h 后,取走水瓶并称重,计算小鼠分别饮用纯水和蔗糖水的重量及对蔗糖水的偏嗜率。蔗糖偏嗜率(%)=蔗糖水饮用量/(蔗糖水饮用量+纯水饮用量)×100%。
1.5 强迫游泳实验[16]
CUMS 开始后第80 天(给药第45 天)进行FST。在给药60 min 后,将小鼠分别放入玻璃水缸(直径10 cm,高20 cm,水深12 cm,水温25℃)中强迫游泳6 min,记录后4 min 内小鼠累计不动时间。判定不动的标准是小鼠在水中停止挣扎,呈漂浮状态。
1.6 悬尾实验[17]
于CUMS开始后第81天(给药第46天)时进行TST。在悬尾箱顶板中心绳上安装一个小夹子,将胶布粘在小鼠尾端1 cm 处,用夹子夹住布条,使小鼠呈倒悬状态,头部处于箱底上方5 cm。在给药60 min 后,将小鼠倒悬固定在悬尾箱上测试6 min,记录后4 min 内累计不动时间。判定不动的标准是小鼠无肢体挣扎。
1.7 新奇抑制摄食实验[18]
于CUMS开始后第82天(给药第47天)时进行NSFT。各组小鼠禁食24 h 后,分别放置于50 cm×50 cm×50 cm的开场活动箱内,在箱子底部中心位置放多块大小相等的饲料。将小鼠从固定的位置放置于箱内,使其自由活动5 min,观察并记录小鼠从进入箱内至开始咬食饲料的时间,即摄食潜伏期。
1.8 高架十字迷宫实验[18]
于CUMS 开始后第83 天(给药第48 天)进行EPMT。高架十字迷宫装置由2 条30 cm×8 cm 的开臂、2条30 cm×8 cm×15 cm的闭臂和8 cm×8 cm的中央区组成,距离地面70 cm。测试前将小鼠放在空旷场地自由活动5 min,而后将小鼠面朝开臂方向放入中央区,观察5 min,记录小鼠分别进入开臂和闭臂的时间和次数,并统计开臂停留时间(time in the open arms,OT)百分比和进入开臂次数(entries in the open arms,OE)百分比。OT百分比(%)=开臂停留时间/(开臂停留时间+闭臂停留时间)×100%,OE百分比(%)=开臂进入次数/(开臂进入次数+闭臂进入次数)×100%。每只小鼠实验结束后,清除粪便,用75%乙醇擦拭迷宫,以去除气味干扰。
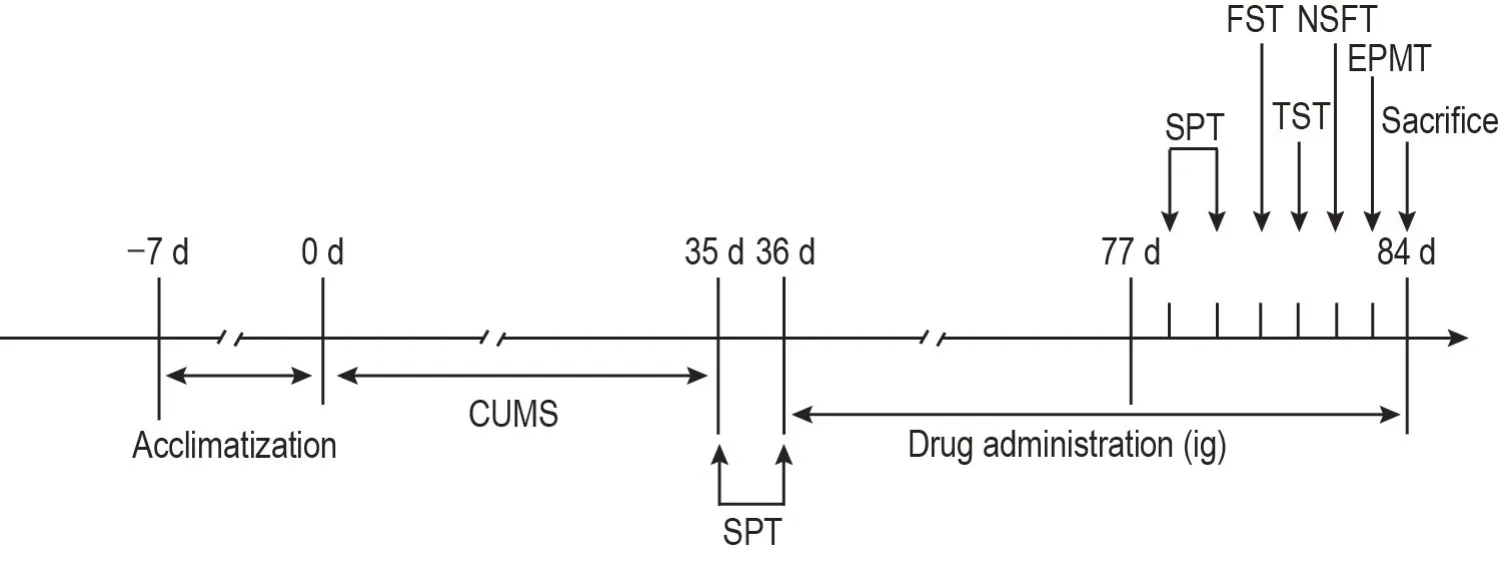
Fig.2 Experimental procedure of chronic unpredictable mild stress (CUMS)and behavioral tests.Except for the normal control group, the depression model was prepared by giving CUMS stimuli to the remaining groups for 35 consecutive days. Mice were ig given agomelatine (Ago, 20 and 40 mg·kg-1), GW117 (5, 10, 20 and 40 mg·kg-1) and water (control and CUMS model groups)from the 35th day of the CUMS procedure once per day for 48 d. SPT: sucrose preference test;FST: forced swimming test;TST: tail suspension test;NSFT:novel inhibition feeding test;EPMT:elevated plus maze test.
1.9 免疫荧光法检测小鼠海马DG区新生神经元密度
CUMS 开始后第84 天(给药第49 天),在每组中随机取5 只小鼠,麻醉后分别用生理盐水和4%多聚甲醛经心脏灌流,至小鼠身体变白变硬。取出全脑,置4%多聚甲醛溶液中4℃固定12 h,再依次置20%和30%蔗糖溶液中梯度脱水,经OCT 包埋后,用冰冻切片机制成厚度为30 μm的切片。
脑切片用0.01 mol·L-1PBS洗3次,每次5 min。用含5% BSA 和0.3% Triton X-100 的PBS 溶液37 ℃封闭1 h,加入DCX抗体(稀释倍数1∶250),在摇床上4 ℃孵育过夜。结束后用0.01 mol·L-1的PBS 洗3 次,每次5 min。加入Alexa Fluor 488 标记的山羊抗兔荧光二抗孵育2 h。用0.01 mol·L-1的PBS洗3 次,每次5 min[19]。滴加含DAPI 的封片剂后封片,使用共聚焦显微镜观察和拍摄小鼠海马DG,用Image J 软件统计DG 区被DCX 标记的新生神经元数量,并计算新生神经元密度。新生神经元密度(mm-2)= DG 区所有新生神经元数量/整个DG 区域面积。
1.10 高效液相色谱一电化学法检测小鼠海马组织中5-HT,DA和NE含量
组织样品制备:给药第49 天,将每组剩余的5 只小鼠处死,在冰上迅速剥取大脑,用预冷的生理盐水冲洗后迅速分离海马组织,-80℃保存。向海马组织中加入预冷的0.4 mol·L-1高氯酸溶液(含EDTA 0.5 mmol·L-1和0.01% 半胱氨酸)制备组织匀浆,冰上避光静置1 h,4℃18 000×g离心20 min。取上清100 μL,加入50 μL含柠檬酸钾20 mmol·L-1、K2HPO4300 mmol·L-1和EDTA 2 mmol·L-1的钾盐溶液,冰上避光静置1 h,再次4℃18 000×g离心20 min 后取上清,置-80℃保存。检测时,取20 μL经过0.22 μm 滤膜过滤后的上清,注入色谱系统分析检测。
色谱条件:Thermo Scientific™Acclaim™120 C18色谱柱(120 Å,3 mm×150 mm,3 μm),柱温:55℃。流动相:乙酸钠(50 mmol·L-1)-柠檬酸(50 mmol·L-1)缓冲液,pH 3.7,含辛烷基磺酸钠0.6 mmol·L-1、EDTA-Na20.1 mmol·L-1、NaCl22 mmol·L-1及11%甲醇(V/V),流速0.9 mL·min-1,进样体积20 μL。标准液:各标准品分别溶解在0.05 mol·L-1含0.1% 半胱氨酸的高氯酸溶液中,浓度400 mol·L-1,-30 ℃保存,临用前以流动相稀释为5,10,25,50,100,250和500 μg·L-1梯度混合标准溶液。检测电极为玻璃碳,参比电极为Ag/AgCl;检测电压为+0.6 V。以峰面积(y)对标准品浓度(x)绘制标准曲线,计算样品浓度(c),并根据稀释倍数、匀浆液体积和组织重量换算组织中5-HT,DA和NE 的含量,组织中待测物质的含量(ng·g-1蛋白)=0.01×c×待测物摩尔质量。
1.11 统计学分析
所有行为学实验均采用双盲实验法,实验结果数据以x±s表示,应用GraphPad Prism 8.0 软件进行统计分析。采用单因素方差分析(one-way ANOVA),组间两两比较采用Dunnett′t检验,P<0.05为差异有统计学意义。
2 结果
2.1 GW117对CUMS模型小鼠蔗糖偏嗜行为的影响
图3结果显示,与正常对照组相比,CUMS模型组小鼠蔗糖偏嗜率显著降低(P<0.01),说明模型构建成功;与模型组相比,模型+Ago 40 mg·kg-1组显著提高小鼠蔗糖偏嗜率(P<0.05);与模型组相比,模型+GW117(20 和40 mg·kg-1)组显著提高小鼠蔗糖偏嗜率(P<0.01)。提示GW117 具有抗抑郁作用。
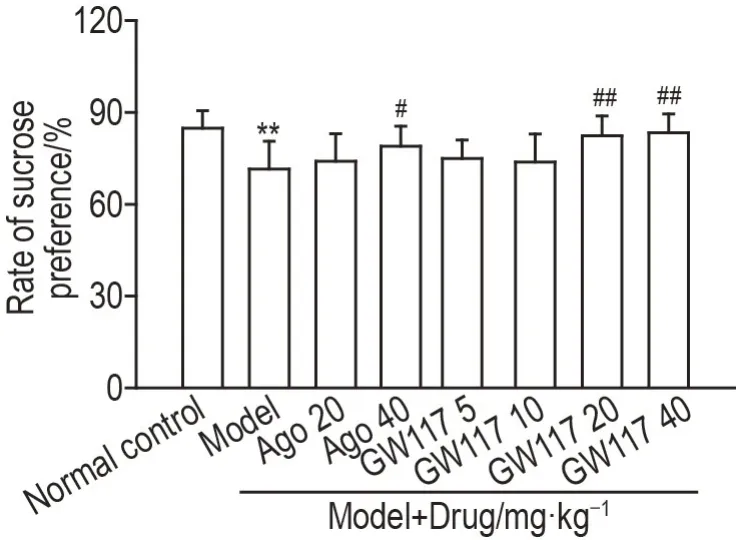
Fig.3 Effect of GW117 on rate of sucrose preference in SPT in CUMS model mice.See Fig.2 for the mouse treatment. ±s,n=10. **P<0.01,compared with normal control group;#P<0.05,##P<0.01,compared with model group.
2.2 GW117 对CUMS 模型小鼠强迫游泳和悬尾行为的影响
FST 结果(图4A)显示,与正常对照组相比,CUMS 模型组小鼠游泳不动时间显著延长(P<0.01)。与模型组相比,模型+Ago(20和40 mg·kg-1)组及模型+GW117(5,10,20和40 mg·kg-1)组小鼠游泳不动时间均显著缩短(P<0.01)。
TST 结果(图4B)显示,与正常对照组相比,CUMS 模型组小鼠悬尾不动时间显著延长(P<0.05)。与模型组相比,模型+Ago 40 mg·kg-1及模型+GW117(10,20和40 mg·kg-1)组小鼠悬尾不动时间显著缩短(P<0.05,P<0.01)。两实验结果均提示GW117具有抗抑郁作用。

Fig.4 Effect of GW117 on immobility time in FST(A)and TST(B)in CUMS model mice. See Fig.2 for the mouse treatment.±s,n=10. *P<0.05,**P<0.01,compared with normal control group;#P<0.05,##P<0.01,compared with model group.
2.3 GW117 对CUMS 模型小鼠新奇抑制摄食和高架十字迷宫行为的影响
NSFT 结果(图5)显示,与正常对照组相比,CUMS 模型组小鼠的摄食潜伏期明显延长(P<0.05);与模型组相比,模型+Ago 40 mg·kg-1组小鼠的摄食潜伏期显著缩短(P<0.05),模型+GW117(10,20和40 mg·kg-1)组小鼠摄食潜伏期也显著缩短(P<0.01),提示GW117具有抗抑郁作用。

Fig.5 Effect of GW117 on latency of feeding in NSFT in CUMS model mice. See Fig.2 for the mouse treatment.x±s, n=10. *P<0.05, compared with normal control group; #P<0.05, ##P<0.01,compared with model group.
EPMT 结果(图6)显示,与正常对照组相比,CUMS 模型组小鼠OT 百分比和OE 百分比显著减少(P<0.01);与模型组相比,模型+Ago 40 mg·kg-1组和模型+GW117(20 和40 mg·kg-1)组小鼠OE百分比显著增加(P<0.01),模型+Ago 40 mg·kg-1组和模型+GW117(20和40 mg·kg-1)组小鼠OT百分比显著增加(P<0.05,P<0.01)。提示GW117具有抗焦虑作用。

Fig.6 Effect of GW117 on percentage of entries in open arms(OE,A)and percentage of time in open arms(OT,B)in EPMT in CUMS model mice. See Fig.2 for the mouse treatment. The percentage of OT(%)=open arm dwell time/(open arm dwell time+closed arm dwell time)×100%;the percentage of OE(%)=open arm entry times/(open arm entry times+closed arm entry times)×100%.x±s,n=10.**P<0.01,compared with normal control group;#P<0.05,##P<0.01,compared with model group.
2.4 GW117 对CUMS 模型小鼠海马DG 神经元再生的影响
免疫荧光染色结果(图7)显示,与正常对照组相比,CUMS 模型组小鼠海马DG 区新生神经元密度显著减少(P<0.05);与模型组相比,模型+Ago(20 和40 mg· kg-1)组小鼠海马DG 区新生神经元密度显著增加(P<0.05),模型+GW117(10,20 和40 mg·kg-1)组小鼠DG 区新生神经元密度也显著增加(P<0.01)。提示GW117 具有促进海马DG 神经元再生的作用。

Fig.7 Effect of GW117 on density of neonatal neurons in hippocampal dentate gyrus in CUMS model mice by immunofluorescence assay. See Fig.2 for the mouse treatment. B was the semi-quantitative result of A. Arrows represent neonatal neurons labeled by doublecortin. x ±s,n=5. *P<0.05,compared with normal control group;#P<0.05,##P<0.01,compared with model group.
2.5 GW117 对CUMS 模型小鼠海马组织内神经递质DA,5-HT和NE含量的影响
经线性回归分析,各待测物的回归方程分别为5-HT:y=9569.3x+4267.3,r2=0.9997;DA:y=8565.9x+ 10038,r2=0.9998;NE:y=5179.5x+3571.4,r2=0.9999。3种待测物的线性范围均为0~521 nmol·L-1。HPLC-ECD 检测结果显示,与正常对照组相比,CUMS 模型组小鼠海马组织DA 含量显著下降(P<0.05),5-HT 和NE 含量无明显改变(图8);与模型组相比,模型+各药物组小鼠海马DA 含量均无显著变化(图8A);模型+Ago(20 和40 mg·kg-1)组和模型+GW117(5,10和20 mg·kg-1)组小鼠海马5-HT 含量显著升高(P<0.05,P<0.01)(图8B),模型+各给药组小鼠海马NE 含量均无显著变化(图8C)。

Fig.8 Effect of GW117 on levels of dopamine(DA,A),5-hydroxytryptamine(5-HT,B)and norepinephrine(NE,C)of hippocampal tissue in CUMS model mice by high performance liquid chromatography-electrochemical detection assay. See Fig.2 for the mouse treatment.±s,n=5.*P<0.05,compared with normal control group;#P<0.05,##P<0.01,compared with model group.
3 讨论
随着对抑郁症发病机制研究的不断深入,多靶点多系统抗抑郁药物的研发已经成为抗抑郁药物研究中重要的方向。多靶点抗抑郁药物的作用机制不限于传统单胺系统,可作用于MT 受体、γ-氨基丁酸受体和DA 受体等,对治疗抑郁症具有独特的优势[20-21]。本课题组前期研究发现,GW117 兼具5-HT2C受体拮抗剂和MT1/MT2受体激动剂特性,在大、小鼠FST、TST、大鼠CUMS 模型和获得性无助模型上均显示出抗抑郁和抗焦虑作用[22],但其作用机制尚未阐明。
本研究通过CUMS 建立小鼠抑郁模型,结果发现,成年雄性ICR 小鼠持续5 周暴露于CUMS 下,可出现快感缺失、游泳和悬尾不动时间延长和摄食潜伏期延长的抑郁样行为改变,且伴随着海马DG神经发生和海马神经递质DA水平的下降。GW117治疗可有效逆转CUMS 模型小鼠的焦虑样和抑郁样行为反应。
研究显示,慢性应激与多种精神疾病相关,尤其是抑郁症。慢性应激可造成海马DG 颗粒细胞层神经发生受损[23-24]。海马对慢性应激高度敏感,海马DG 区神经发生被认为在抑郁症发病机制和药物抗抑郁治疗中发挥重要作用,抑制海马神经元凋亡和促进神经细胞再生对于抑郁症患者恢复健康至关重要[25-26]。DCX 是一种微管蛋白,在动物神经细胞中广泛表达,是神经元迁移和分化所必需的,可用来特异性标记新生神经元的胞质和突起,DCX 阳性细胞数量可反映神经元再生情况[27-29]。文献报道,成年大鼠脑组织切片染色研究发现,Ago 给药3 周后,海马DG 区DCX 标记的新生神经元密度明显增加[30]。本研究免疫荧光染色结果显示,CUMS模型组小鼠海马DG 区DCX 标记的新生神经元密度相比正常对照组显著下降,而Ago 可增加该区域新生神经元密度。此结果与文献[30]报道一致,表明CUMS 明显降低小鼠神经发生;同样GW117 也可增加DG 区DCX 标记的新生神经元的密度,表明GW117和Ago均具有促进神经元新生作用。
单胺假说是阐述抑郁症发病机制经典假说之一,大量研究显示,抑郁症的发生与神经突触间隙5-HT,NE和DA等神经递质的减少有关[31-32]。目前临床一线抗抑郁药物大多是通过增加突触间隙5-HT 和NE 含量而起作用的单胺策略药物[33]。本研究结果表明,GW117 作为对5-HT2C受体具有拮抗作用的多靶点药物,同样可提高小鼠海马组织中5-HT水平,但对DA和NE水平无显著影响。
综上所述,本研究发现GW117 在小鼠CUMS模型上具有抗焦虑和抗抑郁作用,其作用机制可能与促进海马DG 神经元发生和提高海马组织5-HT含量有关。本研究为进一步将GW117 开发为新型抗抑郁、抗焦虑药物提供了实验依据。
