2-羟基-4-甲氧基苯乙酮在有机合成中的应用
2023-07-15安超娜王乙颖刘存芳任传清田光辉
安超娜, 王乙颖, 刘存芳, 任传清, 张 强, 田光辉
(陕西理工大学 陕西省催化基础与应用重点实验室,陕西 汉中 723000)
2-羟基-4-甲氧基苯乙酮俗称为丹皮酚(Paeonol),是由乙酰基、酚羟基、甲氧基、苯环等基团构成的,且具有独特结构的一种天然产物[1],也是较为重要的有机合成中间体[2].丹皮酚中的乙酰基中的羰基基团因碳氧双键电荷分布不均匀而具有显著活性,可参与多种反应,如与硫代氨基脲、盐酸羟胺、肼等亲核试剂发生亲核加成反应[3];酚羟基可进行烷基化,能与苯磺酰基侧链偶联等;酚羟基和甲氧基的强供电子作用使苯环的3位和5位更容易被修饰,因而丹皮酚常被作为构建复杂活性物质的先导化合物[4-7].目前,研究者们不断挖掘丹皮酚及其衍生物在抗炎[8-9]、降血糖[10-11]、抗肿瘤[12-15]、保护神经[16-18]等生物活性方面的潜在作用,并开拓构建丹皮酚衍生物的新途径[19-20].丹皮酚在天然产物中分布广泛,可直接从牡丹皮、徐长卿等中药材中提取[21-22],也可通过多种方法进行合成.丹皮酚的来源丰富、廉价易得,为其结构改造和精深加工提供了充足的原料.
丹皮酚因其具有活性显著和多活性位点的特点,可应用于构建结构稳定、性能优异、用途更为广泛的新型化合物[23-24],如图1所示,以丹皮酚为前体构建衍生物的途径可分为5大类.本文中,笔者综述了近年来丹皮酚应用于有机合成中的研究进展.

图1 丹皮酚的结构及修饰Fig.1 Structure and Modification of Paeonol
1 羰基修饰
1.1 丹皮酚噻唑类衍生物
丹皮酚噻唑类衍生物的合成路线如图2所示.王妙等[25]以乙醇为溶剂、浓H2SO4为催化剂,丹皮酚(A1)与硫代氨基脲反应20 h得到丹皮酚氨基硫脲(A2),产率为75.2 %,A2再分别与取代基不同的α-溴代苯乙酮发生缩合、环化反应得到丹皮酚噻唑类衍生物(A3a~3e),其中N-[4-(2-羟基苯基)噻唑-2-基]-2-羟基-4-甲氧基苯乙酮腙(A3b)和N-[4-(2-甲氧基苯基)噻唑-2-基]-2-羟基-4-甲氧基苯乙酮腙(A3d)的产率分别为82.3 %和87.9 %.Tsai等[4]以乙醇为溶剂、碘为催化剂,A1与硫脲发生缩合、环化反应得到2-氨基噻唑前体(A4),以四氢呋喃(THF)为溶剂,A5与对位不同取代的苯磺酰氯在K2CO3碱催化作用下反应得到丹皮酚-2-氨基噻唑类衍生物(A5a~5g).抗癌活性测试结果显示,这些噻唑类衍生物对受试癌细胞体系都有细胞毒性,其中N-[4-(2-羟基-4-甲氧基苯基)噻唑-2-基] -4-甲氧基苯磺胺(A5c)对AGS细胞(胃癌细胞)和HT-29细胞(人结肠癌细胞)的抑制效果最好.Fu等[26]以A1和2-氯乙基吗啉为原料、丙酮(ACE)为溶剂,在K2CO3碱催化作用下反应12 h得到1-[4-甲氧基-2-(2-吗啉乙氧基)-苯基]乙酮(A6),产率为90 %,以乙醇为溶剂、碘为催化剂,A6与硫脲反应12~16 h得到吗啉-O-丹皮酚氨基噻唑(A7),产率为49 %.

图2 丹皮酚噻唑类衍生物的合成路线Fig.2 Synthesis Route of Paeonol Thiazole Derivatives
1.2 丹皮酚席夫碱类衍生物


图3 丹皮酚席夫碱类衍生物的合成路线Fig.3 Synthesis Route of Paeonol Schiff Base Derivatives
1.3 丹皮酚肟类衍生物
羟基丹皮酚肟类衍生物的合成路线如图4所示.刘志平等[33]以乙醇为溶剂,用醋酸钠调节pH呈弱酸性,A1与羟基羟胺在75 ℃下反应2~4 h得到丹皮酚羟基肟(C1),产率为97.6 %,A1与甲氧基羟胺肟化得到丹皮酚甲氧肟醚(C2),产率为85.8 %,A1与苄氧基羟胺肟化得到丹皮酚苄氧醚(C3),产率为87.9 %.汪波等[34]以二甲基乙酰胺(DMA)为催化剂,A1与氯化亚砜(SOCl2)在室温下反应3 h得到2-乙酰基-5-甲氧基苯基乙酸酯(C4),产率为83.7 %,以吡啶为溶剂,C4与盐酸羟胺在50 ℃下反应5 h得到2-(1-羟基亚胺基)乙基-5-甲氧基苯乙酸酯(C5),产率为92.7 %.王蓉等[35]以DMF为溶剂、NaOH为碱性催化剂,A1与卤代烃在45 ℃下反应0.5 h得到羟基丹皮酚醚(C6a~6g),产率为72.1 %~82.6 %,以乙醇为溶剂、吡啶为催化剂,C6a~6g与盐酸羟胺在50 ℃下反应得到羟基丹皮酚肟(C7a~7g),产率为80.6 %~91.2 %,其中C7a,7b,7g的抗血小板聚集活性是阿司匹林的2倍以上,有较好的应用前景.

图4 羟基丹皮酚肟类衍生物的合成路线Fig.4 Synthesis Route of Hydroxy Paeonol Oxime Derivatives
苄基丹皮酚肟类衍生物的合成路线如图5所示.顾宏霞等[36]以DMF为溶剂、NaOH为碱性催化剂,A1与氯苄在45 ℃下发生亲核取代反应得到苄基丹皮酚(C8),产率为72.2 %,以吡啶为溶剂,C8与盐酸羟胺在50 ℃下反应得到苄基丹皮酚肟(C9),产率为91.2 %,以DMF为溶剂,冰浴中搅拌使C9与1,4-二溴丁烷发生取代反应得到苄基丹皮酚肟溴代丁基醚(C10),产率为81.3 %,以乙腈为溶剂,在pH=8~9条件下,C10与结构不同的有机胺反应得到苄基丹皮酚肟胺基醇醚类衍生物(C11a~11e),如苄基丹皮酚肟 -4-(4-乙基-哌嗪基)丁基醚(C11a),产率为74.7 %.这些苄基丹皮酚肟衍生物的抗血小板聚集活性测试结果表明,苄基丹皮酚肟 -4-(二乙胺基)丁基醚(C11c)和苄基丹皮酚肟 -4-(吗啉基)丁基醚(C11e)的抗血小板凝聚能力相对较强,有开发应用的潜力.

图5 苄基丹皮酚肟类衍生物的合成路线Fig.5 Synthesis Route of Benzyl Paeonol Oxime Derivatives
1.4 丹皮酚腙类衍生物
丹皮酚腙类衍生物的合成路线如图6所示.陈根强等[37]以乙醇为溶剂,A1与苯磺酰肼在室温下反应3 h得到丹皮酚苯磺酰腙(D1),产率为65 %,以三乙胺(Et3N)二氯甲烷溶液为溶剂,D1与取代基不同的磺酰氯在室温下反应得到丹皮酚苯磺酰腙衍生物(D2a~2e),产率为8 %~10 %.杀虫活性测试结果表明,与母体丹皮酚相比,丹皮酚苯磺酰腙类衍生物的杀虫活性提高了,发生碘化反应时取代基不同其对应丹皮酚苯磺酰腙衍生物的杀虫活性不同,取代基为萘环时杀虫活性最高,为开发新型杀虫剂提供了思路.
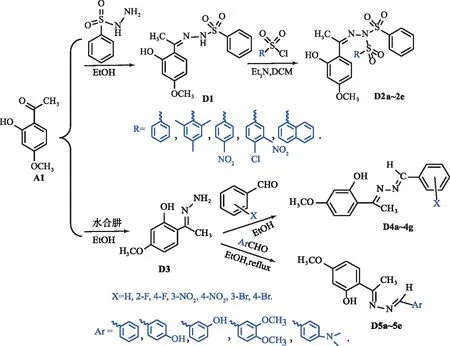
图6 丹皮酚腙类衍生物的合成路线Fig.6 Synthesis Route of Paeonol Hydrazone Derivatives
马献力等[38]以乙醇为溶剂,A1与水合肼反应4 h得到 (E)-2-(1-肼基乙基)-5-甲氧基苯酚(D3),产率为91.1 %,以乙醇为溶剂,D3与取代苯甲醛在70 ℃下反应2~6 h得到N-苄叉丹皮酚腙(D4a~4g),N-(3-硝基苄叉基)丹皮酚腙(D4d)、N-(4-溴苄叉基)丹皮酚腙(D4g)等的产率为50.5 %~91.9 %,其中N-(2-氟苄叉基)丹皮酚腙(D4b)和N-(4-氟苄叉基)丹皮酚腙(D4c)对金黄色葡萄球菌的最小抑制浓度(MIC)分别为4,2 mg/L.刘志平等[33]以A1和水合肼为原料,在60 ℃下搅拌反应2 h得到(E)-2-(1-肼基乙基)-5-甲氧基苯酚(D3),以乙醇为溶剂,D3与芳香醛在60 ℃下回流反应1~4 h得到丹皮酚腙衍生物(D5a~5e),如丹皮酚苄氧醚、丹皮酚甲氧肟醚等,产率为75 %~87.9 %,其中N-(4-羟基亚苄基)丹皮酚腙(D5b)对胃癌细胞SGC-7901的抑制活性较强.庞富华等[39]基于活性拼接原理,将基团腙引入到A1中,使A1与水合肼、芳香醛反应得到芳甲叉基丹皮酚腙衍生物,其对金黄色葡萄球菌的MIC值为2μg/mL.
2 酚羟基上键合修饰
2.1 丹皮酚醚类衍生物
丹皮酚醚类衍生物的合成路线如图7所示.Pao等[40]以丙酮为溶剂,A1与RCl在K2CO3碱催化作用下发生亲核取代反应得到丹皮酚O-烷基化产物(E1a~1c).治疗脂蛋白巨噬细胞脂质聚集的实验分析表明,E1a有抑制脂质聚集的潜力,为未来抗动脉硬化药物的研发带来福音.楚小晶等[41]以丙酮为溶剂、KI为催化剂,A1与1,4-二溴丁烷在室温下反应14 h得到白色固体(E2),产率为83.2 %,室温下E2与(3-异丙基苯基)(苯基)甲酮在KI催化作用下反应1 h,经萃取、干燥、旋蒸得到油状物(E3).非甾体类抗炎药应用广泛,但是长期服用对胃肠道有很大刺激作用,对丹皮酚先导化合物和具有生物活性的结构进行拼凑,为其活性的叠加提供可能.戴卫国等[42]以DMF为溶剂、NaOH为碱性催化剂,A1与二溴烷烃在室温下发生亲核取代反应得到丹皮酚溴代烷基醚衍生物(E4a~4e),产率为8.7 %~75.5 %,以乙腈为溶剂,E4a~4e分别与AgNO3在60 ℃下反应得到丹皮酚硝酸酯醚类衍生物(E5a~5e),产率为9.4 %~75.3 %,其体外抑制血小板凝聚的活性提高,血小板凝聚抑制率(AIR)约为17.33 %~21.32 %,约为阿司匹林的3倍.
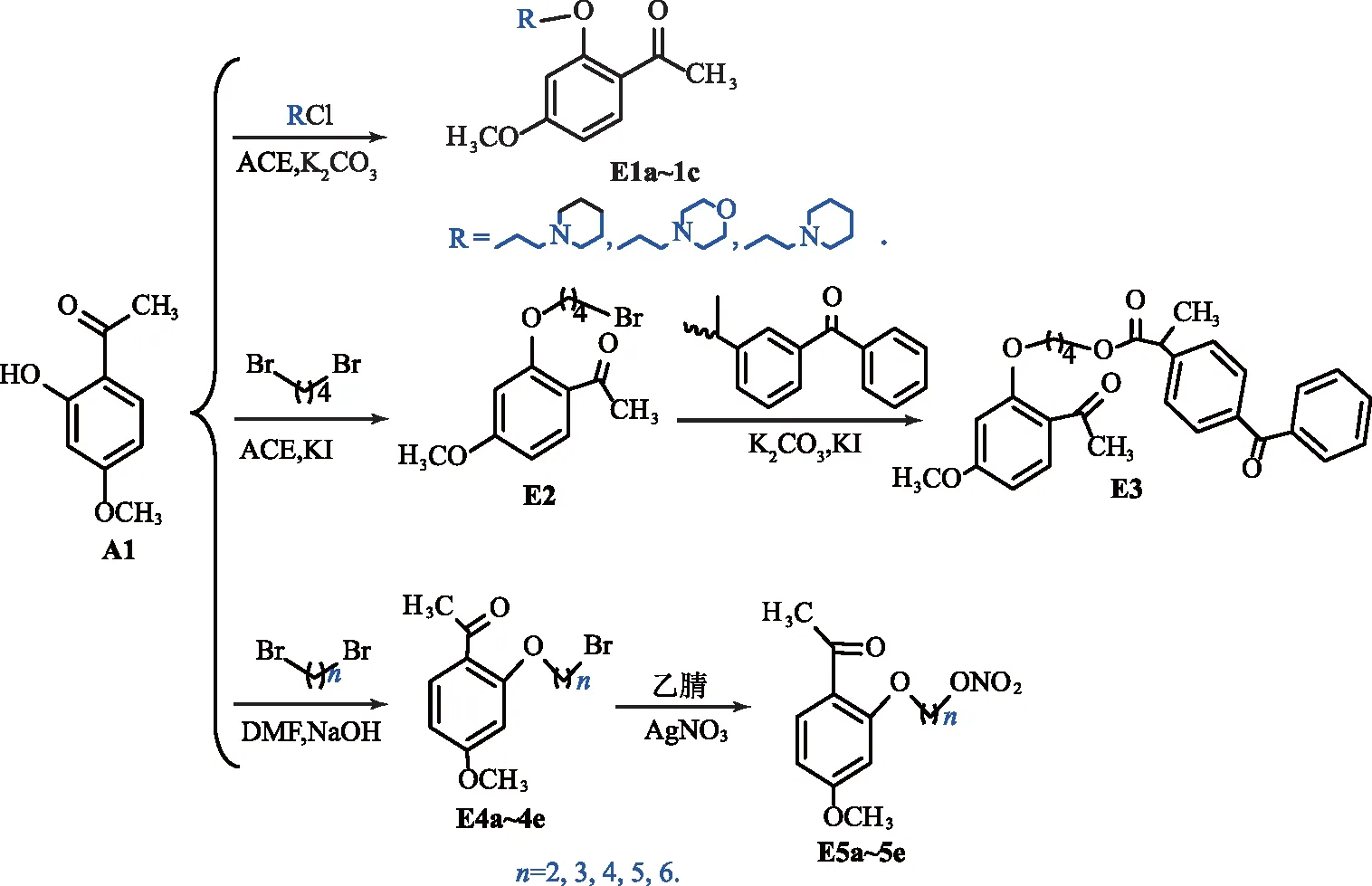
图7 丹皮酚醚类衍生物的合成路线Fig.7 Synthesis Route of Paeonol Ether Derivatives
2.2 丹皮酚酯类衍生物
丹皮酚磺酸酯类衍生物的合成路线如图8所示.屈欢等[43]以丙酮为溶剂,A1与芳基磺酰氯在K2CO3作用下,经油浴加热回流反应得到丹皮酚磺酸酯类衍生物,产率为38 %~98 %.病原菌抑制活性实验结果显示,与A1相比,丹皮酚磺酸酯类衍生物对玉米弯孢菌叶斑病菌的抑制率明显提高,抑制率为25.3 %~80.4 %.Huang等[44]以丙酮为溶剂,A1与取代基不同的苯磺酰氯在KCO3作用下反应得到丹皮酚磺酸酯类衍生物(F1a~1h),产率为5 %~86 %.抗乙型肝炎病毒HBV活性测试发现,4′-甲氧基-2′-[(4-甲氧苯磺酰基)氧基] -乙酰苯(F1f)的抗HBV活性较高,IC50为0.36 μmol/L,为治疗乙型肝炎病毒提供了新思路.

图8 丹皮酚磺酸酯类衍生物的合成路线Fig.8 Synthesis Route of Paeonol Sulfonate Ester Derivatives
丹皮酚醚酯衍类生物的合成路线如图9所示.先将A1中的羟基醚化,再在醚化侧链上进行酯化,刘鹏等[45]以DMF为溶剂,室温下A1与α-溴代异丁酸在NaOH作用下发生取代反应得到丹皮酚醚异丁酸(2-[2-乙酰基-5-甲氧基苯氧基]-2) -甲基丙酸(F2),产率为42 %,F2与不同的醇(TBAB,DMAP,EDCl-HCl)发生酯化反应得到丹皮酚异丁酸酯类衍生物(F3a~3f),产率为1.8 %~43.8 %.体外降血脂活性测试发现,其中F3c和F3f相比于A1有更好的降血脂活性,为A1的修饰提供了新方向,为丹皮酚异丁酸酯类衍生物在降血脂方面的研究应用提供了思路.柏志伟等[46]以DMF为溶剂,A1与溴乙酸在NaOH作用下发生取代反应得到丹皮酚醚乙酸物(F4),产率为81.5 %,以DMF为溶剂、K2CO3为碱性催化剂,F4分别与1,2-二溴乙烷和二溴取代烷烃在50 ℃下反应得到丹皮酚乙酸溴代乙基酯(F5a)以及F5b~5e,产率为4.3 %~78.2 %,以乙腈为溶剂,F5a~5e再分别与AgNO3在60 ℃下搅拌得到NO供体型丹皮酚衍生物(F6a~6e),产率为4.9 %~89.1 %.体外抗血小板聚集和调节血脂的活性测试结果显示,F6c对在ADP诱导作用下的血小板凝聚有较好的抑制效果,F4在调节血脂、降低TC(胆固醇)等方面的效果都比A1效果显著,为治疗血栓等心脑血管疾病的药物开发提供参考.

图9 丹皮酚醚酯类衍生物的合成路线Fig.9 Synthesis Route of Paeonol Ether Derivatives
2.3 丹皮酚嘧啶类化合物
辛懋等[47]以A1为底物,用1,4-二溴丁烷、嘧啶类化合物对A1中的羟基进行修饰得到11种丹皮酚嘧啶类化合物,其对细胞的抑制活性测试结果显示,6-(2-氟苯基)-5-氰基-4-羟基-2-丹皮酚丁巯基嘧啶棕和6-甲基-4-羟基-2-丹皮酚丁巯基嘧啶对人结肠癌细胞的IC50分别为9.22±1.80μg/mL和1.32±0.71μg/mL,与顺铂阳性对照药对比效果更加优良.
3 酚羟基和羰基分步修饰
柏志伟等[48]以DMF为溶剂、NaOH为碱性催化剂,A1与溴乙烷在45 ℃下发生取代反应得到乙基丹皮酚醚(G1),产率为98.2 %,以乙醇为溶剂、吡啶为催化剂,G1与盐酸羟胺在50 ℃下搅拌4 h反应得到乙基丹皮酚肟(G2),产率为93.1 %,以DMF为溶剂、NaOH为碱性催化剂,G2与1,4-二溴丁烷反应得到乙基丹皮酚肟溴代丁基醚(G3),产率为81.2 %,以DMF为溶剂,G3与N-甲基哌嗪在40 ℃下搅拌5 h反应得到乙基丹皮酚肟胺基丁基醚衍生物(G4a~4e),产率为80.3 %~86 %,合成路线如图10所示.体外抗血小板凝集的活性测试发现,当有机胺为甲基哌嗪时,其丹皮酚肟胺基丁基醚衍生物的抗血小板凝集活性最差,而当有机胺为乙基哌嗪时抗血小板凝集活性最强.
Anh等[49]以DMF为溶剂,A1与三氯氧磷(POCl3)在室温下反应0.5 h得到3-甲酰基-7-甲氧基色酮(H1),产率为76 %,室温下H1与2-硫酮-4-噻唑烷酮衍生物在哌啶的催化作用下搅拌5 h反应得到(H2a~2i),如5-[(7-甲氧基-4-氧代-4H-铬-3-基)亚甲基]四氢噻唑-2,4-二酮等9种丹皮酚色氨基噻唑烷衍生物,合成路线如图11所示.测试其对HepG2,HL-60,KB,LLC,LNCaP,LU-1,MCF-和SW480 8种癌症细胞的细胞毒性效应,结果表明这9种丹皮酚色氨基噻唑烷衍生物对试癌细胞均表现出微弱的毒性作用,可为合成成本低、选择性好的抗癌药物提供前体.

图11 丹皮酚色氨基噻唑烷衍生物合成路线Fig.11 Synthesis Route of Paeonol Colored Aminothiazolane Derivatives
4 乙酰基中α-甲基碳的反应
4.1 丹皮酚β-羟基缩合产物
丹皮酚β-羟基缩合产物的合成路线如图12所示.刘存芳等[50]以乙醇为溶剂、NaOH为碱性催化剂,A1与2-溴苯甲醛发生亲核加成反应得到3-羟基-1-(2-羟基-4-甲氧基苯) -3-(2′-溴苯)-1-丙酮(I1),产率为78.6 %,其对油菜菌核病菌、黄瓜枯萎病菌等具有明显的抑制和灭活效果.赖普辉等[51]以乙醇为溶剂,A1与间硝基苯甲醛在NaOH作用下反应得到3-羟基-1-(2′-羟基-4′-甲氧基苯)-3-(3-硝基)苯-1-丙酮(I2),产率为75.1 %,其对伤寒沙门菌50127株和福氏志贺菌51065的MIC值分别为0.02 g/L和0.08 g/L,最小杀菌浓度(MBC)分别为0.04 g/L和0.12 g/L,对实验菌株的抑制和灭活效果强于丹皮酚.刘存芳等[52]以乙醇为溶剂、硅胶负载NaOH为催化剂,A1与4-硝基苯甲醛反应2 h重结晶后得到β-羟基-1-(2′-羟基-4′-甲氧基苯基)-β-(4-硝基苯基) -1-丙酮(I3),产率为77.34 %.
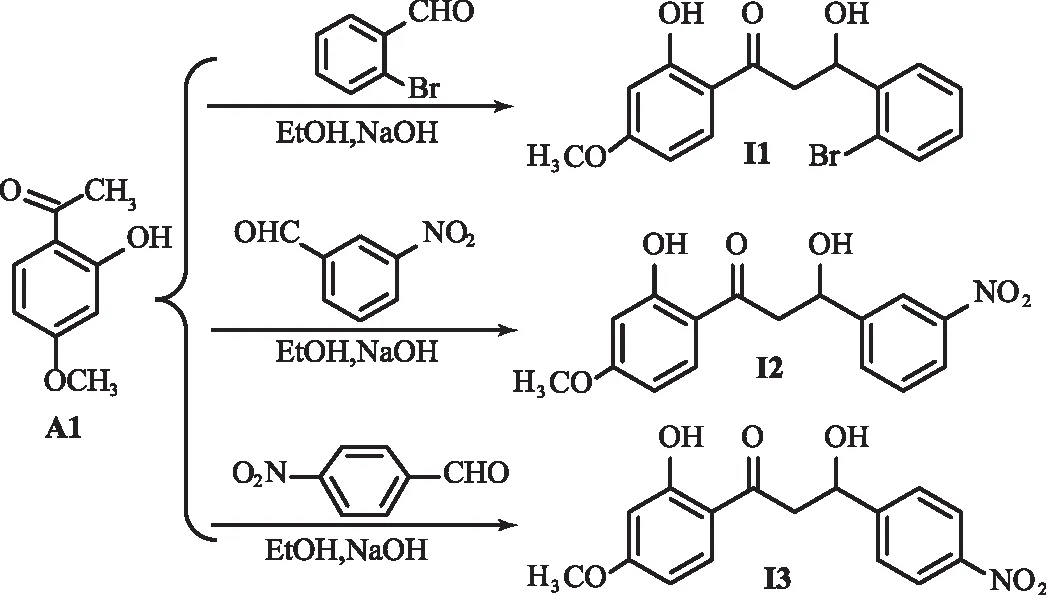
图12 丹皮酚β-羟基缩合产物的合成路线Fig.12 Synthesis Route of β-hydroxyl Condensation Products of Paeonol
4.2 丹皮酚查尔酮
丹皮酚查尔酮的合成路线如图13所示.刘存芳等[53]以乙醇为溶剂、KOH为碱性催化剂,A1与4-甲基苯甲醛发生Claisen-Schmidt反应得到4-甲基-2′-羟基-4′-甲氧基查尔酮(J1),产率为71.57 %.赖普辉等[54]以乙醇为溶剂,A1与间硝基苯甲醛在NaOH碱催化作用下反应得到2′-羟基-4′-甲氧基-3-硝基查尔酮(J2),产率为87.4 %,其对大肠埃希菌ATCC25922株的MIC值和MBC值分别为8.24,8.56 mg/mL.以乙醇为溶剂,KOH为碱性催化剂,A1与对氟苯甲醛在室温下发生缩合反应得到2-羟基-4-甲氧基-4′-氟查尔酮(J3),产率为46.83 %.刘存芳等[55]以乙醇为溶剂,A1与9-蒽醛在NaOH催化作用下发生缩合反应得到丹皮酚蒽醛查尔酮(J4),产率为74.30 %,其在质量浓度为1.0 g/L时对油菜菌核病菌的抑菌率为61.15 %,对铜绿假单胞菌ATCC27853 株的MIC值和MBC值分别为0.66,0.92 g/L.
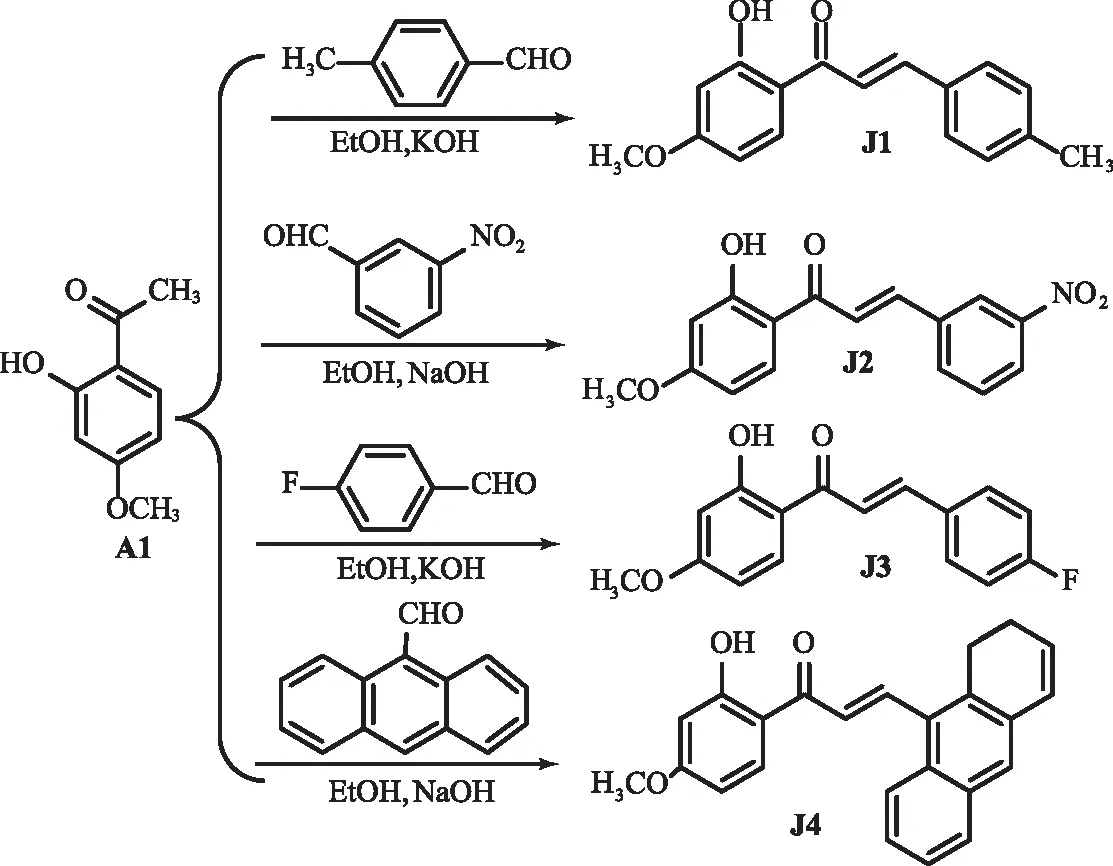
图13 丹皮酚查尔酮的合成路线Fig.13 Synthesis Route of Paeonol Chalcone
4.3 丹皮酚哌嗪类衍生物
孙远东等[56]对丹皮酚乙酰基中的α-甲基引入哌嗪,通过溴代、取代反应得到2-(4-苄基哌嗪-1-基)-1-(2-羟基-4-甲氧基苯基)乙酮(K2a)、1-(2-羟基-4-甲氧基苯基)-2-(4-(4-甲基苄基)哌嗪-1-基)乙酮(K2b)和1-(2-羟基-4-甲氧基苯基)-2-(4-(4-氯苄基)哌嗪-1-基)乙酮(K2c),产率分别为70.50 %,65.3 %,73.2 %,其合成路线如图14所示.3种丹皮酚哌嗪衍生物对ADP、AA诱导的血小板诱导抑制活性测试显示,K2b对AA诱导的血小板诱导抑制活性IC50为7.38 mmol/L,对ADP诱导的血小板诱导抑制活性IC50为16.40 mmol/L,说明苄溴苯环上引入给电子基团会增加对ADP、AA诱导的血小板聚集抑制活性.

图14 丹皮酚哌嗪类衍生物的合成路线Fig.14 Synthesis Route of Paeonol Piperazine Derivatives
5 苯环修饰
对丹皮酚中苯环修饰的合成路线如图15所示.屈欢等[57]以不同取代的苯胺为底物,在0~5 ℃下进行重氮化反应0.5 h得到取代胺的重氮盐溶液,以乙醇为溶剂,调节pH=8,A1与取代胺的重氮盐溶液反应得到丹皮酚偶氮类衍生物(L1a~1h),产率为6.3 %~26.4 %.抗菌活性测试发现,其对番茄灰霉病菌、马铃薯早疫病菌、玉米大斑病菌等具有较好的抑制作用,抑制率大于70 %,可用来设计合成高效低毒的新型抑菌剂.姚日生等[58]借助A1与硝化剂作用得到丹皮酚硝基取代产物(L2).屈欢等[57]将A1与胂酸在高温下胂化得到胂酸基取代产物(L3).

图15 丹皮酚中苯环修饰的合成路线Fig.15 Synthesis Route of Benzene Ring Modification in Paeonol
6 结论与展望
依据丹皮酚的结构特征对其分子中的羰基、酚羟基、α-甲基等活性位点进行修饰,已合成出了多种新型的肟、腙、噻唑、席夫碱、醚、酯、查尔酮、β-羟基化合物等丹皮酚衍生物.新型丹皮酚衍生物的溶解性、挥发性、药理活性、紫外和荧光性能等均得到很大优化,在害虫防治、抗肿瘤、降血压、降血脂、抗动脉硬化等方面有较好的效果.天然产物的改性与修饰对药物的发展有着推动作用,新型丹皮酚衍生物的挖掘是基于多配体药物设计、药效组合、活泼结构修饰等理念,为以丹皮酚为原料合成高价值的天然产物查尔酮和黄酮类化合物提供了新思路.近年来,合成了很多丹皮酚衍生物并研究了其药理活性,这些衍生物的专一药物适应性和靶点响应性以及从体外实验研究到体内实验测试、从实验研究到临床应用还有很大的研究空间.因此,有望提高丹皮酚衍生物的靶向性和高效性,使其对新药的开发设计更加有效和合理,不断探索丹皮酚衍生物的合成方法及其构效关系具有重要的理论价值和实用价值.
