复方赤红颗粒中独活和川芎及芍药苷的含量测定*
2023-07-13郑小丽胡晓波郑志昌李明杨继红廖尚高
郑小丽, 胡晓波, 郑志昌, 李明, 杨继红***, 廖尚高
(1.贵州医科大学附属医院 药剂科, 贵州 贵阳 550001; 2.贵州医科大学 药学院, 贵州 贵阳 550001)
类风湿性关节炎(rheumatoid arthritis,RA)是一种常见的、多发的、难以治愈的自身免疫性炎性关节疾病,以滑膜进行性慢性炎症为特征[1-2]。RA的炎症反应不仅会加重患者关节破坏、畸形及残疾[3- 4],还会对患者心、肺、肾等重要脏器及其它系统组织造成损害,甚至死亡[5]。现代西方医学将RA视为一种无菌性炎症,临床上常使用糖皮质激素、生物制剂及非甾体抗炎药(non steroidal anti-inflammatory drugs,NSAIDs)等抗炎或镇痛药物进行治疗[6-7],但长期使用这些西药不仅会导致胃肠道出血、肝肾功能障碍及骨髓抑制等严重不良反应[8],还会增加患者中风和高血压的风险[9]。近年来,为了解决西药治疗对人体器官的毒性、耐药性以及降低药物治疗成本等问题,中医药辅助治疗RA受到了广泛关注[10-12]。复方赤红颗粒源于本院名中医王光义教授从独活、川芎及赤芍等14味中药提取制备而成,有活血化瘀、舒筋活络及抗炎止痛等功效[13-15],广泛应用于RA的辅助治疗,不仅不会增加肝肾损害等严重不良反应,还能快速有效缓解患者关节疼痛、肿胀等不适。为方便使用、携带和储藏,将此验方研制成的复方赤红颗粒,而对制剂定性鉴别和含量测定法对保证药物的质量和疗效至关重要[16- 17]。复方赤红颗粒成分复杂,目前尚无质量标准,本研究对颗粒剂中独活、川芎的鉴别和主要活性成分芍药苷的含量测定进行分析,为其质量标准的建立提供基础数据。
1 材料与方法
1.1 实验材料
1.1.1材料与主要试剂 独活对照药材(批号120940-200205)、川芎对照药材(批号120918-200406)及芍药苷对照品(批号110736-200424,含量99.5%)均购自中国食品药品检定研究院,复方赤红颗粒3批(批号 20210301、20210302及20210303)、独活及川芎阴性对照样品均由医院提供;甲醇是色谱纯,其余试剂均是分析纯,水是纯化水。
1.1.2主要仪器 LC-10AT输液泵、SPD-10A紫外检测器、WML-2006C-4威玛龙色谱数据工作站及HT-230A色谱柱恒温箱(岛津仪器苏州有限公司),Ultimate 3000高效液相色谱(high performance liquid chromatography,HPLC;美国赛默飞),LIBROR AEL-160万分之一电子天平(常熟双杰测试仪器厂),TG332A十万分之一分析天平(岛津仪器苏州有限公司),HS10260D超声清洗仪(昆山超声仪器有限公司),硅胶G薄层板(批号G20210408,青岛海洋化工有限公司),ZF-90多功能暗箱式紫外投射仪(上海顾村电光仪器厂)。
1.2 研究方法
1.2.1独活的薄层色谱鉴别(thin layer identification,TLC) 取复方赤红颗粒1 g研细,加甲醇溶液10 mL,超声30 min(功率250 W,频率40 kHz)、过滤,即得供试品溶液;另取独活阴性样品1 g和独活对照药材1 g,同法分别制得阴性对照和对照药材溶液;分别吸取上述3种溶液各10 μL,于同一硅胶薄层板上点样,选择石油醚(60~90 ℃)-乙酸乙酯(7∶3)作为展开剂在层析缸中展开,取出晾干,于365 nm紫外光灯下检视。
1.2.2川芎的TLC 取复方赤红颗粒2 g研细,加1%盐酸水溶液0.5 mL润湿,加20 mL石油醚(60~90 ℃)超声30 min(功率250 W,频率40 kHz),滤过、挥干滤液,余下残渣使用三氯甲烷1 mL溶解,即获得供试品溶液;另取川芎阴性样品2 g和川芎对照药材0.1 g,同法分别制备阴性对照样品和对照药材溶液;分别吸取上述3种溶液各10 μL,于同一硅胶薄层板上点样,选择正己烷-乙酸乙酯(6∶1)作为展开剂在层析缸中展开,取出晾干,于302 nm紫外光灯下检视。
1.2.3高效液相色谱(high performance liquid phase,HPLC)含量测定 溶液的制备:取芍药苷的对照品2.09 mg,置于25 mL量瓶,加20%乙醇溶液溶解定容,得每1 mL含83.5 μg的对照品溶液;取复方赤红颗粒3 g研细,置于100 mL锥形瓶,加20%乙醇溶液50 mL,超声处理10 min(功率250 W,频率40 kHz),取出,称定质量,用20%乙醇补足减失的质量,摇匀,滤过,续滤液即为供试品溶液;按照复方赤红颗粒处方比例制备不含赤芍的阴性对照颗粒,照上述供试品溶液同法制备阴性对照溶液;色谱条件为依利特Supersil ODS-B C18色谱柱(250 mm×4.60 mm,5 μm),甲醇-1%冰乙酸(20∶80)为流动相,检测波长243 nm,柱温30 ℃,流速0.90 mL/min,进样量10 μL。
1.2.4专属性、线性关系、精密度、稳定性及重复性测定 精密量取“1.2.3”项下对照品溶液、供试品溶液以及阴性对照溶液,按该项下的色谱条件分别注入HPLC仪中,检测专属性;称取芍药苷对照品适量,加20%乙醇,制得浓度为5.22、10.44、20.88、41.76、83.52及167.04 mg/L的芍药苷系列对照品溶液,按照“1.2.3”项下色谱条件进样测定,记录峰面积,以峰面积(Y)值为纵坐标,芍药苷对照品浓度(Xmg/L)为横坐标,进行线性回归;取“1.2.3”项下对照品溶液,按该项下色谱条件进样,连续进样6次,记录峰面积进行精密度评价;取“1.2.3”项下供试品溶液,放置于室温下,分别于0、2、4、8、12及24 h按该项下色谱条件进样,测定芍药苷峰面积进行稳定性评价;取同一批复方赤红颗粒(批号 20210301)6份,3.0 g/份,按“1.2.3”项下溶液制备同法配置供试品溶液,并按该项下色谱条件进样,记录测得的峰面积进行重复性评价。
1.2.5加样回收试验 取同一批复方赤红颗粒(批号20210301),研成粉末,精密称取9份,1.5 g/份,置于100 mL容量瓶内,编号1~9。编号1~3、4~6及7~9分别精密加167.04 mg/L芍药苷对照品溶液10、13及15 mL,按“1.2.3”项下溶液制备中同法制备供试品溶液,并按该项下色谱条件进样,测定峰面积并计算加样回收率。
1.2.6样品含量测定 分别取20210301、20210302、20210303批次复方赤红颗粒样品2份,3.0 g/份,按“1.2.3”项下溶液制备中同法制备供试品溶液,并按该项下色谱条件进样,记录峰面积并通过线性关系计算芍药苷的含量。
1.3 统计学分析
使用Excel 2019录入数据并计算相对标准偏差(relative standard deviation,RSD)。
2 结果
2.1 独活和川芎的TLC
在独活和川芎的TLC中,供试品与对照药材在对应位置上均显示相同颜色的荧光斑点,阴性无干扰。见图1。
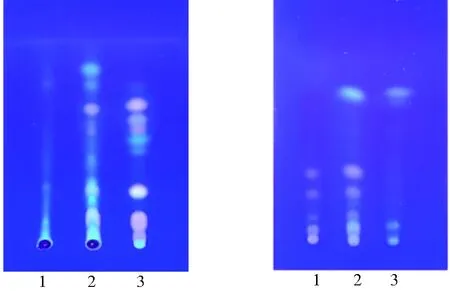
独活川芎注:1为阴性样品,2为供试品,3为对照药材。图1 独活和川芎的TLCFig.1 TLC of heracleum and Ligusticum wallichii
2.2 专属性
结果显示,芍药苷对照的色谱峰保留时间为23 min,供试品在相应的保留时间处有芍药苷色谱峰且与其他峰分离良好,阴性对照在相应的保留时间处无吸收,阴性无干扰,系统适用性及专属性均良好。见图2。
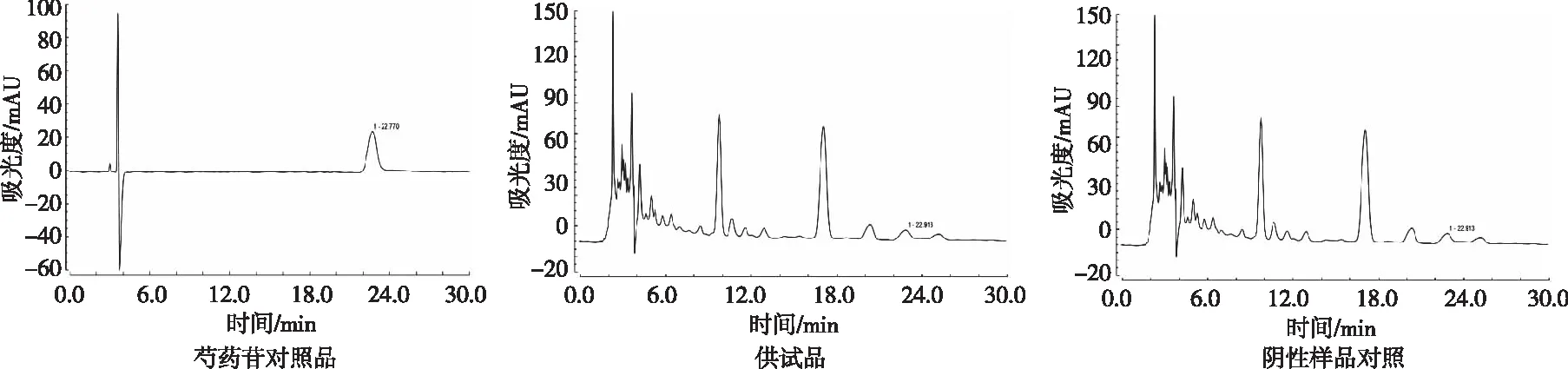
图2 芍药苷的专属性试验结果Fig.2 Specificity test results of paeoniflorin
2.3 线性关系
芍药苷回归方程:Y=7.143×103X-1.101×103(r=0.999 0),结果表明芍药苷在5.22~167.04 mg/L范围内峰面积与对应的浓度具有良好线性关系。
2.4 精密度、稳定性及重复性
在精密度的研究中,根据测定芍药苷峰面积计算得到芍药苷峰面积RSD为1.14%,表明仪器精密度良好;在稳定性研究中,根据测定芍药苷峰面积计算得到芍药苷峰面积RSD为1.45%,表明在室温条件下24 h内供试品溶液稳定;在重复性研究中,根据测定芍药苷峰面积及线性关系计算得到样品中芍药苷平均含量为1.424 7 mg/g,RSD为1.39%,重复性符合实验要求(表1)。
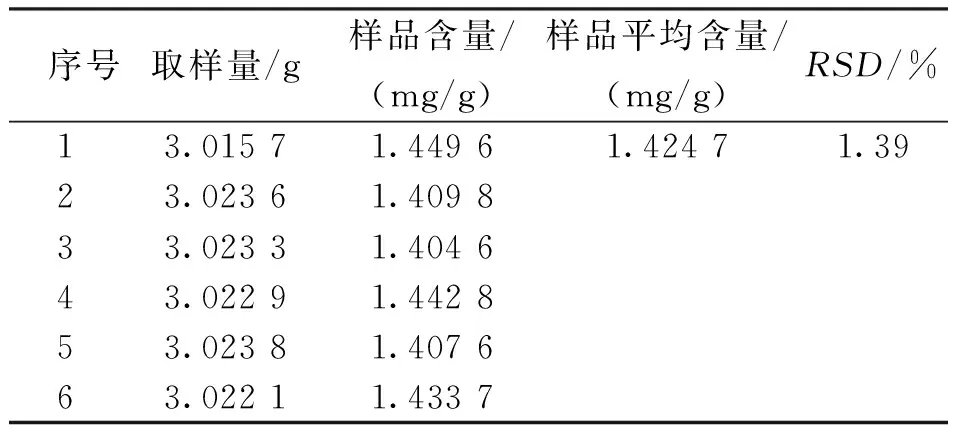
表1 复方赤红颗粒的重复性试验结果Tab.1 Repeatability test results of compound Chihong granules
2.5 加样回收试验
加样回收率的范围为100.4%~104.2%,平均回收率为102.8%,RSD为1.36%。见表2。
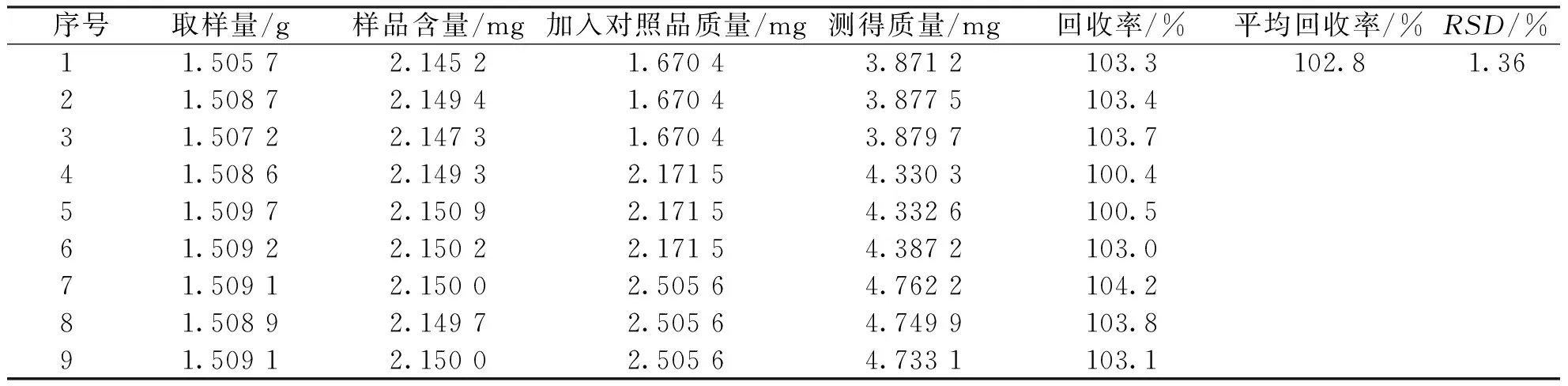
表2 复方赤红颗粒的加样回收试验结果Tab.2 Sample addition recovery test results of compound Chihong granules
2.6 样品含量测定
样品中芍药苷的含量测定结果显示,批号为20210301、20210302、20210303样品中芍药苷平均含量分别为1.424 3 mg/g、1.409 1 mg/g及1.432 7 mg/g。见表3。
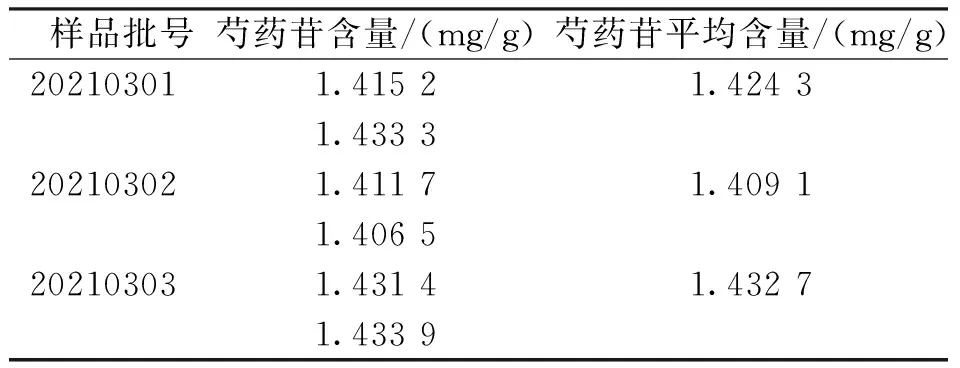
表3 样品中芍药苷的含量测定结果Tab.3 Determination test results of paeoniflorin in test samples
3 讨论
在独活的TLC研究中,首先考察了正己烷-三氯甲烷-乙酸乙酯(2∶1∶1)、石油醚(60~90 ℃)-乙酸乙酯(9:2)、石油醚(60~90 ℃)-乙酸乙酯(7∶3)等不同展开剂,结果显示以石油醚(60~90 ℃)-乙酸乙酯(7∶3)为展开剂时效果最好。在川芎的TLC研究中,首先考察了石油醚(60~90 ℃)-乙醚(2∶1)、氯仿-甲醇(8∶1)、正己烷-乙酸乙酯(6:1)等不同展开剂,结果显示以正己烷-乙酸乙酯(6∶1)为展开剂时效果最好。
在独活和川芎这两味君药的TLC试验中进一步对以石油醚(60~90 ℃)-乙酸乙酯(7∶3)为独活鉴别的展开剂、以正己烷-乙酸乙酯(6∶1)为川芎鉴别的展开剂时,在不同湿度(32%、58%及72%)、不同温度(10 ℃、20 ℃及35 ℃)以及不同预饱和时间(10 min、20 min及30 min)下的耐受性试验,结果显示所建立的独活和川芎TLC法耐用性良好,重现性好。
芍药苷是赤芍含量最高的活性成分之一[18-19],以芍药苷含量为评价时,首先对芍药苷的提取体系、超声时间及检测波长进行筛选。结果显示芍药苷在乙醇浓度为20%、70%时含量最高,20%的分离度比70%的高;超声时间为10 min时含量最高,20~50 min呈递减趋势,最终确定提取方法为20%乙醇超声10 min。芍药苷的最大吸收波长在230 nm,由于本研究中复方赤红颗粒是中药复方制剂,成分复杂,且不同成分间相互干扰,于230 nm处检测赤红颗粒样品中芍药苷时前后有其他成分干扰,分离度较差,经过多次摸索,选择波长243 nm处测定芍药苷含量,此时分离度较好,无干扰,因此选择检测波长为243 nm。
采用HPLC仪进行本研究中的专属性实验、线性关系、精密度、稳定性、重复性、加样回收率及样品含测,芍药苷含量测定时对不同流动相进行了筛选,考察了以甲醇∶水(15∶85)、甲醇∶1%冰乙酸(17∶83)和甲醇∶1%冰乙酸(13∶87)和甲醇∶1%冰乙酸(20∶80)体系,发现当以前3者为流动相时芍药苷出峰时间太长或不出峰且杂质峰干扰大,而甲醇∶1%冰乙酸(20∶80)为流动相时获得的分离效果最好且阴性无干扰,最后确定甲醇∶1%冰乙酸(20∶80)为含量测定的流动相。
另外,本研究进一步考察了流速(0.88 mL/min、0.90 mL/min及0.92 mL/min)、流动相比例[甲醇∶1%冰乙酸(22∶78)、甲醇∶1%冰乙酸(20∶80)及甲醇∶1%冰乙酸(18∶82)]、柱温(28 ℃、30 ℃及32 ℃)以及检测波长(241 nm、243 nm及245 nm)的微小变化对分离效果及含量测定的影响,结果显示系统微小变化不影响复方赤红颗粒中芍药苷的含量测定。此外,使用液相色谱仪进行了中间精密度的考察,结果显示RSD为1.37%(<2%),表明中间精密度良好。
独活和川芎具有祛风除湿、活血行气及通痹止痛的功效[20-21],在验方中均属于君药;芍药苷可通过减少炎症介质的产生可发挥抗炎和免疫调节作用[22-24],也是治疗RA的主要活性成分[25-26]。本研究所建立的独活、川芎两味君药的TLC法专属性高,建立的芍药苷含量测定法专属性好、分离度高及重现性好,可用于复方赤红颗粒的质量控制,为后期开发为医院制剂提供数据支撑。
