突触可塑性在阿尔茨海默病干预中的研究进展
2023-07-10秦志明
秦志明,柏 峰
(1.南京中医药大学附属南京鼓楼医院;2.南京大学医学院附属南京鼓楼医院神经内科,江苏 南京 210008)
阿尔茨海默病(Alzheimer’s disease,AD)是一种复杂的神经退行性疾病,占人类痴呆的大部分,其最初表现为学习和记忆功能下降。研究发现,AD的早期特征之一为突触可塑性受损[1]。突触可塑性是指神经元改变其连接强度的能力,是脑网络损伤后发育和重组的神经生理过程,其功能障碍会导致AD等神经系统疾病的大脑网络破坏,从而影响认知功能[2]。近年来常开发针对突触的修饰治疗方法,以预防和治疗AD中的突触功能障碍[3]。本文针对目前对AD的不同干预方式对突触可塑性的调控进行综述,以期提供新的治疗策略来延缓疾病进展。
1 突触可塑性与AD之间的关系
突触是指由一个神经元冲动传到另一个神经元或细胞间的相互接触的结构,是信息传递的关键部位。突触功能的调节和改变常被称为突触可塑性,可表现为形态和突触蛋白含量等的变化。突触可塑性与认知能力有重要关系,突触之间开始传递信息时,会在突触中产生神经递质以便准确地判断并激发突触前后神经细胞同时活动,从而导致各突触的变化,通过多种修饰来调节突触可塑性进而影响学习与记忆[4]。目前对于AD的病因尚不清楚,淀粉样蛋白-β(Amyloid beta,Aβ)的沉积和由超磷酸化的tau蛋白形成的神经原纤维缠结(Neurofibrillary tangles,NFTs)是AD的两个主要病理特征。Aβ斑块沉积后出现NFTs的时间依赖性表现是AD的公认标志,会改变突触功能,影响突触可塑性并最终导致突触丧失;而抗氧化剂和自由基之间的不平衡会导致氧化应激,而氧化应激也是AD的早期观察的结果,在正常的生理浓度下,自由基对于突触可塑性是必需的,而在AD中,当氧化应激增加时,记忆力和突触可塑性均会受损[5]。因此,突触可塑性作为影响记忆与学习的重要因素之一,与AD的认知功能密切相关。
2 AD的干预方式对突触可塑性的影响
2.1 运动干预突触可塑性是神经元连接强度的活动依赖性变化,一直被认为是学习和记忆的组成部分。研究发现,当突触可塑性受损会导致AD患者脑功能障碍[2],目前并没有针对突触功能障碍的治疗方法。药理方法学的进步虽然拥有巨大的潜力,但也无法逆转AD的病理进程,因此,需寻求新型的替代疗法来治疗突触损伤。运动作为一种干预手段,是神经营养因子的重要调节剂,包括脑源性神经营养因子(Brain-derived neurotrophic factor,BDNF)、血管内皮生长因子(Vascular endothelial growth factor,VEGF)等,此外,运动也会引起突触结构和功能的改变,从而影响AD患者的认知能力[6]。BDNF是一种神经营养蛋白家族的生长因子,广泛分布于中枢神经系统中,是突触可塑性的关键因素,影响神经元的存活、分化,改善神经活动。研究发现,AD患者的大脑中BDNF显著降低,而BDNF的丧失是突触功能障碍,且BDNF的减少与认知功能的下降直接相关[7]。
运动可能会通过调节许多参与突触可塑性的信号通路来产生有益影响。在运动过程中,周围组织分泌的蛋白质及其代谢衍生物(例如组织蛋白酶B和FNDC5/虹膜素(Fibronectin type III domain containing 5,FNDC5)会穿过血脑屏障,升高BDNF表达[8]。BDNF与海马神经元中的原肌球蛋白受体激酶B (Tropomycin receptor kinase B,TrkB),TrkB结合后充当信号级联停靠位点,调控许多不同的细胞过程,影响海马神经的发生[7]。其次,运动过程中肝脏会产生酮体β-羟基丁酸酯(β-hydroxybutyrate,β-DBHB)并释放到血液中,DBHB在海马中积聚诱导BDNF,抑制组蛋白乙酰化酶2(Class I histone deacetylase,HDAC)和HDAC3的水平,而运动后肌肉中释放的乳酸会改变NAD+/NADH比值,激活SIRT1,诱发肌动蛋白irisin的释放,FNDC5/irisin会刺激海马中BDNF的表达,维持神经元活性,对AD中突触可塑性和记忆功能有益[9-10]。
VEGF是一种信号蛋白,参与血管和神经细胞的生长,具有神经保护的作用,研究发现AD患者的VEGF蛋白水平较低。而运动会诱发外周血管的适应性,影响血管生成和血管生长因子,提高大脑中VEGF的转录,直接增强神经发生和突触功能[6]。运动作为一种低成本、高效益的辅助疗法,对于改善认知障碍有一定的潜能,但其在AD患者及老年人群中推广仍然受限。
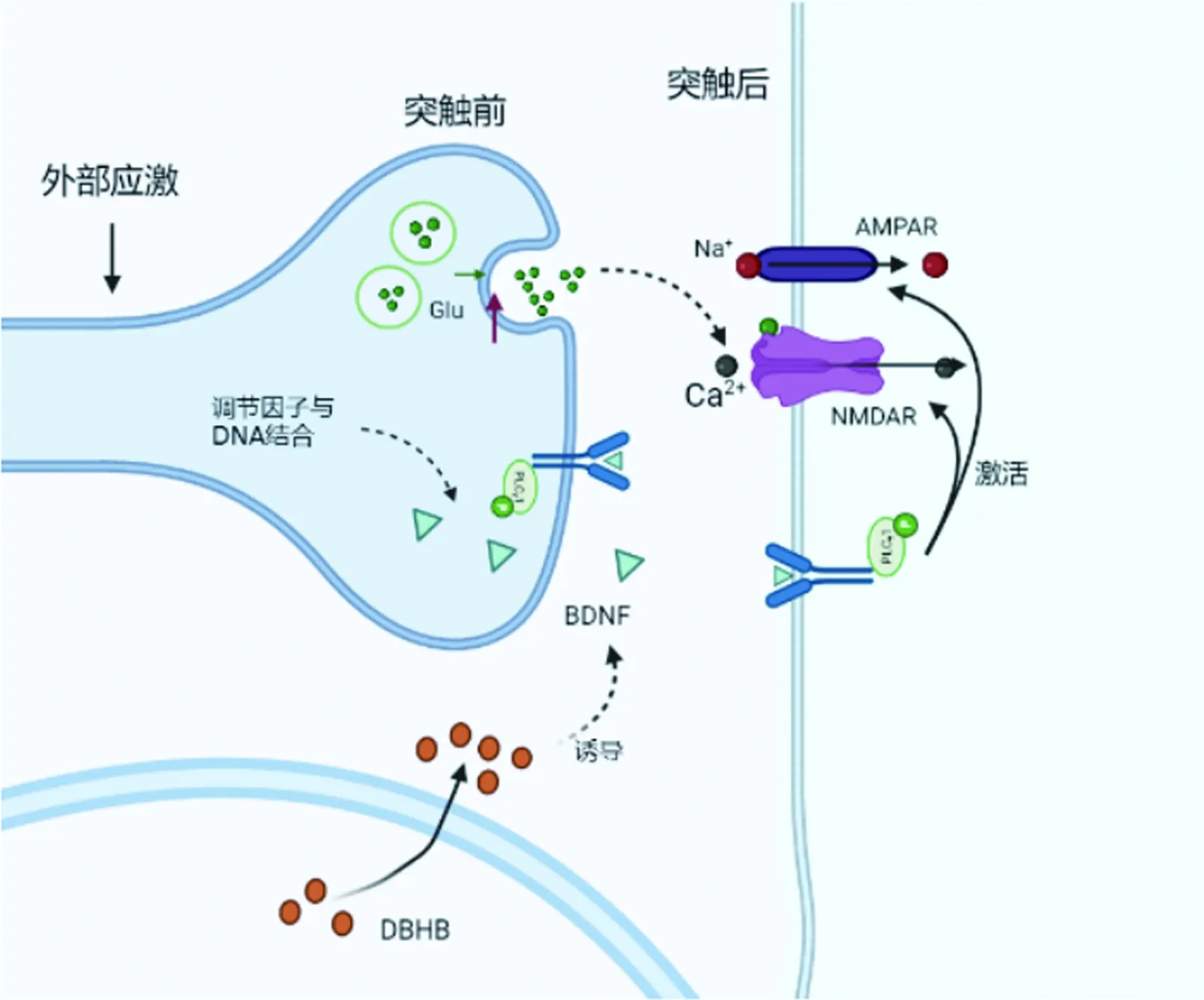
图1 运动过程中BDNF在突触部位作用途径示意图
2.2 针刺干预AD典型病理特征是大脑中淀粉样斑块和NFTs,Aβ和tau蛋白分别是斑块和缠结的主要成分。Aβ的沉积和tau蛋白过度磷酸化d会破坏神经元运输机制,影响突触功能[3],研究发现,针刺可以有效改善突触可塑性。穴位针刺能够改善前额叶皮层中Aβ的沉积,降低tau水平[11-12],但有研究发现tau抑制不能防止Aβ诱导的长期突触可塑性和记忆损伤[13]。神经炎症是导致痴呆的原因之一,会造成神经元损伤和死亡,改变突触传递和突触可塑性,电针治疗可以抑制海马中的促炎细胞因子IL (Interleukin-),IL-6,TNF-α (Tumor necrosis factor-α),改善突触和认知功能障碍[14]。突触素(Synaptophysin,SYN)是突触前可塑性标记物,参与突触小泡的生物发生和胞吞,其失衡会导致突触可塑性受损,影响认知功能;而突触后致密体蛋白-95 (Post-synaptic density protein 95,PSD-95)是突触后标志物,主要参与突触信号的传导,其过表达会导致兴奋性突触传递增强,而电针刺激会增加PSD厚度,促进SYN和PSD-95的表达改善突触功能[11],影响学习和记忆功能。综上所述,针刺可以改善AD的认知功能,并保护神经元,影响突触可塑性。
目前,针灸在临床治疗神经精神性疾病取得了较好疗效,但现有临床报告显示其治疗效果质量参差不齐。针灸治疗轻度至中度AD有益且安全[15],但其不适用于重度AD患者。此外,由于不同的针刺深度或电流强度以及施针手法对全脑网络重组的影响不同,且穴位的选择具有异质性,因此其在临床应用时具有限制性,不过基于其较好的治疗效果,可以将其普遍应用于有轻度认知损害或主观认知衰退人群,以预防认知障碍疾病。
2.3 药物干预目前,临床上使用的药物可以缓解AD的部分症状,但不能改变病理进程。美金刚是一种N-甲基-D-天冬氨酸受体(N-methyl-D-aspartate receptor,NMDAR)拮抗剂,NMDAR常用于治疗中重度AD,为介导谷氨酸能传递的离子通道之一,N-甲基-D-天冬氨酸受体激活是正常脑功能所必需的,在突触可塑性以及学习和记忆相关的细胞中起重要作用,而美金刚可以通过阻断NMDAR来改善AD患者的认知以及记忆缺陷,且很少诱发不良反应[16]。
研究发现,大脑中枢胆碱能神经元的丧失和乙酰胆碱(Acetylcholine,Ach)水平与AD的发生相关,因此乙酰胆碱酯酶抑制剂(Acetylcholinesterase inhibitors,AChEIs)在AD的治疗中起重要作用,而AChEIs是从突触前释放后降解ACh的酶,ACh是一种与记忆相关的神经递质,其含量会抑制神经元的活性,影响突触间的传递。目前,临床上使用的AChEIs有很多(多奈哌齐、加兰他敏和卡巴拉汀),但它们的作用机制略有不同。如多奈哌齐是一种高选择性的AChEI抑制剂,主要通过增加脑中ACh的浓度,来改善AD患者的记忆功能。卡巴拉汀为氨基甲酸胆碱酯酶抑制剂,通过胆碱酯酶可逆抑制Ach水解,增加用于突触传递的ACh的浓度[17-18]。而加兰他敏是种选择性可逆AChEI和烟碱胆碱能受体的变构调节剂,其通过增加突触处ACh的水平,促进神经细胞的增殖和存活;还会增加海马中的促炎细胞因子(IL-6,IL-1),改善LPS[Lipopolysaccharide (LPS,endotoxin)]诱导的海马中突触相关蛋白(SYN和PSD-95)的损失,确保突触的传递功能[19],目前尚未有研究报道用加兰他敏预防由LPS导致的认知功能下降。
除常用于临床上的药物外,还有一些药物也可以通过改善突触可塑性进而达到改善AD患者学习和记忆的功能。如利鲁唑可降低Aβ42、Aβ40、Aβ低聚物水平和Aβ斑块负荷,逆转小胶质细胞和神经元星形胶质细胞的表达,防止海马依赖性空间记忆[20]。此外,动物实验发现表明,中药的有效成分也具有改善AD的突触可塑性的作用。淫羊藿苷、葛根素和黄均会使IL-1β、TNF-α和IL-6的表达显着降低,抑制由氧化应激导致的炎症反应和神经元的凋亡[21]。
AD的病因是多因素的,目前被FDA (The united states food and drug administration)批准使用的药物都是延缓疾病发展而非治疗性的。美金刚与多奈哌齐的联合治疗可能效果更加显著,但其可能会导致更严重的副作用,因此,探索新型的药物以及给药方式非常关键。一项分析近几年在美国国立卫生研究院注册的新药临床试验发现,大多新药安全且耐受性好,PQ912、SAM-760、白藜芦醇、GV-971等对AD具有治疗效果;而尼伐地平、沙利度胺、艾达吡定、依那西普等对AD无治疗效果;但有些药物并未得到研究结果,如HTL0018318、Bapineuzumab等[22]。
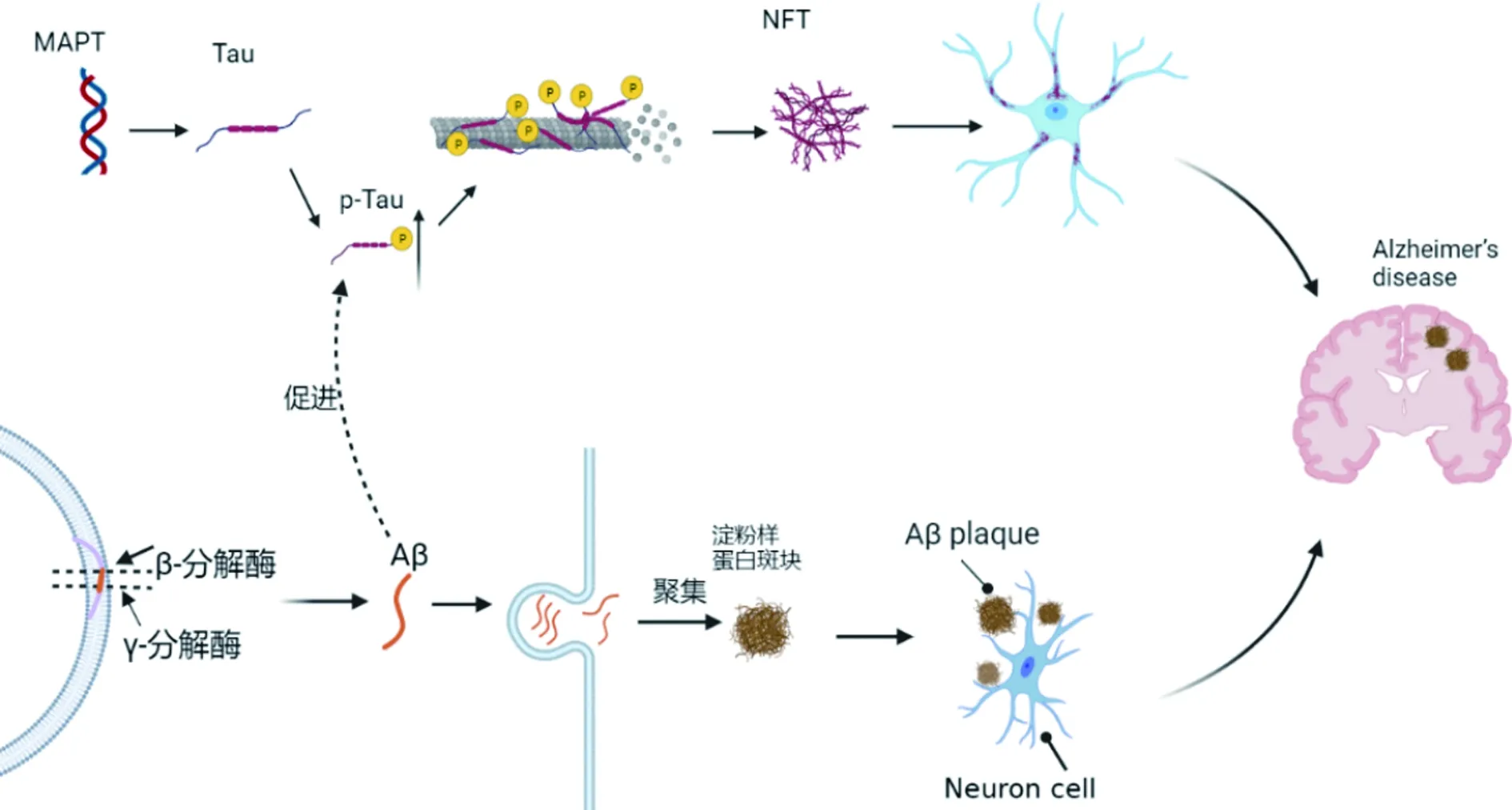
图2 Aβ和tau蛋白的作用机制
2.4 其他干预音乐训练对人脑的功能和结构可塑性具有明显的影响,大脑网络体系的一些关键特征是由不同形式的突触可塑性之间微调而产生的[2]。研究证明,音乐主要通过改善AD患者的神经可塑性、神经再生等机制来改善AD的整体认知功能[23]。音乐疗法相比于药物治疗等具有更小的副作用,应用的局限性更小,初步的研究结果也为未来的应用带来了希望。
重复经颅磁刺激(Repetitive transcranial magnetic stimulation,rTMS)是一种非入侵性神经调控技术,其通过线圈产生可以穿过头皮的磁场来诱导运动皮层的兴奋性变化。研究发现,rTMS通过影响大脑区域,增强不同神经递质的释放,促进神经营养信号的传导,且rTMS会影响谷氨酸的释放,影响钙介导的信号传导,调节突触可塑性,目前被证明的刺激靶点多为背外侧前额叶皮层[24]。rTMS是一种安全有效的脑刺激工具,在将来的研究中有望成为潜在的治疗干预措施。
3 展望
对神经可塑性的研究为相关疾病与认知功能的治疗提供了思路,通过了解认知与神经可塑的关系,为治疗及药物的研发提供了新方向。而非药物干预对AD的治疗安全有效且使用范围广,有很大的经济及社会效益。虽然在临床应用上仍存在问题,但其细胞和分子机制为AD临床实践提供了理论基础。目前的治疗方案并不能根治AD,且存在副作用,因此探索新的治疗策略非常迫切。而基于改善突触可塑性,深入探讨干预神经再生防治相关疾病及并发症,或在药物治疗时联合功能锻炼、认知训练等方法对认知功能改善有广阔的发展前景。
