联合检测血常规、D-二聚体及降钙素原与新生儿败血症继发坏死性小肠结肠炎的关系
2023-07-10王娟马进田庆
王娟 马进 田庆
新生儿坏死性小肠结肠炎(necrotizing enterocolitis,NEC)是多种因素引发的新生儿并发症,能导致肠道受损或坏死,严重影响新生儿的生存质量。有研究报道[1]NEC 的病死率约为20%左右,然而NEC 早期临床症状不典型。因此,探索理想的生物学指标在NEC 新生儿的诊断及预后起着关键作用。近年来,血清学指标因其具有操作简单、敏感度高等优势在临床诊疗中发挥着重要作用。血常规是临床上常用的炎症诊断指标;D-二聚体(D-dimer,D-D)是交联纤维蛋白的降解产物,可反映肠道炎症情况[2];降钙素原(ProcaIcitonin,PCT)是临床诊断及预后评估常用的血清指标,其在细菌感染2~3 h 内异常增加,可作为全身炎症反应的可靠指标[3]。本研究旨在探讨联合血常规、D-D 及PCT 水平检测与新生儿败血症继发坏死性小肠结肠炎的关系,现报道如下。
1 资料与方法
1.1 一般资料
选择2019 年8 月至2022 年9 月皖北煤电集团总医院收治的100 例新生儿败血症患儿,并按是否继发NEC 分为NEC 组(n=12)和非NEC 组(n=88)。纳入标准:①新生儿败血症结合血培养检测及临床特征,符合《新生儿败血症诊疗方案》[4]中相关诊断标准;②NEC 符合《实用新生儿学》[5]相关标准;③入院时接受血常规、D-D 及PCT 检测;④临床资料完整。排除标准:①除败血症外引起的NEC;②合并血液系统疾病;③合并肠旋转不良、先天性巨结肠等先天性消化道畸形者;④临床资料欠缺。本研究已获得所有受试者监护人知情同意。
1.2 方法
1.2.1 资料收集
查阅病历资料获取患儿及孕母围生期的临床资料与实验室指标,患儿资料:胎龄、性别、出生体重、出生方式、喂养方式、脐静脉置管等;孕母围生期资料:年龄、是否合并妊娠期高血压疾病、妊娠糖尿病、产前使用激素等;实验室指标:白细胞计数(White blood cell,WBC)、平均血小板体积(Mean platelet volume,MPV)、红细胞分布宽度(Red Cell volume Distribution Width,RDW)、血小板计数(Platelet,PLT)、中性粒细胞计数(Neutrophil,NEUT)、D-D 及PCT。
1.2.2 实验室检测
新生儿败血症患儿于入院第一天在无菌条件下采集静脉血标本2 mL 注入血培养瓶,使用梅里埃BacT/ALERT 3D120 全自动血培养仪培养。采用希森美康XN-2800 全自动血球仪检测血常规指标,包括WBC、MPV、RDW、PLT、NEUT;采用CS 5100 全自动血凝分析仪及配套试剂以免疫比浊法检测血清D-D 水平;采用万泰全自动免疫荧光酶标仪及配套试剂以酶联荧光分析法检测血清PCT 水平。以上检测工作均由本院专业检验人员严格按照说明书进行并记录检测结果。
1.3 相关定义
妊娠期高血压疾病、妊娠糖尿病等疾病符合《实用妇产科学》[6]第4 版中的相关诊断标准。
1.4 统计学方法
采用SPSS 23.0 统计学软件分析处理数据,计数资料以n(%)描述,行χ2检验;计量资料以()描述,两组间比较行t检验。多因素Logistic 回归分析影响新生儿败血症继发NEC的独立危险因素;采用受试者工作曲线(ROC)分析血常规、D-D 及PCT 对新生儿败血症继发NEC 的预测价值。P<0.05 时表示差异有统计学意义。
2 结果
2.1 两组临床资料比较
NEC 组和非NEC 组患儿的胎龄、喂养方式、脐静脉置管、WBC、MPV、D-D 及PCT 等比较,差异均有统计学意义(P<0.05)。见表1。
表1 两组临床资料比较[n(%),()]Table 1 Comparison of clinical data between the two groups[n(%),()]
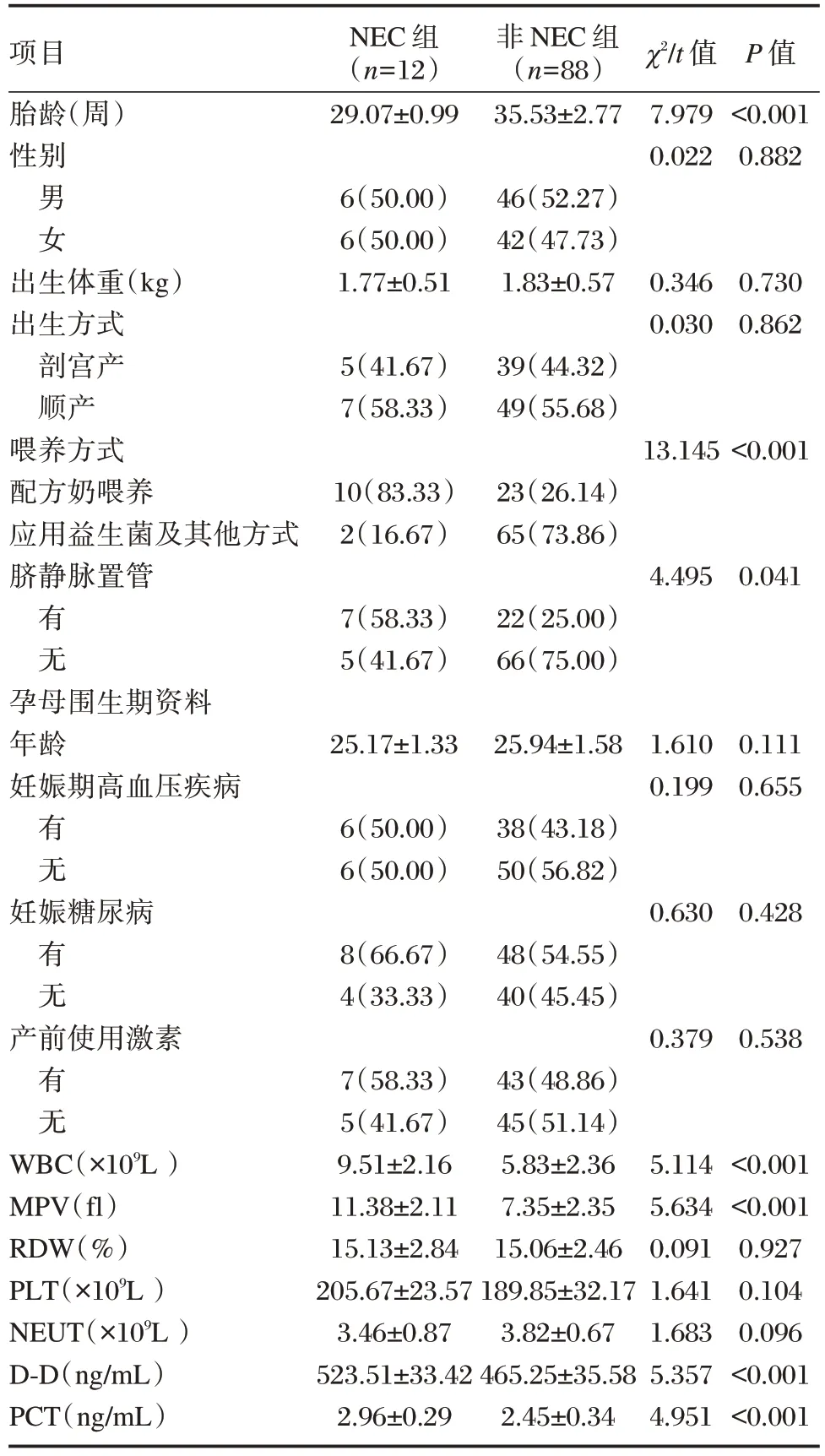
表1 两组临床资料比较[n(%),()]Table 1 Comparison of clinical data between the two groups[n(%),()]
2.2 新生儿败血症继发NEC 的多因素Logistic 回归分析
以新生儿败血症患儿中是否继发NEC 为因变量,将胎龄、喂养方式、脐静脉置管、WBC、MPV、D-D 及PCT 为自变量纳入Logistic 回归模型。多因素Logistic 回归分析显示,胎龄、喂养方式、WBC、MPV、D-D 及PCT 均是新生儿败血症继发NEC 的独立有关(P<0.05)。见表2。
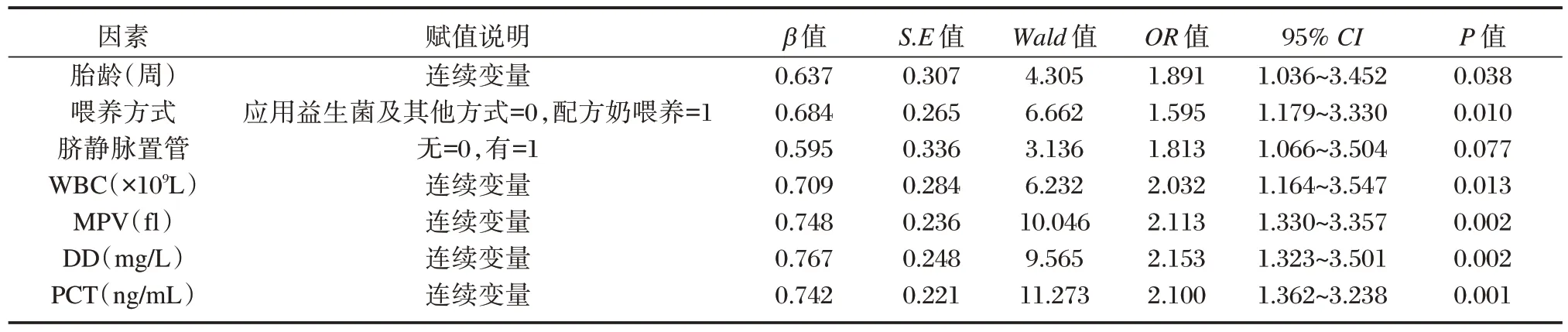
表2 新生儿败血症继发NEC 的多因素Logistic 回归分析Table 2 Multifactorial logistic regression analysis of neonatal sepsis secondary to NEC
2.3 WBC、MPV、D-D 及PCT 对新生儿败血症继发NEC 的预测价值
ROC 曲线显示,WBC、MPV、D-D 及PCT 及四者联合检测曲线下面积为0.685、0.821、0.784、0.703、0.906,其中联合检测的预测价值高于单一检测指标,敏感度0.917、特异度0.932。见表3、图1。

图1 ROC 曲线分析Figure 1 ROC curve analysis
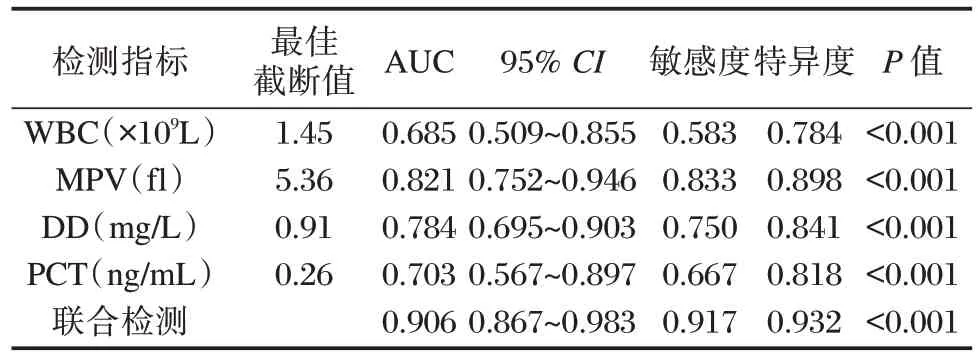
表3 WBC、MPV、D-D 及PCT 对新生儿败血症继发NEC的预测价值Table 3 Predictive value of WBC,MPV,D-D and PCT in neonatal sepsis secondary to NEC
3 讨论
近年来,随着医学水平的完善及快速发展,新生儿存活率逐渐升高,同时NEC 的发病率也在不断呈上升趋势,成为了新生儿主要的死亡原因之一[7]。研究表明[8]败血症是NEC 发病的独立危险因素,而早期NEC 临床症状不典型,以往主要按照患儿的临床表现及影像学进行诊断,欠缺连续性,不利于治疗方案的制定、改善。因此,寻找有效、可靠的早期肠道病变诊断的评估指标,成为新生儿败血症继发NEC 临床诊断面临的挑战之一。
本研究探讨了新生儿败血症继发NEC 的相关影响因素,多因素Logistic 回归分析提示NEC 的发生是由多种因素共同诱发的结果,故了解新生儿败血症继发NEC 的相关因素,对早期制定对应措施以降低或防止NEC 的发生及发展均有积极意义。胎龄越小的新生儿其肠道结构、功能发育较胎龄越大者更不成熟,抵抗病原菌的能力更弱,加之感染败血症后易导致机体内炎症因子上升,使肠道菌群失调,导致NEC 的发风险更高,与既往研究[9]相符。本研究中配方奶喂养的患儿继发NEC的情况显著高于应用益生菌及其他方式喂养的患儿,与刘欣等[10]研究一致,可能因配方奶最缺乏免疫因子、生长发育因子、溶菌酶及乳铁蛋白等这些活性物质,抗感染、免疫调节及抗氧化的能力较弱,故更易继发NEC。
血常规是临床上常用的血液指标已在临床检测广泛应用,本研究中NEC 组的WBC、MPV 均高于非NEC 组,提示血常规中的WBC、MPV 异常表达可能与NEC 的发生有关。白细胞是人体中重要的防御细胞,也是最早了解提示感染的指标之一,当机体处于急性感染期时白细胞会异常上升,可能因当发生NEC 时白细胞会从血管内渗出,并且在细胞因子作用下募集至炎症组织,导致白细胞计数升高[11]。MPV 是炎症过程驱动的血小板活化的直接指标,而本研究中MPV 与新生儿败血症继发NEC的密切相关,与蔡娜等[12]研究报道一致,可能因感染、缺氧、缺血等情况下会激活大量的血小板活化因子,使血小板凝聚成微血栓,造成肠系膜动脉缺血坏死,而在循环中血小板数量的降低可反馈激活巨核细胞,进一步引出更大体积的血小板,从而产生大量的血栓素,致密颗粒和炎症因子被释放,易产生血栓,且以上过程形成恶性循环,增加肠道损伤的程度,进而诱发NEC[13]。D-D 是交联纤维蛋白的降解产物,其水平高低可反映肠道炎症情况、凝血状态以及纤维溶解等情况,NEC 发生时血液往往为高凝状态,血小板异常且体积变小,导致增加活化,进一步释放大量炎性因子,最终导致肠黏膜缺血坏死[14]。姜立军等[15]研究也表示D-D 水平可作为明确NEC 发生及发展的可靠指标,而本研究中NEC 组中的D-D 水平异常升高,提示可作为早期诊断新生儿败血症继发NEC 的有效指标,与以上描述相符。本研究中NEC 组的PCT 水平异常高表达,与新生儿败血症继发NEC 的密切相关,提示其可能是早期诊断新生儿败血症继发NEC 的指标。PCT属无激素活性糖蛋白,正常情况下其表达极低,如机体受到细菌感染后,在4 h 其浓度会提高,并在6~8 h 内达到高峰,对细菌感染具有特异性[16]。因此,如患儿的PCT 水平持续上升,可能提示着NEC的发生,有助于NEC 的早期鉴别。此外,本研究结果提示WBC、MPV、D-D 及PCT 可作为新生儿败血症继发NEC 的早期诊断指标,且结果显示联合检测可提高预测新生儿败血症继发NEC 的敏感度和特异度。
综上,新生儿败血症继发NEC 与胎龄、喂养方式、WBC、MPV、D-D 及PCT 等密切相关,且WBC、MPV、D-D 及PCT 可作为临床诊断新生儿败血症继发NEC 的有效、可靠指标,而联合检测更有助于对新生儿败血症继发NEC 作出更准确地评判,对于降低或预防NEC 具有重要的临床指导意义。
