STAT1诱导的LINC00987调节miR-223-3p/FZD4促进人胶质母细胞瘤相关巨噬细胞向M2型极化
2023-07-05张宝瑞马春晓秦历杰
张宝瑞,马春晓,秦历杰*
河南省人民医院 1.急诊科;2.神经外科,河南 郑州 450003
胶质瘤是中枢神经系统最常见的脑肿瘤,其中又以胶质母细胞瘤(glioblastoma, GBM)恶性程度最高,侵袭性最强[1]。因此,迫切需要提供更有效的治疗手段和策略。
以往有研究表明敲减LINC00987能够抑制急性髓系白血病的进展[2]。也有研究发现其在乳腺癌中能够作为免疫相关lncRNA[3]。STAT1作为转录因子可促进GBM细胞增殖[4]。另外,许多关键的微小RNA(microRNA, miRNAs)与GBM的发病密切相关,如miR-223-3p可抑制GBM细胞的增殖和迁移[5]。卷曲蛋白4(frizzled 4,FZD4)基因作为frizzle基因家族的一员,其表达在细胞增殖、黏附、迁移等细胞活动中起着关键作用,FZD4已被证实在GBM中表达升高并发挥促癌作用[6]。
本研究旨在探索STAT1转录激活的lncRNA LINC00987在GBM中的作用并探究其与GBM相关巨噬细胞极化的关系及其具体机制。
1 材料与方法
1.1 材料与试剂
人单核细胞白血病细胞系THP-1、人正常神经胶质细胞系HEB和人GBM细胞系SNB19、A172、LN229、TG-905细胞、人胚胎肾细胞系HEK-293T(ATCC公司)。LINC00987探针、荧光原位杂交试剂盒(RiboBio公司);Western blot实验相关抗体(Abcam公司);Trizol试剂盒(Invitrogen公司);Lipofectamine 3000转染试剂、TransScript Green One-Step RT-qPCR SuperMix试剂盒、酶标仪(Thermo Fisher公司);反转录试剂盒(TaKaRa公司);DMSO溶液(北京索莱宝科技有限公司);VEGF、TGF-β1 ELISA 试剂盒(上海纪宁实业有限公司);引物设计、过表达质粒及其siRNA干扰质粒(上海吉玛基因公司)。
1.2 方法
1.2.1 生物信息学分析数据库:从GEO数据库下载GBM相关芯片GSE100736。JASPAR数据库(http://jaspar.genereg.net/)测试转录因子与lncRNAs的潜在结合位点。通过RNA22(https://cm.jefferson.edu/rna22/Interactive/)、lncBook(https://bigd.big.ac.cn/lncbook/index)和lncRNASNP在线靶点预测网站搜索lncRNAs的靶miRNAs。miRDB(http://mirdb.org/index.html)、miRWalk(http://mirwalk.umm.uni-heidelberg.de)和StarBase(http://starbase.sysu.edu.cn/)获取miRNAs的下游靶基因。利用在线工具Venn图(http://bioinformatics.psb.ugent.be/webtools/Venn/)取得靶miRNAs和靶基因的交集。利用DAVID数据库(https://david.ncifcrf.gov/summary.jsp)进行KEGG富集分析。并利用DisGeNET数据库(https://www.disgenet.org/)获取GBM的疾病风险基因,筛选条件设置为GDA Score≥0.5。将筛选出的基因使用STRING(https://string-db.org)进行蛋白互作用关联分析。TIMER 2.0(http://timer.cistrome.org/)用于预测基因与免疫细胞的相关性。
1.2.2 临床组织标本的收集:GBM组织取自2018年9月至2020年6月在河南省人民医院神经外科行胶质瘤根治性切除术的39例患者,其中男23例,女16例。患者年龄在39~65岁,平均年龄(47.3±3.6)岁。患者在术前均未接受任何同步放射治疗和化学治疗(放化疗)、辅助化疗、免疫治疗等任何治疗手段。取患者癌组织和癌旁组织,-80℃保存。样本采集前获得所有患者的书面知情同意并获得了河南省人民医院医学伦理委员会的批准(审批编号:2018-110-014)。
1.2.3 细胞的分组与转染:HEB细胞在YM11琼脂培养基中培养。GBM细胞SNB19、A172、LN229、TG-905培养于DMEM培养基中,细胞培养条件为37 ℃、5% CO2、湿度100%,连续培养24 h。待细胞培养至汇合度为80%进行传代,传代具体操作详见说明书。采用LipofectamineTM3000依据试剂盒说明书将si-LINC00987、over-expression(oe)-LINC00987、miR-223-3p inhibitor、si-FZD4及各自阴性对照序列对细胞进行转染。将THP-1巨噬细胞接种于96孔板上,用100 nmol/L 佛波醇酯(phorbol-12-myristate-13-acetate,PMA)处理48 h,以诱导M0型巨噬细胞,随后将M0型巨噬细胞用100 ng/mL LPS、20 ng/mL IFN-γ持续孵育24 h以诱导M1型巨噬细胞,用20 ng/mL IL-4持续孵育24 h以诱导M2型巨噬细胞。为模拟胶质瘤浸润微环境,将THP-1细胞与GBM细胞共培养。取LINC00987表达最高的GBM细胞系和THP-1细胞共培养24 h后转染并分为如下组:si-NC组(细胞转染si-LINC00987阴性对照载体)、si-LINC00987组(细胞转染si-LINC00987载体)、oe-NC组(细胞转染oe-LINC00987阴性对照载体)、oe-LINC00987组(细胞转染oe-LINC00987载体)、inhibitor-NC组(细胞转染miR-223-3p inhibitor阴性对照载体)、miR-223-3p inhibitor组(细胞转染miR-223-3p inhibitor载体)、miR-223-3p inhibitor+si-NC组(细胞转染miR-223-3p inhibitor和si-LINC00987阴性对照载体)、miR-223-3p inhibitor+ si-LINC00987组(细胞转染miR-223-3p inhibitor和si-LINC00987载体)、si-FZD4-NC组(细胞转染si-FZD4的阴性对照载体)、si-FZD4组(细胞转染si-FZD4)、si-FZD4+oe-NC组(细胞转染si-FZD4和oe-LINC00987阴性对照载体)、si-FZD4+oe-LINC00987组(细胞转染si-FZD4和oe-LINC00987载体)。
1.2.4 RT-qPCR检测mRNA:借助Trizol试剂对细胞及组织中的总RNA进行提取,利用反转录试剂盒反向转录合成第一链cDNA,利用SYBRPremix EX Taq 试剂盒完成RT-PCR合成及Q-PCR。反应体系和反应条件均依据试剂盒说明书配制和进行。引物序列见(表1),miR-223-3p以U6作为内参,STAT1、LINC00987、FZD4以GAPDH作为内参,2-△△Ct法计算相对表达量。

表1 RT-qPCR引物
1.2.5 酶联免疫吸附试验检测VEGF、TGF-β1浓度:收集细胞培养上清液,按照人VEGF、TGF-β1 ELISA 检测试剂盒说明书要求,设置标准品孔或待测样品孔分别加入50 μL的标准品和待测样本,之后加入HRP标志的待测抗体100 μL,封住反应孔,恒温箱温育60 min。加入底物进行反应,之后加入50 μL终止液并在15 min内借助酶标仪测定各孔450 nm处吸光度值。
1.2.6 荧光原位杂交(fluorescence in situ hybridization experiment, FISH)检测LINC00987的亚细胞定位:按照FISH试剂盒说明书要求,首先培养细胞,待细胞汇合度达到70%左右时固定并通透细胞。加入预杂交液和杂交液,避光条件下加入2.5 μL的LncRNA FISH Probe Mix储存液,弃预杂交液,加入100 μL探针杂交液,避光清洗细胞,DAPI染色,PBS冲洗细胞后显微镜观察染色情况。
1.2.7 双荧光素酶报告基因实验检测分子间的靶向关系:采用双荧光素酶分析报告试验验证LINC00987和miR-223-3p、miR-223-3p和FZD4的靶向关系。依据试剂盒说明书要求构建LINC00987的野生型(LINC00987-WT)和突变型(LINC00987-MUT)以及FZD4的野生型(FZD4-WT)和突变型质粒(FZD4-MUT)。用LipofectamineTM 3000转染试剂分别将上述质粒与miR-223-3p或mimic-NC两两共转染HEK-293T细胞。转染48 h后,使用双荧光素酶报告基因分析系统试剂盒检测荧光素酶活性。
1.2.8 染色质免疫沉淀(chromatin immunoprecipitation, ChIP)试验:将细胞在室温下与1%甲醛交联10 min,然后加入125 mmol/L甘氨酸终止交联。吸弃培养皿中的甲醛-甘氨酸复合物。将培养皿转移至冰上,加入1 mL预冷的PBS,12 μL的PMSF和10 μL的蛋白酶抑制剂。将细胞悬浮后转移至EP管中4 ℃ 10 000 r/min离心5 min,超声处理后加入氯化钠溶液在65 ℃下孵育。2 h后加入1 μL的蛋白酶K继续孵育1 h。加入酚氯仿提取DNA,随后用1.5%的琼脂糖凝胶电泳进行检测。将磁珠和抗体的混合物在3 000 r/min离心2 min,弃去上清后加入RIPA裂解液清洗,随后加入超声处理后的染色质和RIPA溶液。RNA结合蛋白免疫沉淀后纯化DNA,对输入的DNA进行RT-qPCR分析。
1.2.9 流式细胞仪检测巨噬细胞表面标志物的表达:取共培养后的巨噬细胞,胰蛋白酶消化,每管细胞数约 5×105,1 000 r/min离心1 min,PBS冲洗,再次离心后重悬细胞。每管细胞加入 1 μg FITC标志的CD14抗体和1 μg PE标记的CD206抗体,4 ℃孵育 30 min,1 000 r/min离心 1 min,无菌 PBS洗去游离抗体,300 μL含 10%FBS 无菌 PBS 重悬细胞后上样检测细胞表面CD14和CD206的表达。
1.3 统计学分析

2 结果
2.1 LINC00987在GBM中的表达
GSE100736数据集揭示了在GBM中的差异表达lncRNAs(图1A)。LINC00987在GBM中升高且差异显著。相对于癌旁组织,GBM组织中LINC00987的表达明显增强(图1B)。且相对于HEB细胞,LINC00987在SNB19、A172、LN229、TG-905细胞中的水平均上调,且在LN229中水平最高(P<0.05)(图1C)。

A.differentially expressed lncRNAs in GSE100736 dataset; B.expression levels of LINC00987 in paracancerous and cancerous tissues(n=39); C.expression levels of LINC00987 in HEB and GBM cell lines n=3); *P<0.05 compared with adjacent tissue; #P<0.05 compared with HEB cells.
2.2 LINC00987与STAT1的关系
LINC00987启动子与STAT1存在结合位点(图2A)。相对于癌旁组织,STAT1在GBM组织中表达上调(P<0.05)(图2B)。此外,与HEB细胞相比,STAT1在SNB19、A172、LN229、TG-905细胞中表达增强(P<0.05)(图2C)。相对于si-NC,si-STAT1组中LINC00987表达降低,而相对于pcDNA3.1组,pcDNA3.1-STAT1组LINC00987表达增强(P<0.05)(图2D)。相对于anti-IgG组,anti-STAT1组中富集的LINC00987表达更高(P<0.05)(图2E)。

A.binding site of LINC00987 and STAT1; B.expression of STAT1 in GBM tissues and adjacent tissues(n=39); C.expression of STAT1 in different cell lines ; D.effects of STAT1 on the expression of LINC00987 in LN229 cells; E.chIP experimental results in LN229 cells n=3); *P<0.05 compared with adjacent tissue, #P<0.05 compared with HEB cells; △P<0.05 compared with si-NC; ▲P<0.05 compared with pcDNA3.1; ★P<0.05 compared with anti-IgG.
2.3 LINC00987对M2型巨噬细胞极化的影响
构建稳定转染si-LINC00987、oe-LINC00987的LN229细胞(图3A)。与M0组相比,M2组中LINC00987的表达水平显著增高(P<0.05)(图3B)。与oe-NC组相比,oe-LINC00987组CD14+/CD206+巨噬细胞数目增多,而si-LINC00987组与si-NC组相比CD14+/CD206+巨噬细胞数目减少(均P<0.05)(图3C)。此外,与si-NC组相比,si-LINC00987组细胞培养上清液中M2型细胞因子VEGF,TGF-β1浓度减少,而oe-LINC00987组VEGF、TGF-β1较oe-NC组浓度增多(均P<0.05)(图3D)。
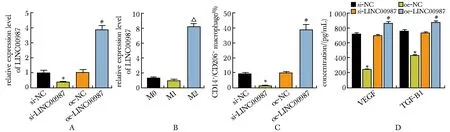
A.transfection efficiency of oe-LINC00987 and si-LINC00987; B.expression of LINC00987 in M0, M1, and M2 macrophages; C.proportion of CD14+/CD206+ macrophages detected by flow cytometry; D.ELISA was used to detect the concentration of VEGF and TGF-β1; *P<0.05 compared with si-NC; #P<0.05 compared with oe-NC; △P<0.05 compared with M0.
2.4 miR-223-3p和LINC00987的关系验证
LINC00987主要分布于胞质中(图4A)。LINC00987的靶miRNAs交集见(图4B)。RT-qPCR证实GBM标本中miR-223-3p的表达明显低于Adajcent组(P<0.05)(图4C),且与LINC00987的表达水平呈负相关(r=-0.3755,P<0.05)(图4D)。4株GBM细胞中miR-223-3p的水平相较于对照组也有明显的下调(P<0.05)(图4E)。双荧光素酶分析结果印证miR-223-3p是LINC00987的直接作用靶点(图4F)。

A.FISH assay was used to detect the subcellular localization of LINC00987 in LN229 cells(scale bar=25 μm); B.intersection of downstream target miRNAs of LINC00987; C.RT-qPCR was used to detect the expression level of miR-223-3p in GBM tissue and adjacent tissue(n=39); D.Pearson correlation analysis of miR-223-3p and LINC00987 expression levels; E.miR-223-3p expression levels in each group of cell lines; F.miR-223-3p and LINC00987 binding sites and dual luciferase reporter assay result in LN229 cells; *P<0.05 compared with adjacent tissue; #P<0.05 compared with HEB; △P<0.05 compared with mimic-NC.
2.5 抑制miR-223-3p对M2型巨噬细胞极化的作用
转染miR-223-3p inhibitor后LN229细胞中miR-223-3p水平显著下调,而同时敲减LINC00987后miR-223-3p的表达显著升高(均P<0.05)(图5A)。与M0组相比,M2组中miR-223-3p的表达水平显著下降(P<0.05)(图5B)。miR-223-3p inhibitor组与inhibitor-NC组相比CD14+/CD206+巨噬细胞数目增多,VEGF、TGF-β1释放增多,而miR-223-3p inhibitor+si-LINC00987组与miR-223-3p inhibitor+si-NC组相比CD14+/CD206+巨噬细胞数目减少,VEGF、TGF-β1释放减少(均P<0.05)(图5C, D)。

A.expression of miR-223-3p in each group of cells; B.expression of miR-223-3p in M0, M1, and M2 macrophages; C.proportion of CD14+/CD206+ macrophages detected by flow cytometry; D.ELISA was used to detect the concentration of VEGF and TGF-β1; *P<0.05 compared with inhibitor-NC; #P<0.05 compared with miR-223-3p inhibitor+si-NC; △P<0.05 compared with M0.
2.6 FZD4与miR-223-3p的关系验证
在miRDB、miRWalk和StarBase获取miR-223-3p的下游靶基因并取交集,共有181个结果(图6A)。miR-223-3p的靶基因显著富集在癌通路中(图6B)。将富集在癌通路中的基因与GBM的疾病风险基因(EGFR、PTEN、MTOR和人H3-3A)进行互作用分析(图6C)。在TIMER数据库还发现FZD4在GBM中与巨噬细胞存在正相关关系(图6D)。相对于癌旁组织和HEB细胞,GBM组织和细胞中FZD4表达显著增强(图6E, F)。此外,相对于inhibitor-NC组,miR-223-3p inhibitor组中FZD4表达增强,相对于miR-223-3p inhibitor+si-NC组, miR-223-3p inhibitor+si-LINC00987组FZD4的表达被抑制(均P<0.05)(图6G)。FZD4和miR-223-3p的结合位点见图6H,双荧光素酶报告实验进一步验证了二者的靶向关系(图6I)。
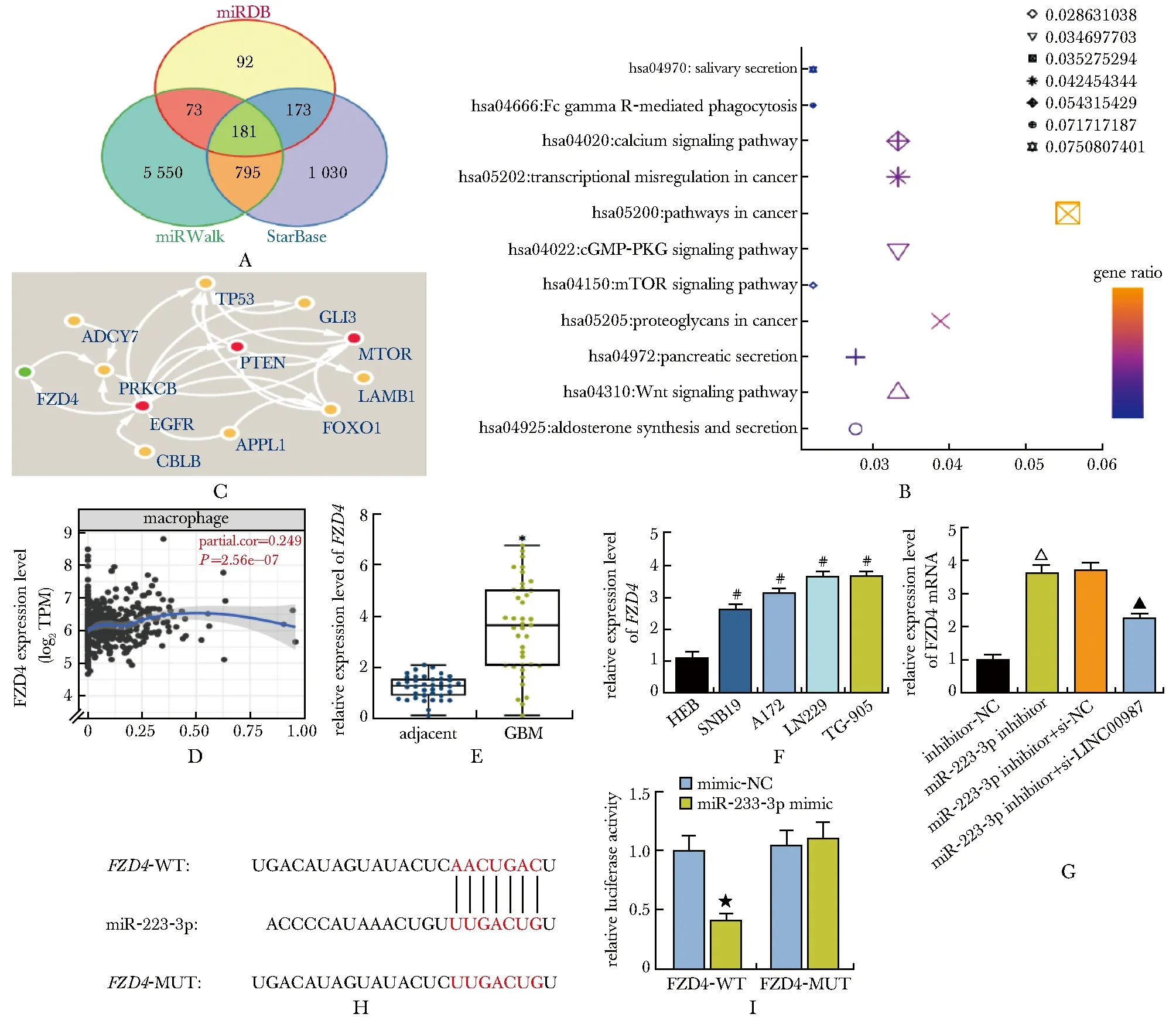
A.miRDB, miRWalk and StarBase were used to predict the target genes of miR-223-3p; B.KEGG analysis results; C.protein interaction analysis results; D.TIMER website prediction results; E.RT-qPCR was used to detect the expression level of FZD4 in GBM tissue and adjacent tissue(n=39); F.FZD4 mRNA expression levels in each group of cell lines; G.effects of miR-223-3p and LINC00987 on FZD4 expression levels in LN229 cells; H.binding sites between FZD4 and miR-223-3p; I.dual luciferase reporter assay results in LN229 cells; *P<0.05 compared with adjacent tissue; #P<0.05 compared with HEB cells; ΔP<0.05 compared with inhibitor-NC; ▲P<0.05 compared with miR-223-3p inhibitor+si-NC; ★P<0.05 compared with minic-NC.
2.7 敲减FZD4对M2型巨噬细胞极化的抑制作用能被过表达LINC00987部分消解
转染si-FZD4后LN229细胞中FZD4mRNA水平显著下调,而同时转染oe-LINC00987后FZD4的mRNA表达显著升高(均P<0.05)(图7A)。与M0组相比,M2组中FZD4的表达水平显著上调(P<0.05)(图7B)。与si-FZD4-NC组相比,si-FZD4组CD14+/CD206+巨噬细胞数目减少,VEGF、TGF-β1浓度减少,而si-FZD4+oe-LINC00987组与si-FZD4+oe-NC相比CD14+/CD206+巨噬细胞数目增多,VEGF、TGF-β1浓度增加(均P<0.05)(图7C, D)。
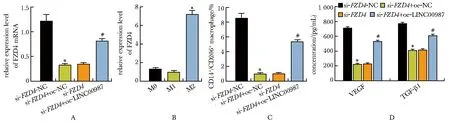
A.expression of FZD4 mRNA in each group of cells; Bexpression of FZD4 in M0, M1, and M2 macrophages; C.proportion of CD14+/CD206+ macrophages detected by flow cytometry; D.ELISA was used to detect the concentration of VEGF and TGF-β1; *P<0.05 compared with si-FZD4-NC; #P<0.05 compared with si-FZD4+oe-NC; △P<0.05 compared with M0.
3 讨论
本研究通过GEO数据库对GBM相关lncRNAs进行预测,发现LINC00987在GBM标本中显著上调。LINC00987以往被证实在急性髓系白血病中表达上调并参与了疾病的进展[2]。此外,LINC00987也被发现与乳腺癌免疫微环境有关[3]。然而其在GBM中的作用尚不清楚。结合生信分析结果,本研究借助RT-qPCR对GBM组织和细胞中LINC00987的表达进行检测,结果显示相对于癌旁组织和正常细胞,GBM组织和细胞中LINC00987的表达显著增强。为探究其在GBM中的具体机制及影响效果,本研究通过JASPAR数据库,在LINC00987的启动子区域发现结合分数最高的为STAT1转录因子。以往有研究表明,STAT1能够直接与SH2B3启动子结合并在转录水平激活SH2B3的表达,在功能上诱导GBM细胞增殖、迁移进而促进GBM进展[7]。本研究通过ChIP试验验证了STAT1转录因子与LINC00987启动子的结合,并且验证了STAT1能够激活LINC00987的表达从而参与GBM的进展。
肿瘤中的巨噬细胞分为M1型和M2型两个主要亚群,M1型巨噬细胞具有抗原呈递能力,可诱导Th1反应并且与抗肿瘤有关,而M2型巨噬细胞则主要与肿瘤活性促进有关[8]。本研究发现LINC00987在M2型巨噬细胞中显著高表达。CD14和CD206均为M2型巨噬细胞的标志物[8]。将THP-1细胞与LN229细胞共培养后,相对于oe-NC组,oe-LINC00987组的CD14+/CD206+巨噬细胞数目显著增加也提示了LINC00987在促进GBM向M2型巨噬细胞极化的作用。TGF-β和VEGF能够诱导巨噬细胞的M2型极化,而肿瘤细胞则进一步联合分化而来的M2型巨噬细胞从而分泌大量炎性因子抑制机体的抗肿瘤免疫等[9]。
miR-223-3p可以作为抑癌基因阻碍GBM的发展[10]。本研究证实miR-223-3p为LINC00987的靶标。实验结果表明抑制miR-223-3p显著提高了CD14+/CD206+巨噬细胞的数目以及TGF-β1和VEGF浓度。通过生物信息学分析筛选,FZD4被确认为本实验中miR-223-3p的下游靶基因。在以往的研究中发现,FZD4能调控胶质瘤干细胞的干性和侵袭性,严重影响着GBM的复发和预后不良[11]。本研究证实FZD4在GBM中水平显著上调, 敲减FZD4能够诱导巨噬细胞向M2表型极化,但该作用能被过表达LINC00987部分消解, 证明了STAT1/LINC00987/miR-223-3p/FZD4调节轴的存在及对GBM细胞生物学功能的调控作用。
综上所述,本研究证明转录因子STAT1能够通过激活LINC00987调控miR-223-3p/FZD4进而诱导巨噬细胞向M2型极化从而发挥促癌和免疫抑制作用,本研究首次披露了LINC00987在GBM中的调控作用和机制。干预LINC00987的表达有望成为GBM治疗的新策略。
