胃食管交界部SMARCA4缺陷型未分化癌
2023-07-05陈淑梅黄汉兴
陈淑梅 黄汉兴
莆田市第一医院病理科 (福建 莆田 351100)
SMARCA4基因位于19p13染色体,属于SWI/SNF的核心催化亚基之一,编码BRG1蛋白,表达于所有正常细胞。BRG1蛋白是一种磷酸化核蛋白,主要通过ATP依赖的方式破坏组氨酸-DNA的接触、改变染色体结构从而调节基因的表达。SWI/SNF复合体(SWitch/sucrose-nonfermenting complexes)是染色质重塑家族的重要成员,最初被描述为诱导型和谱系特异性基因的转录调控因子,由12-15个亚基构成。SWI/SNF复合体中的常见亚基包括SMARCA4(BRG1)、SMARCA2(BRM)、SMARCB1(INI1)、ARID1A、ARID1B和PBRM1。SWI/SNF复合体已被证实与许多人类疾病相关,尤其是恶性肿瘤,约20%的肿瘤中发现了涉及SWI/SNF复合体各种亚基的突变、易位和缺失,使该复合体成为恶性肿瘤中最常见的靶点之一[1]。95%的非典型畸胎样/横纹肌样肿瘤、95%的恶性横纹肌肿瘤和90%的上皮样肉瘤具有SMARCB1缺失表达[1-3],约50%的卵巢透明细胞癌中和30%的子宫内膜样癌中发现了ARID1A的缺失表达[1,4-5],41%的透明细胞肾细胞癌具有PBRM1突变[6],约97%的卵巢高钙血症型小细胞癌和约5-35%的非小细胞肺癌(NSCLC)中存在SMARCA4缺失表达[1,7-10]。除此之外,还有许多类型的肿瘤中发现了SWI/SNF复合体中各种亚基缺失的肿瘤,包括乳腺癌、胰腺癌、胃肠道癌、淋巴瘤等。新近报道了几篇消化道原发的SMARCA4缺陷型未分化癌,该类肿瘤在组织学上表现出与SMARCB1缺陷型肿瘤相似的横纹肌样形态学特征,临床表现为高度恶性生物学行为,发现时常伴有淋巴结转移甚至远处转移,预后不良。我们报道2例胃食管交界部SMARCA4缺陷型未分化癌,结合相关文献复习,探讨消化道SMARCA4缺陷型未分化癌的临床病理特征、鉴别诊断及预后等。
1 病例材料
收集2例莆田市第一医院病理科2017年至2020年间诊断的胃食管交界部SMARCA4缺陷型未分化癌。病例资料由查阅电子病历获得,随访信息通过电话咨询获取。随访截至2021年4月12日,生存时间为确诊日到死亡日或随访截止日。
例1,男性,60岁,于2017年2月6日因进行性吞咽困难半月余入院,胃镜示:食管下段、贲门、胃底巨大溃疡型不规则新生物。腹部CT平扫及盆腔CT平扫示:贲门部胃壁不规则增厚,胃周围见多发肿大淋巴结,大者约2.3cm×1.8cm,考虑胃Ca伴胃周淋巴结转移;肝右后叶及左外叶占位。肝脏MRI平扫+动态增强扫描示:胃底贲门部长T1长T2高DWI信号影肿物,侵犯浆膜层外,大小约57.39mm×57.14mm×35.00mm,其下方多发淋巴结转移,腹膜后多发小淋巴结;肝Ⅲ、Ⅶ段转移瘤,长径分别约22.74mm、20.97mm。入院10天后全麻下行“腹腔镜辅助胃癌姑息性切除术+空肠肠袢Roux-en-y代胃术+左肝肿物切除术”。术后予“紫杉醇+顺铂”方案化疗3周期,后改“多西他赛+替吉奥”方案化疗联合靶向治疗2周期,肿瘤持续进展,更改为“奥沙利铂+替吉奥”方案化疗1周期,后改行“奥沙利铂+CF+5-Fu”方案化疗2周期,术后11个月死于肿瘤复发/转移。
例2,男性,80岁,于2020年12月18日因反复上腹部闷痛1月余入院,外院电子胃镜示:贲门占位:癌可能性大。有前列腺电切术及膀胱肿瘤切除术史,2兄弟1姐姐均患有胃癌(具体不详)。胸部+全腹部CT增强扫描示:胃贲门区占位,大小约30.4mm×24.0mm,考虑MT。入院后4天全麻下行“腹腔镜辅助全胃根治性切除,食管空肠Roux-en-y端侧吻合术”。术后4月复查CT示:肝内新见数个结节,考虑肝内多发转移瘤(图5)。
2 结 果
例1大体标本显示肿瘤中心位于贲门(胃食管交界线下2cm内),累及食管下段,瘤体大小7cm×6.5cm×1.5cm,边缘隆起,中央溃疡形成。镜下见肿瘤伴地图样坏死,肿瘤细胞呈失黏附性的上皮样细胞弥漫片状排列,胞浆嗜酸,胞质丰富,核圆形,常偏位,类似横纹肌样细胞,可见核仁(图1、图2),可见双核及多核瘤巨细胞。核分裂像易见(32/10HPF),最高可达8/HPF,可见病理性核分裂像。免疫组化示:BRG1(缺失表达),BRM(表达),INI1(表达),AE1/AE3、CAM5.2、EMA(-),Vimentin(+),P53(-),错配修复蛋白(MLH1、PMS2、MSH2、MSH6)均表达,Ki-67(约70%+),CK7、CK20、Villin、CD45、CD38、CD34、CD117、MyoD1、Desmin、S100、HMB-45、Melan-A均阴性(图3、图4)。
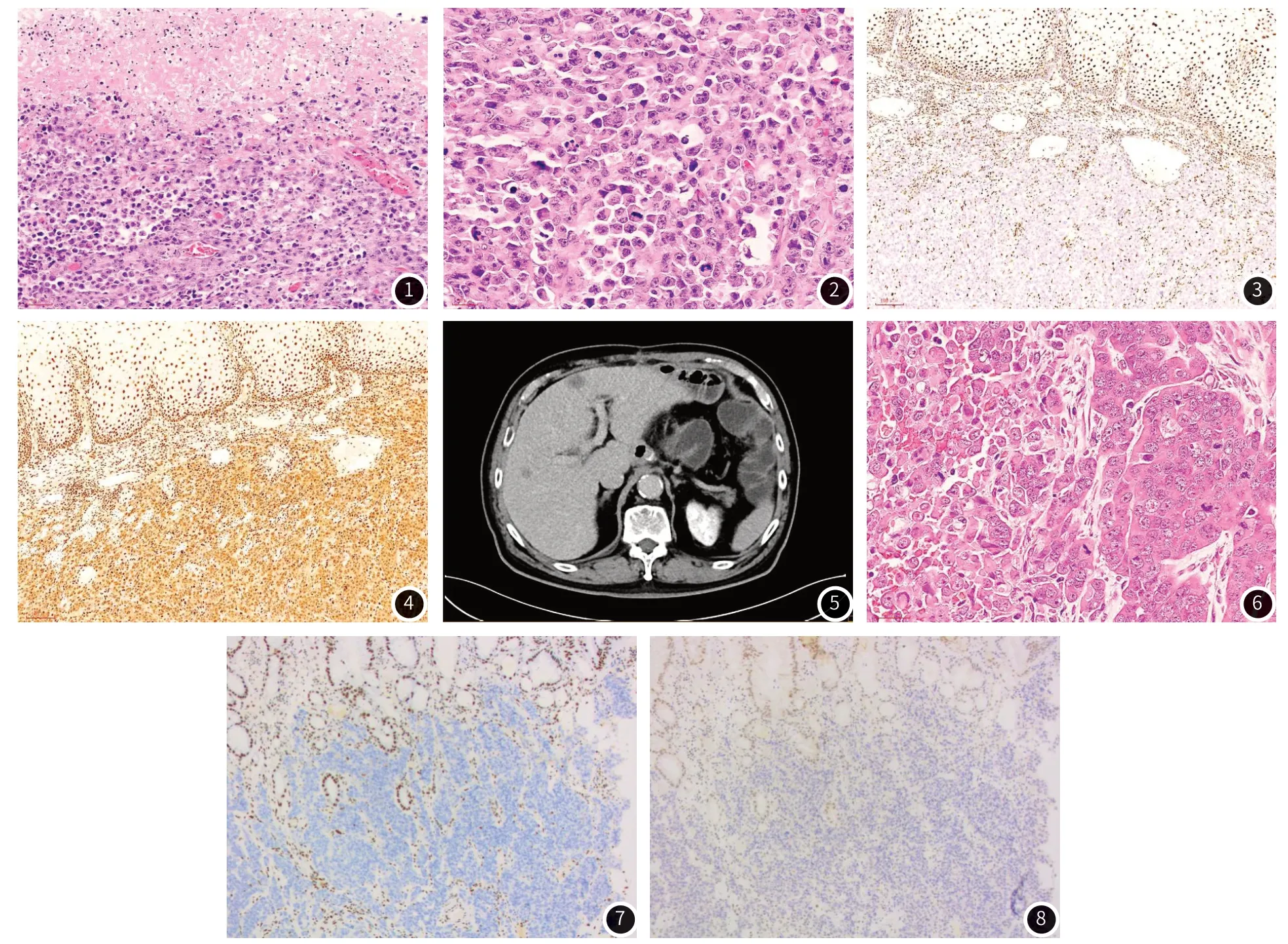
图1~图4为例1;图1 肿瘤内见大片坏死,肿瘤细胞弥漫松散排列。图2 肿瘤细胞呈横纹肌样特征,可见双核/多核,核分裂像易见。图3 免疫组化示SMARCA4缺失表达。图4 免疫组化示SMARCA2保留表达。图5~图8为例2;图5 术后4个月复查CT见肝内多发结节状稍低密度影,考虑转移瘤。图6 镜下见左边肿瘤细胞松散排列,呈横纹肌样特征,右边肿瘤细胞呈巢状排列,细胞大而异型。可见双核/多核瘤巨细胞,核分裂像常见。图7 免疫组化示SMARCA4缺失表达。图8 免疫组化示SMARCA2缺失表达。
例2大体标本显示肿瘤中心位于贲门,累及食管下段,瘤体大小3cm×2.5cm×1.2cm,边缘隆起,中央溃疡形成。镜下见肿瘤伴地图样坏死,部分肿瘤细胞呈失黏附性的上皮样细胞弥漫片状排列,胞浆嗜酸,胞质丰富,核圆形,常偏位,类似横纹肌样细胞,可见核仁,并查见双核及多核瘤巨细胞,另一部分呈黏附性的巢团状排列,肿瘤细胞呈间变样大细胞,核浆比高,核圆形,呈空泡状,核仁常见(图6)。核分裂像易见(52/10HPF),最高可达10/HPF,可见病理性核分裂像。肿瘤边缘见少许贲门腺上皮高级别上皮内瘤变。免疫组化示:BRG1(缺失表达),BRM(缺失表达),INI1(表达),AE1/AE3、CAM5.2、EMA(局灶+),Vimentin(部分+),P53(弥漫强+),错配修复蛋白(MLH1、PMS2、MSH2、MSH6)均表达,Ki-67(约90%+),Syn(部分弱+),CK7、CK20、Villin、CgA、CD56、CD45、CD3、CD79a、Desmin、MyoD1、Myogenin、S100、HMB-45、Melan-A均阴性(图7、图8)。
2例病例最终都诊断为胃食管交界部SMARCA4缺陷型未分化癌。
3 讨 论
原发于消化道的未分化癌罕见,可发生于包括食管、胃食管交界部、胃、结直肠、胰腺等消化道部位。第五版世界卫生组织消化肿瘤分类中提到食管未分化癌好发于食管下段及胃食管交界部[11],有研究显示发生于胃食管交界部的未分化癌占所有食管未分化癌的44%[12]。食管未分化癌的发病年龄范围较广,39-84岁,男性相对多见。临床症状多表现为进行性吞咽困难,其次是胃食管反流、体重减轻和贫血,确诊时常伴有淋巴结转移甚至远处器官转移,最常转移至肝脏,对放化疗效果差。本组2例均位男性患者,平均年龄70岁,肿瘤均位于胃食管交界部。例1确诊时伴有同期淋巴结转移和肝脏多发转移,术后治疗效果差,例2确诊时伴有淋巴结转移,行根治术后4个月复查发现肝脏多发转移。
组织学上该类肿瘤常出现大面积坏死,部分肿瘤细胞呈失黏附性弥漫分布,形态单一,含有丰富的嗜酸性胞浆,核增大,核仁明显,呈横纹肌样形态特征,核分裂像常见,可见病理性核分裂像。本组2例均可见上述横纹肌样特征的肿瘤细胞和活跃的核分裂像,例2中还可见到呈黏附性巢团状分布的间变样大细胞。有学者认为SMARCA4的缺失表达和横纹肌样特征细胞之间存在基因型-表型相关性,其独特的形态对应潜在的分子改变[13]。
Horton RK等[13]研究发现,食管及胃食管交界部SMARCA4缺陷型未分化癌在免疫组化上几乎均有BRG1缺失表达,伴有或不伴有BRM缺失表达,个别病例出现BRM缺失表达但BRG1保留表达,且后者表现出和前者相似的组织学形态特征。该研究同时表示该类肿瘤在起源上更倾向上皮来源,但角蛋白在其中的表达差异很大,约28%的患者广泛表达1种或1种以上的角蛋白抗体,43%的病例则表现为散在或局灶表达,而近30%的病例角蛋白完全阴性。最后,他们还发现近30%的SMARCA4缺陷型未分化癌免疫组化显示P53突变表达,其中75%表现为弥漫阳性,25%表现为全部缺失表达。本组2例免疫组化表达结果既有相同,又有差异。2例患者均表现为BRG1缺失表达,但例1不伴有BRM缺失表达,同时AE1/AE3、EMA、CAM5.2均完全阴性,而例2则伴有BRM缺失表达,同时见AE1/AE3、EMA、CAM5.2局灶阳性。2例患者免疫组化均显示P53突变表达,但例1表现为完全缺失表达,例2表现为弥漫阳性。
鉴别诊断:(1)低分化腺癌:临床表现与本病相似,部分病例形态学与本病有交叉,但免疫组化总是表达广谱角蛋白和低分子角蛋白,且BRG1保留表达。(2)横纹肌肉瘤:瘤细胞具有典型的横纹肌样形态特征,但多发生于儿童及婴幼儿,成人少见,多表达肌源性标记物(如Desmin、MyoD1、myogenin)。(3)恶性黑色素瘤:部分病例与本病具有相似的形态学,瘤细胞形态更多样,大部分病例可见黑色素,且表达黑色素相关标记物(如Melan-A和HMB-45)。(4)上皮样血管肉瘤:多发生于四肢深部软组织,肿瘤可呈实性片状生长,常伴有出血、坏死。部分病例可表达AE1/AE3,血管内皮标记物CD31、ERG、FactorⅧ等可帮助鉴别。(5)滑膜肉瘤:多见于青少年,好发于四肢尤其靠近大关节处,但任何部位均可发生,分化差的滑膜肉瘤可伴有横纹肌样形态,其特异的染色体易位t(X;18) (p11;q11)有助于鉴别。(6)上皮样胃肠道间质瘤:瘤细胞成上皮样,胞浆丰富嗜酸,表达CD117和Dog-1,c-kit或PDGFRA基因有助于鉴别。
BRG1与INI1蛋白具有相似的功能。SMARCA4缺陷型肿瘤最近在卵巢、子宫、肺、鼻窦等多种器官中均有报道[7-10,14-16],并表现出与SMARCB1缺陷型肿瘤相似的形态学。由于角蛋白表达的不确定性且缺乏明确的上皮分化的形态学特征和基因谱表达,一些研究认为原发于胸部的SMARCA4缺陷型肿瘤属于间叶源性肿瘤[17-18]。但随后的多项研究表明,SMARCA4缺失表达是非小细胞肺癌中去分化的一部分。原发于胸部的SMARCA4缺陷型肿瘤到底是来源上皮还是来源间叶尚不完全确定,但越来越多的共识认为发生于胸部的这些肿瘤代表肺的去分化癌[19-20]。而在食管SMARCA4缺陷型未分化癌中,部分病例未分化癌边缘见少许腺上皮肠化、高级别上皮内瘤变及明确的腺癌成分,并在不同肿瘤成分中观察到相同的免疫组化BRG1和P53的改变,因此大部分学者认为SMARCA4缺陷型未分化癌系腺上皮高级别上皮内瘤变和/或腺癌去分化所致。本组例2中发现未分化癌和其边缘的腺上皮高级别上皮内瘤变有相同的免疫组化P53突变模式,支持上述观点。
胃食管交界部SMARCA4缺陷型未分化癌属于罕见的高度恶性肿瘤,临床表现为高侵袭性,确诊时多为晚期,常伴有转移,常见的转移部位为淋巴结和肝脏,复发和/或转移率高,预后不良,病程短,多于术后1年内死亡[11]。本组例1术后11个月死亡,例2术后4个月出现肿瘤转移,目前带瘤生存(5个月)。
胃食管交界部SMARCA4缺陷型未分化癌是食管未分化癌的一组特殊亚群,具有独特的临床病理及分子特征,为这一组肿瘤的基因型-表型相关性提供了一个解释的可能性。包括BRG1、BRM在内的SWI/SNF复合体蛋白的缺失表达对未分化癌的诊断和预后有重要作用,并可能影响新的免疫检查点抑制剂的预测生物标记物[21]。
