茶树CsNCED2 启动子互作转录因子筛选及在非生物胁迫中的响应
2023-07-03李佳思刘迎庆张永恒张迎澳肖烨子刘露余有本
李佳思,刘迎庆,张永恒,张迎澳,肖烨子,刘露,余有本
西北农林科技大学园艺学院,陕西 杨凌 712100
脱落酸(Abscisic acid,ABA)是一种重要的植物激素,在植物种子休眠、萌发、生长、开花、果实成熟等生理活动中发挥关键作用[1-5]。同时,ABA 也是植物中的关键抗逆因子,参与了植物对多种逆境胁迫的响应过程,如植物在遭受干旱[6]、低温[7]、盐害[8]、病害[9]等胁迫时,植物体内会迅速积累ABA,从而诱导一系列依赖于 ABA 信号的抗逆基因上调表达,引起植物抗逆性的增加[10]。近年来,大量的研究揭示了植物体内ABA 的合成途径,其中,9-顺式-环氧类胡萝卜素双加氧酶(NCED)被鉴定为ABA 合成过程中的关键限速酶,它的表达往往受到逆境胁迫诱导并与植物抗逆性相关[11-12]。水稻中的研究表明,干旱胁迫能诱导OsNCED5的表达,从而促进ABA 合成,增加了水稻的抗旱性[13]。而抑制GhNCED1会导致棉花体内的ABA 含量降低,增加了棉花对干旱和盐胁迫的敏感度[12]。
研究表明,转录因子可以介导胁迫所诱导的NCED转录水平变化,一些转录因子通过激活NCED的表达来增加植物的抗逆性,也有一些转录因子通过抑制其表达从而降低植物的抗逆性。例如,拟南芥AtWRKY57 通过结合到AtNCED3的启动子并激活其表达,促进ABA 的积累,提高拟南芥的抗旱性[14]。在盐胁迫下,水稻OsERF19 可以通过激活OsNCED5的表达,进而影响水稻体内的ABA 含量和耐盐性[15]。番茄中,bHLH 类转录因子SlBZR1通过直接激活SlNCED1的表达来增加番茄中的ABA 含量以提升番茄的抗寒能力[16]。也有一些转录因子通过抑制NCED的表达从而在植物应对逆境胁迫过程中发挥负面作用,如水稻OsWRKY67 能抑制OsNCED3和OsNCED4的表达,过量表达OsWRKY67,导致水稻的抗旱性降低[17]。
茶树中鉴定了5 个NCED基因,它们的表达量在茶叶加工过程中会发生显著变化[18-19]。此外,茶树NCED成员在茶树对低温[20]和干旱胁迫[21-22]的响应过程中也发挥着重要作用,但茶树中NCED响应胁迫条件的转录调控机制还有待进一步研究。 本研究通过对CsNCED2上游调控因子进行挖掘,并探究它们在不同胁迫下的表达模式,以期为进一步了解CsNCED2响应胁迫的转录机制奠定基础。
1 材料与方法
1.1 试验材料与处理方法
试验材料为一年生龙井长叶无性系水培苗,培养于西北农林科技大学科研温室。培养条件为白天25 ℃,晚上22 ℃,自然光照;选取健康且长势一致的茶苗进行不同胁迫处理。盐、干旱处理:将茶苗根部用水洗净后移入配制好的NaCl(200 mmol·L-1)和20% PEG 6000溶液中分别进行高盐和干旱胁迫;低温处理:使用光照培养箱进行4 ℃低温胁迫。3 个处理均在处理后0、1、4、6、8、12、24、48 h 剪取幼嫩叶片,用液氮快速冷冻后保存于-80 ℃冰箱用于提取RNA,每个时间点的样品均设置3 个生物学重复。
1.2 酵母单杂交文库筛选
用课题组前期克隆的CsNCED2的启动子做模板,将-836 至-1415 区域构建至pABAi载体上获得诱饵载体(引物见表1)。用限制性内切酶BstbI线性化诱饵载体并转化至Y1HGold 酵母中,涂布于SD/-Ura 培养基,30 ℃培养 3 d。挑取单克隆用 Matchmaker Insert Check PCR Mix 1 进行菌落PCR 鉴定,获得诱饵菌株 Y1H-pAbAi-proCsNCED2。取适量Y1H-pAbAi-proCsNCED2涂布于含有不同金担子素A(Aureobasidin A,AbA)浓度的SD/-Ura 培养基上,30 ℃倒置培养3 d,观察菌落的生长情况,以确定能够完全抑制Y1H-pAbAi-proCsNCED2自激活的 AbA 浓度。按照SK2400 经典酵母转化试剂盒(酷来搏,北京)说明书制作Y1H-pAbAi-proCsNCED2感受态细胞,并转化本实验室前期构建的茶树叶片文库质粒,转化后的菌涂布于 SD/-Leu(100 ng·mL-1AbA)培养基上,30 ℃倒置培养3 d 后,挑取单克隆进行PCR 扩增,并对PCR 产物进行测序鉴定。

表1 本研究所用引物Table 1 Primers used in this study
1.3 酵母单杂交点对点验证互作蛋白
测序信息提交到NCBI 进行BLASTx 比对后,根据候选转录因子CsDof5.4(GenBank登录号XP_028116390.1) 和CsERF38(GenBank 登录号XP_028084536.1)序列信息设计特异引物(表1),以龙井长叶cDNA为模板将它们的编码序列(CDS)构建至pGADT7(AD)载体上,形成 AD-Dof5.4 和AD-ERF38重组载体,并转化至Y1H-pAbAi-proCsNCED2感受态细胞中,涂布于SD/-Leu(100 ng·mL-1AbA)培养基上,30 ℃培养3 d,观察菌斑生长状况,AD 空载体转化Y1H-pAbAi-proNCED2菌株为阴性对照。
1.4 转录活性鉴定
设计特异引物(表 1)将CsDof5.4与CsERF38的CDS 序列构建至pGBKT7(BD)载体,获得BD-Dof5.4 与BD-ERF38 重组载体,并将它们分别转化入Y2HGold 酵母感受态细胞中,涂布于SD/-Trp 培养基,30 ℃培养3 d,将长出的单克隆转移至SD/-Trp-His-Ade(X-a-gal)培养基上,30 ℃条件下进行培养,观察它们的生长状态及颜色变化。转化有BD 空载体的Y2HGold 酵母菌作为阴性对照。
1.5 亚细胞定位分析
设计特异引物(表1)构建35S::CsDof5.4-GFP 和35S::CsERF38-GFP 用于亚细胞定位试验。将35S::CsDof5.4-GFP、35S::CsERF38-GFP 和35S::GFP 分别转化至根癌农杆菌GV3101 中,在28 ℃分别培养至浑浊后,3 000 r·min-1离心5 min,弃去培养基,用侵染液(10 mmol·L-1MgCl2,10 mmol·L-1MES,120 μmol·L-1AS,pH=5.7)分别重悬菌体至OD600为0.8 后注射到烟草叶片中,48 h后使用荧光显微镜BX63(奥林巴斯,日本)对注射区域进行GFP 信号的观察。
1.6 双荧光素酶(Dual-LUC)试验
用实验室前期保存含有的CsNCED2pro::LUC 的GV3101(pSoup)作为报告菌株,转化有 35S::CsDof5.4-GFP、35S::CsERF38-GFP 和35S::GFP 的根癌农杆菌GV3101 作为效应菌株。用侵染液分别将它们的OD600调整至0.8,报告菌株和相应的效应菌株按照体积比为1∶1 的比例混匀后注射至烟草叶片中,注射48h后按照Double-Luciferase Reporter Assay Kit(全式金,北京)试剂盒说明书进行萤火虫荧光素酶(LUC)和海肾萤光素酶(REN)活性测定。
1.7 RNA 提取和实时荧光定量PCR(qRT-PCR)分析
茶树RNA 提取根据多糖多酚植物总RNA提取试剂盒(天根,北京)说明书进行。根据CsNCED2,CsDof5.4和CsERF38基因序列信息设计特异定量引物(表1)用于 qRT-PCR试验,茶树GADPH基因作为内参基因(TEA003029)。使用 ChamQ SYBR qPCR Master Mix 试剂盒(诺维赞,南京)在Lightcycler480Ⅱ型定量 PCR 仪进行qRT-PCR。设置3 个生物学重复,用法计算基因的相对表达量,并利用 GraphPad Prism 8 作图。
1.8 数据统计与分析
用Excel 软件进行数据统计,IBM SPSS 19 软件进行Student’st检验,P≤0.05 被认为有统计学意义。
2 结果与分析
2.1 CsNCED2 启动子互作蛋白筛选
诱饵载体pAbAi-proNCED2用限制性内切酶BstbⅠ线性化后转化Y1HGold 酵母感受态细胞,涂布于SD/-Ura 培养基上30 ℃培养3 d,挑取单菌落进行 PCR 鉴定,获得Y1H-pAbAi-proCsNCED2诱饵菌株,将其涂布于SD/-Ura 培养基上,AbA 质量浓度分别为0、50、100、150 ng·mL-1。结果显示,诱饵菌株在不含AbA 的SD/-Ura 培养基上生长良好(图1A),而在含50 ng·mL-1AbA 的SD/-Ura培养基上不能生长(图1B),因此选择质量浓度为50 ng·mL-1的AbA 作为CsNCED2启动子酵母单杂交的工作浓度。文库质粒转化至诱饵菌株后,筛选到17 个单克隆能在50 ng·mL-1AbA 的SD/-Leu 培养基上生长(图1C),对它们分别进行菌落PCR 鉴定后得到16 个条带大小为1 000~2 000 bp 的PCR 产物(图1D)。
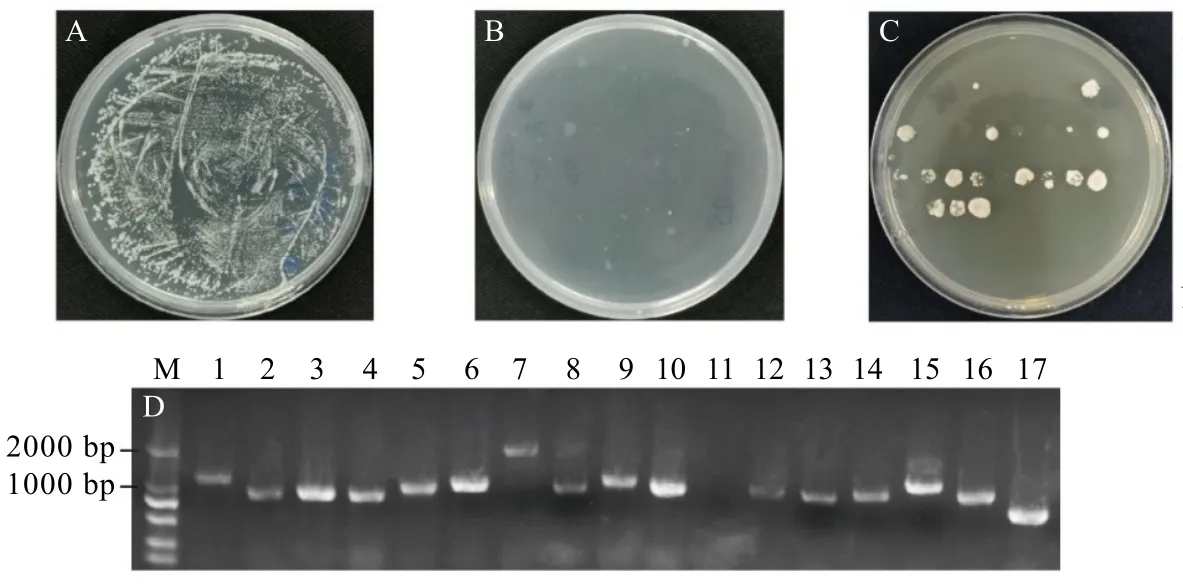
图1 CsNCED2 启动子酵母单杂交文库筛选结果Fig. 1 Yeast single hybrid library screening results of CsNECD2 promoter
2.2 EST 序列的功能注释
将16 个PCR 产物测序得到的EST 序列提交到NCBI 网站(https://www.ncbi.nlm.nih.gov)进行BLAST 比对和注释,如表2 所示,多个EST 编码的蛋白参与胁迫响应过程,如与植物病虫害免疫相关的 GDSL 酯酶/脂肪酶[23](EST5),与干旱、盐胁迫相关的水通道蛋白[24](EST11),脱落酸、胁迫、成熟诱导蛋白ASR[25](EST10)和甘油-3-磷酸酰基转移酶[26](EST13)等。同时,EST6 被注释为AP2/ERF转录因子,EST15 被注释为Dof 转录因子,说明它们可能直接参与了CsNCED2的转录调控。根据他们与其他植物的同源蛋白的进化关系(图2)将它们分别命名为 CsERF38 和CsDof5.4。

表2 EST 序列对比结果Table 2 Comparison of EST sequence

图2 转录因子进化分析Fig. 2 Phylogenetic analysis of transcription factors
2.3 CsDof5.4 和CsERF38 转录激活鉴定和亚细胞定位分析
CsDof5.4和CsERF38的CDS 构建至BD载体上用于转录活性分析,结果如图3A 所示,在 SD/-Trp-His-Ade(X-a-gal)培养基上转化有BD 空载体的Y2HGold 菌株不能生长,而转化有BD-CsDof5.4和BD-CsERF38的Y2HGold能激活报告基因HIS3、ADE2和MEL1的表达,从而正常生长并显示蓝色,说明CsDof5.4和CsERF38均具有转录激活的作用。烟草叶片中的亚细胞定位显示 35S::CsDof5.4-GFP 和35S::CsERF38-GFP 的荧光均只在细胞核中观察到,说明CsDof5.4和CsERF38均定位于细胞核(图3B)。

图3 CsDof5.4 和CsERF38 的转录活性鉴定和亚细胞定位分析Fig. 3 Transcriptional activity identification and subcellular localization analysis of CsDof5.4 and CsERF38
2.4 CsDof5.4 和CsERF38 对CsNCED2 的表达调控
为了进一步分析CsDof5.4 和CsERF38 与CsNCED2启动子结合情况,将CsDof5.4和CsERF38的全长CDS 分别构建至AD 载体并转化至诱饵菌株进行验证。如图4A 所示,转化有 AD-ERF38 和 AD-Dof5.4 的菌株在SD/-Leu(100 ng·mL-1AbA)培养基上能正常生长,而转化AD 空载体质粒的菌株则不能,说明CsDof5.4 和CsERF38 能结合CsNCED2的启动子。同时,在烟草叶片进行荧光素酶试验来验证CsDof5.4 和CsERF38 对CsNCED2表达的调控,结果如图4B 所示,在烟草叶片中表达CsDof5.4 和CsERF38 都显著增强了CsNCED2启动子驱动的 LUC 信号,说明CsDof5.4 和CsERF38 都能激活CsNCED2的表达。
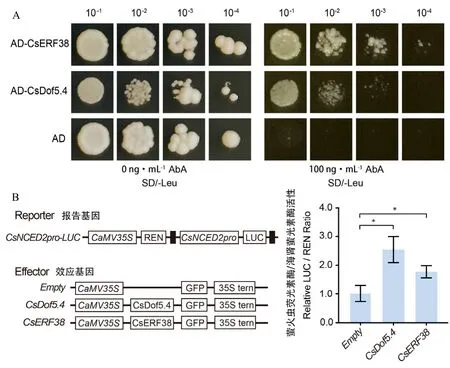
图4 酵母单杂交验证CsDof5.4 和CsERF38 与CsNCED2 启动子结合Fig. 4 Y1H verification of CsDof5.4 and CsERF38 binding to CsNCED2 promoter
2.5 CsNCED2、CsERF38 和CsDof5.4 在胁迫下的表达分析
利用qRT-PCR 分别检测了CsNCED2、CsERF38和CsDof5.4对盐、干旱和低温胁迫的响应,结果如图5 所示,CsNCED2的表达量在盐胁迫和干旱胁迫下上升,而在低温处理下没有显著变化。同样地,盐胁迫和干旱胁迫也诱导了CsERF38的表达,且在盐胁迫和干旱胁迫下CsERF38表达水平的变化趋势与CsNCED2表达水平的变化趋势相关性分别为0.79 和0.77。CsDof5.4的表达水平不受干旱胁迫和低温胁迫的影响,但在盐胁迫下逐渐上升,且在盐胁迫下CsDof5.4表达水平的变化趋势与CsNCED2表达水平的变化趋势相关性高达0.85。
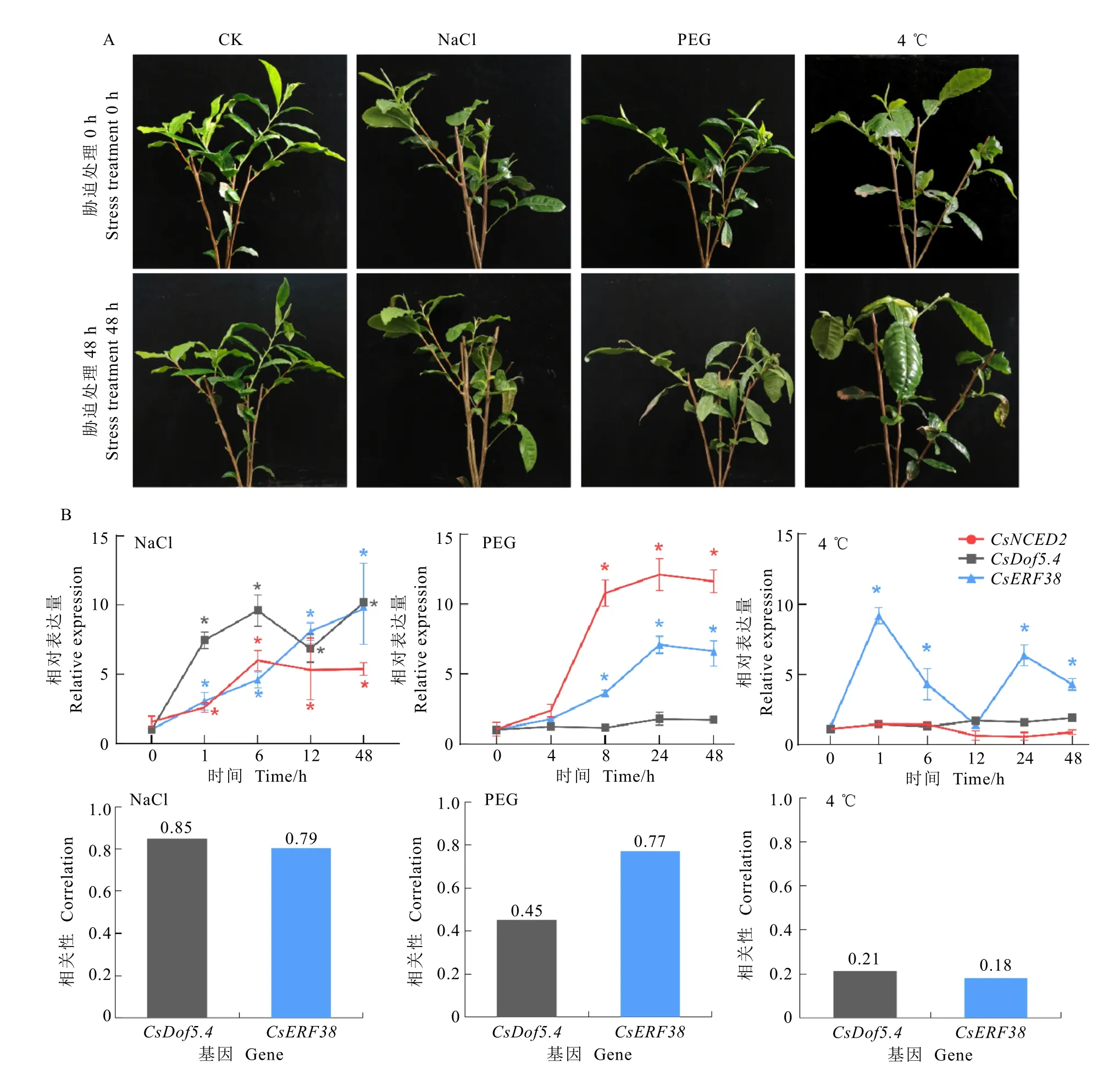
图5 盐、干旱和低温胁迫下的表型及CsNCED2,CsERF38 和CsDof5.4 的表达分析Fig. 5 Phenotype and expression analysis of CsNCED2, CsERF38 and CsDof5.4 under salt, drought and low temperature stresses
3 讨论
酵母单杂交技术库筛文选能高效的鉴定到与目的基因启动子互作的转录因子,因此被广泛运用到葡萄[27]、香蕉[28]、桃[29]等多种植物的研究中。本研究通过酵母单杂交技术鉴定到CsERF38 和CsDof5.4 能结合CsNCED2的启动子,同时,通过CsERF38 和CsDof5.4 的亚细胞定位分析、转录活性鉴定及在烟草中的荧光素酶试验进一步证实了 CsERF38 和CsDof5.4 可以直接激活CsNCED2的表达,表明它们在茶树在CsNCED2转录调控中发挥重要作用。
NCED基因的表达能响应逆境胁迫并调控内源ABA 的含量水平,从而提高植物的抗性[30-31]。同样地,茶树中的研究发现,ABA含量在干旱胁迫下快速上升,导致气孔关闭以减少水分散失[22];Wan 等[32]研究表明,ABA信号在茶树对盐胁迫响应过程中也发挥重要作用。本研究发现,CsNCED2的表达量在干旱和盐胁迫下上升,表明它在茶树中参与了干旱和盐胁迫导致的ABA 积累过程。另外,Ni等[33]研究表明低温胁迫增强了茶树叶片中ABA 的合成过程,王赞等[20]的研究证实了1个茶树NCED基因参与了低温诱导的ABA 合成过程,而本研究结果表明CsNCED2的表达不受低温胁迫诱导。综上所述,茶树不同NCED基因成员在响应胁迫过程存在差异,CsNCED2主要参与了茶树对干旱和盐胁迫的响应过程。
已有大量研究表明,植物中的转录因子通过调控NCED的表达来响应胁迫环境[34-35]。本研究证实,CsERF38和CsDof5.4参与了茶树对盐胁迫的响应过程,同时CsERF38参与了茶树对干旱胁迫的响应过程。尽管它们在茶树响应盐胁迫和干旱胁迫过程中的具体功能还需进一步验证,但CsERF38和CsDof5.4在盐胁迫下与CsNCED2的表达高度相关,同时,CsERF38的表达在干旱胁迫下与CsNCED2也高度相关,结合它们对CsNCED2表达的激活作用,我们推测 CsERF38 能通过调控CsNCED2的转录从而参与茶树对盐胁迫和干旱胁迫的响应过程,而CsDof5.4 能通过调控CsNCED2的转录参与茶树对盐胁迫的响应过程。本研究结果为茶树中CsNCED2响应盐胁迫和干旱胁迫的转录调控机制研究奠定了一定的理论基础。
