小儿血管瘤的诊治及进展
2023-06-26刘海金
刘海金
血管瘤是小儿最常见的肿瘤之一,发病率高达4%~10%,尤其好发于2岁以内婴幼儿,以头面部最多见,可并发溃疡、出血、感染、疼痛和功能障碍、美容问题等并发症,影响病人容貌、视力、心理,严重者可致呼吸道阻塞、毁容,甚至死亡。目前,血管瘤发病机制仍不清楚,治疗方法众多,主要包括定期随访观察治疗、药物治疗(口服、局部注射,少数情况下静脉给药)、硬化治疗、激光治疗、物理治疗等。随着对婴幼儿血管瘤(infantile hemangioma,IH)生物学自然病程、病理认识的加深,临床诊断、治疗方法逐渐规范,疗效评价体系及副作用监测体系也不断建立,不当治疗、过度治疗现象也随之减少。本文小儿血管瘤诊治的新进展进行综述。
一、血管瘤的分型与诊断
随着脉管性疾病ISSVA分类的不断推广,提高了各专科医师对IH生物学自然病程、病理的认识,也提升了临床诊断治疗规范化水平。目前,最新的分类方法仍然是ISSVA2018分类法。根据其分类标准,IH按瘤体分布可分为局灶性,多灶性,节段性,不确定性等;按瘤体深度位置可分为浅表型,深部型,混合(浅表+深部),网状/最小生长型,其他类型。IH可以根据临床表现及影像学确诊,然而特殊类型的血管瘤的鉴别诊断具有一定的挑战性,如早期浅表型IH需要与微静脉畸形鉴别、深部型IH应与卡波西血管内皮瘤、先天性血管瘤及脉管畸形相鉴别。此外,需要注意有无IH合并其他关联病变的综合征情况。如与PHACE综合征、LUMBAR综合征。目前,有相关案例将PHACE 综合征误诊为葡萄酒色斑(PWB)或血管畸形[1],此外存在一些特殊类型的IH须鉴别诊断,如多发型IH更有可能与婴儿肝血管瘤相关,目前认为,多于5处IH病灶的患儿多数合并肝脏血管瘤,要进行肝脏筛查。面部或腰部较大的IH分别需要对PHACE和LUMBAR综合征进行筛查。腰椎IH需要检查下半身 IH 和其他皮肤缺陷、泌尿生殖系统异常、溃疡、脊髓病、骨畸形、肛门直肠畸形、动脉异常和肾异常(LUMBAR)综合征。在诊断不确定的情况下,需要借助相关辅助检查。目前认为,比色法、皮肤镜、高频超声、MRI/CT和活检可能有助于IH的鉴别诊断。
使用比色技术区分早期IH与PWB是一项具有广泛应用价值的诊断工具,然而现今还没有开发出相应的设备。研究发现,PWB 具有更高的RGB 值,与厚度无关。用RGB用于与区分PWB和早期IH时具有其他方法无法比拟的准确性(90%)、灵敏度(92%)、特异性(98%)和阳性预测值(98%)[2]。此外,比色分析还用与IH治疗后疗效随访的精确分析。有学者建议将皮肤镜检查作为早期婴儿血管瘤的辅助诊断工具,其IH的皮肤镜特征包括红色腔隙、红/红-蓝/红-白的背景和线性蜷曲、蛇行、卷曲的血管形态[3],皮肤镜检查似乎可以促进血管性皮肤病变的检测和诊断,然而仍缺乏针对性的大样本研究,但在评估IH治疗疗效方面具有很大优势,可以观察到IH治疗后微观的改变[4]。高频超声是诊断深部型IH首选的检查方式,IH超声的声像图特征取决于其所处的自然阶段。在灰阶超声图像上,IH和VM多见于皮下软组织,但VM可侵犯肌肉。大多数 DIH 表现为强回声结构,具有明确的边界,并且是回声均匀的,而大多数VM表现为混合回声和无回声结构,边界不清,并且是不均匀的。在彩色多普勒超声上,大多数 IH 显示高血管密度,而在大多数 VM 中仅发现少量血流信号。在弹性超声上,VM比IH软[5]。在血管瘤和血管畸形之间在平均动脉峰值速度方面不存明显差异,但AVM 的平均静脉峰值流速明显高于其他血管畸形和血管瘤。
磁共振成像(MRI)可用于评估深部或大病灶的IH范围,但通常需要镇静或者麻醉。当病人存在麻醉禁忌证时,计算机断层扫描(CT)具有图像采集时间较短的优势,但由于存在与婴儿辐射暴露相关的风险,因而CT不作为常规检查。CE-MRI结合TWIST可以准确分类血管畸形与血管肿瘤。在MRI上,IH在T1加权图像上与肌肉等信号,在T2加权图像上呈高信号,并显示强烈、均匀的强化。而大多数VM是浸润性T2高信号病变,具有变化不均的内部对比增强、并且大多数 VM 中均存在静脉石[6]。
活组织检查是有创的,一般很少有组织活检的适应指征。在组织病理学上,增殖期血管内皮细胞密集成片,呈卵圆形或上皮样形态,血管腔化不明显,可见细胞凋亡;消退期血管内皮细胞较稀疏,呈纤细梭形或扁平状,血管腔可见,多量脂肪纤维组织增生。GLUT-1染色是IH的一个敏感标记,在大多数其他血管肿瘤和血管畸形中都为阴性。
二、IH的综合评估
1.、IH的风险评估:普萘洛尔是治疗IH的一线用药,如果在增殖期结束前开始治疗,疗效更好,后遗症风险更低,但大多数儿童转诊治疗时间均为延迟[7]。因此需要合适用于制定临床决策的IH严重程度评估工具,目前常用的工具包括血管瘤活动评分(HAS)和血管瘤严重程度量表(HSS)。2019年中国发表的血管瘤与血管畸形诊断与治疗专家共识建议将血管瘤分为3个风险等级(低风险、中风险和高风险)。根据风险等级制定治疗策略,中高风险血管瘤应尽早治疗。低风险血管瘤:如很稳定,可随诊观察,或尝试外用药物;如瘤体生长迅速,则升级治疗方案,遵循中高等风险血管瘤治疗方案。
2020年Léauté-Labrèze等[8]开发了一项婴儿血管瘤转诊评分(IHReS)工具用于促进IH病人及时、准确地接受专业治疗。IHReS是一个由两部分组成的算法,共有12个问题(表1)。如IHReS评分≥4分须转诊至专业中心接受治疗,如评分<4分则不需要转诊,但需定期监测及评分。IHReS在IH病人的治疗决策方面,IHReS比HSS具有更高的效率和敏感性,但IHReS的特异性低于HSS[9]。
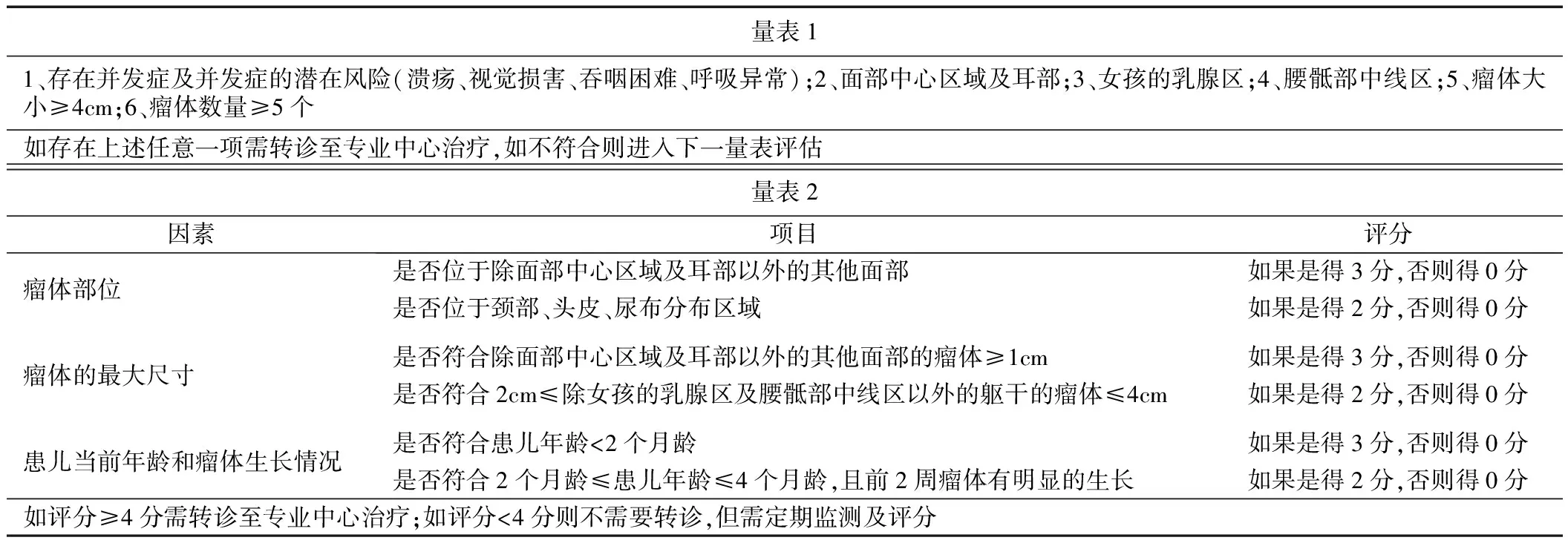
表1 IHRes评分表
2.IH病人及家属心理的评估:血管瘤从出现到完全消退需要持续1~9年时间,且好发于头、颈、面部,可伴有感染、出血及溃疡等,位于上眼睑的遮住眼裂可能引起眼失明。即便可自行消退,但仍可能出现皮肤松弛或萎缩、脂肪组织增生、色素沉着等后遗症,影响正常容貌。临床观察发现,很多IH患儿家长产生复杂、影响其作出正常判断的精神心理特征。这种复杂的精神体验不仅会阻碍医患之间的沟通及家长们对IH的理解,更直接影响着患儿家长对IH的治疗方式选择及治疗的持续性。应关注患儿及其家长的精神心理,进行必要的心理评估、心理疏导和干预也是IH诊治的重要任务[10]。
Chamlin等[11]开发了IH生活质量问卷(IH-QoL),用以评估IH病人及其家人的生活质量。它由四个量表和29个项目组成,涉及身体症状、(心理)社会互动和情绪功能几个维度,评估发现,头颈部、增殖期和需要治疗的血管瘤对患儿及家属的生活质量影响更大。在国内的一项病例队列研究中,IH-QOL评估IH儿童及其父母生活质量的可行性和可靠性得到验证,并且发现血管瘤大小、部位和母亲受教育程度是IH患儿及其父母生活质量的重要影响因素[12]。
目前普遍认为,在儿童长期记忆形成和心理社会疾病发展之前应完成IH的治疗达成了共识,否则IH可能会直接影响患儿的心理健康。尽管普萘洛尔治疗IH具有较好的疗效,但仍有37.5%的IH病人在平均年龄为70.3个月时仍需要手术或激光治疗,而手术的主要原因是瘢痕、纤维脂肪或血管瘤残留[13],并且部分IH存在晚期生长[14]。因此,非常有必要重视IH患儿的心理评估,制定综合的个体化治疗。
三、血管瘤的治疗
1.口服普萘洛尔治疗:普萘洛尔是公认的IH治疗的一线药物,目前其作用机制尚不明确,最近的研究认为转录因子SOX18是普萘洛尔治疗婴儿血管瘤的靶点。普萘洛尔是S(-)和R(+)对映体的混合物,普萘洛尔的疗效依赖于R(+)对映体对SOX18蛋白活性的调节,而不是S(-)对映体引起的抗β肾上腺素能作用,S(-)对映体是导致大多数不良反应的原因,使用R(+)对映体或SOX18抑制剂可以提高当前IH治疗疗效并降低相关不良的副作用[15]。
在普萘洛尔治疗IH的用药时机方面,尽管建议在5周龄前开始用药可明显减少并发症,但最近的研究发现,在9~12个月后晚期生长的IH口服普萘洛尔仍具有较好的疗效[16]。普萘洛尔的停药时间通常在12~18个月龄,国内指南推荐将血管瘤完全消退或者血管瘤消退停止超2个月以上作为停药标准,些病人可能需要更长的疗程,因为停药后反弹生长相对常见,反弹生长频率大概在19%~25%之间。面部IH在口服普萘洛尔治疗后复发得更早、更频繁。因此,停止普萘洛尔治疗后应对患有面部IH的病人进行随访监测[17]。在口服普萘洛尔治疗前常规评估包括心电图和超声心动图,然而是否需要进行常规心脏筛查是有争议的,几项回顾性队列研究发现,心电图和超声心动图发现的轻微异常都不是口服普萘洛尔的禁忌,并且在随访期间没有证据证明心电图的这些异常和口服普萘洛尔的副作用具有相关性[18]。对于母体患有心动过缓、具有PHACE综合征相关特征、有心律失常病史、早期心源性死亡或先天性心脏病家族史或有结缔组织病的病人,建议保留治疗前心电图筛查[19]。
国际最新的指南提出,大多数婴儿可以在门诊启用普萘洛尔治疗,最常用的给药方案是每天两次,每次1 mg/kg[20]。该方案在门诊环境中被证明是安全可行的,并且每天两次给予普萘洛尔是有效的,专业团队的多学科评估对于普萘洛尔门诊启动管理至关重要[21]。
睡眠质量改变是口服普萘洛尔治疗IH最常见的不良反应,Ji等[22]发现,严重的睡眠障碍是停用普萘洛尔的最常见原因。在接受普萘洛尔治疗IH的婴儿中经常出现睡眠问题,这可能是对中枢神经系统功能产生负面影响的标志。一项队列研究发现,普萘洛尔会导致夜间睡眠效率下降和白天睡眠需求增加,但总体影响轻微,其对行为发育评分不受影响[23]。一项双中心横断面研究证实,接受普萘洛尔治疗的IH儿童的长期神经认知功能没有差异,然而治疗的男性智商得分明显低于一般人群中接受治疗的女性,这一点需要进一步的调查[24]。由于担心普萘洛尔可能会增加动脉缺血性中风的风险,因此其在PHACE综合征病人中的应用一直存在争议。然而最近的研究发现,口服普萘洛尔治疗PHACE综合征期间严重不良反应的发生率与治疗普通IH病人之间没有显著差异[25]。
2.其他β受体阻滞剂的全身治疗:虽然普萘洛尔已被确定为IH的金标准,但对其副作用的担忧导致选择性β阻滞剂的使用增加,如阿替洛尔及纳多洛尔。一项多中心随机临床试验发现,阿替洛尔在治疗IH方面与普萘洛尔相比具有相似的疗效和更少的不良反应[26]。Sabbah等[27]证明,阿替洛尔治疗不会影响IH病人的行为结果。此外,口服纳多洛尔治疗IH不劣于口服普萘洛尔,表现出更快、更好的反应,并且具有相似的安全性,它可能是一种有效且安全的替代方案。未来,普萘洛尔作为治疗IH的金标准可能将有所改变。
3.局部治疗:(1)外用马来酸噻吗洛尔:2019 AAP CPG提出,0.5%马来酸噻吗洛尔凝胶形成眼用溶液可以局部应用于小的、薄的和表面的IH,剂量为1~2滴,每天两次,持续6~9个月,直到12个月年龄或偶尔更长取决于IH大小[28]。Novoa等[29]研究发现,口服普萘洛尔(1.0 mg/kg,片剂,每天一次)和外用马来酸噻吗洛尔(0.5%滴眼液,每天两次)在24周时同样可以使血管瘤直径缩小50%以上,并且外用马来酸噻吗洛尔几乎无全身反应。对于混合型及深部IH其疗效有限,有学者对马来酸噻吗洛尔进行化学修饰可增强噻吗洛尔皮肤渗透,使其可潜在的使用于治疗深厚的IH病灶[30]。Xu等[31]研究发现,局部噻吗洛尔给药对唇部 IH无效,然而这个结果需要进一步的验证。(2)激光治疗:激光作用于含氧血红蛋白的红细胞,红细胞吸收光使病变部位发热引起凝血,从而发挥治疗作用,不同的激光器具有不同的应用范围。在一项儿童IH管理干预措施的Cochrane评价中比较了PDL、LPDL、Nd:YAG和PDL+Nd:YAG中使用的4种激光模态,发现脉冲染料激光通常是血管瘤激光治疗的首选,由于其在透皮深度方面的优势,较长的脉冲具有较高的效率。口服普萘洛尔与PDL联合应用时发生溃疡、色沉、色减等不良反应最少。此外,PDL的使用可以减少普萘洛尔的用量和疗程,效缩短治疗周期,减少不良反应[32]。(3)局部注射治疗:局部注射药物治疗 IH 具有作用范围精确、局部药物浓度高和全身不良反应少的特点,常用药物包括博莱霉素、平阳霉素、糖皮质激素和泡沫硬化剂。目前,该方法使用的适应证及治疗时机仍存在争议,局部注射药物疗法目前主要用于普萘洛尔耐药及治疗后残留的IH患儿[33]。
4.联合治疗:研究发现,普萘洛尔口服联合激光治疗较单药治疗可提高疗效。无论是否在6个月以下的儿童中,使用局部 β 受体阻滞剂联合激光都比其他单一方法更有效。长脉冲染料激光可能是最好的激光疗法。口服更高剂量和更长治疗持续时间的普萘洛尔可获得更高的成功率,但增加了不良反应。如果普萘洛尔联合脉冲染料激光治疗,则发生溃疡、色沉、色减等不良反应发生率最低。因此,β受体阻滞剂和激光的组合可能是IH的一线治疗[32]。Chelleri等[34]研究发现,接受治疗的IH病人仍有41.4%存在病灶残留,残留病灶使用激光和外用噻吗洛尔仍有效,因而激光疗法和外用噻吗洛尔是减少残留病变发生率的潜在有效治疗方法,必要时可以采取手术切除。Qiao等[35]认为,局部噻吗洛尔和口服普萘洛尔联合治疗IH可能比任何一种单一治疗策略更有效。但由于两种属于同类药物,其中的机制不明,是否存在联合用药的意义仍有待进一步探讨。
