共轭聚合物m-PPEASO3Na荧光检测非离子表面活性剂临界胶束浓度
2023-06-14孙礼林李佳眉
孙礼林 李佳眉
摘要:折线型水溶性荧光共轭聚合物聚(1-丙氧磺酸基-3,5-苯撑-乙炔撑-9,10-蒽撑),m-PPEASO3Na,其主链骨架在水中及低浓度非离子表面活性剂的水溶液中以螺旋形构象存在,因而在630 nm处表现出很弱的荧光发射。然而一旦水溶液中非离子表面活性剂的浓度增大达到临界胶束浓度以上,荧光发射急剧增强同时有较大的蓝移,这直接指示了表面活性剂胶束的形成过程,提供了测定一些常见的非离子表面活性剂如Brij-35、曲通、吐温临界胶束浓度的简便荧光分析方法。尤其是Brij-35,荧光发射峰蓝移最大达到85 nm,且在紫外灯下裸眼可见明亮的黄绿色荧光。m-PPEASO3Na和表面活性剂胶束之间强烈的疏水相互作用导致聚合物主链螺旋形构象向伸展的无规线团构象转变,作为其结果,聚合物的荧光发射有极大的增强且发射峰蓝移。
关键词:m-PPEASO3Na;荧光检测;非离子表面活性剂;临界胶束浓度
中图分类号:O657.3文献标志码: A文章编号:1001-2443(2023)02-0131-07
引言
近几十年来,荧光共轭聚合物由于其独特的性质吸引了许多研究者的广泛关注。许多基于荧光共轭聚合物的化学和生物传感器已被广泛应用于金属离子、蛋白质和酶等物质的检测[1]。目前研究和报道的荧光共轭聚合物其主链大多具有直线型的链状结构,在荧光传感等领域里各种直线型的水溶性荧光共轭聚合物的合成和应用已被人们进行了充分的探讨[2],而主链为折线型的水溶性共轭聚合物的研究报道还相对欠缺。2004 年Tan等人报道了一种折线型的水溶性聚苯撑乙炔撑(PPE)共轭聚电解质,并研究了其光学性质和构象变化[3]。他们发现折线型水溶性聚合物存在着溶剂诱导的自组装现象,在水溶液中聚合物疏水性主链发生内折叠形成螺旋形构象以避开水相,而在良溶剂中聚合物主链是伸展的,呈无规线团构象。这两种构象在水和良溶剂构成的混合溶剂中随溶剂组成的变化和溶液 pH 值的变化而相互转变,进而影响聚合物的紫外吸收和荧光发射等光学性质。螺旋形的主链有效地减少了水溶液中聚合物疏水主链之间的链间聚集,表现出比无规线团构象的聚合物更大的荧光淬灭效应,可望进一步提高聚合物的荧光传感性能[3-5]。由此可见,合成各种新的折线型水溶性荧光共轭聚合物对其进行荧光传感等方面应用的深入研究是很有价值的。
基于这样的认识,我们在前期工作中制备了一种新的折线型水溶性共轭聚合物m-PPEASO3Na,即聚(1-丙氧磺酸基-3, 5-苯撑-乙炔撑-9, 10-蒽撑)[poly1-(propyloxysulfonate-3, 5-phenylene-ethynylene-9, 10-anthrylene),结构与合成见有关文献[6]]。希望既保留链节有相似组成的直线型水溶性共轭聚合物低背景干扰、长波激发和近红外发射的优点[7-8],又利用折线型主链的螺旋形构象减小聚合物链间聚集,研究其构象转化对荧光性质的影响,进一步提高荧光传感性能。利用Cu2+对m-PPEASO3Na 的荧光淬灭效应,建立了一种灵敏的近红外荧光检测 Cu2+ 的方法,并取得了较好的效果[9]。
我们进一步考察了一些常见的非离子表面活性剂(Brij-35、曲通和吐温)在水溶液中和m-PPEASO3Na的相互作用及其对聚合物主链不同构象之间的变化和荧光性质的影响。结果表明, m-PPEASO3Na是指示这些非离子表面活性剂胶束形成过程和测定其临界胶束浓度(CMC)的简便而理想的荧光探针。表面活性剂的两亲性使得它们在达到一定浓度(即临界胶束浓度CMC)时,在极性溶剂如水[10]中可以发生自缔合组装形成胶束。CMC是表征表面活性剂的表面活性大小的重要参数。当表面活性剂浓度达到CMC时,其表面张力、粘度、光散射强度、渗透压、电导率等物理性质往往发生急剧变化。常用的CMC测定方法有表面张力法、电导法、光散射法、荧光法等[11]。不同方法的灵敏度不同,CMC的实测值也不完全相同。使用表面活性剂来调节荧光共轭聚合物的荧光性质或使用荧光共轭聚合物测定表面活性剂浓度等已被人们广泛研究[12-17],然而利用折线型水溶性荧光共轭聚合物构象转变和荧光性质的变化测定表面活性剂的CMC目前尚未见报道。本文提出的利用折线型水溶性荧光共轭聚合物作为荧光探针的CMC简易测定方法具有一定的新颖性和实用性,并可为拓宽这一类折线型聚合物的应用范围提供参考和借鉴。
1 实验部分
1.1 仪器与试剂
仪器:FS5全功能稳态荧光光谱仪(英国爱丁堡公司);UV-3010紫外-可见分光光度计(日本Hitachi公司);PHS-3C酸度計(上海伟业仪器厂)。
试剂:Brij-35、吐温-20(Tween-20)、吐温-40(Tween-40)、吐温-60(Tween-60)、吐温-80(Tween-80)购于Alfa Aesar公司。曲通X-100(TX-100)购于上海国药集团化学试剂有限公司。其它化学试剂均为商业购买的分析纯试剂,使用时未进一步纯化。所有溶液用二次水配制。聚合物 m-PPEASO3Na参照文献[6]合成。
1.2 实验方法
浓度为0.54 mM(按聚合物重复结构单元计算)的m-PPEASO3Na溶液用二次水配制。将适量的表面活性剂溶液及0.05 mL pH 6.64的 Tris-HCl 缓冲溶液加到到2 mL刻度离心管中,用二次水稀释至刻度,然后加入300 μL 0.54 mM m-PPEASO3Na溶液,充分混合均匀。在460 nm的激发波长下测定m-PPEASO3Na在表面活性剂存在和不存在时的荧光强度。
2 结果与讨论
2.1 实验条件优化
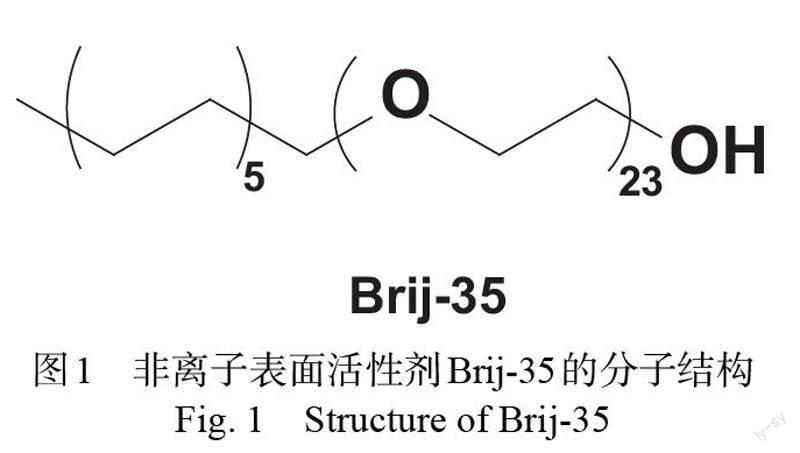
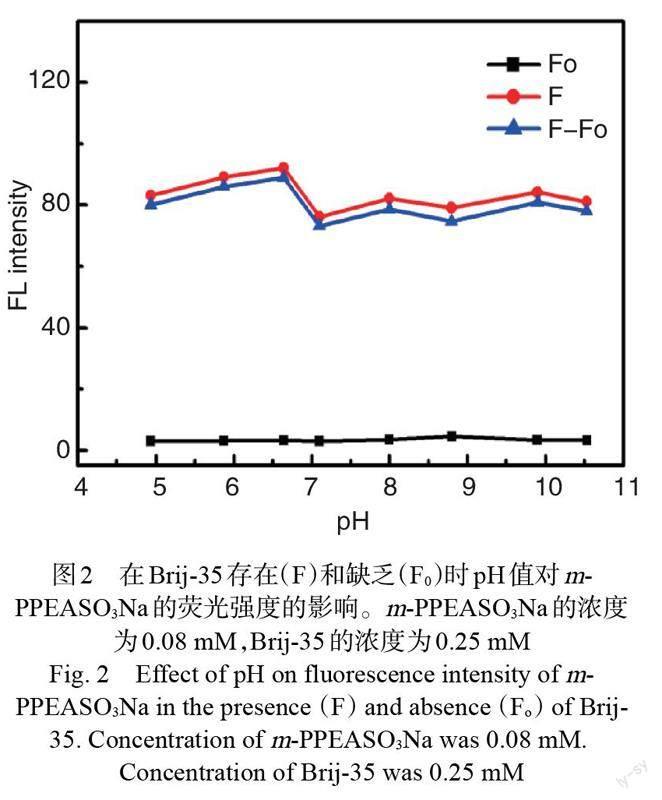
在Tris-HCl (pH 4.93, 5.87, 6.64, 7.1, 8.0, 8.8)、Na2CO3-NaHCO3(pH 9.9, 10.53)两种缓冲体系中研究了pH对m-PPEASO3Na荧光性质的影响,测量了在表面活性剂Brij-35(其分子结构见图1)缺失(F0)和存在(F)时的聚合物的荧光强度。从图2中可见,当pH为6.64时,荧光强度差异(F-F0)最大。此外在此pH值時,当Brij-35的浓度达到CMC时,荧光发射的蓝移更大。因此,以下测量都在pH 6.64的Tris-HCl缓冲介质中进行。
在CMC测定中,需要得到荧光行为的突变。实验表明,当m-PPEASO3Na浓度过低时,CMC的荧光发射太弱,在紫外灯下难以观察。但当m-PPEASO3Na浓度过高时,表面活性剂引起的荧光发射光谱的蓝移不够明显。因此从荧光行为有较大变化的角度考虑,最终选择m-PPEASO3Na工作溶液的浓度为0.08 mM。
2.2 Brij-35等非离子表面活性剂对m-PPEASO3Na光学性质的影响
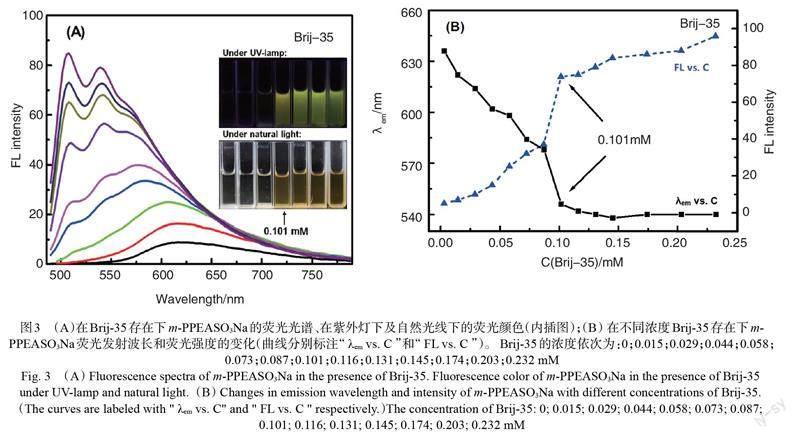
图3反映了非离子表面活性剂Brij-35对m-PPEASO3Na荧光性质的影响。在低浓度的表面活性剂水溶液中,聚合物在~ 630 nm处有较弱且较宽的荧光发射峰。随着Brij-35的不断加入,由于微环境的变化,m-PPEASO3Na的荧光强度逐渐增强(图3A),紫外灯下可见明亮的黄绿色荧光(图3A插图)。一旦Brij-35在水溶液的浓度达到其CMC时,荧光急剧增强近20倍,同时,荧光发射波长从580 nm大幅蓝移到545 nm(图3B)。其他非离子表面活性剂(TX-100,Tween-20,Tween-40 Tween-60)在浓度达到CMC时也有类似的荧光发射强度及发射波长的急剧变化(图4)。这是利用m-PPEASO3Na简便快速测定表面活性剂CMC值的基础。
2.3 m-PPEASO3Na与非离子表面活性剂的相互作用
荧光共轭聚合物的构象和荧光性质对它所处的微环境的变化非常敏感。折线型水溶性m-PPEASO3Na的聚合物主链在水溶液中倾向于形成螺旋形构象,疏水主链与水分子的接触最小,而带电荷的离子侧链位于螺旋的外侧,并向水中延伸,以保持其水溶性。聚合物疏水主链在水溶液中的疏水相互作用和螺旋中的π-π堆砌作用是稳定其主链螺旋构象的两个主要因素。螺旋形构象不仅导致聚合物紫外-可见吸收的吸收强度减小和波长红移,而且也使聚合物的荧光发射强度变弱,发射峰变宽,最大发射波长红移。
当水溶液中加入低浓度( 当Brij-35等在水溶液中的浓度达到或超过CMC时,表面活性剂开始大量形成疏水性的胶束,胶束的内核(如同一些良溶剂THF、DMSO等那样)将为聚合物构象进一步的转变提供更为适宜的微环境。胶束内核中的疏水效应应该远远大于聚合物-表面活性剂复合物的疏水效应,并足以抵消整个聚合物螺旋主链中的疏水作用和π-π堆砌作用,从而极大地破坏了聚合物在水溶液中的螺旋形构象[15-16]。聚合物的主链迅速地完全地转变为伸展的无规线团构象,使得聚合物荧光发射迅速增强和光谱蓝移更加明显[3-4]。如果表面活性剂浓度继续增加(>CMC),则发射波长基本维持不变,荧光强度增加趋缓。聚合物荧光发射波长随表面活性剂浓度变化的曲线会出现一个急剧变化的拐点,而拐点对应的浓度即为表面活性剂的临界胶束浓度CMC,这使得聚合物m-PPEASO3Na作为荧光探针测定非离子表面活性剂的CMC的数值成为可能。 值得注意的是,Tween-80浓度达到其CMC时,聚合物水溶液的荧光性质却没有发生突变(见图4I、J)。这种现象可能是由于Tween-80的CMC值过低造成的。常见的非离子表面活性剂CMC值由大到小依次为TX-100 > Brij-35 > Tween-20 > Tween-40 > Tween-60 > Tween-80。在m-PPEASO3Na水溶液中加入Tween-80只能观察到荧光发射波长由长到短的持续渐变,没有明显的突变拐点。这很可能是因为Tween-80和Tween-60虽有相似的分子量和分子尺寸,但其CMC值远小于Tween-60,当其浓度达到CMC时,其在水溶液中的实际浓度仍然较低。因此,Tween-80形成的胶束不管是数量还是体积都太小,无法提供一个迅速破坏m-PPEASO3Na螺旋构象的微环境。因此,聚合物的构象和光学性质的变化不够迅速,在Tween-80的浓度达到CMC时无法观察到聚合物荧光发射行为的突变。 2.4 利用m-PPEASO3Na测定一些常见非离子表面活性剂的CMC 实验中通过明显的荧光发射波长的变化或荧光颜色变化,由聚合物发射波长随表面活性剂浓度变化曲线的拐点所对应的浓度可以方便地得到被测表面活性剂的CMC值。表1给出了利用m-PPEASO3Na借助本方法测定的Brij-35及其它一些非离子表面活性剂的CMC数值。这些数值与文献中给出的用其它方法测出的CMC数值一致性很好,但本方法无疑更加简单,m-PPEASO3Na是用于测定非离子表面活性剂CMC值的理想探针。 3 结论 研究了Brij-35、曲通、吐温等常见非离子表面活性剂对折线型水溶性荧光共轭聚合物m-PPEASO3Na构象转化和荧光性质的影响。实验表明,m-PPEASO3Na可以作为测定这些非离子表面活性剂CMC数值的理想探针。水溶液中这些非离子表面活性剂的浓度超过CMC时可以观察到聚合物荧光发射的显著增强,特别是发射峰波长较大的蓝移以及发光颜色的显著变化。在水中和低浓度( 在不同浓度的表面活性剂中m-PPEASO3Na的构象变化可能对其的荧光行为的改变起到了关键的作用。通过主链为折线型的水溶性荧光共轭聚合物构象及光学性质的变化作为荧光探针来检测表面活性剂的CMC值迄今尚未见报道。折线型水溶性荧光共轭聚合物的合成和研究可以大大拓宽各种结构类型的荧光共轭聚合物在荧光传感等领域中的进一步应用。 参考文献: [1] THOMAS III S W, JOLY G D, SWAGER T M. Chemical sensors based on amplifying fluorescent conjugated polymers[J]. Chemical Reviews, 2007, 107(4): 1339-1386. [2] ZHANG T, FAN H L, ZHOU J G, et al. Fluorescent conjugated polymer PPESO3:A novel synthetic route and the application for sensing protease activities[J]. Macromolecules, 2006, 39(23): 7839-7843. [3] TAN C, PINTO M R, KOSE M E, et al. Solvent-induced self-assembly of a meta-linked conjugated polyelectrolyte. Helix formation, guest intercalation, and amplified quenching[J]. Advanced Materials, 2004, 16(14): 1208-1212. [4] ZHAO X Y, SCHANZE K S. Meta-linked poly(phenylene ethynylene) conjugated polyelectrolyte featuring a chiral side group: Helical folding and guest binding[J]. Langmuir, 2006, 22(10): 4856-4862. [5] 黄艳琴. 阳离子型水溶性聚芳撑乙炔的合成, 表征与光物理性质研究[D]. 上海: 复旦大学, 2006: 1-104. [6] 李佳眉, 孙礼林. 折线型水溶性荧光共轭聚合物m-PPEASO3Na的合成及其光学性质[J]. 安徽师范大学学报(自然科学版), 2021, 44(5): 441-447. [7] 孙礼林. 荧光共轭聚合物的制备及其在发光分析中的应用[D]. 芜湖: 安徽师范大学, 2012: 1-112. [8] SUN L L, HAO D, SHEN W L, et al. Highly sensitive fluorescent sensor for copper (II) based on amplified fluorescence quenching of a water-soluble NIR emitting conjugated polymer[J]. Microchimca Acta, 2012, 177(3-4): 357-364. [9] 孙礼林, 李佳眉. 折线型水溶性共轭聚合物m-PPEASO3Na荧光检测铜离子[J]. 安徽师范大学学报(自然科学版), 2021, 44(3): 238-243. [10] SCHWARTZ A M, PERRY J W. Surface Active Agents—Their Chemistry and Technology[M]. New York: Interscience Publishers Inc, 1949:1-110. [11] 赵喆, 王齐放. 表面活性剂临界胶束浓度测定方法的研究进展[J]. 实用药物与临床, 2010, 13(2): 140-144. [12] CHEN L H, XU S, MCBRANCH D, et al. Tuning the properties of conjugated polyelectrolytes through surfactant complexation[J]. Journal of the American Chemical Society, 2000, 122(38): 9302-9303. [13] DALVI-MALHOTRA J, CHEN L H. Enhanced conjugated polymer fluorescence quenching by dipyridinium- based quenchers in the presence of surfactant[J]. The Journal of Physical Chemistry B, 2005, 109: 3873-3878. [14] TREGER J S, MA V Y, GAO Y, et al. Tuning the optical properties of a water-soluble cationic poly(p-phenylenevinylene): Surfactant complexation with a conjugated polyelectrolyte[J]. The Journal of Physical Chemistry B, 2008, 112: 760-763. [15] LAVIGNE J J, BROUGHTON D L, WILSON J N, et al. “Surfactochromic” conjugated polymers:Surfactant effects on sugar-substituted PPEs[J]. Macromolecules, 2003, 36(20): 7409-7412. [16] CHEN X Q, LEE J, JOU M J, et al. Colorimetric and fluorometric detection of cationic surfactants based on conjugated polydiacetylene supramolecules[J]. Chemical Communications, 2009, 45, 3434-3436. [17] MIGUEL M G, BURROWS H D, FORMOSINHO S J, et al. Fluorescence studies of polymer-surfactant association[J]. Journal of Molecular Structure, 2001, 563-564: 89-98. [18] AL ATTAR H A, MONKMAN A P. Effect of surfactant on water-soluble conjugated polymer used in biosensor[J]. The Journal of Physical Chemistry B, 2007, 111: 12418-12426. [19] HINZE W L, RIEHL T E, SINGH H N, et al. Micelle-enhanced chemiluminescence and application to the determination of biological reductants using lucigenin[J]. Analytical Chemistry, 1984, 56(12): 2180-2191. [20] YEOM I T, GHOSH M M, COX C D, et al. Micellar solubilization of polynuclear aromatic hydrocarbons in coal tar-contaminated soils[J]. Environmental Science and Technology, 1995, 29: 3015-3021. [21] HINZE W L, SINGH H N, BABA Y, et al. Micellar enhanced analytical fluorimetry[J]. Trends in Analytical Chemistry, 1984, 3:193-199. [22] BECHER P. Nonionic Surfactants[M]. New York: Marcel Dekker Inc, 1967: 478–515. [23] ACHARYA K R, BHATTACHARYA S C, MOULIK S P. Effects of urea and thiourea on the absorption and fluorescence behaviours of the dye safranine T in micellar medium[J]. Journal of Molecular Liquids, 2000, 87(1): 85-96. Fluorescence Detection of Critical Micelle Concentration of Nonionic Surfactants by the Meta-Linked Conjugated Polymer m-PPEASO3Na SUN Li-lin, LI Jia-mei (College of Chemistry and Materials Science, Anhui Normal University, Wuhu 241000, China) Abstract: It was found that m-PPEASO3Na exhibited a weak fluorescence emission maximum at 630 nm due to its helix conformation in water and in aqueous solution containing a low concentration of nonionic surfactants below their critical micelle concentration (CMC). However, a dramatic fluorescence enhancement simultaneously with a large emission blue-shift was found once the concentration of nonionic surfactants reached the CMC. Especially for Brij-35, the blue-shift is up to 85 nm, and a bright yellow-green fluorescence was observed even with naked-eyes under UV-lamp, which gave a direct indication for the micelle forming process and provided a simple method for the CMC determination of some common nonionic surfactants (such as Brij-35, Triton, Tween). The dramatic emission change observed could be ascribed to the intensive hydrophobic interaction between m-PPEASO3Na and surfactants micelle, which greatly disrupts the helix conformation of the polymer chain and causes the main chain of polymer to appear as an extended random-coil conformation. As a result, the fluorescence emission of the polymer was greatly enhanced and blue shifted. Keywords: m-PPEASO3Na; fluorescence detection; nonionic surfactant; critical micelle concentration (責任编辑:王海燕)
