含氢空位氢化金刚石2 维原子晶体体系与硫酸吲哚酚和水分子相互作用的第一性原理计算
2023-06-11耿俊杰张兆春鄢奇桢郭海波
耿俊杰, 张兆春, 鄢奇桢, 郭海波, 王 洋
(1. 上海大学材料科学与工程学院, 上海 200444; 2. 上海大学计算机工程与科学学院, 上海 200444)
基于2 维原子晶体微机械剥离与其生长、制备等方面的一系列进展, 形成通过识别和构建关键结构单元, 进而实施组装(即随需而制) 的研究策略[1-2], 已经引起人们极大的关注. 该研究策略旨在通过微机械剥离与生长工艺, 制备2 维原子晶体; 利用化学功能化、应变工程、杂质工程等, 对2 维原子晶体的晶体结构、电子结构以及物理、化学性质进行修饰; 将2 维原子晶体作为基本结构单元进行多重堆叠, 构建新型3 维晶体材料. 依据这种策略, 从理论上讲,可以构建几乎无限的、具有不同结构和性质的2 维、3 维原子晶体. 在理论上定性或定量地将2 维原子晶体的点缺陷视为化学实物, 利用化学热力学原理研究点缺陷的生成、浓度与分布、化学反应与平衡等一系列问题, 应该被视为对于经典缺陷化学知识体系加以适度拓展的重要内容之一. 研究人员已经在相关领域进行了初步的计算与实验研究, 如①掺杂或含氢空位石墨烷对于部分气体分子的吸附和传感特性[3-5]; ②将石墨烷电子学性质进行调制, 并将其应用于热敏二极管、场效应晶体管、生物分子传感器等诸多研究[6-8].
研究发现, 硫酸吲哚酚是一种蛋白结合类毒素, 可诱导全身氧化应激并造成心血管损害,最终导致血管硬化与心功能不全等病理改变[9-10]. 实施对血清中硫酸吲哚酚含量的监测与清除, 对防治心血管疾病、保护心脏功能具有重要的临床意义. 检测硫酸吲哚酚的方法主要有高效液相色谱-荧光法[11-12]以及高效液相色谱-串联质谱法[13]. 在分子水平上研究硫酸吲哚酚和蛋白质、酶结合的分子生物学机制, 以及在监测与清除过程中硫酸吲哚酚与传感器、吸附剂核心材料表面相互作用的物理化学机制则鲜有报道.
本工作目的是利用第一性原理探究硫酸吲哚酚和含氢空位氢化立方金刚石2 维原子晶体的相互作用, 以期在分子尺度上深化对硫酸吲哚酚与2 维原子晶体相互作用物理化学机制的理解. 本工作的计算结果可以为基于2 维原子晶体研发新型的生物活性分子、人体血液毒素分子传感器核心材料以及设计吸附剂提供参考.
1 计算方法
本工作基于密度泛函理论和平面波赝势方法进行第一性原理计算, 执行软件为VASP (Vienna Ab-initio simulation package)[14-17]. 交换关联相互作用采用广义梯度近似(generalized gradient approximation, GGA) 方法且结合PBE (Perdew-Burke-Ernzerh)方法进行描述, 电子与离子之间的相互作用采用投影扩充波(projector augmented wave,PAW) 方法表示. 氢(H)、硼(B)、碳(C)、氮(N)、氧(O)、硫(S) 元素的价电子数分别为1(1s1)、5(1s22s22p1)、6(1s22s22p2)、7(1s22s22p3)、8(1s22s22p4)和6(1s22s22p2). 采用4×4×1超晶胞, 布里渊区采样使用Monkhorst-Pack 方法. 由平面波截断能和k 点密度测试可知, 当二者分别为400 eV 和3×3×1 时, 计算能量误差为0.001 eV·atom−1. 超晶胞中的所有原子都进行充分的弛豫, 收敛判据为每原子受力小于0.005×10−9eV·m, 电子自洽能量差小于10−6eV.
2 计算结果与分析
2.1 含氢空位氢化立方金刚石2 维原子晶体
如果沿着与金刚石晶体[0001] 垂直的方向剥离出一层原子晶面并进行氢化, 以使所有的不饱和碳原子(sp2杂化) 形成C(sp3)-H 键, 得到石墨烷2 维原子晶体. 仿此思路, 如果由金刚石晶体直接剥离出2 层相邻的碳原子晶面并进行氢化, 就可以获得一种含有2 层碳原子(sp3杂化)的2 维原子晶体,即氢化立方金刚石(hydrogented cubic diamond, HCD)2 维原子晶体.另外一种构建氢化立方金刚石2 维原子晶体的过程可以描述如下: 将2 片石墨烷的相邻面进行脱氢处理, 生成的不饱和碳原子再相互键合形成C(sp3)—C(sp3) 键. 构建氢化立方金刚石2 维原子晶体过程的第3 种描述为将金刚烷分子沿着由C-3, 4, 5, 6, 7, 10 形成的椅式环己烷所在的平面加以扩展. 上述3 种构建过程皆可形成氢化立方金刚石2 维原子晶体(见图1(a)).在某些特定实验过程, 如石墨烷暴露于氢等离子体中, 分析结果显示石墨烷通常存在氢空位点缺陷. 形成氢空位导致石墨烷具有更高的化学活性, 氢空位位点对于探针分子亦具有更高的敏感度[18]. 本工作通过在氢化立方金刚石2 维原子晶体碳原子层中央直接生成氢空位的方法,构建含氢空位氢化立方金刚石(hydrogen vacancy-HCD, Hv-HCD) 2 维原子晶体(见图1(b)).

图1 氢化立方金刚石与含氢空位氢化立方金刚石2 维原子晶体结构(球棒分子结构模型)Fig.1 Crystal structures of hydrogenated two-dimensional atomic diamonds with and without hydrogen vacancy (Ball-and-stick models)
对于HCD 2 维原子晶体, 经过计算优化所得的C—H 键长为1.11×10−10m, 与典型碳氢化合物的C—H 键长相同; C—C 键长为1.52×10−10m, 与金刚石晶体结构sp3杂化碳原子键长(1.53×10−10m) 极为接近, 同时远大于石墨晶体结构sp2杂化碳原子键长(1.42×10−10m). 对于Hv-HCD 2 维原子晶体, 氢空位碳原子与其紧邻碳原子之间的键长计算值为1.48×10−10m, 小于HCD 2 维原子晶体的C—C 键长值, 由此可以推知, 氢空位导致HCD 2 维原子晶体在氢空位碳原子格点产生压缩应变.
HCD 和Hv-HCD 2 维原子晶体的形成能(Ef) 可计算为
式中: E2D、E(C)、E(H) 分别为2 维原子晶体、碳原子、氢原子的能量; m、n 分别为2 维原子晶体中碳原子和氢原子的数目. 氢空位形成能(Ef,Vac) 可计算为
式中: N 为氢化立方金刚石2 维原子晶体的总原子数目; E(N,Vac) 表示为含有一个氢空位氢化立方金刚石2 维原子晶体的能量; E(N) 表示为没有任何点缺陷的氢化立方金刚石2 维原子晶体的能量.
本工作的HCD 2 维原子晶体禁带宽度计算值为2.80 eV. 对于石墨烷(椅式) 2 维原子晶体, 利用第一性原理计算得出的禁带宽度为4.71 eV[18]. 如前所述, HCD 2 维原子晶体可以视为由2 层石墨烷产生的衍生结构. 2 种2 维原子晶体因为碳原子晶面数不同而导致禁带宽度发生改变, 说明该类2 维原子晶体可以通过调整碳原子晶面数对禁带宽度进行调制. 由此可以推知, 对于石墨烯、石墨烷、石墨炔等2 维原子晶体, 通过精确控制碳原子晶面数(层数), 便可以实现该类材料禁带宽度的调制, 从而设计出具有特殊光电性质的新型2 维原子晶体半导体材料与结构. 另外, 杂质和结构缺陷也对半导体材料的性质产生重要的影响. 本工作Hv-HCD 2 维原子晶体禁带宽度计算值为1.78 eV, 与HCD 2 维原子晶体相比, 其禁带宽度因氢空位而有所减小.
将不同的2 维原子晶体按照一定的规则进行堆积, 可以构建出众多新颖的层状结构. 图2为由单层石墨烯(G) 和六方氮化硼(h-BN) 与氢空位氢化立方金刚石2 维原子晶体构建的范德华异质结(G/Hv-HCD、h-BN/Hv-HCD) 的晶体结构. 有关G/Hv-HCD、h-BN/Hv-HCD范德华异质结、HCD 和Hv-HCD 2 维原子晶体体系的形成能和氢空位形成能计算值如表1所示.

表1 4 种2 维原子晶体体系的形成能和氢空位形成能Table 1 Formation energies and formation energies of hydrogen vacancy for four two-dimensional atomic diamond systems
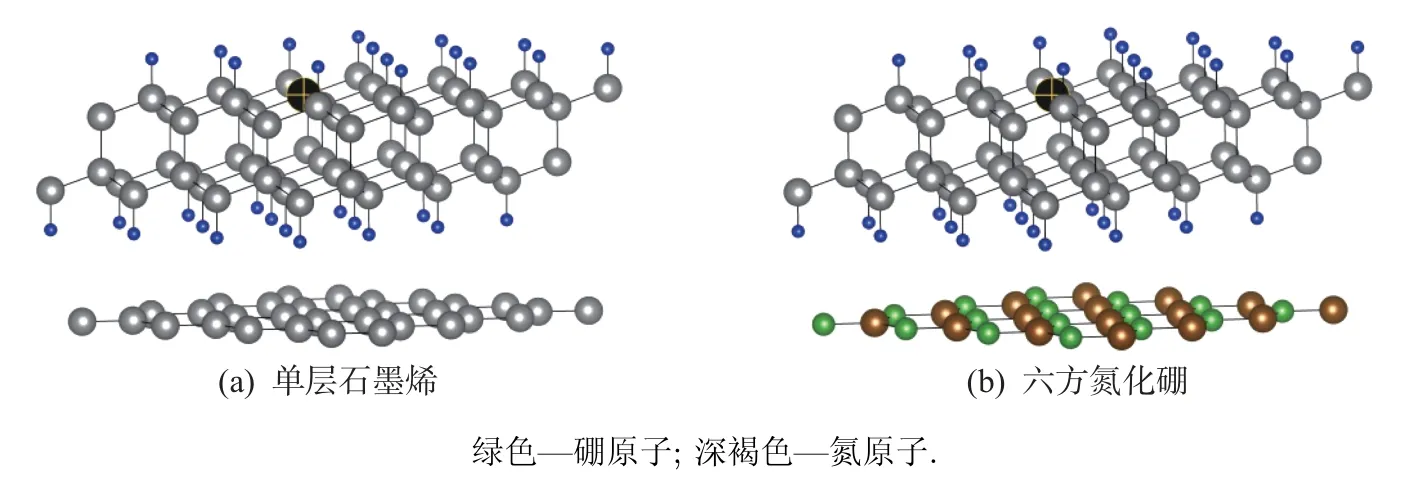
图2 单层石墨烯和六方氮化硼与含氢空位氢化立方金刚石2 维原子晶体范德华异质结Fig.2 Van de Waals heterostructures consisting of hydrogenated two-dimensional atomic diamond with hydrogen vacancy on top of a monolayer graphene and hexagonal boron nitride (The boron atom is represented by a small green ball, the nitrogen atom by a dark brown ball)
h-BN 是一种宽带隙绝缘体, 其禁带宽度为5.97 eV[19]; Hv-HCD 2 维原子晶体是一种半导体, 其禁带宽度为1.78 eV (T = 0 K). 当单层h-BN 与Hv-HCD 2 维原子晶体构建范德华异质结时, 由于二者禁带宽度相差较大, 故倾向于形成类型Ⅰ能带结构[20], 即包容型结构. 在这种结构中, 较大的能带阶跃将异质结电子和空穴限制于Hv-HCD 2 维原子晶体中. 从载流子隧穿速率视角也可以对这种电子结构特征加以分析, 即当载流子在单层h-BN 与Hv-HCD 2 维原子晶体之间传输时, 其隧穿速率为Γ ∼exp(−(2m∆E/ħ2)1/2∆x), 其中m∗为电子有效质量, ∆E 为隧穿势垒高度, ∆x 为隧穿势垒宽度. 由此关系式可知, 载流子隧穿速率Γ 将随势垒高度∆E 的增大呈指数式下降.
石墨烯原胞含有2 个晶体学等价的碳原子,2 个隶属于不同不可约表示,且显现pz特性的子能带在动量空间K 点和K′点费米能量处相互交叉, 因此未掺杂的石墨烯是一种零间隙半导体[21]. 子能带线性色散导致石墨烯产生质量为0 的准粒子, 即狄拉克费米子. 在能量接近简并点时, 电子态形成完美狄拉克锥. 零能隙亦阻止狄拉克费米子获得有限质量[22]. 当石墨烯与Hv-HCD 2 维原子晶体构建范德华异质结时, 将形成类似于金属-半导体接触式结构. 基于固体能带理论分析, 电子从石墨烯扩散至Hv-HCD 2 维原子晶体应是畅通的. 如果从载流子隧穿速率角度分析, 当载流子在单层石墨烯与Hv-HCD 2 维原子晶体之间传输时, 其隧穿速率Γ将随电子有效质量m∗的减小呈指数级增大. 这种载流子传输特征意味着石墨烯对Hv-HCD 2 维原子晶体的氢空位碳原子(碳自由基) 能够起到一定程度的稳定作用, 类似于在3 苯甲基自由基中, 因共轭效应的缘故, 该自由基稳定到可以进行分离研究. 由表1 可知, G/Hv-HCD 2 维原子晶体异质结的氢空位形成能(正值) 低于Hv-HCD 和h-BN/Hv-HCD 2 维原子晶体体系, 而其形成能(负值) 之绝对值又高于Hv-HCD 和h-BN/Hv-HCD 2 维原子晶体体系, 这种差异直接反映了3 种含氢空位2 维原子晶体体系在能量效应和热力学稳定性方面的特征.
2.2 Fukui 函数
作为能简捷而准确地探测分子反应信息的一种方式, 基于电子能量和密度表征分子局部反应的敏感性的特征参数——Fukui 函数, 已经被广泛地应用于有机反应与生物体系. 本工作采用有限差分近似定义的Fukui 函数, 其计算公式如下[23-26]:
表2 列出了HCD 2 维原子晶体碳原子、Hv-HCD、h-BN/Hv-HCD 和G/Hv-HCD 2 维原子晶体氢空位碳原子的Fukui 函数计算值, 2 种特征碳原子在各自的2 维原子晶体体系中皆拥有最大的Fukui 函数值.

表2 4 种2 维原子晶体体系的特征碳原子Fukui 函数值Table 2 Values of condensed Fukui function at characteristic carbon atoms for four two-dimensional atomic diamond systems
Fukui 函数值是分子反应位点敏感度的一种度量. 具有正的、较大的Fukui 函数值表明相应原子位置的软度亦较大, 按照软硬酸碱理论, 较大的软度表明原子位点的反应趋势较为显著. 由表2 可知, 对于3 种含氢空位2 维原子晶体体系而言, 氢空位碳原子与HCD 2 维原子晶体碳原子相比皆具有较大的f+(r) 和f−(r) 值, 表明氢空位碳原子呈现较大的亲核或亲电反应趋势. 另外, Hv-HCD 和h-BN/Hv-HCD 体系氢空位碳原子的f−(r) 略高于f+(r), 意味着此2 种体系氢空位碳原子的亲电反应趋势略为显著. 然而, G-Hv-HCD 2 维原子晶体异质结氢空位碳原子的f−(r) 明显小于f+(r), 似乎表明其氢空位碳原子具有明显的亲核反应趋势.由上述分析可见, 通过设计构建2 维原子晶体范德华异质结构, 可以对2 维原子晶体的能带结构、载流子输运及其表面物理化学性质进行调制, 实现人工结构的改性.
2.3 水-含氢空位氢化立方金刚石2 维原子晶体相互作用体系
Fukui 函数计算结果显示, 水氧原子具有较大的f+(r) 值, f+(r) = 0.010, 而水氢原子具有较大的f−(r) 值, f−(r)=0.022. 由此可以得知, 当水分子与含氢空位氢化立方金刚石2 维原子晶体发生相互作用时, 可能存在2 种吸附位点和取向, 即①水氧原子(亲核反应位点) 与氢空位碳原子(亲电反应位点); ②水氢原子(亲电反应位点) 与氢空位碳原子(亲核反应位点).按照2 种作用位点与取向方式, 将单一水分子置于Hv-HCD、h-BN/Hv-HCD、G/Hv-HCD 2 维原子晶体4×4×1 超级晶胞表面, 构建相互作用体系初始结构, 其对应的表面覆盖度为10%. 2 种体系初始结构经计算优化, 所得体系能量最为有利的终态结构几乎是相同的, 即水氢原子(非氧原子)接近2 维原子晶体中氢空位碳原子(见图3).
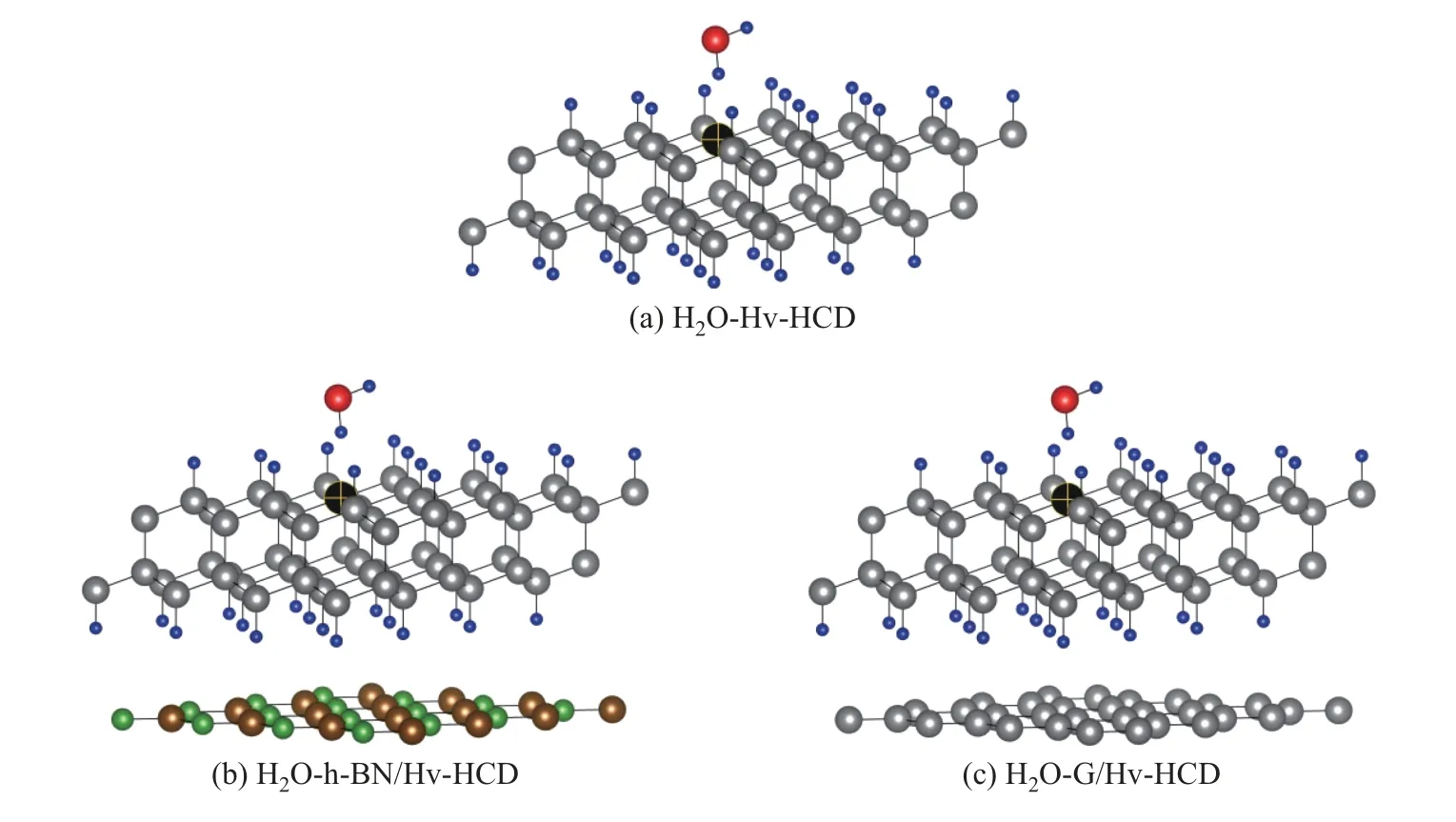
图3 水分子-含氢空位氢化立方金刚石2 维原子晶体作用体系能量最为有利的构型Fig.3 Most energetically favorable configurations resulting from interactions of water molecules on surfaces of hydrogenated two-dimensional atomic diamonds with hydrogen vacancy
以水与Hv-HCD 2 维原子晶体作用体系为例, 水氢原子(亲电反应位点) 与氢空位碳原子(亲核反应位点) 的Fukui 函数的和为f−(r) + f+(r) = 0.022 + 0.081 = 0.103, 该值大于水氧原子(亲核反应位点) 与氢空位碳原子(亲电反应位点) 的Fukui 函数之和(f+(r)+f−(r) = 0.010+0.014 = 0.024), 说明当水分子与Hv-HCD 2 维原子晶体相互作用时, 位点与取向②较①具有更大的相互作用几率. 有关2 种作用位点与取向的优化结构, 第一性原理计算结果与此按照软度分析的结果是一致的.
值得注意的是, 水分子在含氢空位碳原子位点处仍以分子形式存在, 并未发生解离产生羟基自由基. 就此现象而言, 氢空位氢化立方金刚石2 维原子晶体与部分氧化物原子晶体不同, 如TiO2的水分子在其表面吸附时通常发生解离[27-28]. 水分子-含氢空位氢化立方金刚石2 维原子晶体体系的相互作用能(Eint) 可以定义为
式中: E(H2O −HvD)、E(H2O)、E(HvD) 分别表示为水分子氢空位氢化立方金刚石2 维原子晶体体系、水分子、氢空位氢化立方金刚石2 维原子晶体的基态能量. 基于第一性原理和式(5) 计算的水分子与Hv-HCD、h-BN/Hv-HCD、G/Hv-HCD 2 维原子晶体体系的相互作用能分别为−11.50、−7.72、5.79 kJ·mol−1, 隶属弱相互作用类型, 其中水分子与G/Hv-HCD 2 维原子晶体的相互作用能为正值, 即为一个吸热过程.
与氟、氧、氮等原子不同, 碳原子因其具有较小的电负性, 一般不形成氢键. 然而, 当碳原子与氮、氯等原子直接相连, 或像本工作研究的2 维原子晶体存在氢空位时, 碳原子的电负性,即吸引电子的能力增强, 也可以产生氢键. 氢原子与碳原子的范德华半价[29]之和为0.110 +0.160 = 0.270 (nm), 2 种原子的共价半价[30]之和为0.031 + 0.076 = 0.107 (nm). 由图4 所示的取向②的优化结构可知: 水氢原子与Hv-HCD、h-BN/Hv-HCD、G/Hv-HCD 2 维原子晶体氢空位碳原子的距离分别为0.203、0.201、0.195 nm, 该值小于氢原子与碳原子的范德华半价之和, 却大于氢原子与碳原子的共价半价之和; 氢键的键能一般约为8∼50 kJ·mol−1. 综合考虑水氢原子和氢空位碳原子的距离和体系相互作用能, 可以认为水分子和氢空位碳原子之间形成了氢键.
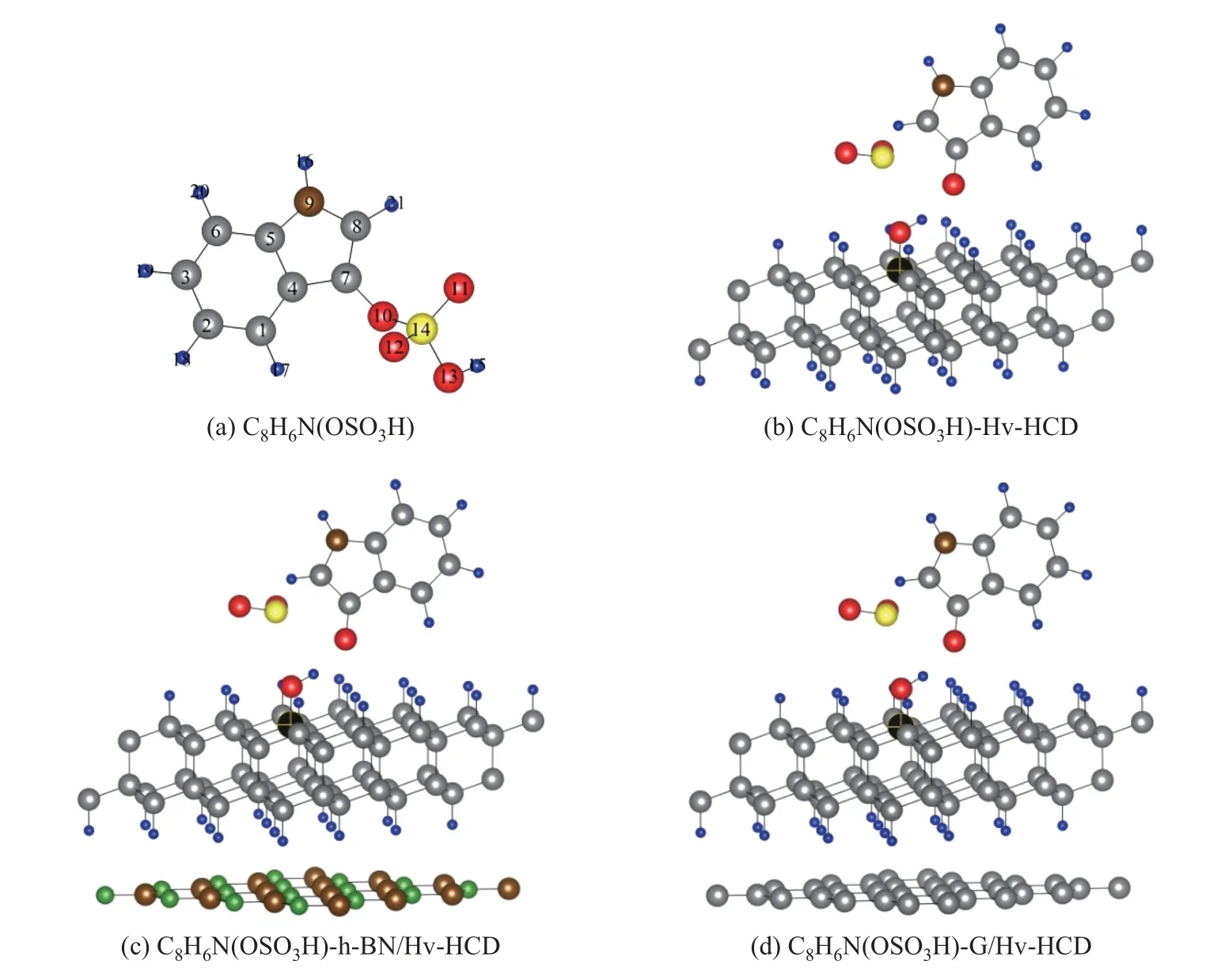
图4 硫酸吲哚酚(C8H6N(OSO3H))-含氢空位氢化立方金刚石2 维原子晶体作用体系能量最有利的构型Fig.4 Most energetically favorable configurations resulting from interactions of indoxyl sulfate molecules on surfaces of hydrogenated two-dimensional atomic diamonds with hydrogen vacancy
2.4 硫酸吲哚酚-含氢空位氢化立方金刚石2 维原子晶体相互作用体系
对于硫酸吲哚酚分子, 原子O-13 具有较大的f+(r) 值, 原子C-7 则具有较大的f−(r) 值.由此亦可以推知, 当硫酸吲哚酚分子与含氢空位氢化立方金刚石2 维原子晶体体系相互作用时, 可能存在2 种作用位点和取向, 即①硫酸吲哚酚O-13 原子(亲核反应位点) 与氢空位碳原子(亲电反应位点); ②硫酸吲哚酚C-7 原子(亲电反应位点) 与氢空位碳原子(亲核反应位点). 以硫酸吲哚酚与Hv-HCD 2 维原子晶体作用体系为例, 根据Fukui 函数计算结果以及软硬酸碱理论, 硫酸吲哚酚O-13 原子(亲核反应位点) 与氢空位碳原子(亲电反应位点) 的f+(r)+f−(r) 值为0.008 + 0.014 = 0.022, 该值小于硫酸吲哚酚C-7 原子(亲电反应位点) 与氢空位碳原子(亲核反应位点) 的f−(r)+f+(r) 值: 0.021 + 0.081 = 0.102, 说明当硫酸吲哚酚分子与氢空位氢化立方金刚石2 维原子晶体体系相互作用时, 二者沿着位点与取向②较①具有更大的几率. 硫酸吲哚酚分子-含氢空位氢化立方金刚石2 维原子晶体体系相互作用初始结构的构建同水-含氢空位氢化立方金刚石2 维原子晶体体系, 经由第一性原理计算, 所得硫酸吲哚酚分子-含氢空位氢化立方金刚石2 维原子晶体体系的能量最有利的构型如图4 所示.
对图4 进行分析可知, 当硫酸吲哚酚与Hv-HCD、h-BN/Hv-HCD、G/Hv-HCD 2 维原子晶体体系发生相互作用时, 硫酸吲哚酚分子皆发生化学分解, 生成3-吲哚酮和二氧化硫, 原硫酸吲哚酚磺酸基之羟基则与氢空位碳原子键合形成醇羟基. 这种作用机理与水分子-氢空位氢化立方金刚石2 维原子晶体相互作用体系具有明显的差异, 存在化学键的生成、破坏以及原子重排. 基于第一性原理基态能量计算结果, 通过式(5) 计算的硫酸吲哚酚与Hv-HCD、h-BN/Hv-HCD、G/Hv-HCD 2 维原子晶体相互作用体系的作用能分别为−162、−135、−112 kJ·mol−1, 预示其作用类型隶属强相互作用.
2.5 水与硫酸吲哚酚共存体系
对于人体体液毒素分子的检测与清除, 需要考虑水组分对毒素分子与传感或吸附核心材料相互作用的影响. 图5 为含氢空位氢化立方金刚石2 维原子晶体4×4×1 超晶胞表面,首先与单一水分子相互作用, 然后引入硫酸吲哚酚分子发生竞争、相互作用的过程. 经由第一性原理计算可知, 水分子在氢空位碳原子位点形成氢键, 硫酸吲哚酚分子随即替代水分子竞争、相互作用, 并且在氢空位碳原子位点发生化学解离, 该相互作用过程的能量变化为∆E =−79.1 kJ·mol−1.

图5 水和硫酸吲哚酚与含氢空位氢化立方金刚石2 维原子晶体相互作用示意图Fig.5 Schematic plot of interaction of coexisting water and indoxyl sulfate with hydrogenated two-dimensional atomic diamond with hydrogen vacancy
3 结束语
本工作基于立方金刚石晶体结构构建了2 种新型的碳基2 维原子晶体, 即HCD 和Hv-HCD, 进而基于Hv-HCD 又构建了2 种2 维原子晶体范德华异质结, 即h-BN/Hv-HCD和G/Hv-HCD; 利用第一性原理分别计算了4 种2 维原子晶体体系、硫酸吲哚酚、水分子的Fukui 函数. 在Hv-HCD、h-BN/Hv-HCD 和G/Hv-HCD 体系中, 氢空位碳原子皆有较大的f+(r) 和f−(r) 值, 成为含氢空位氢化立方金刚石2 维原子晶体体系的亲电和亲核反应活性位点.
当水分子与含氢空位氢化立方金刚石2 维原子晶体体系相互作用时, 水分子没有发生解离, 其O—H 键与2 维原子晶体体系氢空位碳原子形成氢键. 当硫酸吲哚酚与含氢空位氢化立方金刚石2 维原子晶体体系相互作用时, 硫酸吲哚酚分子发生化学分解, 生成3-吲哚酮和二氧化硫, 原磺酸基羟基与氢空位碳原子结合形成醇羟基.
