基底节区大量扩大血管周围间隙病人血清炎性因子水平变化及危险因素分析
2023-06-08仲婷婷邹玉安
郝 光,王 刚,仲婷婷,常 青,薛 茜,邹玉安
扩大血管周围间隙(enlarged perivascular space,EPVS)定义为环绕在颅内静脉、小静脉、动脉和小动脉等血管周围的液体空间扩大的病理状态,基底节区为EPVS发生的主要部位。近年来,越来越多研究证实,基底节区EPVS与神经退行性改变,包括神经功能损害和认知功能障碍的发生息息相关,且与脑梗死、脑出血的发生有密切联系[1-2]。既往多项研究表明,神经退行性改变发病机制之一为炎症级联反应对神经细胞的损伤,基底节区EPVS发生的可能与血源性细胞被动进入脑的渠道,引起或者加重炎症反应有关[3-5]。但目前基底节区大量EPVS病人血清炎性因子指标变化报道极少,相关机制尚未得到证实,探究基底节区大量EPVS病人血清炎性因子水平变化及基底节区大量EPVS发生的危险因素,可为明确基底节区大量EPVS发生机制,制定预防方案提供依据。基于此,本研究选择基底节区大量EPVS病人102例作为研究对象,旨在分析基底节区大量EPVS病人血清炎性因子水平变化及危险因素。
1 资料与方法
1.1 一般资料 选取2018年3月—2019年3月在河北北方学院附属第一医院神经内科就诊并经头颅核磁共振成像(MRI)检查发现基底节区大量EPVS的102例病人作为EPVS组,选择同期102名健康者作为健康对照组,回顾性收集其临床资料。纳入标准:基底节区大量EPVS诊断标准依据为《中国脑血管病影像应用指南2019》[6]中基底节区大量EPVS定义为EPVS数目过多无法统计或超过40个以上形成“筛孔”样者;年龄>18岁;具有完整的实验室及影像学检查结果。排除标准:合并急性期脑出血、急性期蛛网膜下隙出血者;合并神经系统退行性疾病包括血管性痴呆、阿尔茨海默病等;合并动脉夹层、烟雾病、肌纤维营养不良等血管病变证据者;合并多发性硬化、遗传变性疾病、中毒导致脑白质病变严重者;合并肝肾功能衰竭者;既往有大血管闭塞致大面积脑梗死病史及病灶表现者等。本研究经河北北方学院附属第一医院医学研究伦理委员会审核并批准。
1.2 方法
1.2.1 头颅MRI 使用BrivoMR355型1.5T MRI仪(美国GE公司),扫描序列包括轴位T1加权成像(T1WI)、T2加权成像(T2WI)序列、液体衰减反转恢复序列(T2FLAIR)、扩散加权成像(DWI)序列,矢状位T1WI,层厚5 mm,间隔1.5 mm,矩阵192×256,视野20~24 cm,激励次数为2次。
1.2.2 血清炎性因子水平 抽取研究对象检查当日的外周静脉血5 mL,对血液标本进行离心处理,离心半径为13.5 cm,离心转速为3 000 r/min,离心时间为10 min,分离得到血清后,采用酶联免疫吸附试验(ELISA)检测血清中白介素1(IL-1)、白介素6(IL-6)、肿瘤坏死因子α(TNF-α)及C反应蛋白(CRP)表达水平,试剂盒由踏石生物科技(苏州)有限公司提供。
1.2.3 资料收集 根据本院电子病历系统收集两组一般资料,包括年龄、性别、吸烟史(连续或累积吸烟6个月)、饮酒史(男性或女性饮酒>20 g或每次饮酒10 g,每周饮酒≥2次,时间≥1年)、糖尿病病史、高血压病史、白细胞计数(WBC)、糖化血红蛋白(HbA1c)、空腹血糖(FPG)、三酰甘油(TG)、总胆固醇(TC)、高密度脂蛋白胆固醇(HDL-C)、低密度脂蛋白胆固醇(LDL-C)、血肌酐(Scr)、血尿酸(UA)、同型半胱氨酸(Hcy)。通过SC-5290CRP型全自动血液细胞分析仪(深圳开立生物医疗科技股份有限公司)检测WBC水平;通过AU400型全自动生化分析仪(深圳市海拓华擎生物科技有限公司)检测血清TG、TC、HDL-C、LDL-C水平;通过高效液相离子交换层析法检测HbA1c水平(美国赛默飞公司);通过ELISA检测血清FPG、Hcy、Scr、UA水平,试剂盒由上海酶联生物科技有限公司提供。
1.3 观察指标
1.3.1 基底节区大量EPVS影像表现特点及分级标准 基底节区大量EPVS确诊的MRI影像学特征为基底节下部明显扩大,T2WI为高信号,T1WI、T2FLAIR为低信号,血管周围间隙直径≥1 mm,多穿过脑部半球白质呈向心性走行者为基底节下部明显扩大。计算基底节受累最严重层面的一侧半球的基底节区EPVS情况,参照文献[7]进行EPVS分级,1级:EPVS直径<2 mm;2级:EPVS直径2~3 mm;3级:EPVS直径>3 mm。
1.3.2 血清炎性因子水平变化 比较EPVS组及健康对照组血清IL-1、IL-6、TNF-α、CRP水平。
1.3.3 危险因素分析 通过单因素分析比较EPVS组、健康对照组年龄、性别、吸烟史、饮酒史、糖尿病病史、高血压病史、WBC、TG、TC、HbA1c、FPG、HDL-C、LDL-C、Scr、UA等,再通过多因素Logistic回归分析法分析基底节区大量EPVS发生的危险因素。
2 结 果
2.1 基底节区大量EPVS分级 基底节区大量EPVS病人中1级22例(21.57%),2级36例(35.29%),3级44例(43.14%)。
2.2 两组血清炎性因子水平比较 EPVS组血清IL-1、IL-6、TNF-α、CRP水平高于健康对照组(P<0.001)。详见表1。
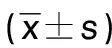
表1 两组血清炎性因子水平比较
2.3 基底节区大量EPVS发生的影响因素分析
2.3.1 基底节区大量EPVS发生的单因素分析 EPVS组、健康对照组吸烟史、高血压病史、血清UA水平比较,差异均有统计学意义(P<0.05)。详见表2。
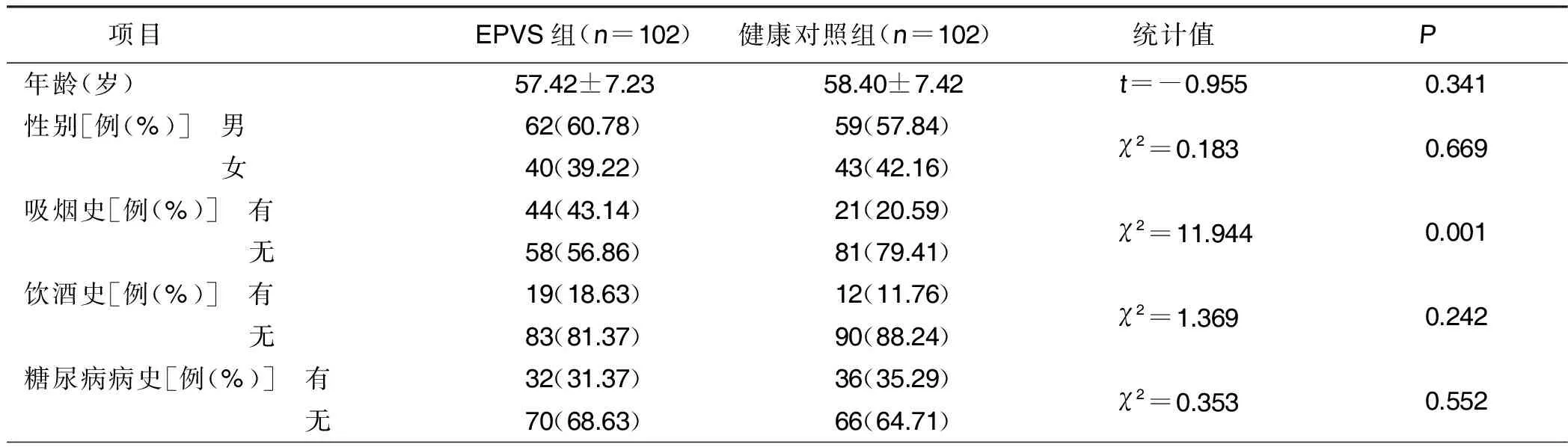
表2 基底节区大量EPVS发生的单因素分析
2.3.2 基底节区大量EPVS发生的多因素Logistic分析 以单因素分析具有统计学意义的因素作为自变量,基底节区大量EPVS发生情况作为因变量。多因素Logistic分析结果显示,血清IL-1、IL-6、TNF-α、CRP水平升高及合并吸烟史、合并高血压病史为基底节区大量EPVS发生的危险因素(OR值分别为1.881,2.020,2.065,2.413,3.939,4.740,P均<0.05)。详见表3。
表3 基底节区大量EPVS发生的多因素Logistic分析
3 讨 论
基底节区大量EPVS结构中的外界是神经胶质界膜,内界是血管外层,是脑组织间液排出的主要通道,既往研究多认为其很少导致脑组织损害[8-9],并未引起学界重视。近年来,随着影像学技术的进步及腔隙性脑梗死、脑白质疏松等脑部器质性疾病发病机制研究的深入,基底节区大量EPVS在其发病中的意义逐渐被认知,也成为脑小血管病相关性头晕、急性缺血性脑卒中病人认知功能以及脑淀粉样血管病诊断的重要标准,但目前其形成机制仍然不明[10-12]。本研究结果显示,基底节区大量EPVS病人1级22例,2级36例,3级44例,提示基底节区大量EPVS病人病情分级进展迅速,以3级为主,临床亟须进行其发病机制、诊治标准的完善工作。
炎症反应为多种脑组织退行性疾病的病理基础,IL-1可诱导黏附分子表达,募集白细胞到组织损伤部位,IL-6可诱导细胞毒性T淋巴细胞的增殖分化,刺激肝细胞合成急性期蛋白,TNF-α则是免疫炎症反应的最初启动者,CRP在肝脏内合成,为炎症免疫反应的急性期蛋白,IL-6对其合成具有促进作用,均为临床常见炎症级联反应相关因子,可能是血管白质损伤外周生物标志物[13-14]。生理状态下,免疫细胞通过脑血管运输到大脑组织的作用会受到限制,但炎症反应介导的内皮损伤可导致脑组织中血管壁通透性增加,大脑的免疫豁免发生显著变化,使血浆物质渗漏到血管壁和血管周围组织,形成基底节区大量EPVS;同时脑组织血管周围间隙内小胶质细胞形态改变,可释放促炎细胞因子,使IL-1、IL-6、TNF-α、CRP和炎性细胞浸润到中枢神经系统,进而诱导血管壁和血管周围组织纤维化甚至闭塞,损害血管扩张和营养物质转运,导致神经血管耦合调控机制功能障碍,最终形成基底节区大量EPVS[15-16]。本研究结果显示,EPVS组血清IL-1、IL-6、TNF-α、CRP水平高于健康对照组,且多因素Logistic分析结果显示,血清IL-1、IL-6、TNF-α、CRP水平升高为基底节区大量EPVS发生的危险因素,提示EPVS的发生机制可能与炎症反应加剧存在联系,血清IL-1、IL-6、TNF-α、CRP水平可能作为基底节区大量EPVS预防治疗的靶点。
此外,本研究多因素Logistic分析结果还显示,合并吸烟史、合并高血压病史为基底节区大量EPVS发生的危险因素。既往研究证明,合并吸烟史为脑梗死、脑出血等疾病的独立危险因素,合并吸烟史病人摄入多环芳烃、尼古丁、一氧化碳、焦油等成分,可增加机体氧化应激损伤,增加血管内皮功能障碍,提高血液中的脂质及纤维蛋白原含量,最终诱导脑梗死、脑出血的发生[17-18],与本研究中合并吸烟史为基底节区大量EPVS发生的危险因素相互印证。合并高血压病史病人长期血压升高,一方面,可导致脑内小动脉的血管阻力增加,同时增加对血管壁的压力,导致动静脉通透性增加,提高脑小血管内皮功能紊乱,可诱导血脑屏障渗漏,从而使组织间液漏出增多,形成基底节区大量EPVS[19];另一方面,可使甚至引起血浆蛋白等分子外渗进入脑实质,并诱导局部动静脉出现炎症反应,导致内皮细胞被破坏,减少了脑组织的氧气和营养供应,打乱大脑内稳态环境,增加组织间液,形成基底节区大量EPVS[20]。
综上所述,基底节区大量EPVS病人病情分级进展迅速,以3级为主,血清炎性因子水平升高,可能作为基底节区大量EPVS预防治疗的靶点,血清IL-1、IL-6、TNF-α、CRP水平升高、合并吸烟史、合并高血压病史为基底节区大量EPVS发生的危险因素,临床可根据以上因素对其进行干预。本研究的样本量有限,且为单中心研究,基底节区大量EPVS发生的影响因素及分子生物学机制,仍有待进一步大样本量、多中心研究予以验证。
