微生物法测定蔬菜中叶酸含量
2023-06-08李白玉
蒋 伟,李白玉
(湖南省产商品质量检验研究院,湖南长沙 410007)
叶酸是人体所必需的一种B族维生素,其在代谢循环过程中的作用非常重要。人体缺乏叶酸会导致各种各样的问题,包括巨幼细胞贫血、神经管畸形等疾病[1]。叶酸无法由人体自身合成,只能从外界摄取,一般从食物中得到[2]。因此,人体对于叶酸的摄入状况是非常值得注意的问题。蔬菜是人类获取叶酸的重要来源之一[3],了解当地常见蔬菜的叶酸含量对于指导人们日常补充叶酸具有重要意义。本文以某地区较常食用的蔬菜作为研究材料,通过微生物法使用鼠李糖乳杆菌测定分析蔬菜中叶酸的含量[4]。
1 材料与方法
1.1 材料与试剂
鼠李糖乳杆菌Lactobacillus rhamnosus(ATCC7469);菌种储备琼脂培养基:Becton,Dickinson and Company;叶酸测定用培养基:海博生物公司。叶酸标准品:纯度99.7%,上海安谱实验科技股份有限公司。
磷酸盐缓冲液终浓度为0.05 mol·L-1,pH 6.8;氢氧化钠乙醇溶液终浓度为0.01 mol·L-1;蛋白酶-淀粉酶液配比为200 mg木瓜蛋白酶、200 mg α-淀粉酶、20 mL磷酸盐缓冲液,蛋白酶-淀粉酶液需要现用现配;氢氧化钠-乙醇溶液中氢氧化钠终浓度为1 mol·L-1,乙醇溶液中乙醇与水的体积配比为2∶8。
1.2 方法
1.2.1 鼠李糖乳杆菌菌种的活化
使用菌种储备用琼脂培养基活化鼠李糖乳杆菌,具体方法是36 ℃培养1 d,并用相同的方法传种2次。最新的菌株即储备菌株,保存于4 ℃环境。实验前两天,将储备菌株活化,使用同种培养基于36 ℃继续培养1 d。
正式实验的前一天,将活化的菌株转种至液态培养液中进一步活化增殖,36 ℃培养1 d。取0.5 mL活化增殖后的菌种转种至5 mL无菌的叶酸测定培养基,不添加叶酸,36 ℃培养6 h即得接种液。此步骤注意无菌操作,培养时间可适当延长,确保接种液中残存的多余叶酸被消耗掉。
1.2.2 叶酸测定的标准曲线绘制
将叶酸标准品先用氢氧化钠-乙醇溶液逐级稀释为浓度0.200 µg·mL-1的中间液,再用水将中间液稀释为终浓度0.200 ng·mL-1的标准工作液,注意此工作液需要现用现配。叶酸测定的标准曲线配制体系见表1,每个浓度梯度做3个平行,即标准曲线测定管。后续混菌及加入培养基培养步骤与样品测定管采用相同操作。待检测工作完成后,以标准管的叶酸含量作横坐标,各标准点的吸光值均值作纵坐标,生成标准曲线。
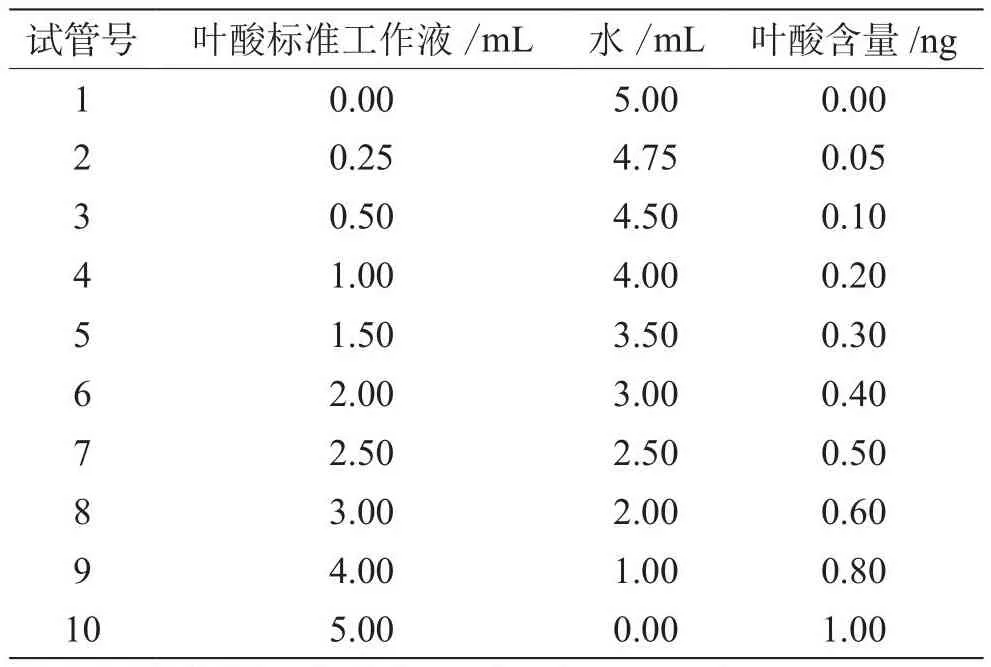
表1 标准曲线系列管的配制
1.2.3 蔬菜样品制备与测定
本实验所用的蔬菜全部购自某地区的菜市场及超市。将买来的新鲜蔬菜分别匀浆混匀,称取适量蔬菜试样转进适当大小的锥形瓶,加入30 mL磷酸缓冲液,摇匀,121 ℃高压水解15 min。待锥形瓶冷却至室温,继续加入蛋白酶-淀粉酶液和鸡胰腺液各1 mL,摇匀后加入甲苯4滴,36 ℃恒温酶解20 h。将所有内容物转移至100 mL的容量瓶中,加水定容,过滤。另准备单独的锥形瓶同上操作,不加样品,即酶空白液。最终的待测液需要根据试样中叶酸的含量进一步进行适当稀释,待测液最佳叶酸含量需要控制在0.2~0.3 ng·mL-1。
每个样品的待测液需要做3个不同浓度梯度的测定系列管,具体测定系列管的配制见表2,每个浓度梯度做3个平行,另取3支试管加入酶空白液。将叶酸测定培养基和全部测定管分别121 ℃高压灭菌15 min,待两者都降温到室温后,将接种液按4 mL·L-1的比例混入叶酸测定培养基,混匀,接着将培养基按5 mL/管的量分装到各测定管,再次混匀。放入36 ℃培养箱培养一天,直到混浊度最大时拿出测定吸光值。另备一支既不接种也不含叶酸的标准管作0对照管。培养结束后,各系列管需要在测定前再次漩涡,将紫外可见分光光度计调至540 nm处测定吸光值,留意用0对照管调零。按叶酸标准曲线求出各样品待测液浓度,再按照处理步骤中不同的稀释倍数,换算求出每100 g新鲜蔬菜中叶酸的含量。

表2 样品测定系列管的配制
2 结果与分析
2.1 蔬菜叶酸含量测定结果
在某地区不同的菜市场和超市中购得常见的25种蔬菜,具体检测得到的叶酸含量平均值见表3。由表3可知,菠菜叶酸含量最为丰富,为236.0 μg/100 g;其次为西兰花,叶酸含量为137.0 μg/100 g。其余蔬菜的叶酸含量都低于100 μg/100 g。

表3 不同种类蔬菜的叶酸含量
2.2 不同品种蔬菜的叶酸含量比较
此次检测的25种不同种类的蔬菜,叶酸含量平均值为10.7~236.0 μg/100 g,不同种类的蔬菜叶酸含量差异较大。深色蔬菜以菠菜叶酸含量最为丰富,浅色蔬菜以大白菜的叶酸含量较为丰富。整体而言,深色蔬菜较浅色蔬菜的叶酸含量略高。相比豆类、瓜类和根茎类蔬菜,叶类蔬菜整体叶酸含量相对较高。
2.3 不同售卖途径的同品种蔬菜叶酸含量比较
此次检测的25种蔬菜,从整体上看,不同售卖途径的同种蔬菜的叶酸含量也有明显差异。例如,5处不同来源的菠菜,叶酸含量平均值为236.0 μg/100 g,实际含量为82.2~332.0 μg/100 g;5处不同来源的西兰花,叶酸含量平均值为137.0 μg/100 g,实际含量为41.5~203.0 μg/100 g。推测蔬菜的叶酸含量不仅受到具体品种的影响,也会受到产地的种植环境、采摘后的运输储存条件等因素的影响。
2.4 置放时间对叶酸含量的影响
为探讨蔬菜置放后叶酸是否有流失,选取菠菜和大白菜在置放一周后重新测定叶酸含量,发现菠菜叶酸平均含量由236.0 μg/100 g下降至54.3 μg/100 g,残留率仅为23.0%;大白菜叶酸平均含量由93.4 μg/100 g下降至40.1 μg/100 g,残留率仅为42.9%。由此可见,新鲜蔬菜的叶酸含量并不稳定,在置放过程中蔬菜里的叶酸会被逐渐消耗或分解。由此可以推测,蔬菜本身的新鲜程度会对叶酸的留存量产生较大影响,由较近产地直接运来的较为新鲜的蔬菜,叶酸检测值会相对较高。而经过多重清理和运销作业等操作的蔬菜,尤其是经过长时间转运的蔬菜,增加了叶酸被破坏的可能性,可能会导致相应蔬菜的叶酸检测值偏低。
2.5 关于检测方法的一些思考
微生物法检测叶酸含量,本质上检测的是具有生物活性的多种叶酸母体及其衍生形式的总量。相比起仪器分析法针对单一组分的检测,微生物法的数据能更好地反映蔬菜中天然叶酸的总量。微生物法检测过程中,相关器皿的清洁程度非常重要,异物残留会引起菌液的异常增殖,进而导致定量失败。建议实验中使用到的相关玻璃器皿,实验前先用硫酸重铬酸甲溶液浸泡24 h以上,蒸馏水清洗后再用烘箱250 ℃干热2 h。
3 结论
测定了25种人们经常食用且容易购买到的蔬菜的叶酸含量,结果显示菠菜的叶酸含量最为丰富。叶酸含量虽因蔬菜而异,但大多数蔬菜中叶酸的含量在10~100 μg/100g。由于蔬菜是人们摄取叶酸的主要食物来源之一,因此本实验数据可为初步估算人们叶酸摄取量提供参考。富含叶酸的叶类蔬菜在置放一周后存在叶酸流失的情况,因此估算叶酸可获率时,应考虑蔬菜的食用时间以及保存状况等信息。值得注意的是,近年来许多研究亦显示叶酸在心血管等慢性疾病治疗中扮演非常重要的角色[5]。因此,含叶酸食品的摄入量与人们患慢性疾病的相关性,以及增进叶酸摄取对维护人体健康的效益,仍是待研究与了解的问题。
