遮阴对柠檬香茅中萜类化合物及其合成酶基因影响研究
2023-06-02张少平邱珊莲黄惠明李海明李洲鞠玉栋郑开斌
张少平, 邱珊莲, 黄惠明, 李海明, 李洲, 鞠玉栋, 郑开斌
遮阴对柠檬香茅中萜类化合物及其合成酶基因影响研究
张少平1, 邱珊莲1, 黄惠明1, 李海明1, 李洲1, 鞠玉栋1, 郑开斌2*
(1. 福建省农业科学院亚热带农业研究所,福建 漳州 363005;2. 福建省农业科学院农业生态研究所,福州 350003)
为获取柠檬香茅()中萜类化合物及其合成酶基因信息,以正常生长及遮阴下的柠檬香茅嫩叶为材料,进行代谢组学和转录组学结合qRT-PCR验证分析。代谢组分析结果表明,柠檬香茅所含萜类共23种,包括单萜4种、倍半萜4种、二萜8种、三萜3种和四萜4种。在遮阴下,柠檬香茅的二萜类银杏内酯C和四萜类虾青素相对含量更高。转录组测序结果表明,单萜生物合成涉及4类合成酶的24个基因,二萜生物合成涉及11类合成酶的49个基因,倍半萜和三萜生物合成涉及12类合成酶的58个基因,其中6类合成酶的8个基因在遮阴下的相对表达量显著提高,而前萘二烯加氧酶(c64786.0)基因正好相反。qRT-PCR分析表明,遮阴下4个FPKM值差异明显的萜类合成酶基因表达的变化趋势与转录组测序结果一致,但不同合成酶基因的差异表达量存在差异。因此,柠檬香茅所含4类共23种萜类化合物由27类合成酶共131个基因编码而来,不同光照强度影响9个合成酶基因的表达和2种萜类化合物含量。
柠檬香茅;萜类;合成酶;代谢组;转录组
柠檬香茅()又称柠檬草、香茅草及香茅等,为禾本科(Gramineae)香茅属多年生密丛型具香味草本[1]。广泛分布于热带及南亚热带等地[2],中国福建、广东、广西、云南等地有栽培。柠檬香茅具有浓郁的柠檬香气,可提取香茅精油[3–5]。香茅精油主要成分为挥发性萜类(单萜)物质[6–7],具有杀菌消炎,平喘止咳,舒筋活络,抒解抑郁及提振心情等功效[8–10]。萜类也叫萜烯类或类异戊二烯类化合物,为自然界中种类极为丰富的次生代谢产物,数量多达55 000多种[11–12]。萜类在植物初生和次生代谢中均起重要调节作用,都是从五碳原子(C5)的异戊二烯单元IPP (异戊烯二磷酸)及其异构体DMAPP (二甲基烯丙基二磷酸)合成而来, 再形成C10单萜、C15倍半萜、C20二萜、C30三萜及C40类胡萝卜素等化合物[13–14]。萜类化合物有来源于细胞质中的法尼基焦磷酸的甲羟戊酸途径(MVA途径)和质体中牻牛儿焦磷酸的甲基赤藓醇磷酸途径(MEP途径) 2种, 其中单萜、二萜和类胡萝卜素来源于MEP途径, 倍半萜和三萜来源于MVA途径[15–16]。萜类化合物种类繁多,其生物合成所涉及相关酶基因也多种多样[17–19]。
香茅为喜阳植物,光照充分环境下生长更为旺盛,阴凉条件下其生物产量明显降低,但目前并未见遮阴环境下香茅萜类成分及其含量差异研究。有大量关于香茅精油(挥发性单萜)提取及其成分测定等研究报道[20–22],然而香茅种类繁多, 不同种类香茅所含挥发性单萜成分差异明显[23–24]。即使同一种类香茅由于不同提取方式或检测手段不同,导致其所含挥发性单萜具体成分及含量存在差异[25–27]。此外,还未见香茅萜类形成相关合成酶基因的研究报道。本试验以大田自然生长柠檬香茅为研究对象, 以同环境生长但覆盖60%遮阳网为对照,通过代谢组检测萜类具体成分,同时,结合转录组测序,分析萜类合成代谢相关酶基因,为进一步进行香茅萜类生物合成及其基因工程等研究打下良好基础。
1 材料和方法
1.1 材料
试验材料柠檬香茅()为福建省漳州地区野生种,于2021年3月中旬分株种植于穴盘,其中一半放置大田阳光照射充足处,另一半放置大田覆盖遮光率60%的遮阳网。6月中旬取不同环境下生长的2组植株嫩叶各6份,及时放入液氮并转至–80 ℃冰箱保存备用。
1.2 代谢组检测及萜类成分筛选
取光照和遮阴下生长的香茅嫩叶各3份,经真空冷冻干燥(冻干机:Scientz-100 F)后研磨(MM 400研磨仪, Retsch)成粉末状;称取100 mg粉末溶解于0.6 mL 70%甲醇提取液,4 ℃下放置10 h,期间涡旋4~6次;离心取上清液用微孔滤膜过滤,滤液保存于进样瓶中,用于超高效液相色谱串联质谱(UPLC-MS/MS)检测分析[28]。基于百迈客科技有限公司数据库MWDB (metware database),根据二级谱信息对6个样品中的萜类成分进行定性和定量分析,萜类化合物相对含量取3份的平均值。
1.3 转录组测序及萜类合成酶筛选
采用Trizol法提取香茅嫩叶总RNA,获得cDNA后进行Illumina HiSeqTM 2500转录组测序及数据分析[28]。经KEGG数据库注释获得单萜、二萜、倍半萜和三萜代谢途径具体合成酶基因信息。
1.4 差异表达基因的qRT-PCR验证
光照(标号:阳1-1)及遮阴(标号:阴1-1)样本经转录组测序获得的总RNA,用超微量核酸蛋白测定仪(scandrop100)测定OD值。检测合格后采用Aidlab公司反转录试剂盒(TUREscript 1st Stand cDNA Syn- thesis Kit)进行反转录,根据反转录试剂盒中反应体系和反应条件合成光照及遮阴香茅cDNA, 以其为模板,进行4个差异表达明显的萜类合成酶基因(根据转录组测序结果中FPKM值)进行qRT-PCR检测,每个基因检测3次,取平均值。具体基因及其引物序列见表1。

表1 荧光定量PCR分析的5个基因及其引物
2 结果和分析
2.1 代谢组检测萜类化合物
根据代谢组检测光照及遮阴下生长的柠檬香茅代谢产物进行萜类成分及其相对含量分析。结果表明,柠檬香茅含萜类23种,包括单萜、倍半萜和四萜各4种,二萜8种,三萜3种。遮阴下二萜类的银杏内酯C和四萜类虾青素相对含量更高,而其他萜类成分相对含量在不同光照环境下影响不大,尤其是作为香茅精油主要成分的挥发性单萜相对含量差异不明显。4种挥发性单萜相对含量由高到低依次为-罗勒烯、脱氢马钱素四乙酸酯、橙花醇和-蒎烯(表2)。

表2 23种萜类化合物及其相对含量
2.2 萜类合成酶基因信息
转录组测序后经KEGG数据库注释,进行单萜、二萜以及倍半萜和三萜等合成酶基因信息分析。
2.2.1 单萜生物合成酶基因信息
单萜生物合成酶包括羧基吲哚合成酶的9个家族基因、新薄荷醇脱氢酶的13个家族基因、芳樟醇合成酶和荆芥内酯单氧化酶各1个基因(表3)。不同光照下,羧基吲哚合成酶基因和荆芥内酯单氧化酶相对表达量均很低,芳樟醇合成酶相对表达量均较高,而新薄荷醇脱氢酶的13个家族基因相对表达量相差显著,其中基因在光照下的表达量显著低于遮阴环境。
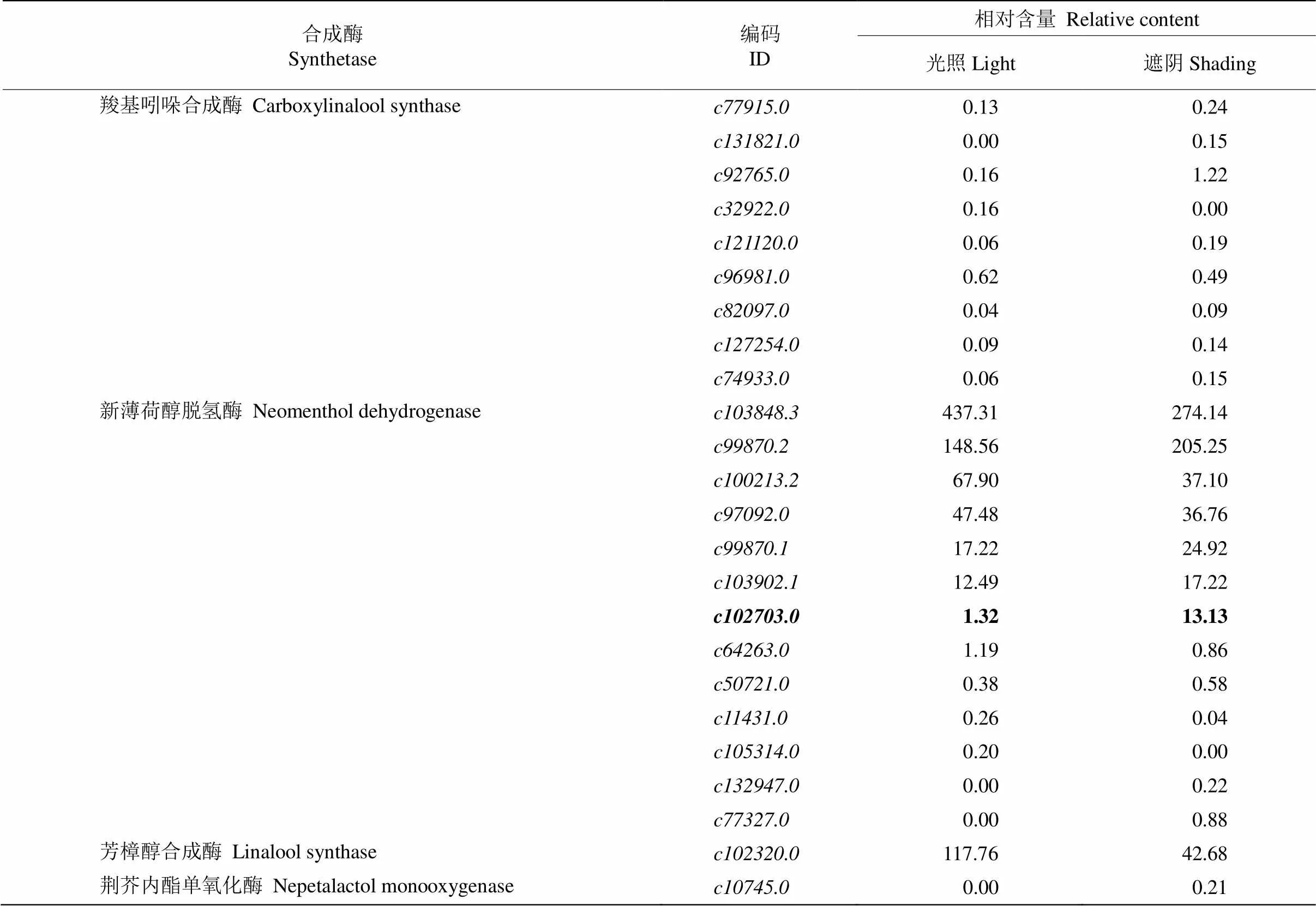
表3 编码4类单萜生物合成酶的24个基因
2.2.2 二萜生物合成酶基因信息
二萜生物合成酶包括赤霉素2-双加氧酶的26个家族基因、贝壳杉烯合成酶的5个家族基因、异贝壳杉烯羟化酶、莫米内酯-合成酶及赤霉素20氧化酶各3个家族基因、贝壳杉烯酸单加氧酶及三甲基十三碳四烯合成酶各2个家族基因、二烯11-羟化酶、共丙基二磷酸合成酶、二烯氧化酶及荆芥内酯合成酶各1个基因(表4)。对比光照环境,遮阴下赤霉素2-双加氧酶(和)、贝壳杉烯合成酶(和)、莫米内酯-合成酶()和贝壳杉烯酸单加氧酶()等6个二萜生物合成酶基因的相对表达量显著提高。
2.2.3 倍半萜和三萜生物合成酶基因信息
倍半萜和三萜生物合成酶包括大根香叶烯合成酶的16个家族基因、蓍醇B合成酶的15个家族基因、橙花叔醇合成酶的13个家族基因、法呢基二磷酸法呢基转移酶的4个家族基因、前萘二烯加氧酶的3个家族基因、法尼醇脱氢酶的2个家族基因、羽扇豆醇合成酶、无环倍半萜合成酶、-法尼烯合成酶、-大蒈烯合成酶以及马兜铃烯1,3-二羟基酶各1个基因(表5)。大根香叶烯合成酶、蓍醇B合成酶及橙花叔醇合成酶等虽含有大量家族基因,但大多数基因在光照及遮阴环境下相对表达量均很低,且不存在差异表达极显著基因。前萘二烯加氧酶()在光照环境下相对表达量更高,而法尼醇脱氢酶)在光照环境下相对表达量正好相反。
2.3 差异表达基因的qRT-PCR检测
对比光照和遮阴下柠檬香茅的转录组测序结果,挑选FPKM值差异明显的4个参与萜类合成的酶基因进行qRT-PCR检测,结果表明,4个萜类合成酶基因在光照及遮阴下的表达趋势与转录组的FPKM值结果一致,但2种检测结果差异表达倍数存在差异。前萘二烯加氧酶()基因在光照环境下表达量更高,而其他3个合成酶基因在遮阴环境下表达更高(图1)。
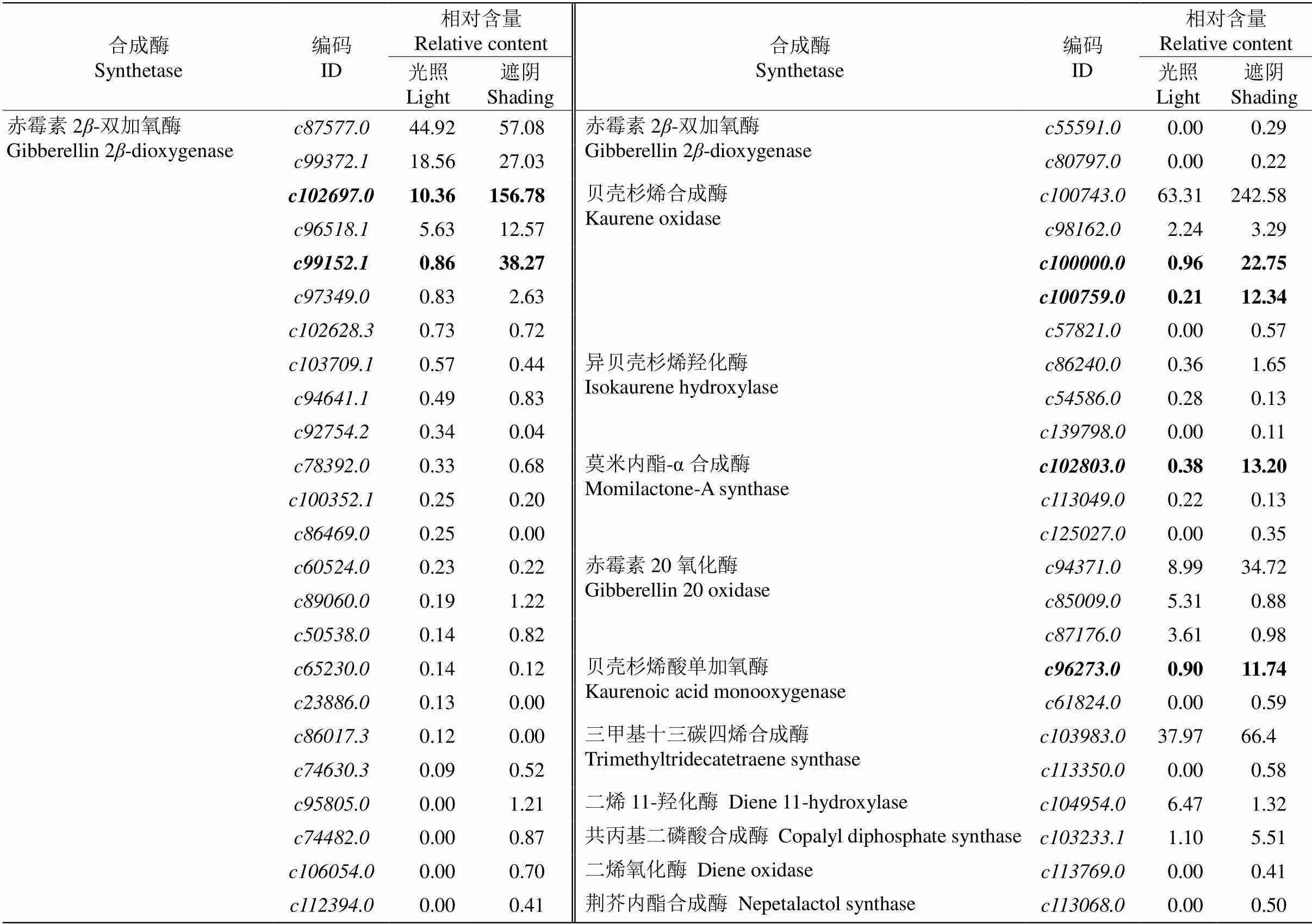
表4 编码11类二萜生物合成酶的48个基因

表5 编码12类倍半萜和三萜生物合成酶的58个基因
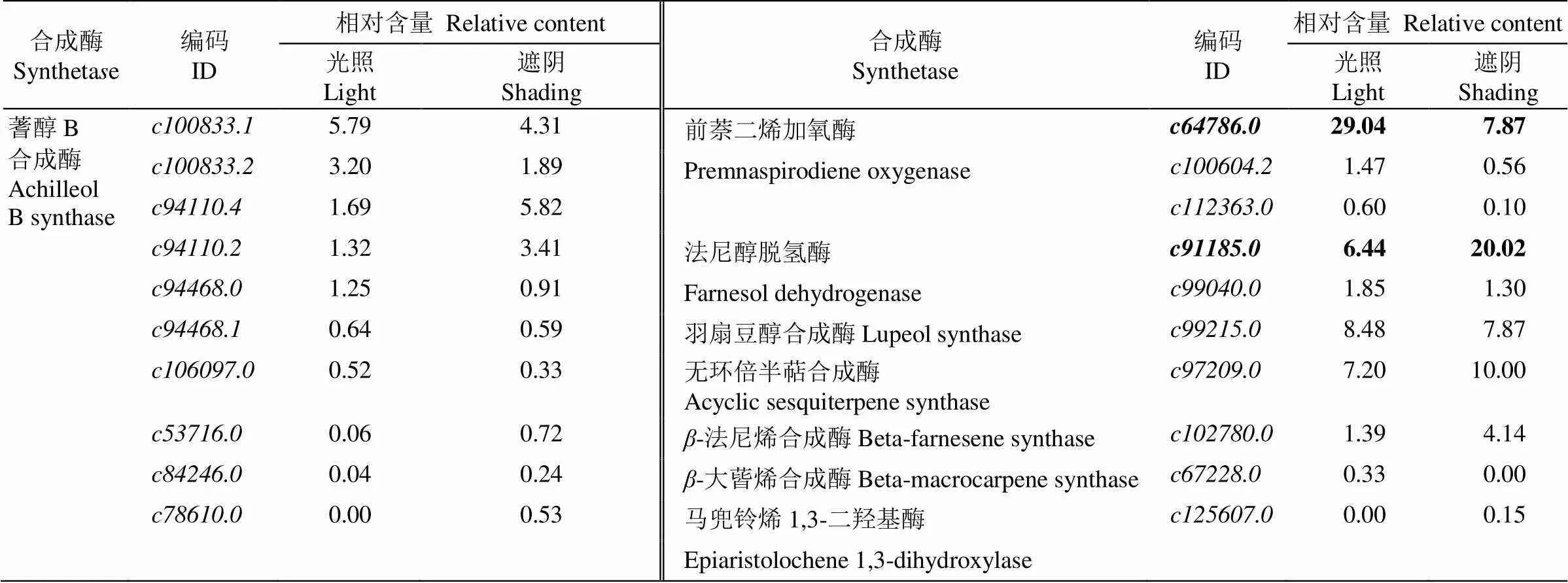
续表(Continued)

图1 4个差异表达基因的qRT-PCR验证
3 结论和讨论
香茅种类繁多,不同品种香茅提取的精油中挥发性萜类(单萜)物质差异明显[29],柠檬香茅精油的挥发性萜类主要为开链单萜有机物柠檬醛(香叶醛和橙花醛)等;而爪哇香茅()提取精油所含挥发性萜类主要为无环单萜香茅醛及香叶醇等。此外,同品种柠檬香茅在不同地域栽培,其精油单萜类成分及含量同样差异明显[1]。前人研究香茅萜类挥发性成分大多通过提取精油,导致具体萜类成分及含量差异较大。本研究首次通过代谢组检测光照和遮阴下柠檬香茅萜类成分及相对含量,其4种挥发性单萜相对含量依次为-罗勒烯>脱氢马钱素四乙酸酯>橙花醇>-蒎烯, 这4种单萜相对含量在光照和遮阴下均差异不明显。这与之前的研究结果[1]不同,可能与同一品种在不同地域栽培有关,或者是分析方法不同,提取精油过程中的高温加热发生了化学反应,从而导致柠檬香茅中单萜类化合物发生变化。本研究进一步对单萜生物合成酶基因进行分析,柠檬香茅单萜有4类合成酶共24个基因,这些家族基因的相对表达量大多在不同环境下均极低,且差异不显著。此外,只有1个新薄荷醇脱氢酶()基因相对表达量在光照下显著低于遮阴环境。
除挥发性单萜外,本研究还检测到柠檬香茅中有19种倍半萜、二萜、三萜及四萜等萜类化合物,除二萜类的银杏内酯C和四萜类虾青素相对含量在遮阴下更高外,其他萜类成分相对含量在不同光照下的影响不大。在11类二萜生物合成酶的38个基因中,有2个赤霉素2-双加氧酶基因(和)、2个贝壳杉烯合成酶基因(和)、1个莫米内酯-合成酶基因()和1个贝壳杉烯酸单加氧酶基因()等6个基因相对表达量在遮阴下显著提高。结合转录组和代谢组研究结果,遮阴环境下生长的柠檬香茅中二萜类成分银杏内酯C相对含量更高,这与其6个合成酶基因相对表达量显著提高成正比。不同光照环境下柠檬香茅的倍半萜和三萜具体成分和含量差异不大,但其合成酶中前萘二烯加氧酶基因()在光照环境下相对表达量更高, 而法尼醇脱氢酶基因()正好相反。
有报道光照能够提高葡萄()的香茅醇及橙花醇等萜类含量及其相关基因的表达量[30],而本研究中遮阴提高了柠檬香茅中银杏内酯C和虾青素等2个萜类化合物含量及其相关的8个基因的表达量,这可能是因为光照等适宜环境能促进植物中某些重要萜类成分的生成,而某些萜类成分的提高是因为植物在遮阴等逆境胁迫后作为响应的防御信号。
本研究采用代谢组结合转录组进行柠檬香茅萜类化合物及其合成酶基因分析,柠檬香茅中有4类共23种萜类化合物,是由27类合成酶共131个基因编码而来;有2种萜类化合物相对含量在遮阴环境明显升高,其对应的6类合成酶8个基因的相对表达量也明显提高,此外还有1个合成酶基因在遮阴环境下相对表达量明显下降,这些为进一步进行香茅萜类生物合成及其基因工程等研究打下良好基础。
[1] QIU S L. Citronella Resources and Their Utilization [M]. Beijing: China Agricultural Science and Technology Press, 2019: 1–172. [邱珊莲. 香茅资源及其利用 [M]. 北京: 中国农业科学技术出版社, 2019: 1–172.]
[2] MACEDO I T F, DE OLIVEIRA L M B, RIBEIRO W L C, et al. Anthelmintic activity ofagainst[J]. Rev Bras Parasitol Vet, 2015, 24(3): 268–275. doi: 10. 1590/S1984-29612015059.
[3] LI M L, LIU B M, BERNIGAUD C, et al. Lemongrass () oil: A promising miticidal and ovicidal agent against[J]. PLoS Negl Trop Dis, 2020, 14(4): e0008225. doi: 10.1371/journal.pntd.0008225.
[4] DA SILVA L C, DE SOUZA PERINOTTO W M, SÁ F A, et al.acaricidal activity of,andagainst(Acari: Ixodidae) [J]. Exp Parasitol, 2020, 216: 107937. doi: 10.1016/j.exppara.2020.107937.
[5] HACKE A C M, MIYOSHI E, MARQUES J A, et al. Anxiolytic properties of(DC.) stapf extract, essential oil and its constituents in zebrafish () [J]. J Ethnopharmacol, 2020, 260: 113036. doi: 10.1016/j.jep.2020.113036.
[6] BRÜGGER B P, MARTÍNEZ L C, PLATA-RUEDA A, et al. Bio- activity of the(Poaceae) essential oil and its terpenoid constituents on the predatory bug,(Hete- roptera: Pentatomidae) [J]. Sci Rep, 2019, 9(1): 8358. doi: 10.1038/s41 598-019-44709-y.
[7] WANI A R, YADAV K, KHURSHEED A, et al. An updated and comprehensive review of the antiviral potential of essential oils and their chemical constituents with special focus on their mechanism of action against various influenza and coronaviruses [J]. Microb Pathog, 2021, 152: 104620. doi: 10.1016/j.micpath.2020.104620.
[8] BAYALA B, BASSOLE I H N, MAQDASY S, et al.andessential oils have cytotoxic effects on tumor cell cultures identification of citral as a new putative anti-proliferative molecule [J]. Biochimie, 2018, 153: 162–170. doi: 10.1016/j.biochi.2018.02.013.
[9] BASERA P, LAVANIA M, AGNIHOTRI A, et al. Analytical investi- gation ofand exploiting the potential of developed silver nanoparticle against the dominating species of patho- genic bacteria [J]. Front Microbiol, 2019, 10: 282. doi: 10.3389/fmicb. 2019.00282.
[10] DA ROCHA L O, DA SILVA LEMOS G C, VIEIRA I J C, et al. Chemical characterization andbiological activity ofextracts againstspp. andspp. nematodes from sheep [J]. Parasitology, 2020, 147(13): 1559– 1568. doi: 10.1017/S0031182020001432.
[11] LIU Q. Isolation of(DC.) stapf endophytic bacteria and their affect on the citral production in host [D]. Changsha: Hunan University, 2017: 6. [柳倩. 香茅草内生产香细菌的分离及其对宿主产柠檬醛的影响 [D]. 长沙: 湖南大学, 2017: 6.]
[12] PU X J, DONG X M, LI Q, et al. An update on the function and regulation of methylerythritol phosphate and mevalonate pathways and their evolutionary dynamics [J]. J Integr Plant Biol, 2021, 63(7): 1211– 1226. doi: 10.1111/jipb.13076.
[13] CHRISTIANSON D W. Structural and chemical biology of terpenoid cyclases [J]. Chem Rev, 2017, 117(17): 11570–11648. doi: 10.1021/acs. chemrev.7b00287.
[14] PICHERSKY E, RAGUSO R A. Why do plants produce so many terpenoid compounds? [J]. New Phytol, 2018, 220(3): 692–702. doi: 10.1111/nph.14178.
[15] CHEN X X, ZHANG C Q, LINDLEY N D. Metabolic engineering strategies for sustainable terpenoid flavor and fragrance synthesis [J]. J Agric Food Chem, 2020, 68(38): 10252–10264. doi: 10.1021/acs.jafc. 9b06203.
[16] MOSER S, PICHLER H. Identifying and engineering the ideal microbial terpenoid production host [J]. Appl Microb Biotechnol, 2019, 103(14): 5501–5516. doi: 10.1007/s00253-019-09892-y.
[17] PRAMASTYA H, SONG Y, ELFAHMI E Y, et al. Positioningas terpenoid cell factory [J]. J Appl Microb, 2021, 130(6): 1839–1856. doi: 10.1111/jam.14904.
[18] AGATONOVIC-KUSTRIN S, KUSTRIN E, GEGECHKORI V, et al. Anxiolytic terpenoids and aromatherapy for anxiety and depression [M]// GUEST P C. Reviews on New Drug Targets in Age-Related Disorders. Cham: Springer, 2020: 283–296. doi: 10.1007/978-3-030- 42667-5_11.
[19] SCHEMPP F M, DRUMMOND L, BUCHHAUPT M, et al. Microbial cell factories for the production of terpenoid flavor and fragrance compounds [J]. J Agric Food Chem, 2018, 66(10): 2247–2258. doi: 10.1021/acs.jafc.7b00473.
[20] AJAYI E O, SADIMENKO A P, AFOLAYAN A J. GC-MS evaluation of(DC) Stapf. oil obtained using modified hydrodistillation and microwave extraction methods [J]. Food Chem, 2016, 209: 262–266. doi: 10.1016/j.foodchem.2016.04.071.
[21] SHAH G, SHRI R, PANCHAL V, et al. Scientific basis for the therapeutic use ofStapf. (lemon grass) [J]. J Adv Pharm Technol Res, 2011, 2(1): 3–8. doi: 10.4103/2231-4040.79796.
[22]KIEŁTYKA-DADASIEWICZ A, LUDWICZUK A, TARASEVIČIENĖ Ž, et al. Chemical and nutritional compounds of different parts of lemongrass ((DC) Stapf.) cultivated in temperate climate of Poland [J]. J Oleo Sci, 2021, 70(1): 125–133. doi: 10.5650/ jos.ess20171.
[23] DE OLIVEIRA E SILVA F, SOARES J C M, VALDEZ A, et al.protects erythrocytes from lipid peroxidation[J]. Cardiovasc Hematol Agents Med Chem, 2022, 20(2): 166– 169. doi: 10.2174/1871525719666210906122948.
[24] KUMAR P, MISHRA S, MALIK A, et al. Housefly (L.) control potential ofStapf. (Poales: Poaceae) essential oil and monoterpenes (citral and 1,8-cineole) [J]. Parasitol Res, 2013, 112(1): 69–76. doi: 10.1007/s00436-012-3105-5.
[25] CHANTHAI S, PRACHAKOLL S, RUANGVIRIYACHAI C, et al. Influence of extraction methodologies on the analysis of five major volatile aromatic compounds of citronella grass () and lemongrass () grown in Thailand [J]. J AOAC Int, 2012, 95(3): 763–772. doi: 10.5740/jaoacint.11-335.
[26] MACHADO M, PIRES P, DINIS A M, et al. Monoterpenic aldehydes as potential anti-agents: Activity ofand citral on,and[J]. Exp Parasitol, 2012, 130(3): 223–231. doi: 10.1016/j.exppara.2011.12.012.
[27] FERIOTTO G, MARCHETTI N, COSTA V, et al. Chemical compo- sition of essential oils froms,, and, and their effects on the HIV-1 tat protein function [J]. Chem Biodiv, 2018, 15(2): e1700436. doi: 10.1002/cbdv. 201700436.
[28] ZHANG S P, QIU S L, HUANG H M, et al. Transcriptome and metabolome analyses of flavonoids metabolism in leaf, stem and root ofL. [J]. Acta Bot Boreali-Occid Sin, 2021, 41(2): 254–261. [张少平, 邱珊莲, 黄惠明, 等. 基于转录组和代谢组分析马齿苋根茎叶中类黄酮代谢[J]. 西北植物学报, 2021, 41(2): 254– 261. doi: 10.7606/j.issn.1000-4025.2021.02.0254.]
[29] SONG X C, LI D X, REN Y F, et al. Research progress on applying of essential oil ofplant to control agricultural pest [J]. China Plant Protect, 2018, 38(7): 25–33. [宋星陈, 李冬雪, 任亚峰, 等. 香茅属植物精油在农业病虫害控制中的应用研究进展[J]. 中国植保导刊, 2018, 38(7): 25–33. doi: 10.3969/j.issn.1672-6820.2018.07. 004.]
[30] SONG J Q, SMART R, WANG H, et al. Effect of grape bunch sunlight exposure and UV radiation on phenolics and volatile composition ofL. cv. Pinot noir wine [J]. Food Chem, 2015, 173: 424– 431. doi: 10.1016/j.foodchem.2014.09.150.
Effects of Shading on the Production and Synthase Genes of Terpenoids in
ZHANG Shaoping1, QIU Shanlian1, HUANG Huiming1, LI Heiming1, LI Zhou1, JU Yudong1, ZHENG Kaibin2*
(1. Subtropical Agriculture Research Institute, Fujian Academy of Agricultural Sciences, Zhangzhou 363005, Fujian, China; 2. Agriculture Ecology Institute, Fujian Academy of Agricultural Sciences,Fuzhou 350003, China)
In order to obtain the information of terpenoids and their synthase genes of, the changes in the transcriptome and metabolome of young leaves under light and shade were studied, and the expression of terpenoid synthase genes was confirmed by qRT-PCR. Metabolomic analysis showed thatcontained 23 terpenes, including 4 monoterpenes, 4 sesquiterpenes, 8 diterpenes, 3 triterpenes and 4 tetraterpenes. The relative contents of ginkgolide C and astaxanthin under shade was higher than those under light. According to transcriptome sequencing, there were 24, 49 and 58 genes encoding 4, 11 and 12 synthases involved monoterpene, diterpene and sesquiterpene and triterpene biosynthesis pathway, respectively, in which the relative expression of 8 genes encoding 6 synthetases significantly increased under shade, but that of premnaspirodiene oxygenase gene was just reverse. The expression patterns of four terpenoid synthase genes with significant difference FPKM values under shading by qRT-PCR was consistent with the transcriptome sequencing results, however, the differential expression of different synthase genes were different. Therefore, it was suggested thatcontains 23 terpenoids in 4 categories catalyzed by 27 synthetases, which are encoded by 131 genes, and light intensity affects the relative content of 2 terpenoids and the expression of 9 synthetase genes.
; Terpenoid; Synthase; Transcriptome; Metabolome
10.11926/jtsb.4600
2021-12-30
2022-02-22
福建省公益类科研院所专项(2020R1030001, 2020R1030005);福建省农业科学院科技创新平台专项(CXPT202103); 福建省农业科学院青年创新团队项目(CXTD2021006-3)资助
This work was supported by the Special Project for Public Welfare Research Institutes in Fujian (Grant No. 2020R1030001, 2020R1030005), the Special Project for Science and Technology Innovation Platform in FAAS (Grant No. CXPT202103), and the Project for Youth Innovation Team of FAAS (Grant No. CXTD2021006-3).
张少平(1975年生),男,硕士,高级农艺师,主要从事功能植物次生代谢产物相关研究。E-mail: zspnc@163.com
. E-mail: 409119296@.qq.com
