腹腔镜袖状胃切除术对肥胖症合并高血压的疗效分析
2023-06-01韩建立郭晨浩
刘 晶,韩建立,郭晨浩
(山西白求恩医院 山西医学科学院 同济山西医院 山西医科大学第三医院普通外科,山西 太原,030032)
现今我国城市化进程加快、饮食结构改变、体力活动减少,超过50%的人群为超重或肥胖[1]。其中,60%~80%的肥胖人群常合并高血压[2],血压水平是心血管风险的独立危险因素且呈正相关[3]。目前降压治疗方案主要为药物治疗及生活方式干预,但长期疗效有限,尤其肥胖患者由于依从性差、自我管理困难等因素导致血压控制欠佳[4]。研究表明,减重代谢手术对肥胖症合并高血压具有显著疗效[5],这些研究主要集中在胃旁路手术[5-6],关于腹腔镜袖状胃切除术(laparoscopic sleeve gastrectomy,LSG)的研究较少。本研究回顾分析2018年6月至2020年5月我院收治的58例肥胖症合并高血压患者的临床资料,分析LSG治疗肥胖症合并高血压的临床效果及患者术前、术后12个月心血管10年风险等级的变化。
1 资料与方法
1.1 临床资料 采用回顾性队列研究方法。收集58例肥胖症合并高血压患者的临床资料,其中男33例,女25例;18~64岁,平均(37±10)岁。术前体重(118.38±26.31)kg,体质量指数(body mass index,BMI)平均(40.79±6.88)kg/m2,腹围为(125.58±16.23)cm,收缩压(155.95±9.68)mmHg,舒张压(97.14±9.59)mmHg,高血压病程(3.8±6.1)年,合并糖尿病31例,吸烟史23例。术前服药数量0~1种40例,≥2种为18例。58例患者均行LSG。
1.2 纳入与排除标准 纳入标准:(1)16~65岁;(2)肥胖症合并高血压;(3)首次行LSG;(4)男性腰围≥90 cm,女性腰围≥85 cm;(5)愿意接受手术、可承担术后饮食习惯、生活方式的改变,签署手术知情同意书。排除标准:(1)肾脏疾病、主动脉狭窄、原发性醛固酮增多症等引起的继发性高血压;(2)术后失访;(3)近期发生过心血管疾病:6个月内发生过心肌梗死或卒中、心绞痛、冠状动脉重建术、心力衰竭等;(4)精神疾病、依从性差。
1.3 手术方法 患者手术适应证符合《中国肥胖及2型糖尿病外科治疗指南(2019版)》[7]。气管插管全身麻醉,患者取仰卧头高足低“大”字位,脐缘做1 cm纵切口,穿刺气腹针建立气腹,压力维持在13 mmHg,置入腹腔镜。脐上10 cm左锁骨中线偏右处置入操作钳,探查腹腔脏器及有无食管裂孔疝,充分游离胃体大弯侧、胃底,暴露胃后壁,显露His角,期间36 Fr支撑胃管协助定位。距幽门4~6 cm处使用腔镜下直线切割吻合器切除大部分胃大弯侧及整个胃底,使残胃呈袖状,容量约为100 mL;残胃切缘用可吸收倒刺线连续包埋缝合;探查腹腔有无出血、渗漏,经Trocar取出胃标本,均放置腹腔引流管,使用筋膜缝合器关闭主操作孔,手术结束。术前检查提示合并胆囊结石需手术的患者,术中一并行胆囊切除术。
1.4 观察指标与评价标准 观察指标:(1)术后合并症及缓解情况:包括术后并发症处理及转归情况。(2)随访及相关指标变化情况:术前患者基本信息,包括年龄、性别、吸烟情况、服用降压药数量及种类、高血压病程等;术前、术后1周、1个月、3个月、6个月、12个月体质量、BMI、收缩压与舒张压的变化情况;术前、术后高血压、糖尿病的缓解情况及服药状况、心血管病10年风险评估[8](China-PAR模型)、总体重减轻百分比(percentage of total weight loss,%TWL)、多余体重减轻百分比(percentage of excess weight loss,%EWL), %EWL以BMI=25 kg/m2为标准计算[9]。(3)各因素与高血压缓解的关系:术前降压药数量及种类、高血压病程、合并糖尿病情况、吸烟情况、年龄、性别、术后12个月%EWL与 %TWL。评价标准[10]:以术后12个月随访期终点进行血压缓解评价,完全缓解:术后无降压药治疗,血压保持在120/80 mmHg以下;部分缓解:术后虽无降压药治疗,但血压能达到收缩压120~140 mmHg,舒张压80~89 mmHg;未缓解:术后仍服用降压药。
1.5 随访 采用门诊、电话、微信等方式进行随访,了解患者术后1周、1个月、3个月、6个月、12个月并发症的情况及肥胖症、高血压相关指标缓解情况,包括体质量、BMI、 %TWL、%EWL、术后12个月的服药情况、心血管10年风险评估。随访时间截至2021年5月。

2 结 果
2.1 随访及相关指标变化情况 58例患者均完成术后12个月的随访,无严重并发症发生。患者的体质量、BMI、收缩压、舒张压与术前相比差异均有统计学意义(P<0.05),见表1。术后12个月,58例患者中,19例血压完全缓解(32.76%);24例部分缓解(41.38%);15例未缓解(25.86%),但口服降压药后血压较术前能得到更好的控制。高血压缓解率(完全缓解+部分缓解)为74.14%(43/58)。31例术前合并糖尿病的患者中,23例完全缓解(74.19%)。根据患者术前及术后12个月的健康资料,采用China-PAR模型工作组与国家心血管病中心联合发布的计算软件得出术前、术后10年心血管发病风险(百分比)与等级,其中术前患者心血管10年风险为10.200%(4.475%,18.575%),12个月后降为1.250%(0.700%,4.075%),两者采用Willcoxon秩和检验,结果显示差异有统计学意义(Z=-6.624,P<0.01);58例患者术前及术后12个月心血管10年风险分级变化结果见表2。

表1 58例患者术前术后各时间点体质量、BMI、血压的变化
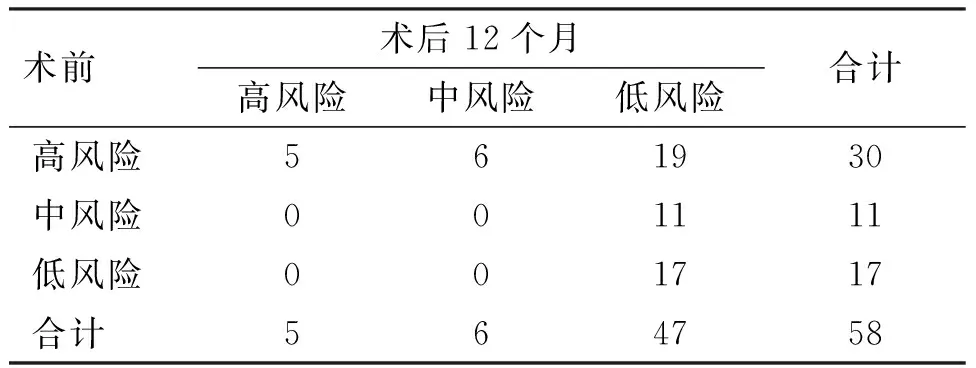
表2 术前与术后12个月心血管风险等级的变化
2.2 各因素与高血压缓解的关系 根据12个月后血压缓解情况将患者分为高血压缓解组与未缓解组,两组间高血压分级、术前降压药数量、吸烟情况、年龄及高血压病程差异有统计学意义(P<0.05);性别、术前合并糖尿病情况、术后12个月%EWL及 %TWL差异无统计学意义(P>0.05),见表3。
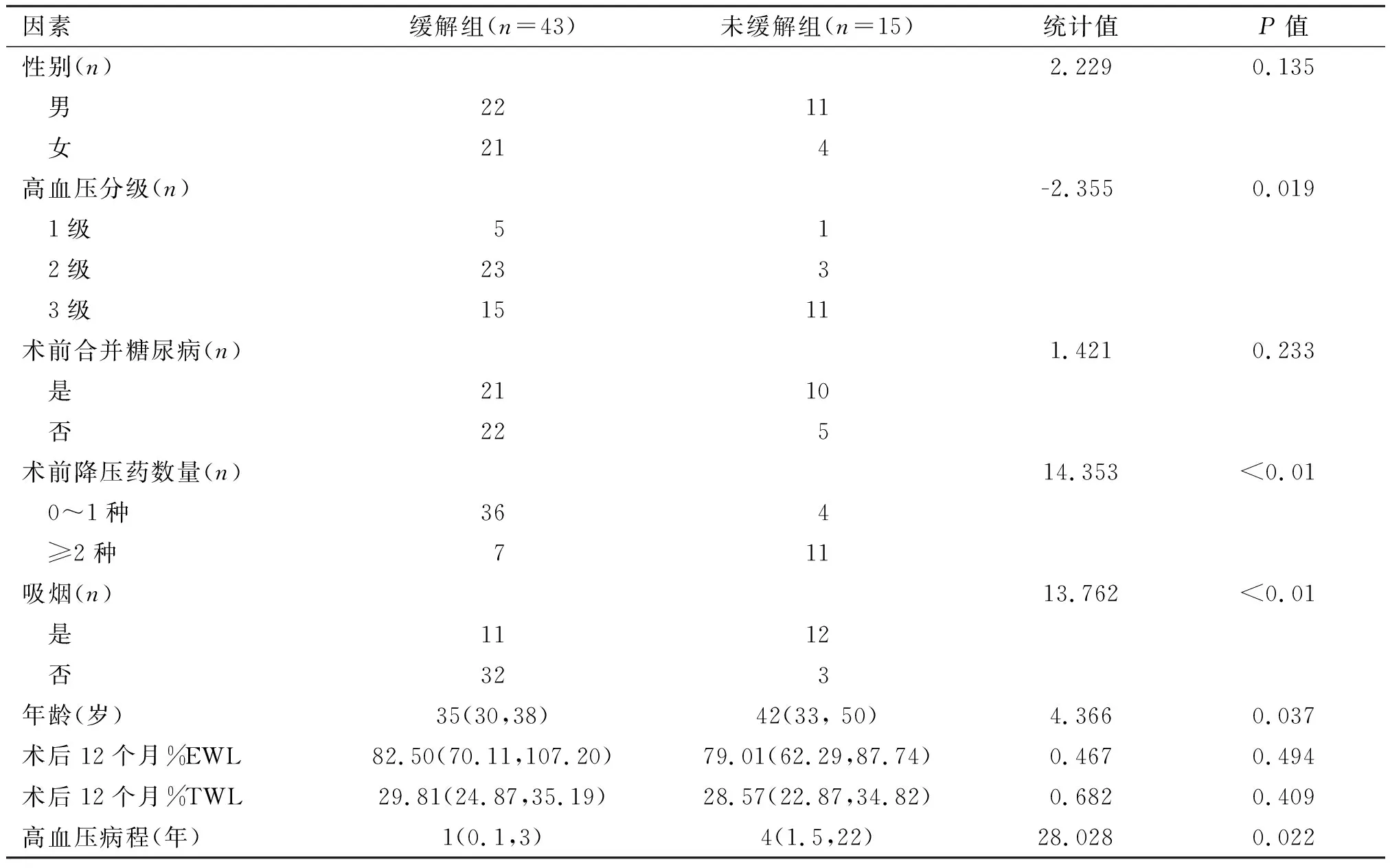
表3 各因素与高血压缓解的关系
将上述有统计学意义的指标作为自变量,以血压缓解为因变量行Logistic回归分析发现,术前服药数量为(0~1)种、术前无吸烟史是术后血压缓解的保护因素,差异有统计学意义(P<0.05),其余指标对因变量的影响均无统计学意义,结果见表4。
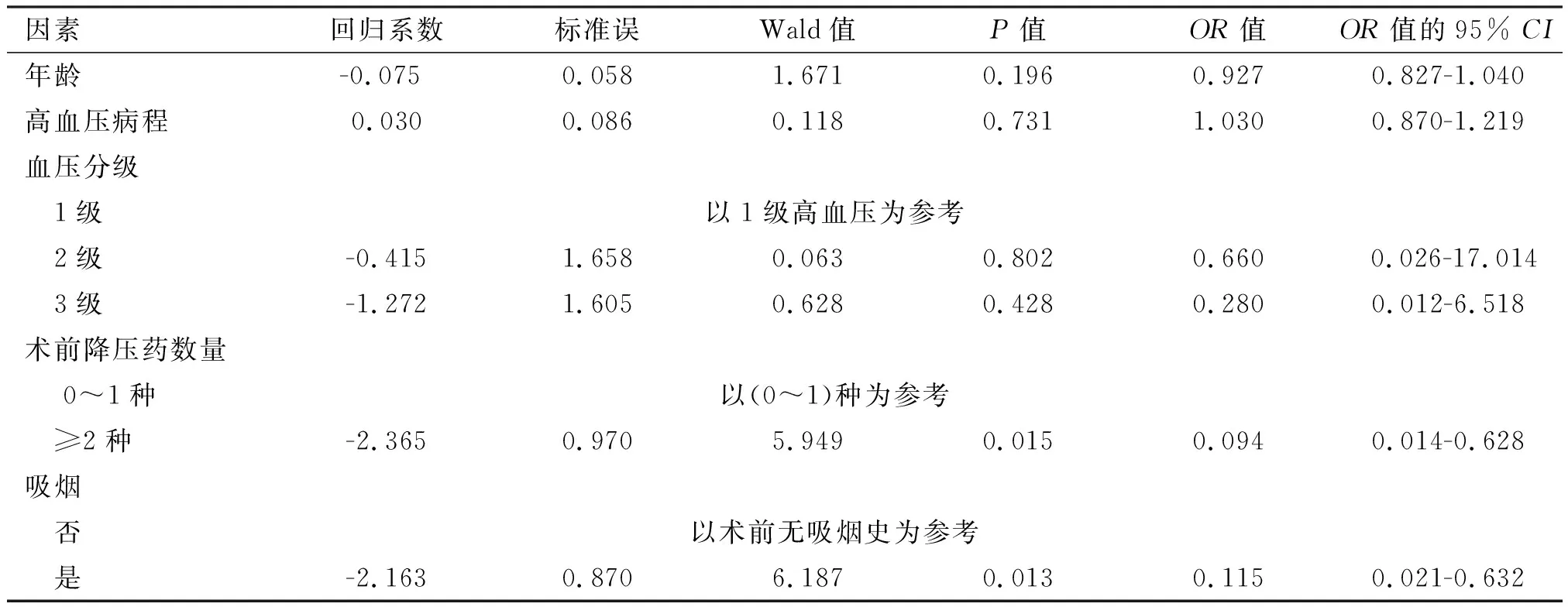
表4 高血压缓解因素的Logistic回归分析
术前无降压药治疗例数为20例,根据服药人群(n=38)术后血压缓解情况分为血压缓解组与未缓解组两组,根据患者术前服用降压药进行分类,分别为血管紧张素转化酶抑制剂/血管紧张素受体拮抗剂、利尿剂、β受体阻滞剂、α受体阻滞剂、钙离子通道阻滞剂五类,各组采用Fisher确切概率法进行比较,结果显示,β受体阻滞剂在血压缓解组与未缓解组中差异有统计学意义(P<0.05),见表5。

表5 5类降压药的比较
3 讨 论
肥胖与高血压均是心血管疾病的重要危险因素,因此联合管理至关重要[11]。研究证实,肥胖患者减重手术后收缩压、舒张压均有显著改善[6,12]。本研究中58例患者均顺利实行LSG,无中转开腹。术后住院时间为5 d(4~8 d),其中1例联合行腹腔镜胆囊切除术;1例术后3 d并发胃吻合口漏,予以禁食、胃肠减压、抑酸、营养支持等保守治疗后痊愈;4例术后出现反酸、烧心症状,口服抑酸药后明显好转,其中1例1年后仍需服药治疗;3例出现脱发,口服药物治疗(硫酸亚铁剂、复合维生素、葡萄糖酸锌口服液等)明显改善,长出新发;2例术后3个月出现月经失调,6个月后自愈,减重手术后并发症少,手术较为安全、可靠。本研究LSG术后12个月高血压的缓解率为74.14%,与Flores等[13]的结果一致(LSG,为71%);显著高于Schiavon等[6]的缓解率(胃旁路手术,为51%),可能因Schiavon等筛选的高血压患者均服用降压药且药物种类至少为2种,而本研究纳入的患者包括未服用或仅服用1种降压药的患者。而Øvrebø等[14]未对术前服药数进行限制,结果显示胃旁路术后高血压的缓解率为78.6%。Neff等[15]的研究表明,胃旁路手术与LSG在高血压缓解方面的区别随着时间的推移而消失。因此,高血压缓解率可能与术式的关系并不显著。
本研究结果显示,术前服药数量更少、术前无吸烟史是术后血压缓解的保护性因素。戒烟虽然不能降低血压[3],但能改善血管内皮功能、降低血浆炎性介质[16],避免自主神经对血压的不利影响[17],对血压缓解具有改善作用。同时,倡导肥胖患者戒烟也能有效降低心血管疾病的发病风险。目前心血管风险评估工具有多种,最著名的如Framingham风险评分模型,而这类评分模型是基于白种人与黑种人数据,不适于亚洲人群[18]。本研究采用中国心血管病风险评估和管理指南发布的用于预测10年心血管疾病发病风险的China-PAR风险评估模型[8],该模型对中国人群有更好的预测效能与价值,根据该工作组与国家心血管病中心联合发布的“心血管风险评估”手机软件,输入患者性别、年龄、血压水平、总胆固醇等健康资料,软件自动算出该患者的10年心血管发病风险与等级,使用简便。本研究结果表明,接受LSG术后1年,患者10年心血管发病风险与等级明显降低,与国外研究减重代谢手术后患者的死亡率、10年心血管风险、心肌梗死的发生率明显降低[19]相一致。
目前常用的降压药物中,钙通道阻滞剂、血管紧张素转化酶抑制剂、血管紧张素受体拮抗剂、β受体阻滞剂对血压控制、改善胰岛素抵抗、减弱交感神经活性及压力反射控制有明显作用[20]。然而本研究发现,β受体阻滞剂可能影响患者术后血压的缓解,与Salman等[21]的研究结果相符,但是否应避免作为肥胖患者降压的首选用药还需要大量临床研究验证。本研究同时发现,术后1周内收缩压与舒张压明显下降,分别为(21.069±1.158)mmHg、(12.431±1.231)mmHg,而体重下降并不明显,仅为(3.278±0.345)kg,且术后12个月%EWL、%TWL与术后血压缓解无显著相关性,这表明高血压的缓解发生于体重明显减轻前,这与Schiavon等[6]的研究相符。
与传统手术相比,腔镜手术治疗肥胖症具有创伤小、康复快、个体化的优势,尤其肥胖症合并2型糖尿病的人群,可达到糖尿病的缓解甚至治愈,国内学者已对LSG的疗效予以肯定,可作为治疗肥胖症的独立术式[7],随着科技的发展,腹腔镜技术也愈来愈成熟,使得减重手术的开展突飞猛进,接受度逐年增长,目前已有团队采用腹腔镜手术机器人系统,同时出台《机器人辅助袖状胃切除术操作指南(2020年版)》[22],这意味着我国减重代谢外科进入智能化发展时期。近年研究发现减重手术对睡眠呼吸暂停综合征、高血压、高尿酸等合并症也有显著的治疗效果[23],但并未达成共识,这是由于我国腔镜减重手术开展较晚、术后随访病例数少,且多数研究集中于2型糖尿病缓解的缘故[24]。笔者相信,未来腔镜减重手术的大规模开展,针对肥胖症的其他合并症的研究将深入开展,肥胖症对高血压等合并症的治疗研究也会更加深入。
综上,LSG治疗肥胖症合并高血压可在短期内有效缓解血压,显著降低患者心血管10年发病风险与等级,短期并发症较少,同时减轻医保及患者负担,有望成为治疗病态肥胖合并高血压的新方法。由于本研究为单中心、样本量较小的回顾性研究,患者随访周期相对较短(12个月),且我们的血压情况多来源于患者的汇报,可能存在偏倚,同时未能知晓患者1年后高血压是否存在复发及对长期心血管疾病发病率、死亡率的影响。研究结果尚需多中心、大样本量、长期观察的前瞻性研究进一步验证。
