角膜基质透镜联合生物工程角膜移植治疗感染性角膜溃疡伴穿孔的临床观察
2023-06-01戴鹏飞王玉倩李晶曹爽章丽马珂珂李云鹏高伟
戴鹏飞 王玉倩 李晶 曹爽 章丽 马珂珂 李云鹏 高伟
感染性角膜溃疡若得不到及时控制,将导致角膜穿孔,可产生前房消失、眼内容物脱出等多种严重并发症,极易发生眼内感染,导致全眼球萎缩而失明[1-2]。对于感染性角膜溃疡伴穿孔的患者,最适宜的治疗方式是行穿透性角膜移植术(Penetrating keratoplasty,PK),既可控制感染又保留可用视力,但我国严重缺乏新鲜角膜材料及PK术后存在发生植片内皮排斥风险高的问题[3-4],限制了此种手术的应用。
飞秒激光小切口角膜基质透镜取出术(SMILE)是目前角膜屈光手术的最新术式,术中取出的角膜基质透镜来源便捷丰富,可用于角膜移植术[5]。生物工程角膜自2015年上市应用于临床后[6],被证实具有较好的人角膜结构替代功能,对未累及全层的感染性角膜疾病起到较好的结构和功能重建作用,可缓解角膜供体来源不足的问题[7]。我们将角膜基质透镜用做修补角膜穿孔的垫片并联合使用生物工程角膜行板层角膜移植(Lamellar keratoplasty,LK)对感染性角膜溃疡伴穿孔的患者进行治疗,取得了满意的效果,现报告如下。
1 对象与方法
1.1 对象
纳入标准:①非瞳孔区感染性角膜溃疡;②角膜溃疡灶局部穿孔;③穿孔直径2~4 mm。排除标准:①患有眼内炎;②患有重度干眼;③睑裂闭合不全者;④全身其他手术禁忌。
回顾性系列病例研究。选取2021 年1—12 月于西安市人民医院眼科所有接受角膜基质透镜联合生物工程角膜移植术治疗感染性角膜溃疡伴穿孔的患者24例(24眼),其中男16例,女8例,年龄39~65(48.1±3.4)岁。结合典型症状、共聚焦显微镜及角膜刮片、培养等微生物学检查,入院诊断包括细菌性角膜溃疡伴穿孔10 眼,病毒性角膜溃疡伴穿孔9眼,真菌性角膜溃疡伴穿孔5眼。角膜溃疡灶均位于非瞳孔区,穿孔直径2~4(3.13±0.92)mm。
本研究过程遵循赫尔辛基宣言,研究中所有患者已被详细告知术中使用的角膜材料来源,均签署手术知情同意书及特殊耗材使用同意书,并已通过西安市人民医院(西安市第四医院)伦理委员会审批(批号:20210004)。
1.2 术前治疗
细菌性角膜溃疡的患者使用敏感抗生素静滴,局部滴用0.5%左氧氟沙星滴眼液抗细菌治疗;真菌性角膜溃疡的患者全身使用注射用伏立康唑静滴,局部滴用5%氟康唑滴眼液或自配的伏立康唑滴眼液(10 g/L)抗真菌治疗;病毒性角膜溃疡的患者予以阿昔洛韦注射液静滴,局部滴用更昔洛韦眼用凝胶抗病毒治疗。术前进行全身和局部用药治疗以控制感染,并随时做好术前准备,待感染控制(包括角膜水肿、浸润减轻,溃疡灶缩小、边缘逐渐清晰时)或感染无法控制穿孔有增大的趋势时均是立即手术的指征。术前30 min使用20%甘露醇注射液250 ml快速静滴。
1.3 角膜基质透镜的制备
角膜基质透镜取自在本院接受S M I L E(VisuMax飞秒激光仪,德国Carl Zeiss公司)手术的近视患者,所有患者均符合角膜捐献者条件并知情同意。SMILE术中取出角膜基质透镜,选取直径为6.0~6.5 mm、厚度 100~120 μm的基质透镜,立即放置于移植供体保存液中,保存在4℃冰箱中待用。本研究中使用角膜基质透镜术前保存时间均不大于2周。
1.4 手术方法及过程
根据溃疡灶范围,用大于角膜溃疡边界0.5 mm的环钻钻切角膜,板层刀剖切、完整清除感染灶区基质至透明的近后弹力层处,制作植床,操作轻柔,避免扩大穿孔范围,清除嵌顿虹膜表面的渗出膜;取生物工程角膜(艾欣瞳,L3型,厚度400 μm),复水15 s,使用与植床等大的环钻钻取生物工程角膜植片备用;取角膜基质透镜修剪为与植床等大后备用;将角膜基质透镜作为垫片,平置于植床底部,覆盖穿孔区,再将制备好的生物工程角膜植片覆盖于基质透镜之上,采用10-0尼龙线将生物工程角膜植片与植床作间断缝合,使植片、垫片与植床贴合紧密;缝合完毕后将线结旋转入角膜植床侧的层间以减少手术后的刺激症状;虹膜嵌顿于穿孔处者,行角膜缘切口,黏弹剂辅助下还纳嵌顿的虹膜,前房成形;涂抗生素眼膏,加压包扎术眼,手术结束。所有手术均由同一位经验丰富的医师完成。
1.5 术后处理
所有术后患者在院观察1周,出院后随访6~18(13.2±2.2)个月,观察视力、眼压、角膜散光度数、角膜植片厚度、感染复发情况、并发症及植片排斥反应等。
1.5.1 细菌性角膜溃疡术后 该类患者加压包扎术眼2 d,每日换药,妥布霉素眼膏1次/d、小牛血清去蛋白眼用凝胶1次/d,继续使用敏感抗生素静滴3 d(无感染复发停用),开放点眼,配戴角膜绷带镜,局部滴用0.5%左氧氟沙星滴眼液4次/d、普拉洛芬滴眼液4次/d、0.1%氟米龙滴眼液3次/d、小牛血清去蛋白眼用凝胶3次/d、妥布霉素地塞米松眼膏1次/晚(睡前),植片上皮化后加用他克莫司滴眼液2次/d。
1.5.2 真菌性角膜溃疡术后 该类患者加压包扎术眼2 d,每日换药,妥布霉素眼膏1次/d、小牛血清去蛋白眼用凝胶1次/d,继续全身使用注射用伏立康唑静滴(围手术期总量不超过2周),术后3 d观察,如无感染复发迹象停用伏立康唑静滴,开放点眼,配戴角膜绷带镜,局部滴用5%氟康唑滴眼液或自配的伏立康唑滴眼液(10 g/L)4次/d、0.5%左氧氟沙星滴眼液4次/d、普拉洛芬滴眼液4次/d、小牛血清去蛋白眼用凝胶3次/d、妥布霉素眼膏1次/晚(睡前),植片上皮化后加用他克莫司滴眼液2次/d。
1.5.3 病毒性角膜溃疡术后 该类患者继续予以阿昔洛韦注射液静滴5 d后停用,加压包扎术眼2 d,每日换药,妥布霉素眼膏1 次/d、小牛血清去蛋白眼用凝胶1次/d,术后3 d如无感染复发开放点眼,配戴角膜绷带镜,局部滴用更昔洛韦眼用凝胶4次/d、0.5%左氧氟沙星滴眼液4次/d、普拉洛芬滴眼液4次/d、0.1%氟米龙滴眼液3次/d、小牛血清去蛋白眼用凝胶3次/d、妥布霉素地塞米松眼膏1次/晚(睡前),植片上皮化后加用他克莫司滴眼液2次/d。
2 结果
2.1 视力情况
术后患者最佳矫正视力(BCVA)均有不同程度的提高。BCVA(国际标准视力表):术前为光感~0.12,其中小于0.1者18眼,0.1~0.25者6眼;末次随诊时为0.02~0.8,其中小于0.1 者5 眼,0.1~0.25者9眼,0.3~0.5者7眼,大于0.5者3眼。
2.2 眼压、屈光情况及角膜植片厚度
术前眼压:T-2(指测)~11 mmHg(1 mmHg=0.133 kPa)。2例患者术后1 d眼压高(分别为28、31 mmHg),给予降眼压药物,3 d后恢复正常,停用后未反复,考虑术中少量黏弹剂残留致一过性高眼压;其余患者术后眼压正常;所有患者末次随诊时眼压均正常。末次随诊时角膜散光度为1.1~3.5(1.76±0.81)D。末次随诊时应用前节光学相干断层扫描(OCT)测量植片厚度为485~561(518±33)μm。
2.3 角膜情况、并发症及植片排斥反应
24例患者手术均顺利完成,2例术中还纳嵌顿虹膜时致前房出血,保留少量黏弹剂,分别于术后3、5 d前房积血完全吸收。所有患者于术后3~7 d均完成植片上皮化,生物工程植片水肿逐渐减轻。在院期间1 例患者(术后2 d)出现轻度双前房,加压包扎3 d后消失,余患者植片、基质透镜垫片与植床均贴附紧密,缝线无松动。
至末次随诊,未见有原发感染复发者。2 例原发病灶位于近角膜缘处的患者分别于术后2、5 个月时出现了植片局部边缘水肿及新生血管长入,予以及时拆除局部缝线及加强使用糖皮质激素联合他克莫司点眼后植片逐渐瘢痕化;1 例在术后6 个月时因特殊原因停用所有滴眼液后,发生严重排斥反应,表现为植片上皮缺损、植片高度水肿、局部溶解,予以局部及全身应用激素联合他克莫司滴眼治疗1周,排斥反应无法控制,故行结膜瓣覆盖术;其余患者植片、基质透镜垫片与植床均贴附紧密,愈合良好,厚度正常。1 例典型患者治疗前后情况检查见图1—2。
3 讨论
感染性角膜病是我国和其他发展中国家的主要致盲眼病之一,占角膜盲的首位[8]。因病毒、细菌、真菌、棘阿米巴等病原微生物侵入角膜致病,病变组织发生坏死、脱落,形成角膜溃疡,如治疗无法控制病情进展,则可发生溃疡处角膜基质完全坏死、脱落,进而形成角膜穿孔,此时眼内外直接交通,眼球又处于低眼压状态,极易导致眼内感染,最终可致眼球萎缩[8]。故感染性角膜溃疡伴穿孔,对手术医师来说相当棘手,急需尽快手术修补,以尽可能挽救视功能。
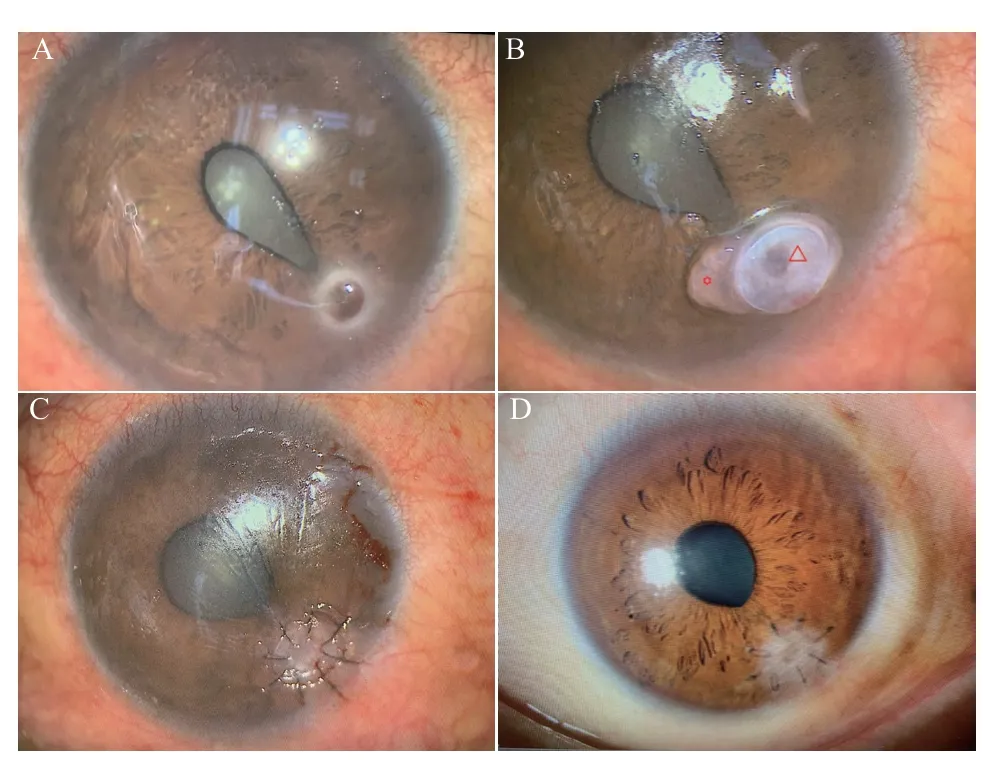
图1.1例细菌性角膜溃疡伴穿孔患者接受角膜基质透镜联合生物工程角膜移植治疗前后情况A:术前裂隙灯显微镜照片见角膜穿孔处虹膜嵌顿,周围感染已控制,瞳孔呈梨形;B:术中制备完毕的基质透镜植片(*)、生物工程角膜植片(△);C:术后1 d时裂隙灯显微镜照片见角膜植片透明,对合良好,未见层间积液;D:术后3 个月时裂隙灯显微镜照片示角膜植片与植床贴合紧密,厚度如常,患者视力为0.8Figure 1.A case of bacterial corneal ulcer with perforation before and after treatment with corneal stroma lens and bioengineered corneal transplantationA: Pre-operative slit lamp photography showed iris incarceration at the corneal perforation,controlled infection,and pear shaped pupils.B: Prepare intraoperative matrix lens grafts (*) and bioengineered corneal grafts (△).C:On the first day after surgery,slit lamp photography showed that the corneal graft was transparent,well aligned,and no interlayer effusion was observed.D: At 3 months after surgery,slit lamp photography showed that the corneal graft was tightly attached to the implant bed,with a normal thickness,and the patient's visual acuity was 0.8.

图2.1例细菌性角膜溃疡伴穿孔患者接受角膜基质透镜联合生物工程角膜移植后眼前节光学相干断层扫描结果生物工程角膜植片(△)、角膜基质透镜植片(*)与植床贴合紧密,穿孔封闭,植片植床交界处吻合良好,厚度如常Figure 2.Results of OCT of anterior segment in a case of bacterial corneal ulcer with perforation after treatment with corneal stroma lens and bioengineered corneal transplantation after operationBioengineered corneal grafts (△) and corneal stroma lens grafts (*) were closely fitted with the implantation bed,with perforation closed,and the junction of the grafts and the bed were well matched,with the thickness as normal.
以往的手术方式包括:①穿透性角膜移植术:是修复穿孔、控制感染、改善视力的最有效方式[9],但我国新鲜角膜材料的匮乏,限制了此术式的应用。②改良的板层角膜移植术:使用保存的角膜板层材料联合自体角膜瓣翻转移植[10]或联合自体角膜层间垫片移植[11],此类术式的共同特点为双板层移植,即使用内层材料作为垫片封闭穿孔,再使用表层保存材料填补植床完成移植,其优点是较PK有更低的术后免疫排斥反应,较单纯LK更少发生双前房、植片不成活等并发症,缺点是术中垫片的制作困难需较高的手术技巧,及在国内除少数眼库外,保存角膜材料的获取同样困难。③异体角膜基质透镜移植术:使用SMILE术中取出的多片角膜基质透镜黏合后作为板层材料用于LK[12],其优点是来源便捷丰富,可修补较大穿孔,缺点是黏合后的多层基质透镜透明度下降,术后形成较重的瘢痕愈合影响视力改善,其治疗意义在于紧急修补穿孔,维持眼球的结构,为进一步的光学性角膜移植手术创造条件[13]。④结膜瓣和羊膜[14]覆盖术:由于材料张力差,只能起到临时封闭较小穿孔的作用,而且容易延误病情,甚至加重感染,失去保存视功能的手术时机。
本研究利用角膜基质透镜联合生物工程角膜移植治疗感染性角膜溃疡伴穿孔,尚未见类似报道。手术的基本原理为使用较薄的异体角膜基质透镜作为植床垫层覆盖角膜穿孔区,进而在生物工程角膜的紧密压迫下能够完全封闭角膜穿孔,故能有效的阻止角膜层间积液的发生,提高生物工程角膜植片的存活率。值得注意的是,在本研究中有较大(4 mm)的穿孔,角膜内皮细胞丢失较多,但术后植片仍能存活。我们考虑原因如下:一方面,角膜基质透镜取自健康角膜的前部基质层,且保存在移植供体保存液中,能够较好的保留基质细胞的数量、活性及胶原纤维致密排列状态[15],从而能够达到紧密封闭穿孔的作用;另一方面,穿孔封闭后形成较规则的平面,有利于周围正常内皮细胞的扩大和移行,其代偿的脱水作用大于房水透入基质的速度,进而可以保持植片的脱水状态。从研究结果上看,术后患者的BCVA均不同程度提高,也证明了这一点。
从安全性上看,术后除2例一过性高眼压发生外,未见继发性青光眼。2 例出现了植片局部边缘水肿及新生血管长入,1例停药后发生严重排斥反应致手术失败。这里值得注意的是,虽然生物工程角膜均已脱细胞,只留下胶原蛋白,而所选患者均为感染性角膜溃疡,角膜缘血管充血、增生,同时滴用大量治疗原发病的眼药水抗病毒、抗细菌及抗真菌,故同样存在角膜基质排斥反应的风险[16]。应加强对患者的宣教,提高随访率,如果出现角膜缝线松动,应及时拆线[17],并积极抗排斥治疗,以提高角膜植片的存活率。
虽然本研究尚缺乏大样本的长期随访结果,但以目前的随访结果看,此术式能够有效地治疗感染性角膜溃疡伴穿孔,较其他手术方式优势如下:①材料获取简便、充足:基质透镜供体来自本院全飞秒激光近视矫正术中所取[18],生物工程角膜已商品化,供应充足;②手术操作简单:同常规LK手术,基质透镜垫层无需缝合,避免了扩大穿孔及医源性穿孔的发生;③扩大了生物工程角膜的适应症:以往生物工程角膜无法修补角膜穿孔,现使用基质透镜垫片封闭穿孔后形成板层植床,再行生物工程角膜移植;④较双层基质透镜移植术,术后植片厚度优势明显,同常规LK、散光较小,视力恢复较好。
综上所述,角膜基质透镜联合生物工程角膜移植是治疗非瞳孔区角膜溃疡伴小穿孔的有效、安全的方法。
利益冲突申明本研究无任何利益冲突
作者贡献声明戴鹏飞:收集数据;资料的分析和解释;撰写论文;根据编辑部的修改意见进行修改。王玉倩、李晶、曹爽、章丽:采集资料及分析数据;马珂珂、李云鹏:参与数据分析。高伟:参与选题、设计和修改论文的结果、结论;对文章的知识性内容作批评性审阅、指导
