分光光度法快速测定酱油中半胱氨酸
2023-05-30刘毅袁莉储文袁嘉怡马卫兴
刘毅 袁莉 储文 袁嘉怡 马卫兴

摘要:基于半胱氨酸与阳离子染料碱性品红发生加成反应,首次提出碱性品红加成反应褪色分光光度法测定半胱氨酸含量的新方法。在硼砂-氢氧化钠缓冲溶液中,半胱氨酸与碱性品红发生加成反应形成无色的硫醚衍生物,溶液褪色,吸光度减小,加成产物最大吸收波长在 542 nm处,据此建立了分析方法。半胱氨酸的浓度C与吸光度差值ΔA呈现良好的线性关系,线性范围为1.00~10.00 mg/L,相关系数r=0.999 3,表观摩尔吸光系数为1.525×104 L/(mol·cm)。方法成功应用于市售酱油样品中半胱氨酸含量的测定,酱油样品加标回收试验平均回收率为97.1%和98.3%,相对标准偏差为 0.85%、1.23%,不同酱油样品测定值的相对标准偏差(n=6)均小于3%。建立的方法操作简单,专属性强,检测成本低,结果准确可靠,可用于酱油中半胱氨酸的快速测定。
关键词:半胱氨酸;碱性品红;酱油;加成反应;褪色分光光度法
中图分类号:TS264.21 文献标志码:A 文章编号:1000-9973(2023)04-0166-04
Abstract: Based on the addition reaction of cysteine with the cationic dye basic fuchsin, a new method for the determination of cysteine content by fading spectrophotometry of basic fuchsin addition reaction is proposed for the first time. In borax-sodium hydroxide buffer solution, the addition reaction between cysteine and basic fuchsin forms a colorless thioether derivative, the solution fades, the absorbance decreases, and the maximum absorption wavelength of the addition product is at 542 nm. Based on this, the analytical method is established. The concentration C of cysteine shows a good linear relationship with the absorbance difference ΔA, with a linear range of 1.00~10.00 mg/L, the correlation coefficient r=0.999 3 and the apparent molar absorbance coefficient of 1.525×104 L/(mol·cm). The method is successfully applied to the determination of cysteine in commercially available soy sauce samples. The average recovery rates of the spiked recovery tests of soy sauce samples are 97.1% and 98.3% with the relative standard deviations of 0.85% and 1.23%, and the relative standard deviations (n=6) of the determined values of different soy sauce samples are all less than 3%. The established method is simple to operate, has strong specificity, low cost, accurate and reliable results, and can be used for the rapid determination of cysteine in soy sauce.
Key words: cysteine; basic fuchsin; soy sauce; addition reaction; fading spectrophotometry
醬油是一种由小麦、大豆经生物发酵制成的传统调味品,在增加菜肴的色泽和鲜味的同时,酱油具有改善人体胃液分泌和促进消化的能力[1-2]。随着人们生活水平的提升,消费者对酱油的质量也愈加关注。氨基酸作为酱油的重要营养成分,种类高达26种[3],半胱氨酸就是其中之一。L-半胱氨酸(L-cysteine,cys)是一种天然存在于果蔬、牛奶、肉制品中的氨基酸,具有抗氧化作用,同时能够清除人体人体内金属离子和有毒物质[4],在食品、制药行业备受关注,具有很大的应用潜力。半胱氨酸缺乏会导致头发脱色、嗜睡、肝损伤、皮肤损伤、肌肉和脂肪减少等症状[5-6],而半胱氨酸过高可能会引起老年痴呆、心血管疾病等[7]。因此,建立一种快速高效的分析方法测定半胱氨酸具有重要意义。
目前测定半胱氨酸含量的方法有高效液相色谱法[8-9]、荧光法[10-11]和电化学法[12-13]等,大多需要昂贵的高精密仪器或者操作繁琐、样品处理复杂。单独测定酱油中半胱氨酸的方法未见报道。紫外可见分光光度法由于操作简单、成本低廉已广泛应用于物质的定量分析。本研究发现在硼砂-氢氧化钠缓冲溶液中,半胱氨酸的巯基可与阳离子染料碱性品红(basic fuchsin)发生加成反应,生成无色的硫醚衍生物,溶液褪色,吸光度减小。通过对溶液酸度、试剂用量、反应时间等影响因素进行优化,建立了能够快速测定半胱氨酸含量的方法,并确定了酱油中半胱氨酸的定量分析方法,结果令人满意。
1 材料与方法
1.1 主要仪器与试剂
752N型紫外可见分光光度计 上海仪电分析仪器有限公司;BS210S分析天平 北京赛多利斯天平有限公司;PHS-3C精密酸度计 上海虹益仪器仪表有限公司。
L-半胱氨酸对照品、氢氧化钠、硼砂:国药集团化学试剂有限公司,批号:20190606,纯度≥98.5%;碱性品红:阿拉丁试剂(上海)有限公司;实验用水:超纯水;酱油:市售欣和酱油、李锦记酱油、海天酱油。
1.2 试剂配制
半胱氨酸标准溶液(100.0 mg/L):称取0.100 0 g半胱氨酸于100 mL棕色容量瓶中,加水溶解后定容至刻度,摇匀,得到1.000 g/L半胱氨酸储备液,放入冰箱中储存。临用时吸取储备液 10.0 mL置于100 mL棕色容量瓶中,定容至刻度,摇匀,得到100.0 mg/L的半胱氨酸标准溶液。
碱性品红溶液(5.00×10-4 mol/L):称取碱性品紅0.169 2 g于100 mL烧杯中,加水溶解后转移至1 000 mL容量瓶中,加水至刻度,摇匀。
硼砂-氢氧化钠缓冲液:pH9.3~10.1,由0.05 mol/L硼砂溶液和0.20 mol/L氢氧化钠溶液按一定比例混合配制,然后用酸度计调节pH。
1.3 实验方法
在室温下,取2支同一型号的10 mL比色管,其中一支加入一定量的半胱氨酸标准溶液或样品溶液,另一支不加半胱氨酸做空白试验。然后于2支比色管中分别加入浓度为5.00×10-4 mol/L的碱性品红溶液1.25 mL、pH 9.8的硼砂-氢氧化钠缓冲溶液2.00 mL,加水至刻度,摇匀。立刻置于分光光度计中,以水作参比,用1 cm比色皿于波长542 nm处测量吸光度(其中含半胱氨酸的为A,空白的为A0),并计算出吸光度差值ΔA=A0-A。
2 结果讨论
2.1 吸收光谱
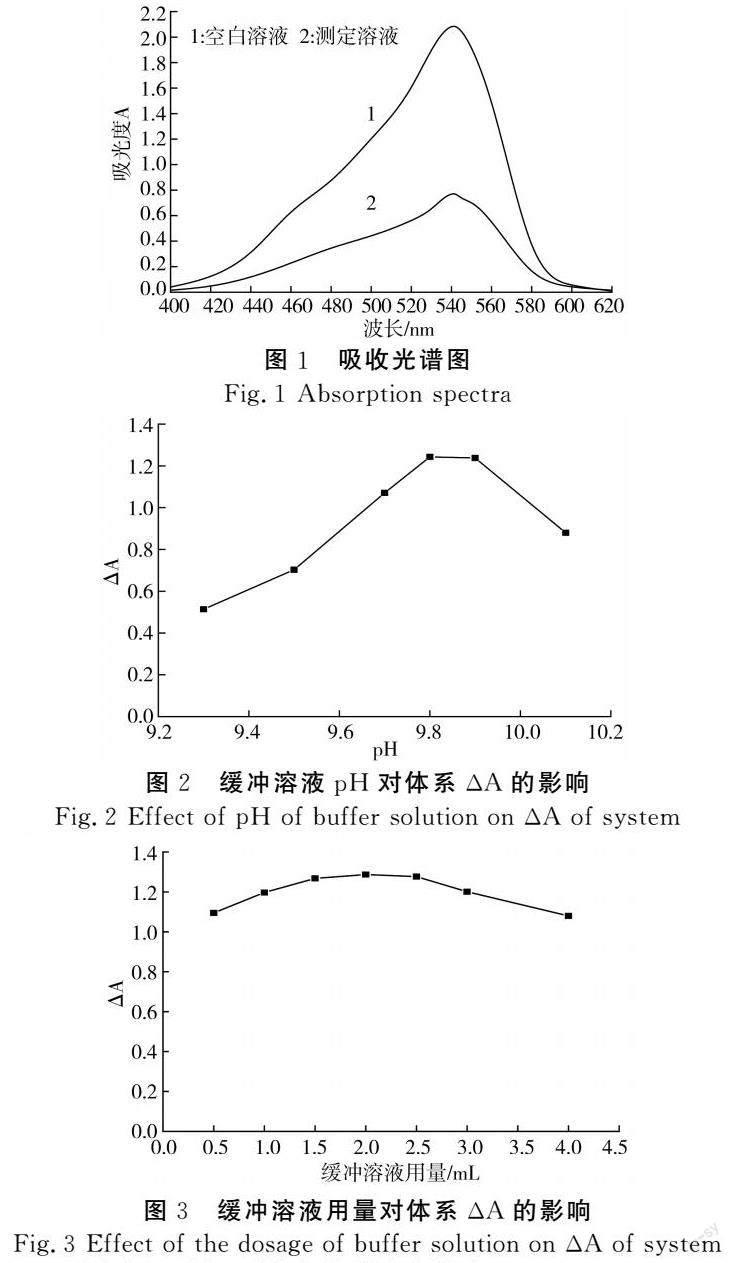
按照1.3的实验方法,在波长400~620 nm范围内用分光光度计测定半胱氨酸与碱性品红反应前后的吸光度,绘制吸收光谱,结果见图1。
由图1可知,曲线1为空白溶液的吸收光谱,在硼砂-氢氧化钠缓冲溶液中,碱性品红的最大吸收峰位于542 nm。曲线2为测定液的吸收光谱,加入半胱氨酸后,半胱氨酸与碱性品红发生加成反应,溶液的红色变浅,吸光度减小,故本体系为褪色反应。且反应后溶液的最大吸收波长也位于542 nm,故选择542 nm为测定波长。
2.2 酸度的影响
取半胱氨酸标准溶液1.00 mL、碱性品红溶液1.00 mL,控制不同pH(pH 9.3~10.1)的硼砂-氢氧化钠缓冲溶液加入量为1.00 mL,考察缓冲溶液pH值对体系褪色程度(ΔA)的影响,结果见图 2。
由图2可知,pH为9.8~9.9时,ΔA达到最大值且较为平稳,增加或减小pH,ΔA均有所减小,故选择缓冲溶液最佳pH为9.8。改变pH 9.8缓冲溶液的用量,观察ΔA的变化,结果见图3。
由图3可知,缓冲溶液用量为1.50~2.50 mL时,ΔA达到最大值且相对平稳,选择2.00 mL为最佳用量。因此,选择pH 9.8的硼砂-氢氧化钠缓冲溶液2.00 mL进行试验。
2.3 碱性品红用量的选择
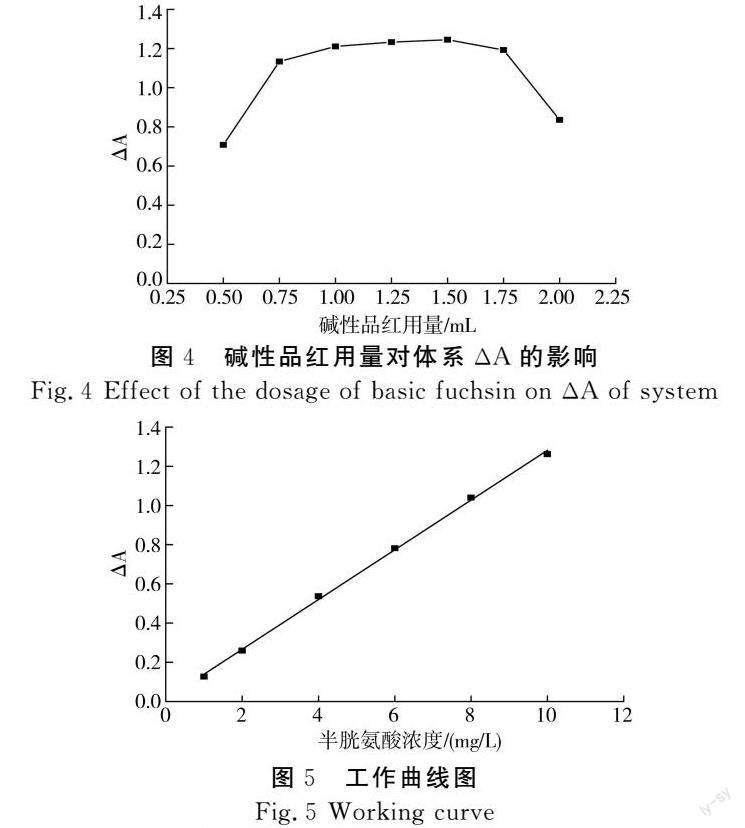
取半胱氨酸标准溶液1.00 mL、pH 9.8的硼砂-氢氧化钠缓冲溶液2.00 mL,加入不同体积(0.50~2.00 mL)浓度为5.00×10-4 mol/L的碱性品红溶液,按实验方法测定吸光度,考察碱性品红用量对ΔA的影响。
由图4可知,碱性品红用量为0.75~1.75 mL时,ΔA达到最大值且较为平稳,故选择5.00×10-4 mol/L的碱性品红溶液最佳用量为1.25 mL。
2.4 反应时间的影响
选择以上最佳条件,按照“1.3”项下实验方法每隔5 min测定一次吸光度值,考察反应时间对ΔA的影响。结果表明,在室温下,半胱氨酸能够快速与碱性品红发生加成反应,溶液褪色。且随着时间的增加,A、A0均减小,ΔA也减小。故本实验选择即配即测法,配完溶液立刻用分光光度计进行测定。
2.5 标准曲线
在上述选定的最佳条件下,在测定液中加入浓度为100.00 mg/L不同体积(0.10,0.20,0.40,0.60,0.80,1.00 mL)的半胱氨酸标准溶液,按照实验方法,于最大吸收波长542 nm处测定吸光度,同时测定空白溶液的吸光度,并计算出吸光度差值ΔA,绘制工作曲线(见图5)。半胱氨酸的浓度C与吸光度差值ΔA呈现良好的线性关系,线性范围在1.00~10.00 mg/L,线性回归方程为ΔA=0.126C+0.012,相关系数r为0.999 3,摩尔吸光系数为1.525×104 L/(mol·cm),可见本方法有较宽的线性范围。
2.6 干扰实验
考察了酱油中存在的其他氨基酸是否会干扰测定结果。对于80.00 μg/10 mL的半胱氨酸,相对误差不超过±5%,使以下倍数的其他氨基酸不造成干扰:谷氨酸、丙氨酸(200倍);甘氨酸、异亮氨酸、亮氨酸、天冬氨酸(150倍);缬氨酸、丝氨酸、赖氨酸(100倍);苏氨酸、脯氨酸、苯丙氨酸(50倍),可见本方法具有良好的选择性。
2.7 精密度实验
按照“1.3”项下实验方法,于542 nm处测定吸光度,平行测定10次,所得数据及分析处理结果见表1。回收率在97.3%~102%之间,平均回收率为99.7%,相对标准偏差RSD为1.95%,可见本方法的精密度较高。
2.8 样品分析
2.8.1 酱油样品加标回收实验
取5.00 mL 酱油于50 mL棕色容量瓶中,用超纯水定容,摇匀,得到酱油样品溶液。于10 mL比色管中加入1.00 mL酱油样品溶液,按“1.3”项下实验方法测定吸光度,平行测定6次。
取5.00 mL酱油样品于50 mL棕色容量瓶中,再加入适量浓度为100.0 mg/L的半胱氨酸标准溶液,用水定容,即得加标后的酱油样品溶液。按“1.3”项下实验方法移取1.00 mL测定吸光度,平行测定6次。
由回归方程计算出酱油样品中半胱氨酸的含量以及加标回收实验的测定值。结果表明,酱油样品中半胱氨酸的含量为0.260 mg/mL,不同加标水平的平均加标回收率分别为97.1%、98.3%,相对标准偏差RSD分别为0.85%、1.23%,符合国家标准 GB/T 27417-2017《合格评定 化学分析方法确认和验证指南》的规定。
2.8.2 不同酱油样品中半胱氨酸含量的测定
选取了市售3种不同品牌和级别的酱油,分别为欣和酱油(特级,氨基酸态氮≥1.00 g/dL)、李锦记金标生抽(一级,氨基酸态氮≥0.700 g/dL)、海天酱油(三级,氨基酸态氮≥0.400 g/dL)。分别取5.00 mL以上3种酱油于50 mL棕色容量瓶中,用超纯水定容,摇匀,得到酱油样品溶液A(欣和)、B(李锦记)、C(海天)。取3支10 mL比色管,编号为1#、2#、3#,分别加入1.00 mL酱油样品溶液A、B、C,按“1.3”项下实验方法测定吸光度,各平行测定6次。通过回归方程计算的测定结果见表3。欣和特级酱油、李锦记一级酱油和海天三级酱油中半胱氨酸的含量分别为0.377,0.261,0.153 mg/mL,且相对标准偏差均在3%以内,符合定量分析的要求。
3 反应机理
已有文献对亚硫酸根离子使碱性品红溶液褪色的机理做了讨论[14-16]。张文德[17]利用亚硫酸盐与碱性品红的加成反应,建立了分光光度法测定食品中游离型亚硫酸盐及总亚硫酸盐的含量。碱性品红的分子结构是一个三苯甲烷型的共轭体系,碱性品红因生色基团——共轭的“醌式”结构而显现颜色,亚硫酸根离子中的硫原子具有一对孤对电子,能够与碱性品红中心碳原子(C14)发生加成反应,破坏共轭结构,颜色消失。按照类比思维,半胱氨酸分子上的巯基硫原子具有两对孤对电子,同样能够与碱性品红发生加成反应,生成无色硫醚衍生物:3-{[二(4-氨基苯基)-(3-甲基-4-氨基)苯甲基)]硫醚基}-2-氨基丙酸根,生色基团的共轭结构被破坏,溶液褪色(反应机理见图6)。随着半胱氨酸浓度的增加,溶液的颜色越来越浅,测得的吸光度也逐渐减小,且半胱氨酸的浓度与褪色程度呈线性关系,通过实验优化了最佳反应条件后建立标准曲线,用对照品标准曲线法测定样品中半胱氨酸的含量。
4 结论
本研究对基于碱性品红加成反应褪色分光光度法测定半胱氨酸含量的影响因素进行了考察和优化。通过对溶液酸度、试剂用量、反应时间等影响因素的考察,得到了反应的最佳条件:反应在pH 9.8的硼砂-氢氧化钠缓冲溶液中进行,缓冲溶液用量为2.00 mL,5.00×10-4 mol/L碱性品红溶液用量为1.25 mL,采用即配即测法,建立了能够快速测定半胱氨酸含量的方法,并确定了酱油中半胱氨酸的定量分析方法。该方法具有以下优点:该方法为一步反应,原理简单;使用的试剂种类较少,且材料廉价易得;仪器操作简单且普及率高;具有较宽的线性范围,较高的精密度和较强的专属性,可以应用于酱油中半胱氨酸含量的快速测定。
参考文献:
[1]KATAYAMA H, TATEMICHI Y, NAKAJIMA A. Simultaneous quantification of twenty Amadori products in soy sauce using liquid chromatography-tandem mass spectrometry[J].Food Chemistry,2017,228:279-286.
[2]ZHAO G Z, DING L L, YAO Y P, et al. Extracellular proteome analysis and flavor formation during soy sauce fermentation[J].Frontiers in Microbiology,2018,9:1872.
[3]宋衛得,苏征,惠希东,等.离子色谱-积分脉冲安培检测法同时测定酱油中20种氨基酸和6种糖[J].色谱,2019,37(9):996-1003.
[4]解放,刘楠.半胱氨酸代谢途径调控与肿瘤治疗新策略[J].中国药科大学学报,2021,52(5):522-528.
[5]SHAHROKHIAN S. Lead phthalocyanine as a selective carrier for preparation of a cysteine-selective electrode[J]. Analytical Chemistry,2001,73(24):5972-5978.
[6]刘红丽,胡慧,周晓东,等.半胱氨酸传感器的研究进展[J].分析科学学报,2013,29(2):271-276.
[7]肖志友,司恒丹,王建文,等.基于钌配合物作荧光探针测定半胱氨酸的新型DNA荧光传感器[J].山东化工,2019,48(15):100-102,104.
[8]AMARNATH K, AMARNATH V, AMARNATH K, et al. A specific HPLC-UV method for the determination of cysteine and related aminothiols in biological samples[J].Talanta,2003,60(6):1229-1238.
[9]KONO Y, IIZUKA H, ISOKAWA M, et al. HPLC-fluorescence determination of thiol compounds in the serum of human male and female subjects using HILIC-mode column[J].Biomedical Chromatography,2014,28(5):589-593.
[10]HUANG Z, WU C Y, LI Y Q, et al. A fluorescent probe for the specific detection of cysteine in human serum samples[J]. Analytical Methods,2019,11(26):3280-3285.
[11]韩蕊,吴琼,赵昕,等.基于荧光探针对食物中半胱氨酸的检测方法建立[J].食品工业科技,2022,43(4):305-311.
[12]GUNASEKARAN M, GOVINDHASAMY M, RANGASAMY T, et al. Facile synthesis of CeO2-SnO2 nanocomposite for electrochemical determination of L-cysteine[J].Journal of Alloys and Compounds,2019,792:1150-1161.
[13]刘陈,张慢乐,于鑫垚,等.L-半胱氨酸电化学传感器的研究与应用[J].化学传感器,2019,39(3):22-31.
[14]郑天龙,左香华.二氧化硫使品红溶液褪色的实验与理论研究[J].化学教育,2017,38(9):66-73.
[15]万如锴,曹桂能,陈红.品红褪色机理的探究[J].化学教育,2008,38(2):67-68.
[16]温培娴,丁伟.品红褪色机理的实验探究[J].化学教育(中英文),2020,41(7):96-100.
[17]张文德.利用碱性品红的加成反应动力学光度法测定痕量亚硫酸盐[J].分析化学,1995,23(12):1405-1408.
