走进合成生物学
2023-05-30刘虎虎田云
刘虎虎 田云

隨着国家“十四五”规划、“中国制造2025”以及“健康中国行动”等一系列政策和文件的出台与实施,我国生物技术产业已经进入快速发展时期。其中新出现的合成生物学一词经常出现在新闻头条上,伴随着人工合成微生物、人工合成酵母染色体、青蒿素的发酵生产以及人工合成淀粉、葡萄糖和脂肪酸的实现,合成生物学被喻为是“认识生命的钥匙”(建物致知)和“改变未来的颠覆性技术”(建物致用)[1,2]。
合成生物学的诞生与发展
19世纪初,人们普遍认为有机物是与生命现象密切相关的,是生物体内一种特殊的、神秘的“生命力”作用下产生的,只能从生物体内得到,不能人工合成,这就是当时的“生命力”学说。1828年,德国化学家维勒(F. Wohler)使用无机物氰酸铵人工合成了有机物尿素,从而给“生命力”学说以沉重打击。20世纪初,法国化学家勒杜克(S. Leduc)试图通过物理的理论来解释生命的现象。他通过溶质渗透和扩散方法模拟了人工合成细胞及其次生细胞群,揭示了无机营养与人工丝状真菌发育的关系,并用矿物质模拟了生物的趋光性、趋化性和趋电性。这些研究结果揭示,生物学仅仅是流体物理学的一个分支,物质的物理学机制可能导致生命的出现。但是,因为当时知识和观察能力的局限,这些研究只能停留于生命表型和流体物理表型相关的“合成”描述,距离真正认识和改造生命的科学研究还很远。1913年,《自然》周刊系统评述了勒杜克的相关研究,合成生物学一词首次正式在学术期刊出现。
1950—1960年代,DNA双螺旋结构和胰岛素一级结构等先后被确定,具有生物活性的核酸和蛋白质等也实现了人工合成。我国科学家在1965年和1981年分别首次人工合成了牛胰岛素和酵母丙氨酸tRNA,证实蛋白质和核糖核酸都可以人工合成,从根本上推翻了所谓的“生命力”学说。20世纪70年代,随着重组DNA技术的发展和日益成熟,“合成生物学”被再次提出。波兰遗传学家斯吉巴尔斯基(W. Szybalski)提出了合成生物学的愿景:“一直以来,人们都在做分子生物学描述性方面研究,但当我们进入合成生物学的阶段,真正的挑战才开始。我们会设计新的调控元素,并将新的核酸序列加入已存在的基因组内,甚至建构一个全新的基因组”,并认为“这将是一个拥有无限潜力的领域,几乎没有任何事能限制我们去做一个更好的控制回路。最终,将会有合成的有机生命体出现”。
1990年代后期,随着人类基因组计划的成功推进,各种“生物组学”以及生物信息学、系统生物学等交叉学科迅速发展,在世纪之交,研究者在“设计—建造—测试”的工程学理念基础之上,成功实践出利用生物元件构建成逻辑线路,如美国普林斯顿大学的伊洛维兹(M. B. Elowitz)等运用3个转录抑制系统相互抑制的关系,研制出新型基因振荡器。鉴于此,在2000年的美国化学学会年会上,斯坦福大学的库尔(E. Kool)重新定义了“合成生物学”概念,即基于系统生物学的遗传工程和工程方法的人工生物系统研究,从基因片段、DNA分子、基因调控网络与信号传导路径到细胞的人工设计与合成。这标志着合成生物学的正式出现,随后迅速获得广泛关注,被认为是继DNA双螺旋结构发现和人类基因组计划之后的“第三次生命科学技术革命”。
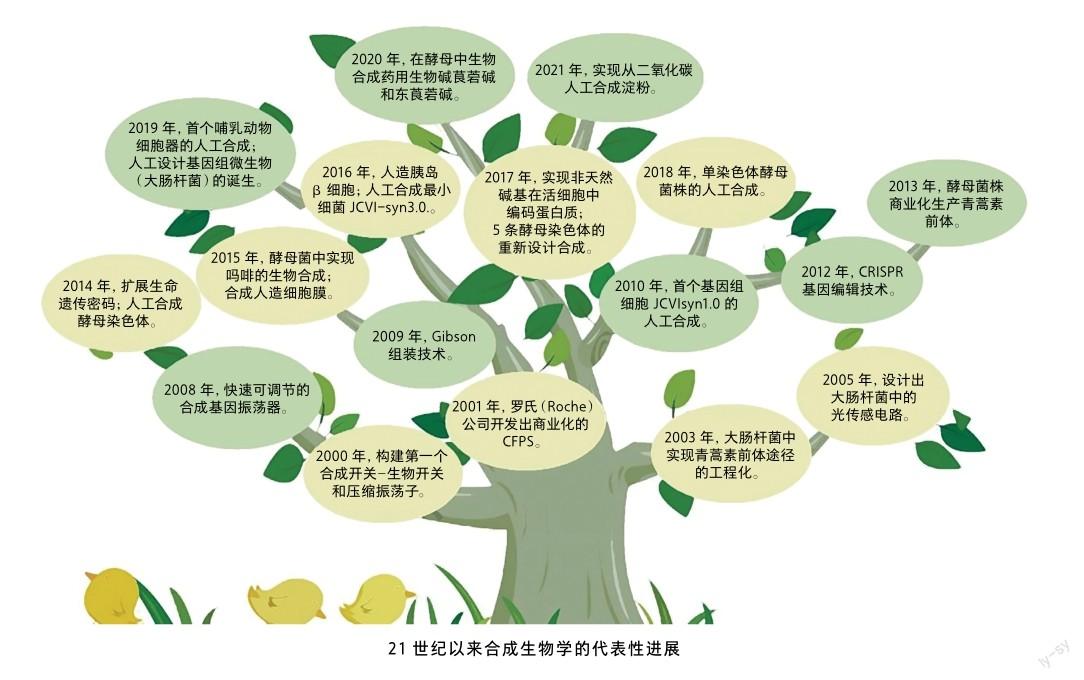
进入21世纪以来,合成生物学发展迅速,大致可以分为4个阶段:①合成生物学的创建时期(2000—2003年),这个时期产生了许多具备领域特征的研究手段和理论,特别是基因线路工程的建立及在代谢工程中的成功运用;②摸索完善时期(2004—2007年),这个时期的重要特征是虽然领域有扩大趋势,但工程技术进步比较缓慢;③快速创新和应用转化时期(2008—2013年),这个时期涌现出了大量新技术和新工程手段,特别是人工合成基因组能力的提升,以及基因组编辑技术的突破等,从而使合成生物学的研究与应用领域大为拓展;④飞速发展新时期(2014年至今),该时期研究成果全面提升,特别是酵母染色体的人工合成等领域取得突破性成果,为人类实现“能力提升”的宏伟目标奠定了重要基础。
合成生物学的应用
作为21世纪生物学领域催动原创突破和学科交叉融合的前沿代表,合成生物学不仅推动人类实现从“认识生命”到“设计生命”的伟大跨越,也将在一定程度上对生命科学研究范式进行改写,即通过设计、改造和创造生命体系来理解生命,从而探寻是否具有支配生命复杂体系的自然法则。此外,合成生物学通过基因网络工程,形成多学科交叉融合,其研究领域、研究内容和产业化应用等方面将迎来新的突破,也将为解决人类社会相关的全球性重大问题提供重要途径。
合成生物学与人工合成生命
2010年,美国文特尔(J. C. Venter)研究团队设计、合成和组装了1.08 Mb长的蕈状支原体基因组,并把它移植到已经剔除遗传信息的山羊支原体受体细胞中,创造了世界上第一个仅由人工化学合成染色体控制的、具有自我复制能力的新细胞“Synthia”;2016年,研究人员在Synthia的基础之上,不断尝试删除基因组中的不必要基因,最终把901个基因删除到只剩下473个基因,制造出最简单的人造合成细胞——Syn 3.0合成细胞[3],文特尔也因此被誉为“人造生命之父”。2019年,英国剑桥大学泰真(J. W. Chin)研究组通过将大肠杆菌4 Mb长的基因组全部替换为合成基因组,创造出只使用61种密码子的人造基因组大肠杆菌Syn61,打破了传统生命体中共有64个密码子编码蛋白质的认知,这是迄今为止完成的最大人工合成基因组[4]。
2011年,中國、美国、英国等多国研究机构联合开始实施第一个真核生物基因组合成计划——合成酵母基因组计划(Sc2.0),旨在对酿酒酵母的整个基因组进行重新设计、改造与人工合成。2014年,安娜卢儒(N. Annaluru)等报道了首条完整的合成型真核生物染色体——合成型酿酒酵母3号染色体(synⅢ)。2017年,Sc2.0团队完成了酿酒酵母synⅡ、synⅤ、synⅥ、synⅩ和synⅫ共5条合成型染色体的从头设计与合成,宣布有关合成型酵母基因组1/3的工作已经完成。其中,中国科学家领衔完成了其中的4条:天津大学元英进教授团队完成了5号、10号酿酒酵母染色体的化学合成[5,6];清华大学戴俊彪研究员团队完成了当前已合成酿酒酵母染色体中最长的12号染色体的全合成[7];深圳华大基因研究院团队联合英国爱丁堡大学团队完成了酿酒酵母2号染色体的设计与合成[8]。2018年,美国博克(J. D. Boeke)团队利用基因编辑技术将酿酒酵母的16条染色体融合在一起,构建出只含有2条染色体的“16合2”染色体新酵母菌株。与此同时,我国科学家通过15轮的染色体融合将酿酒酵母天然的16条染色体逐一融合,人工创建了只含有单条线型染色体的“16合1”染色体酵母细胞SY14 [9]。
单条染色体虽然在三维结构上有极大的改变,但是单染色体的酵母具有与野生型菌株相似的转录组和表型组,并且单染色体的酵母还保持了减数分裂的能力,说明单染色体的酿酒酵母可以具有正常的细胞功能,颠覆了染色体三维结构决定基因时空表达的传统观念,揭示了染色体三维结构与实现细胞生命功能的全新关系。
合成生物学与绿色生物制造
合成生物学通过设计和构建细胞工厂,能够使细胞以淀粉、纤维素、CO2等可再生碳为原料,生产重要的化工产品、天然药物、食品、生物能源以及生物材料等产品,具有清洁、高效、可再生等优点,开创了传统石化产品、天然药物等产品的全新生产模式。
青蒿素是一种应用非常广泛的抗疟药物,目前市售的青蒿素主要是从植物黄花蒿中进行提取,由于植物中青蒿素的含量稀少且青蒿素需求广泛,从而导致青蒿素供应不稳定。为了有效解决青蒿素的来源问题,迫切需要建立一种环境友好、廉价的青蒿素生产方法。
2004年,美国加州大学伯克利分校的基斯林(J. D. Keasling)课题组和生物技术公司Amyris合作开展半合成青蒿素项目。首先,研究人员根据植物中部分已知的青蒿素合成途径,设计青蒿素如何在微生物中进行合成。然后探讨青蒿素的合成途径在不同的微生物底盘细胞中是否适配。通过在大肠杆菌中异源表达不同来源的甲羟戊酸途径以及黄花蒿来源的紫穗槐—4,11—二烯合酶基因,成功合成了紫穗槐—4,11—二烯,产量达到27克/升,进一步将催化紫穗槐—4,11—二烯转化为青蒿酸的植物源P450氧化酶CYP71AV1组装到大肠杆菌中,最终获得了能够生产1克/升青蒿酸的重组大肠杆菌,但仍不能满足生产的需求。
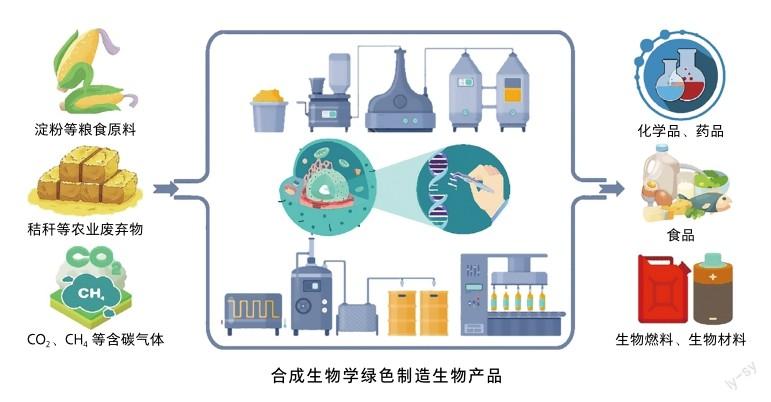
因此,项目组尝试改用酿酒酵母来生产青蒿酸。首先,通过对酵母MVA途径中代谢调控关系的调整、关键酶基因表达量优化、前体物法尼基焦磷酸代谢支路的削弱,结合氧化酶CYP71AV1的表达,成功构建能够生产100毫克/升青蒿酸的酵母菌株;然后,研究人员进一步通过基因挖掘、体系优化等系列措施,最终获得了能够生产25克/升青蒿酸的重组酵母菌株及其生产工艺,在此基础上,研究人员开发了从青蒿酸到青蒿素的化学合成方法,整个转化过程的收率为40%~45%。至此,项目组耗时10年完成了青蒿素的半合成工艺(微生物合成加化学合成)[10]。
2013年4月,法国制药业巨头赛诺菲(Sanofi)公司宣布开始应用Amyris开发的青蒿素生产工艺工业化生产青蒿素。2013年5月,世界卫生组织批准微生物合成的青蒿素作为临床药物使用。2014年,赛诺菲公司生产的青蒿素正式上市出售。青蒿素微生物发酵生产商业化的成功成为了合成生物技术的重大应用典范。此外,笔者实验室以FDA认证安全的解脂耶氏酵母为底盘细胞,通过“锦上添花”“移花接木”等方式设计合成途径,构建细胞工厂,实现了角鲨烯、前列腺素、二十二碳二烯酸以及虫草素等高附加值产品的绿色生物制造。这些事例证明了合成生物系统在生物产品绿色制造上具有巨大的潜力。
合成生物学与伦理
合成生物学对生命现象的探讨从认知转向合成,研究对象从自然生命转向合成生命,其发展也非常迅猛,具有广阔的应用前景,也引发了大量相关伦理问题与争论,其主要表现在以下几个方面。
首先,设计新生命带来的伦理困境。人类是否具有构造新生命,打破自然约束和超越自然界限的权力?设计新生命的依据与重构的标准是什么?在多元文化交织的时代背景下,人类应该赋予新生命怎样的道德地位?人工新生命所带来的影响甚或危害该由谁来负责?另外,人的意志和文化将通过新生命的设计嵌入生命的进化当中,不仅将挑战以生物进化自然法则为基础的生命伦理,还将使人类进化的方向和前途面临更大的不确定性。
其次,合成生物学涉及的安全风险包括生物安全和生物安保两个方面。生物安全主要是指由于合成生物的功能以及进化的不确定性,所以导致其研究从设计、制备、存储到运输、应用与环境释放等各环节都存在一定的安全风险;生物安保的重点是防止生物制剂和技术被某些群体滥用。例如,生物剂是检测、鉴定、预防和治疗等方面的基础资源,但细菌、病毒、真菌、毒素等生物剂也可通过生物学诱导、基因改构与合成等技术被制造成生物武器。