中国马凡综合征并发主动脉疾病患者基因型-表型关联分析研究
2023-05-18武玉多张宏家何怡华
武玉多,张宏家,何怡华
马凡综合征(Marfan syndrome,MFS)是由位于15号染色体上的原纤维蛋白-1(FBN-1)基因突变导致的常染色体显性遗传性结蹄组织疾病,是遗传性大血管疾病中较常见的一类[1]。FBN-1基因突变主要累及患者的眼球,骨骼及心血管系统等,其中心血管系统并发症的出现是威胁患者生命安全最重要的因素。据文献报道,在MFS患者中出现心血管系统并发症的患者可占MFS患者总数的80%,其中主动脉夹层和动脉瘤是主要死因,约2/3的患者于50岁前死亡[2]。
因此明确MFS患者出现主动脉事件与FBN-1基因突变的相关性很有必要。目前关于MFS患者基因型-表型的关联分析结果显示,FBN-1基因突变与患者所出现的多系统表型之间尚无明确的联系,也无明确的突变热点区域[3,4]。因此通过本研究,聚焦MFS患者主动脉相关的并发症与突变基因之间的联系,以期改善此类患者的预后,为临床提供关于MFS伴主动脉并发症患者更多有价值的信息。
1 资料和方法
1.1 研究对象本研究纳入于首都医科大学附属北京安贞医院就诊的MFS主动脉疾病患者95例,其中包括70名先证者及其家系中的成员(家系成员先证者筛选处理:由于很多家系成员找到的低频有害位点相同,为避免这种由于家系关系加重对某一个位点的偏好性并影响结果,我们仅提取了这些家系中的先证者样本。由于某些家系没有先证者,如果家系只有一名成员则选择这名成员作为先证者,如果多于一人则随机选择一位患者作为先证者,最终得到70个样本组成的集合)。入组的马凡综合征患者的诊断是依据2010年新修订的Ghent标准[5],患者的人口统计学和相关的临床资料,均来自于首都医科大学附属北京安贞医院的超声诊断科与心脏外科的病历系统及通过电话、微信、门诊复查等渠道取得的可靠信息。脱氧核糖核酸(DNA)分析的知情同意书,是在采集入组的马凡综合征患者的血液样本和临床相关信息时,根据当地机构审查委员会的要求从患者本人及其家属那里获得的。
1.2 遗传测序
1.2.1 DNA的提取与测序入组的马凡综合征患者均抽取外周血4 ml,从中提取基因组DNA,经Covaris破碎仪,将收集的基因组DNA随机打断为长度约180~280 bp的片段,经末端修复和加A尾后,分别在片段两端连接上接头,以此来制备DNA文库。与生物素标记的探针进行液相杂交的是需要带有特异索引的文库池化后,去使用带链霉素的磁珠,将相应基因上的外显子序列捕获下来,经聚合酶链式反应(PCR)扩增后去进行DNA文库的质检,其中建库和捕获实验是采用的Agilent SureSelect Human All Exon V6试剂盒(安捷伦公司,美国加利福尼亚)。对人的全外显子区域DNA进行高效富集,利用Illumina Novaseq 6000平台(Illumina Inc.,美国,加利福尼亚,圣地亚哥)对需要检测的基因组DNA进行全外显子组测序(Whole Exome Sequencing, WES),产生配对末端读取的大小为150 bp,最小的覆盖率为10×(约99%的基因组),而平均覆盖率为100×。
1.2.2 Sanger测序所有入组的马凡综合征患者在完成全外显子组测序之后,随后对先证者和相关受影响的家系中的成员通过Sanger测序进一步验证获得的突变位点。用正向引物(caactcctgtggttgc)和反向引物(acgttgccacaggtcc)进行聚合酶链式反应扩增,将获得的序列与FBN-1参考基因(NM_000138.4)进行比较,以确定突变及准确性。
1.3 变异分类为更好地预测变异位点的致病性,此部分参考了本中心以往的研究分类[6]。美国医学遗传学与基因组学学会(The American College of Medical Genetics and Genomics, ACMG)的突变分类建议被用于所有报告的突变。值得注意的是,以下两种错义变异情况被认为是致病性的有力证据:“支持对基因或基因产物产生有害影响的成熟的体外或体内功能研究”,①一种产生或破坏半胱氨酸残基的错义变异;③一种影响EGF样结构域一致序列(D/N)X(D/N)(E/Q)Xm(D/N)Xn(Y/F)中保守残基的错义变异(m和n代表可变数量的残基)。分类如下所示:
阳性结果:与报告中的表型相关的已知疾病基因中的致病性或可能致病的突变。可能的诊断:已知疾病基因中可能与所报告表型有关的变异。此类别包括新发突变,包括与患者提供的表型重叠的疾病基因中的错义突变或符合读框的插入/缺失,以及已知与解释疾病的基因中的致病性/可能致病性变异反式表达的单个罕见或高度可疑的意义不确定的突变(VUS)报告的表型。候选基因:预计在先前未参与马凡综合征的基因中被预测为有害的,或已发表的支持关联的数据可能尚不确定的突变被视为潜在的新候选基因。支持数据基于模型生物数据,拷贝数变异数据,基因对序列变异的耐受性,有关组织的表达或发育时间的数据或基因功能和途径分析的知识。不确定的结果:已知疾病基因中的高度可疑的意义不确定的突变和患者表型与报告的疾病谱一致(由于缺乏评估新出现和确定突变阶段的亲本样本,不确定性仅限于突变的致病性在隐性疾病中)。该类别还包括与为胎儿提供的表型重叠的隐性疾病,其中仅鉴定出单个致病/可能致病的突变。
阴性结果:未发现与报道的表型有关的基因变异。
1.4 统计学分析采用SPSS 22.0软件进行统计分析。计数资料和计量资料分别采用平均值±标准差(SD)和频率或百分比的形式来表示。计量资料之间的比较采用Student's t检验。以P<0.05为差异具有统计学意义。
2 结果
2.1 患者一般资料本研究共入组有主动脉事件的MFS患者95例,其中男性52例,女性43例,发病年龄平均为(24.26±14.49)岁。本组中主动脉增宽患者43例,主动脉瘤25例,主动脉夹层27例(A型主动脉夹层21例,B型主动脉夹层4例,A+B型主动脉夹层2例),表1。
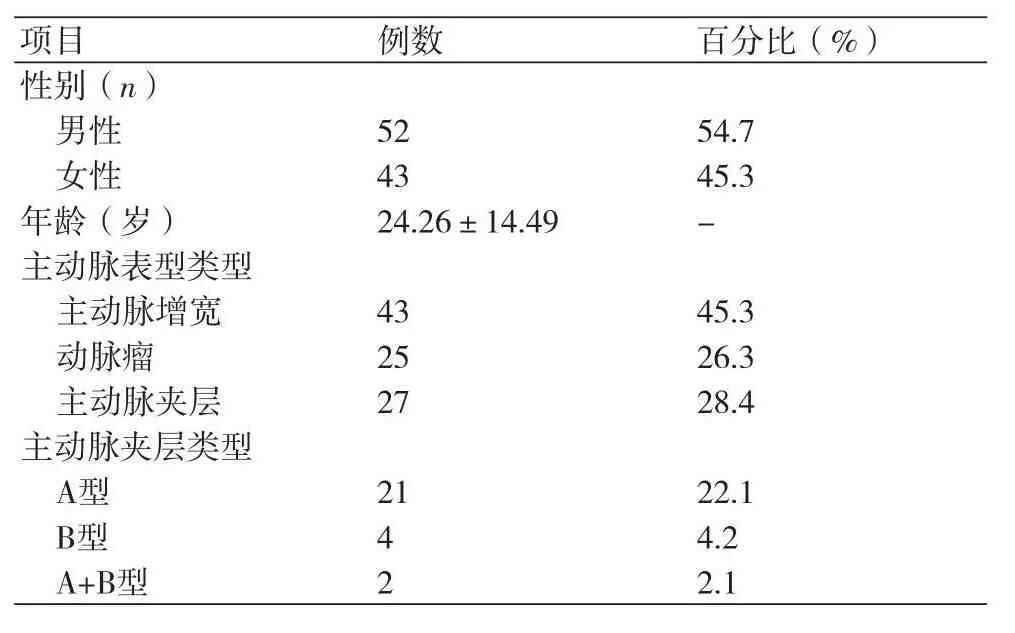
表1 患者的一般资料
2.2 遗传学检测结果基因检测结果(表2)提示,本组患者中,出现错义突变的MFS并发主动脉疾病患者最多,共53例(55.8%);还发现了3例内含子突变(位于与外显子位置相近的检测部位)的MFS患者,其中2例为母女,3例患者为主动脉夹层1例,母女二人均出现主动脉瘤样病变;WES检测位于第二位的是移码突变。

表2 本组患者WES检测结果
2.3 基因型-主动脉表型关联分析本组患者中出现FBN-1错义突变的MFS患者在每一种主动脉并发症组均占比最高;尤其是在主动脉增宽组(58.1%);在与外显子测序相近的内含子区域发现了突变,经验证后证明是导致患者出现MFS的致病位点(表3)。
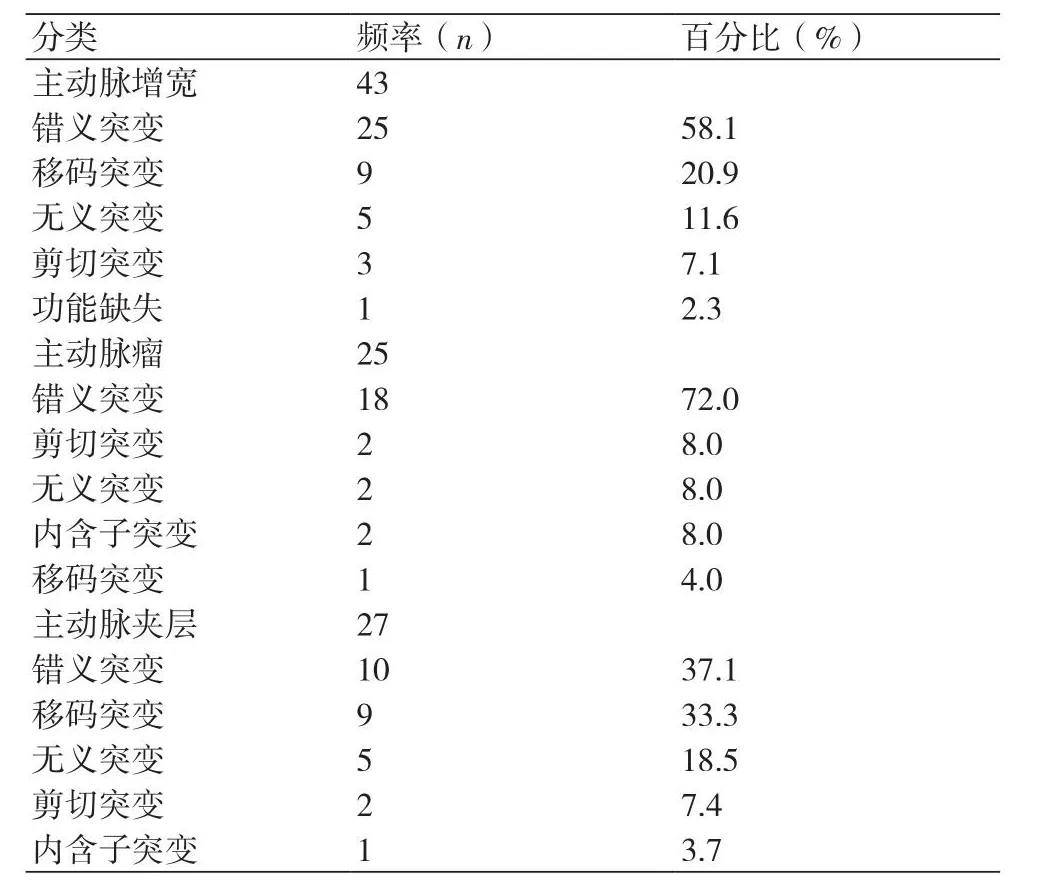
表3 不同主动脉表型患者基因突变类型汇总
2.4 不同主动脉表型在FBN-1基因上的分布结果我们绘制了图1所示的相关主动脉表型所对应的FBN-1基因位点的分布图。该图根据发生该变异的样本是否有主动脉表型进行了划分,图中标记为黑色圆圈的位点为发生该位点变异的样本均没有主动脉表型,红色圆圈为发生该位点变异的样本均存在主动脉表型,而绿色圆圈标记的位点说明部分样本中存在主动脉表型。但从图中并不能看出是否有主动脉表型的样本携带的FNB-1位点在基因结构上有明显的富集现象。
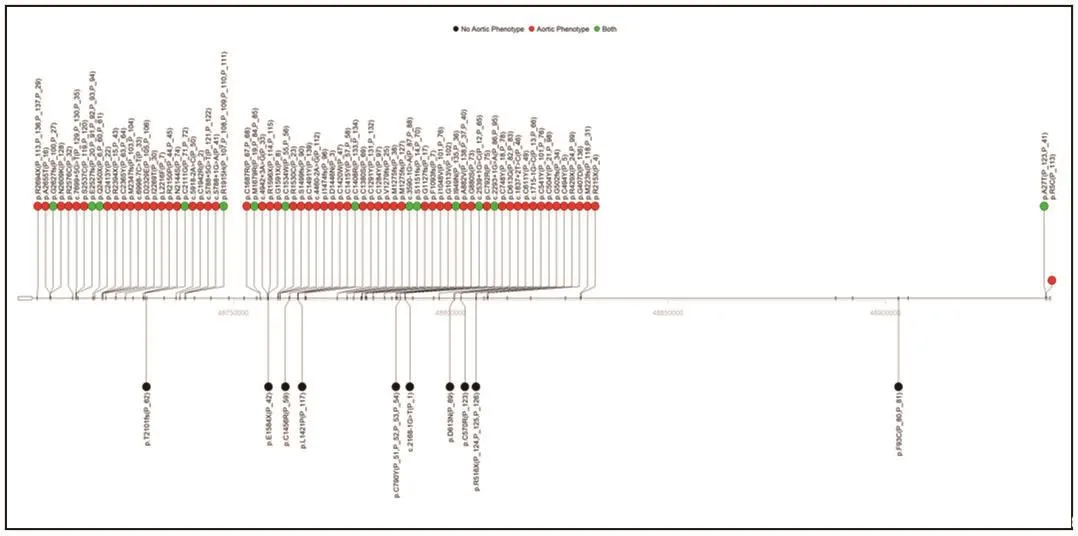
图1 马凡综合征患者主动脉表型-FBN-1基因对应突变位点分布图
同时,我们针对马凡综合征患者的一些其他表型进行了分类和探索,发现不同表型在新的候选基因范围内的变异数量上并不存在显著的差异,提示马凡综合征患者表型上的差异可能另有其他影响因素。此外,马凡综合征患者的基于基因的共有结果中,有多个基因,如TTN,NEFH,PLEC,CASQ2,SYNE1等都与心肌病或心血管疾病相关,而马凡综合征患者常伴有心血管系统的问题,提示此类患者似乎普遍携带有心肌病相关的基因上的低频有害位点,为后续开展相关的分析提供了可能。
3 讨论
MFS是一种常染色体显性遗传性结缔组织病,根据美国CDC的数据,患病率约为0.2‰,影响全球超过140万人[7];国内患病人数约30~40万,患者可能会出现眼(晶状体移位等)、骨骼(肢体细长,脊柱、胸骨畸形等)、皮肤和肺的异常,另外80%的马凡患者会出现心血管系统病变,其中主动脉瘤和夹层是主要致死原因,2/3患者50岁以前可因救治不及时或突发心血管系统疾病而死亡[2,8]。因此及时明确诊断,同时控制心血管系统并发症的发生,可很好地改善患者预后,提高生存寿命。
本研究中共入组95例有主动脉事件的MFS患者,以主动脉增宽患者最多,夹层患者以主动脉A型夹层多见。虽然目前已发现的MFS相关FBN1突变超过2000种,但位点和表型间无明显联系,在本研究中也得到验证[1,9]。尽管马凡综合征患者的外周结缔组织经常受累,但主动脉相关并发症的出现仍是导致患者死亡的主要的危险因素。先前的研究表明,具有严重表型的马凡综合征患者易在外显子24-32区域的FBN-1基因中发生突变(目前文献报道的除了在新生儿期的马凡综合征基因突变与相关的临床表型具有明确关联,在其他阶段的患者中尚无明确关联)[10]。本中心早期研究表明,患有FBN-1移码突变和无义突变的马凡综合征患者易发生主动脉夹层,而出现错义突变的马凡综合征患者则易于发生主动脉瘤[6]。
多因素(遗传因素与环境因素共同)作用导致马凡综合征患者的临床异质性较明显,如外部表现、发病年龄、疾病严重程度等[11]。目前已知的可导致马凡综合征患者发生主动脉夹层的非遗传学因素为高血压,但其他导致心血管疾病的危险因素如:吸烟、饮酒、糖尿病、冠心病等危险因子,是否也会对马凡综合征患者的出现主动脉夹层产生影响,之前研究并未明确报道[12]。以往研究影响马凡综合征患者预后因素的统计建模方法,通常基于各因素相互独立的前提,建立逻辑回归模型,根据统计分析得出的比值比(OR)反映各危险因子与马凡综合征患者预后之间的相关性。马凡氏综合征累及眼,可导致失明;侵犯骨骼,患者走路双腿外撇,呈现出“鸭步”的特点,可出现“鸡胸”或“漏斗胸”,但不会危及生命[11]。马凡氏综合征还会累及心脏,导致患者出现主动脉瘤、主动脉夹层或瓣膜关闭不全等,可能危及生命[10]。马凡综合征患者的预后不是单一因素决定的,在目前的研究基础上,多因素协同作用的效应难以被考虑和准确估计,还需进一步的研究与探索。
本研究中,我中心仅研究了马凡综合征患者DNA的外显子区域,但相关研究报道显示马凡综合征患者也可能是FBN-1基因内含子区域的突变引起的,这些突变可能影响患者的预后和临床表型[13]。努力获取更大量的样本和多中心的数据,以分析马凡综合征患者内含子区域突变的基因信息,完善患者的遗传信息谱。另有研究指出,TGFBR1、TGFBR2基因也是马凡综合征患者的致病基因,研究表明FBN-I突变使转化生长因子-β的活性和信号转导失调,导致纤维蛋白原-1的合成质量下降,数量减少,干扰原纤维的组装,引起结缔组织的伸展过度,致使携带者出现相应的临床表型[14-16],此部分内容也需要我们进一步研究,在前期工作中,已检测出了相关基因。虽然本研究中未进一步深入分析,后续将会对此部分内容进行深入研究。
近年来由于散发的马凡综合征患者病例的高发生率,长期以来人们怀疑其患者中可能存在嵌合体突变的现象[17]。散发病例的新生突变主要来自于两种情况:一是发生在胚胎发育过程中,二是由于父母为生殖细胞嵌合体所致。生殖细胞嵌合体是指当突变只发生在胚胎发育早期的生殖细胞形成过程中,携带突变的细胞系只占生殖细胞的一部分,机体其他组织细胞不携带该突变,因此在对外周血提取的基因组中可能不携带该突变或该突变携带的细胞比例太少而检测不到[18]。若突变发生在胚胎发育早期,将导致个体体细胞和生殖细胞均处于嵌合状态,这种类型的嵌合体外周血便可检测到嵌合突变[18]。依据突变发生的时期与组织分布,嵌合体分为三种类型:体细胞嵌合(仅发生于体细胞,不含生殖细胞),生殖腺嵌合(仅发生在生殖细胞,不含体细胞)以及体细胞和生殖腺均嵌合[18]。后两种类型的嵌合体亲代可将突变遗传给子代[19-21],所以早期识别和明确亲代嵌合体对家庭遗传咨询非常重要。
目前随着遗传学的发展,对于大多数马凡综合征患者,通过谱系分析,致病基因直接测序,高通量测序技术全外显子测序、全基因组测序等的研究方法可在遗传学方面深入研究,根据各个患者家系遗传学特点制定个体化的遗传学研究方法,可达到既快捷又经济的筛选患者致病基因的目的[4]。国际上针对马凡综合征患者的基因检测已十分成熟稳定,并广泛应用于临床检测。
本研究通过对中国人群MFS合并主动脉表型患者的全外显子组测序,进一步验证了FBN-1基因对MFS患者的致病性作用;同时认为FBN-1基因突变是导致MFS患者出现主动脉相关并发症的主要因素;可为临床更好地评判MFS患者的预后和预防主动脉不良事件的发生提供重要依据,突显出FBN-1基因全外显子序列分析在MFS诊断中的重要性和必要性。
