麸炒枳壳标准汤剂质量标准研究*
2023-05-11李国卫何嘉莹索彩仙邱韵静胡绮萍孙冬梅陈向东
李国卫,何嘉莹,索彩仙,邱韵静,胡绮萍,孙冬梅,陈向东
(广东一方制药有限公司·广东省中药配方颗粒企业重点实验室,广东 佛山 528244)
麸炒枳壳的原料为芸香科植物酸橙Citrus aurantiumL. 及其栽培变种的干燥未成熟果实[1]。传统炮制方法包括麸炒、蜜制、盐制等,其中麸炒应用最广泛,目的是“去燥性而和胃”[2],以缓和其辛燥之性,增强其理气消滞之功。目前,关于枳壳炮制的研究包括对其基原、炮制、提取工艺及质量标志物的研究[3-19],多侧重于炮制前后黄酮类成分的变化,作为临床使用汤剂的物质传递的量值关系研究较少。因此,本研究中参考《中药配方颗粒质量控制与标准制定技术要求》[20],制备12 批麸炒枳壳标准汤剂,在建立其超高效液相色谱(UPLC)特征图谱的基础上,通过多指标定量测定,从定性及定量两方面对其进行综合评价。特别是在定量指标选择方面,参考2020年版《中国药典》麸炒枳壳质控指标成分柚皮苷和新橙皮苷[1],深化对黄酮类活性物质的研究,以期为麸炒枳壳标准汤剂质量标准的制订提供参考。现报道如下。
1 仪器与试药
1.1 仪器
Waters H - Class 型超高效液相色谱仪(美国沃特世公司);HWS28 型恒温水浴锅(上海一恒科技有限公司);ME204E 型分析天平(精度为万分之一),XP26 型分析天平(精度为百万分之一),均购于瑞士梅特勒-托利多公司;Milli-Q Direct型超纯水系统(德国默克股份有限公司);KQ500DE 型数控超声波清洗器(昆山市超声仪器有限公司,功率为250 W,频率为40 kHz)。
1.2 试药
橙皮苷对照品(批号110721-201818,纯度96.20%),新橙皮苷对照品(批号111857-201804,纯度99.4%),柚皮苷对照品(批号110722-201714,纯度93.4%),均购于中国食品药品检定研究院;橘红素对照品(批号wkq16011401,纯度98.6%),芸香柚皮苷对照品(批号wkq19041908,纯度98.0%),川陈皮素对照品(批号wkq20031701,纯度98.0%),水合橙皮内酯对照品(批号wkq20031904,纯度98.0%),均购于四川维克奇生物科技有限公司;马尔敏对照品(武汉天植生物技术有限公司,批号CFS201901,纯度98.0%);甲醇为分析纯,磷酸、乙腈均为色谱纯,水为超纯水;麸炒枳壳药材为芸香科植物酸橙Citrus aurantiumL. 及其栽培变种的干燥未成熟果实,经广东一方制药有限公司魏梅主任中药师鉴定均符合药典标准,炮制品为实验室自制,样品信息见表1。

表1 麸炒枳壳样品信息Tab.1 Information of bran-fried Aurantii Fructus samples
2 方法与结果
2.1 麸炒枳壳炮制
取枳壳片200 g,照2020年版《中国药典(四部)》通则0213 麸炒法[21]炒至色变深。形如枳壳片,色较深,偶有焦斑,符合2020年版《中国药典(一部)》枳壳项下麸炒枳壳饮片炮制规定。
2.2 标准汤剂制备
参考《中药配方颗粒质量控制与标准制定技术要求》制备。取麸炒枳壳饮片100 g,加水煎煮2次,第1次煎煮加10 倍量水,浸泡30 min,武火煮沸,文火煮30 min,趁热滤过(350 目筛)后迅速冷却;第2 次煎煮加7 倍量水,武火煮沸后,文火煮25 min,趁热滤过(350 目筛)后迅速冷却。合并滤液,浓缩至清膏,分装至西林瓶中,每瓶分装2 mL,真空冷冻、干燥,取出,轧铝盖,即得标准汤剂冻干粉(编号为S1-S12)。
取枳壳饮片(编号为F1)3 份,每份100 g,按标准汤剂制备工艺平行制备标准汤剂3 份,测定出膏率和水分。结果3 份饮片样品的出膏率分别为26.61%,26.73%,27.13%,RSD为0.99%;水分分别为7.64%,7.77%,7.46%,RSD为2.04%。表明该标准汤剂制备工艺稳定性良好。
2.3 出膏率测定
测定上述浓缩液室温下总体积为V,经磁力搅拌后,精密吸取25 mL,置干燥至恒重的蒸发皿中。样品经水浴蒸干后,105 ℃干燥3 h,置干燥器中冷却至恒重后迅速精密称定质量(m1),所取饮片质量为m2。出膏率(%)=(m1×V)/(0.025 ×m2)× 100%。计算平均出膏率,结果12 批麸炒枳壳标准汤剂平均出膏率为26.01%,标准偏差(SD)为1.86%。详见表2。

表2 12批麸炒枳壳标准汤剂出膏率测定结果(%)Tab.2 Results of extraction rate determination of 12 batches of bran-fried Aurantii Fructus Standard Decoction(%)
2.4 色谱条件
色谱柱:Agilent SB C18柱(100 mm × 2.1 mm,1.8 μm);流速:0.4 mL/min;检测波长:320 nm;柱温:30 ℃;进样量:2 μL;流动相:乙腈(A)- 0.05%磷酸溶液(B),梯度洗脱(0~7 min 时15%A~25%A,7~8 min时25%A~40%A,8~10 min 时40%A~45%A,10~13 min时45%A~60%A,13~15 min时60%A~15%A)[20]。
2.5 溶液制备
取芸香柚皮苷、柚皮苷、橙皮苷、新橙皮苷、水合橙皮内酯、马尔敏、川陈皮素、橘红素对照品各适量,精密称定,加甲醇制成质量浓度分别为16.930 0,90.094 0,11.0803,31.7290,3.4590,1.1270,2.1970,2.5640μg/mL的混合对照品溶液[18]。取标准汤剂样品适量,研细,取0.2 g,加甲醇100 mL,称定质量,超声处理(功率为250 W,频率为40 kHz)30 min,补足减失的质量,摇匀,滤过,取续滤液,即得供试品溶液。
2.6 方法学考察
精密度试验:取标准汤剂样品(编号为S4)适量,依法制备供试品溶液,按2.4项下色谱条件连续进样测定6 次,以新橙皮苷为参照峰。结果11 个共有峰的相对保留时间及相对峰面积的RSD均小于3%(n=6),表明仪器精密度良好。
稳定性试验:取标准汤剂样品(编号为S4)适量,依法制备供试品溶液,分别于0,2,4,6,8,12 h时按2.4项下色谱条件进样测定,以新橙皮苷为参照峰。结果11个共有峰的相对保留时间及相对峰面积的RSD均小于3%(n=6),表明供试品溶液12 h内稳定性良好。
重复性试验:取标准汤剂样品(编号为S4)适量,依法制备供试品溶液,平行6 份,按2.4 项下色谱条件进样测定,以新橙皮苷为参照峰。结果11个共有峰的相对保留时间及相对峰面积的RSD均小于3%(n=6),表明方法重复性良好。
2.7 特征图谱建立及相似度评价
以中药色谱指纹图谱相似度软件2012A 版对12 批样品UPLC 特征图谱进行共有峰标识,以S1 为参照,设置时间窗宽度为0.2,以平均数法建立对照图谱(R)和叠加图谱,确定11 个共有峰,详见图1。经对照品指认,1~4 号峰、10~11 号峰为黄酮苷类成分,峰1 为芸香柚皮苷,峰2为柚皮苷,峰3为橙皮苷,峰4为新橙皮苷,峰10为川陈皮素,峰11为橘红素;5号峰和9号峰为香豆素类成分,峰5为水合橙皮内酯,峰9为马尔敏。详见图2。其中,4 号峰(新橙皮苷)分离度好,色谱峰位置居中,便于其他色谱峰的定位,故以4 号峰(新橙皮苷)为参照峰(S)。由图1 可知,叠加指纹图谱共11 个,以对照指纹图谱为参照,计算12批样品间的相似度均不低于0.99,表明各批次标准汤剂的化学成分组成较稳定。结果见表3。

表3 12批标准汤剂相似度评价Tab.3 Similarity evaluation of 12 batches of standard decoction

图1 12批枳壳对照图谱(R)和叠加图谱Fig.1 Reference chromatogram(R)and superimposed chromatogram of 12 batches of Aurantii Fructus
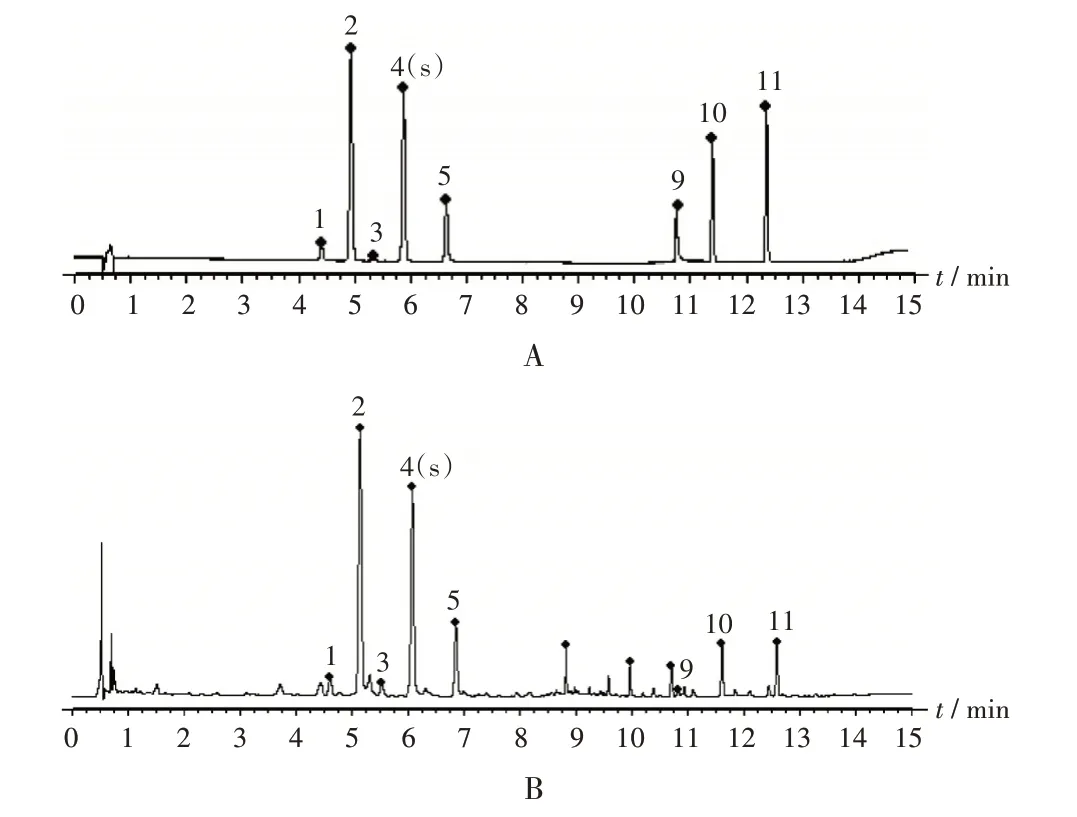
图2 共有峰归属超高效液相色谱图A.Mixed reference solution B.Test solution1.Narirutin 2.Naringin 3.Hesperidin 4(S).Neohesperidin 5.Meranzin hydrate 9.Marmin 10.Nobiletin 11.TangeratinFig.2 UPLC chromatograms of common peak attribution analysis
2.8 含量测定
2.8.1 方法学考察
线性关系考察:取1.2 项下8 种对照品各适量,精密称定,加甲醇制成质量浓度分别为芸香柚皮苷33.563μg/mL、柚皮苷128.71μg/mL、橙皮苷11.08μg/mL、新橙皮苷105.76 μg/mL、水合橙皮内酯6.92 μg/mL、马尔敏2.25 μg/ mL、川陈皮素6.92 μg/ mL、橘红素5.13 μg/mL的混合对照品溶液。加甲醇分别稀释得系列不同质量浓度的对照品溶液,并以质量浓度(X,μg/mL)为横坐标、峰面积(Y)为纵坐标进行线性回归。结果见表4,表明各成分的质量浓度在各自范围内与峰面积线性关系良好。
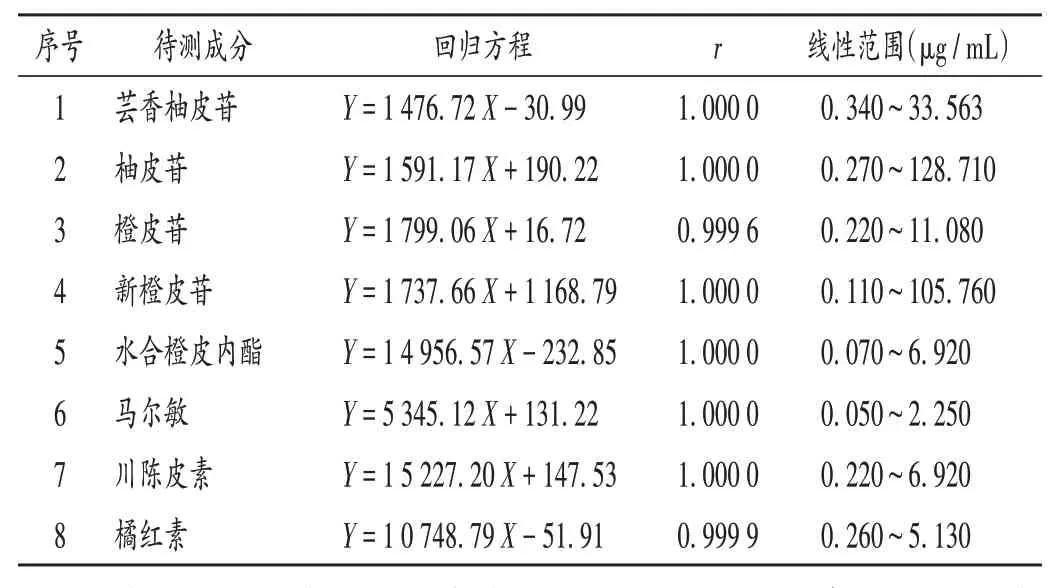
表4 8个待测成分线性关系考察结果Tab.4 Results of the linear relation test of eight components
检测限和定量限确定:取2.5 项下混合对照品溶液适量,以甲醇稀释,按2.4项下色谱条件进样测定,分别以信噪比(S/N)为3∶1 和10∶1 时的质量浓度确定检测限和定量限。结果见表5。
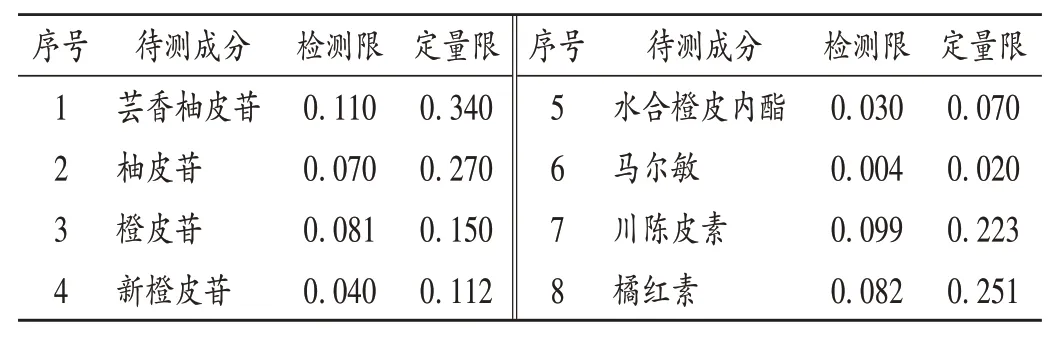
表5 8个待测成分的检测限及定量限(μg/mL)Tab.5 Limit of detection and limit of quantification of eight components(μg/mL)
精密度试验:取2.5 项下混合对照品溶液适量,按2.4项下色谱条件连续进样测定6次。结果芸香柚皮苷、柚皮苷、橙皮苷、新橙皮苷、水合橙皮内酯、马尔敏、川陈皮素、橘红素8个成分峰面积的RSD均小于2%(n=6),表明仪器精密度良好。
稳定性试验:取标准汤剂样品(编号为S4)适量,研细,取0.2 g,精密称定,按2.5 项下方法制备供试品溶液,分别于0,2,4,6,8,12 h时按2.4项下色谱条件进样测定。结果上述8个成分峰面积的RSD均小于2%(n=6),表明供试品溶液12 h内稳定性良好。
重复性试验:取标准汤剂样品(编号为S4)适量,研细,取0.2 g,精密称定,平行6 份,按2.5 项下方法制备供试品溶液,按2.4 项下色谱条件进样测定。结果上述8 个成分含量的RSD均小于2%(n= 6),表明方法重复性良好。
加样回收试验:取已知含量的枳壳饮片样品(编号为F4)0.1 g,精密称定,平行6 份,加入与样品中含量等量的对照品,按2.5 项下方法制备供试品溶液,按2.4项下色谱条件进样测定,计算加样回收率。测得上述8个成分的平均加样回收率分别为100.04%,97.23%,98.03%,97.46%,102.11%,97.45%,96.75%,95.16%,RSD分别为0.97%,1.80%,1.67%,1.72%,1.99%,2.96%,2.42%,2.28%(n=6),表明方法准确度良好。
2.8.2 含量测定
取12批饮片样品,参考文献[22]进行测定;另取12批标准汤剂样品,按2.5 项下方法制备供试品溶液,按2.4 项下色谱条件进样测定,根据公式标准汤剂转移率(%)=(标准汤剂冻干粉指标成分含量×标准汤剂冻干粉量)/制备标准汤剂所用饮片指标成分总量×100%[23]计算标准汤剂中8个成分的转移率。12批麸炒枳壳饮片的含量、标准汤剂含量、转移率测定结果见表6和表7。

表6 12批麸炒枳壳饮片中8个成分含量测定结果(mg/g)Tab.6 Results of content determination of eight components in 12 batches of bran-fried Aurantii Fructus decoction pieces(mg/g)

表7 12批标准汤剂中8个成分含量测定结果与转移率Tab.7 Results of the content determination and transfer rate of eight components in 12 batches of standard decoction
3 讨论
本研究中根据《中药配方颗粒质量控制与标准制定技术要求》,以出膏率、特征图谱、含量及转移率4 个考察指标对麸炒枳壳标准汤剂的质量控制开展研究。其中,标准汤剂代表性的影响因素包括样品来源及制备工艺,从枳壳的道地及主产区江西、湖南等地选取了12批样品,参考2020年版《中国药典》《中药配方颗粒质量控制与标准制定技术要求》对12 批枳壳药材进行规范炮制并制备标准汤剂,保证标准汤剂的质量稳定。
中药标准汤剂因失去了传统的性状特征,仅以单一指标进行定性和定量分析难以反映其质量优劣,故需建立标准汤剂的指纹图谱或特征图谱作为其质量控制指标。本研究中基于12 批不同产地样品的麸炒枳壳标准汤剂质量标志物的UPLC 特征图谱,从定性角度对标准汤剂进行指标成分量值研究,使其在失去外观性状的情况下实现质量可控。
本研究中在参考2020年版《中国药典》定量质量控制的基础上,选择8个质量标志物,即芸香柚皮苷、柚皮苷、橙皮苷、新橙皮苷、水合橙皮内酯、马尔敏、川陈皮素、橘红素,从定量角度对麸炒枳壳标准汤剂进行综合评价。从标准汤剂制备、表征及传递3 个角度研究多指标成分的量值传递规律,以控制产品的质量均一性。《中药配方颗粒质量控制与标准制定技术要求》中规定,在制订标准含量及转移率范围时,以X±3SD(或均值的70%~130%)为依据。因此,本研究中对12 批麸炒枳壳标准汤剂及其饮片的含量及转移率分别计算了均值及SD,为其质量标准的制订提供参考。其中,饮片及标准汤剂的柚皮苷SD值均较大,表明不同产地样品的含量存在一定差异;8 个指标成分中芸香柚皮苷的转移率SD值较大,提示在提取过程中不同样品的提取率差异较大,推测可能与不同产地样品的质地有关。本研究结果显示,不同指标间的转移率波动较大,其中橙皮苷、橘红素的转移率均较小,考虑为橙皮苷、橘红素的水溶性较差;芸香柚皮苷、柚皮苷、新橙皮苷、水合橙皮内酯的转移率均较高,可能与热水能提高这些成分的溶解度有关,且水煎煮过程中新橙皮苷的参与改变了柚皮苷的分子排列方式,形成了柚皮苷- 新橙皮苷共簇体,提高水溶液中柚皮苷的溶解度[24]。
综上所述,本研究中从麸炒枳壳标准汤剂原料的代表性、制备工艺的标准化及全面的质量控制体系出发进行研究,可为麸炒枳壳配方颗粒与传统汤剂的临床用药质量的一致性评价提供参考。
