基于网络药理学及分子对接探讨三黄泻心汤治疗脓毒症心功能障碍的作用机制研究
2023-05-09陈芳良古惠文卫劲沂
陈芳良,古惠文,卫劲沂,毛 帅,2
脓毒症是一种临床常见疾病,具有发病急、病情进展快等特点,严重影响病人的健康及生命安全。脓毒症发病机制复杂,多和机体感染、免疫、炎症等病理生理过程相关,其中炎症反应过度、免疫系统失衡是病情发展的重要环节[1]。脓毒症所导致的免疫功能紊乱贯穿于整个疾病的发生发展过程,并可诱发多器官功能障碍,包括呼吸系统、神经系统、泌尿系统及心血管系统等。脓毒症心功能障碍的发生率为50%~70%[2-4]。心脏功能的损伤对脓毒症预后影响较大,心功能障碍会显著减少心排血量,导致有效循环容量减少,从而加剧组织缺氧、线粒体功能和代谢障碍,前期研究表明,合并心功能障碍使脓毒症病人死亡率增高3~5倍[5]。因此,探索防治脓毒症心功能障碍的新方法、新策略是目前重症医学领域亟待解决的问题。研究表明,脓毒症心功能障碍的发病可能与炎性因子对心肌的抑制、心肌线粒体酶的抑制以及凋亡蛋白酶的激活等过程相关[6]。因此,清除心肌炎性因子、调节免疫功能、改善心肌能量代谢和抑制心肌细胞凋亡可能是治疗脓毒症心功能障碍的关键[7]。研究表明,中医药能够抑制脓毒症病人炎症反应、降低炎性因子水平、改善微循环和减轻心肌缺血缺氧等从而发挥治疗脓毒症心功能障碍的作用[8]。
三黄泻心汤又名“三黄汤”“伊尹三黄汤”,由大黄、黄连、黄芩组成。该方首载于东汉张仲景所撰《金匮要略·惊悸吐衄下血胸满瘀血病脉证治第十六》:“心气不足、吐血、衄血,泻心汤主之。大黄二两,黄连、黄芩各一两,右三味以水三升,煮取一升,顿服之[9]”。现代药理学研究发现,三黄泻心汤具有抗菌、抗炎、胃黏膜保护、改善高脂血症、改善血液黏稠度等作用,临床应用较为广泛[10]。三黄泻心汤具有抑制细胞凋亡、减轻炎症反应和抗氧化等作用[11]。三黄泻心汤中的大黄酸、小檗碱和黄芩苷被证实具有抑制氧化应激、清除炎性介质的作用[12]。但既往研究多是对某一作用机制进行研究。
网络药理学通过“目标药物-疾病-基因”网络的构建和数据的可视化处理,用于预测药物活性成分靶点和相对应的靶向疾病途径,有助于从多维度探讨药物治疗疾病的作用机制[13-14]。本研究运用网络药理学和分子对接的方法,利用多种相关的网络数据库,构建“三黄泻心汤-靶点-信号通路-脓毒症心功能障碍”网络,多维度探讨三黄泻心汤对脓毒症心功能障碍的潜在机制,为临床和基础研究提供科学依据和新的思路。
1 资料与方法
1.1 三黄泻心汤活性成分的获取及靶点筛选 以“三黄泻心汤”和“高效液相色谱/HPLC”为关键词,在中国知网进行文献检索,共获得3篇相关文献:2020年傅丹青等[15]运用高效液相法研究三黄泻心汤中主要成分大黄素、黄芩苷、盐酸小檗碱的溶出规律,但其研究成分较少;2018年李智勇等[16]采用高效液相色谱法研究发现,三黄泻心汤配方颗粒与标准煎剂的化学成分存在一定差异,但缺乏生物等效研究;而2018年水栋等[17]运用高效液相色谱技术(包括专属性试验、线性范围检查、精密度试验、稳定性试验、重复性、加样回收试验、供试验品含量测定)对三黄泻心汤13个有效成分(巴马汀、表小檗碱、大黄酚、大黄素、大黄酸、汉黄芩苷、汉黄芩素、黄连碱、黄芩苷、黄芩素、芦荟大黄素、药根碱、小檗碱)的含量进行了测定,各成分的含量测定结果见图1,其中,蒽醌类和黄酮类共8种成分的含量在同一色谱条件下进行测定,所用方法快捷、准确、专属性强,具有良好的精密度和重复性,故选为本次研究的主要有效成分。使用有机小分子生物活性数据库(PubChem,http://pubchem.ncbi.nlm.nih.gov)查询成分相应分子结构(Canonical SMILES格式),上传至Swiss Target Prediction数据库获取三黄泻心汤潜在作用靶点,由于Swiss Target Prediction数据库中未收录芦荟大黄素的作用靶点,因此,借助中药系统药理学数据库(TCMSP)补充预测芦荟大黄素的潜在作用靶点,最后在Uniprot(https://www.uniprot.org)数据库将蛋白质靶点名称规范化。
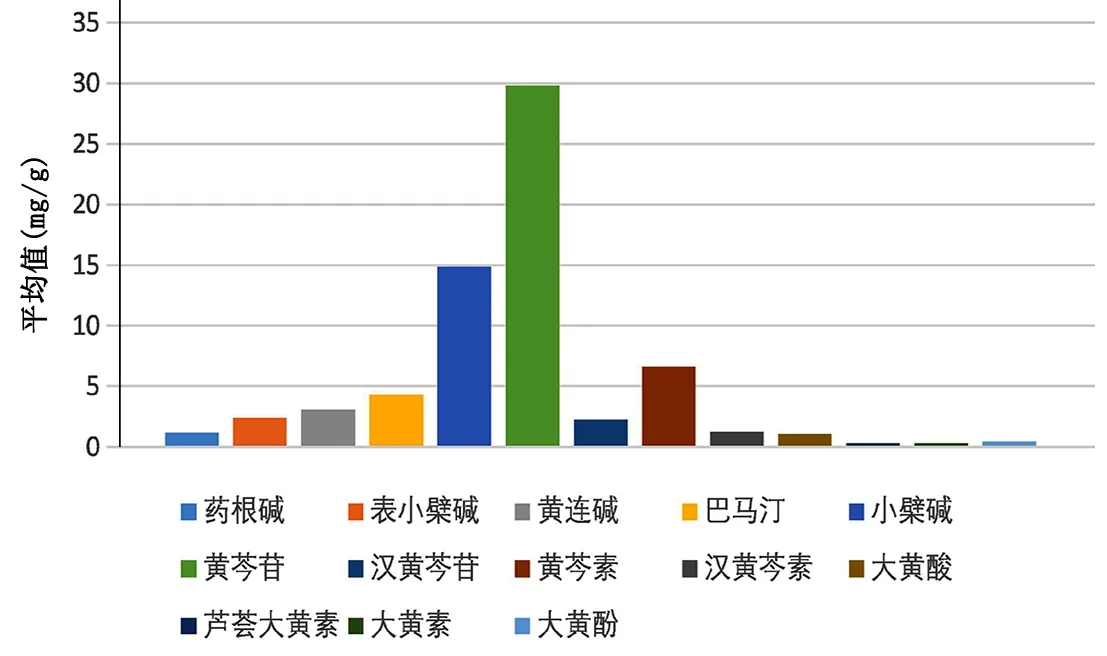
图1 三黄泻心汤中主要成分含量柱状图
1.2 脓毒症心功能障碍疾病靶点筛选 以“sepsis-induced myocardial dysfunction”为关键词在人类基因数据库(GeneCards,https://www.genecards.org/)和人类孟德尔遗传数据库(OMIM,https://omim.org/)中获取脓毒症心功能障碍相关潜在靶点,汇总并删除重复靶点后获得脓毒症心功能障碍对应的疾病靶点。
1.3 药物-疾病共同靶点的筛选 将三黄泻心汤活性成分的靶点与脓毒症心功能障碍的靶点同时导入Venn 2.1.0在线软件作图工具平台进行Venn分析,获得药物与疾病靶点的交集靶点,即为三黄泻心汤治疗脓毒症心功能障碍的潜在作用靶点。
1.4 构建核心靶蛋白相互作用(PPI)关系网络 将上述获得的交集靶点上传至蛋白质相互作用分析数据库(STRING,http://string-db.org/),并将物种设置为人(Homo sapiens),将最低作用阈值设置为0.400,其他参数则保留默认设置,隐藏未关联的节点,并运用Cytoscape 3.8.2软件构建药物与疾病之间的交集蛋白相互作用关系网络图。
1.5 构建药物-成分-靶点网络图 将三黄泻心汤13种有效成分及交集靶点导入Cytoscape 3.8.2软件中,构建“药物-成分-靶点”网络图。利用软件中的“Network Analyzer”功能进行分析,并根据Degree值筛选出关键活性成分及靶点。其中药物活性成分和作用靶点以“节点”表示,节点之间的相互作用以“边”表示。
1.6 基因本体(geneon tology,GO)功能富集和京都基因及基因组百科全书(Kyoto Encyclopedia of Genes and Genomes,KEGG)通路分析 运用注释、可视化和综合发现数据库(DAVID,https://david.ncifcrf.gov/home.jsp),设置“Homo sapiens”,对交集靶点进行GO功能及KEGG通路富集分析。使用微生信在线绘图网站(http://www.bioinformatics.com.cn/)将结果进行可视化。
1.7 分子对接 在蛋白质结构数据库(PDB,https://www.rcsb.org/)检索并下载PPI网络柱状图排名前3位的核心靶点的3D结构PDB格式文件,并用PyMOL 2.5.0软件进行去除水分子和配体的操作及运用Autodock Tools1.5.6软件进行加氢处理。在PubChem数据库检索三黄泻心汤的13种有效成分并下载其化学成分的3D结构SDF文件,通过PyMOL软件转换成PDB文件。利用Autodock Tools 1.5.6软件将化合物及靶点结构文件转换为pdbqt格式,确定对接受体的活性口袋。利用Autodock Vina进行虚拟对接,输出20个预测结果。最后使用PyMOL软件进行可视化处理。
2 结 果
2.1 三黄泻心汤活性成分的获取及潜在靶点筛选 删除重复值后获得三黄泻心汤13种主要有效成分、511个相关潜在作用靶点,由此可以推测三黄泻心汤具有多成分、多靶点的药理特点。
2.2 脓毒症心功能障碍疾病靶点筛选 从GeneCards数据库和OMIM数据库中检索并删除重复值,共获得脓毒症心功能障碍相关靶点基因352个;将三黄泻心汤活性成分靶点与脓毒症心功能障碍靶点同时在线导入Venn 2.1.0在线软件作图工具平台进行Venn分析,获得三黄泻心汤与脓毒症心功能障碍交集靶点51个(见图2)。由此可知,三黄泻心汤可以通过多种成分作用于脓毒症心功能障碍的多个相关靶点来发挥作用。
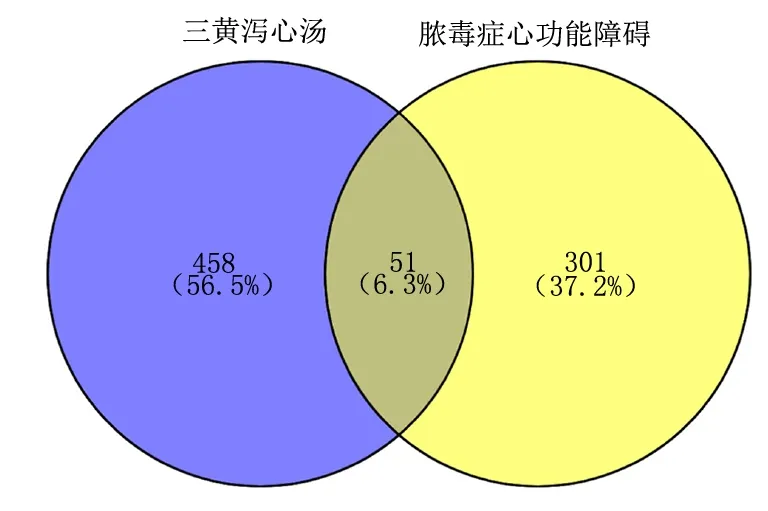
图2 三黄泻心汤与脓毒症心功能障碍相关交集基因韦恩图
2.3 药物-成分-靶点网络图的构建 将三黄泻心汤13种有效成分及三黄泻心汤与脓毒症心功能障碍的交集靶点导入Cytoscape 3.8.2软件中,构建“药物-成分-疾病靶点”网络图(见图3)。利用软件中的“Network Analyzer”功能进行分析,并根据Degree值筛选出关键有效成分,有效成分的Degree值越大,表明其在网络中的作用越大,其中Degree值排名前3位的有效成分是大黄酸、大黄素、表小檗碱。所构建网络共包括65个节点、143条边线,蓝色椭圆形代表三黄泻心汤有效成分,青色八边形代表交集靶点,每个潜在的药物活性成分都与疾病靶点基因存在相互作用,体现了三黄泻心汤通过多成分、多靶点干预治疗脓毒症心功能障碍。
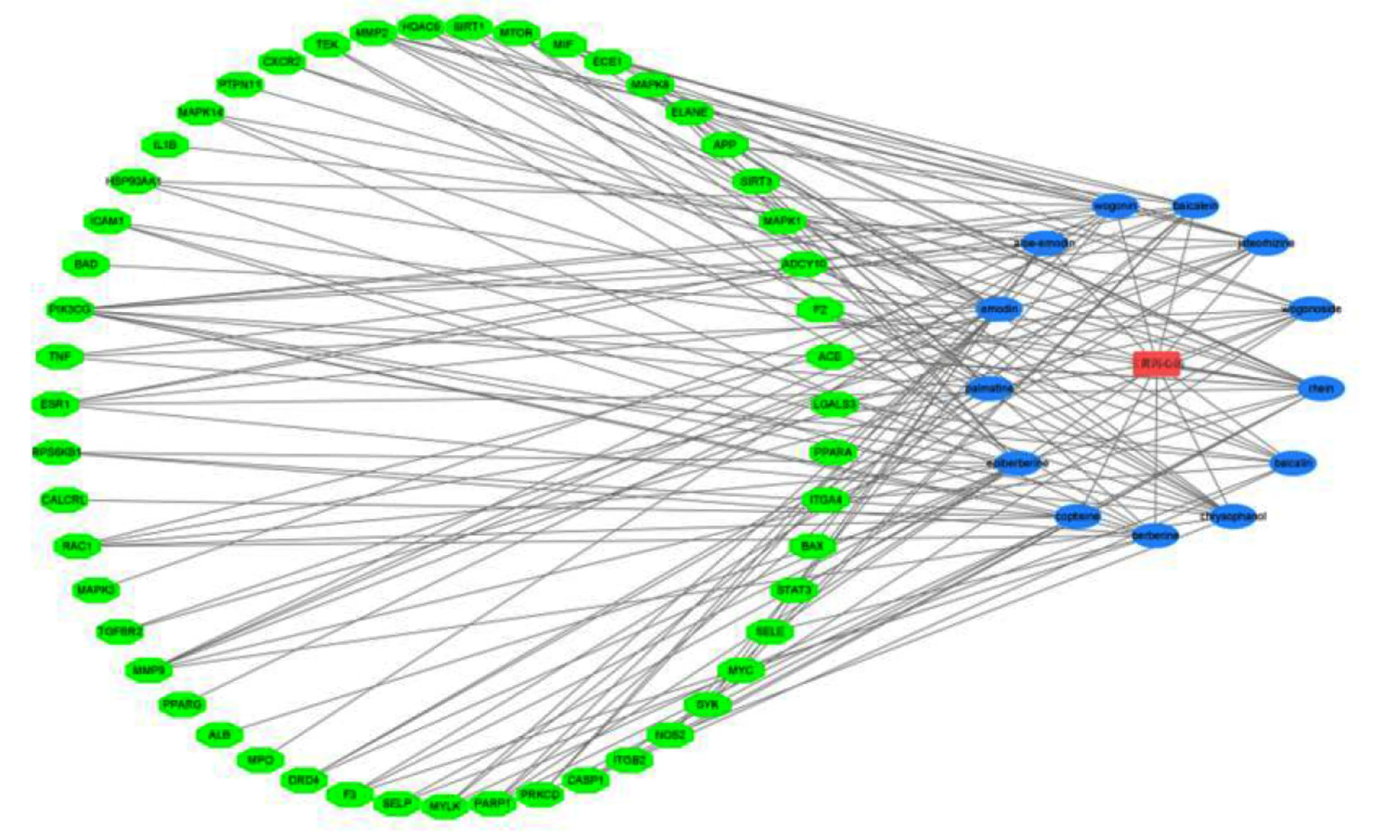
图3 药物-成分-疾病靶点网络图
2.4 交集靶点相互作用关系网络的构建 将获得的交集靶点导入STRING数据库获得交集蛋白相互作用的tsv文件,运用Cytoscape 3.8.2软件构建药物与疾病之间的交集PPI关系网络图(见图4),并利用软件中的“Network Analyzer”功能进行网络拓扑分析,网络拓扑分析结果显示49个节点、489条边。节点表示靶点,连接线代表功能相关性,节点大小、线条多少与节点的Degree值呈正相关。

图4 交集靶点相互作用关系PPI网络图
将STRING数据库中获得的交集靶点相互作用的tsv文件使用R语言进行处理得到PPI核心基因柱状图(见图5)。其中大于Degree值中位数2倍的核心靶点为丝裂原活化蛋白激酶3(MAPK3)、肿瘤坏死因子(TNF)、血清清蛋白(ALB)。Degree值排名前10位的核心靶点包括MAPK3、TNF、ALB、丝裂原活化蛋白激酶1(MAPK1)、丝裂原活化蛋白激酶8(MAPK8)、白细胞介素-1β(IL-1β)、基质金属蛋白9(MMP9)、MYC基因(MYC)、信号转导和转录激活因子3(STAT3)、细胞间黏附分子1(ICAM1)。PPI网络也体现了三黄泻心汤是通过多途径、多靶点治疗脓毒症心功能障碍。

图5 PPI核心基因柱状图
2.5 GO功能和KEGG通路富集分析 运用DAVID数据库对51个潜在作用交集靶点进行GO功能富集分析,且设置显著富集(P<0.01)后共获得165个条目,其中生物过程125个、细胞组分21个、分子功能19个,依据基因计数值(Count值)升序排列,生物过程、细胞组分、分子功能各选取排名前10位制作气泡图(见图6)。结果显示,生物过程主要涉及信号转导、RNA聚合酶Ⅱ启动子转录的正调控、凋亡过程、蛋白磷酸化、炎症反应、凋亡过程的负调控等,由此可见,三黄泻心汤有效成分主要通过调控细胞凋亡、炎症反应等对脓毒症心功能障碍起潜在治疗作用。

图6 GO富集分析气泡图
KEGG通路富集分析共获得显著富集(P<0.01)80条通路,选取富集排名前20条的通路绘制气泡图(见图7),结果显示,三黄泻心汤治疗脓毒症心功能障碍的主要信号通路涉及磷酸肌醇-3-激酶/蛋白激酶B(PI3K/Akt)信号通路、肿瘤坏死因子(TNF)信号通路、丝裂原活化蛋白激酶(MAPK)信号通路、缺氧诱导因子1(HIF-1)信号通路及自然杀伤细胞介导的细胞毒性信号通路等,表明三黄泻心汤主要通过PI3K/Akt信号通路、TNF信号通路、MAPK信号通路、HIF-1信号通路等来发挥对脓毒症心功能障碍的潜在治疗作用。
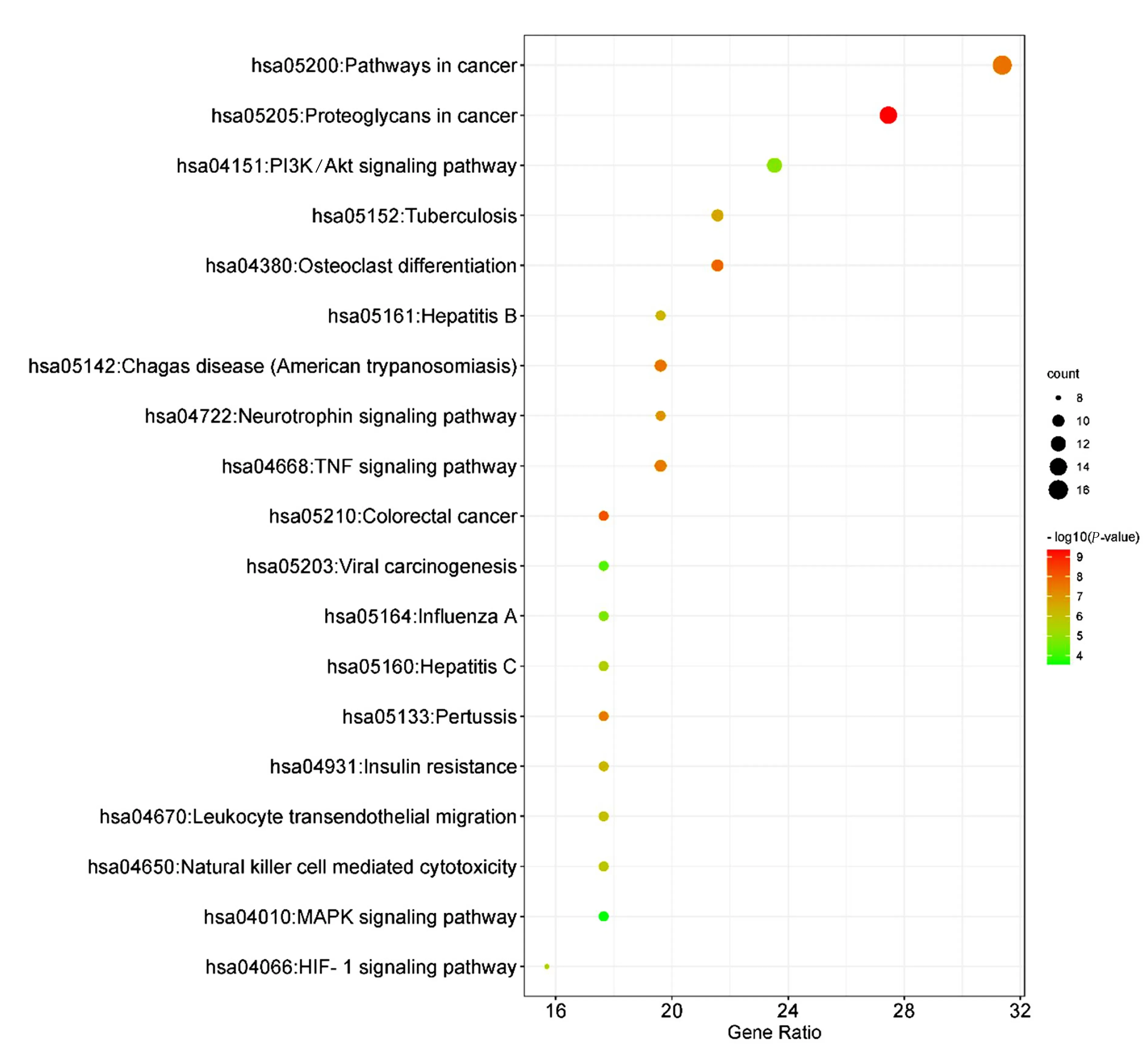
图7 KEGG通路富集分析图
2.6 分子对接验证 将三黄泻心汤的13种有效成分与PPI网络中排名前3位的核心靶点MAPK3、TNF、ALB分别进行分子对接,结合能<-20.920 kJ/mol表明活性成分与靶点有较好的结合活性,结合能<-29.288 kJ/mol表明分子与靶点的结合构型具有强烈的结合活性[18]。结果显示,三黄泻心汤13种有效成分与MAPK3、TNF、ALB关键靶点具有较好的结合力,详见表1。其中,与核心靶点MAPK3结合最强的是大黄酸(-38.074 kJ/mol)。详见图8。

表1 分子对接结果
3 讨 论
王今达等[19]遵循六经辨证、卫气营血辨证理论提出了“三证三法”辨证治疗脓毒症,将脓毒症分为热证、瘀证和虚证,与之相对应的治疗方法是清热解毒法、活血化瘀法和益气固脱法。大量基础及临床研究证实了“三证三法”对脓毒症具有治疗作用,其在一定程度上降低了脓毒症的病死率[20]。三黄泻心汤为张仲景经方,具有清热解毒的功效,用于治疗脓毒症心功能障碍具有充足的理论基础。三黄泻心汤的关键活性成分包括汉黄芩素、黄芩素、大黄素、大黄酸、芦荟大黄素、大黄酚、汉黄芩苷、黄连碱、黄芩苷、小檗碱等。现代药理研究发现,汉黄芩素通过抑制一氧化氮、细胞因子、趋化因子和生长因子在巨噬细胞中发挥抗炎作用[21]。汉黄芩素通过减少胞内活性氧,达到降低细胞内的核转录因子-κB(NF-κB)活性、弱化NF-κB介导的炎症基因转录作用来减弱巨噬细胞的炎症反应[22]。黄芩素快速抑制肿瘤坏死因子-α(TNF-α)的释放,导致白细胞介素-6(IL-6)和一氧化氮的减少发挥抗炎作用[23]。黄芩素通过PI3K/Akt信号通路,保护糖尿病心肌病大鼠免受氧化应激和心肌组织炎症的损害[24]。黄芩素具有解热和广泛的抗病毒作用,对RNA、DNA病毒均有良好的抗病毒作用,可通过抑制p38MAPK信号通路,对急性胰腺炎引发的肺组织损伤具有保护作用,亦能抑制心肌细胞氧化应激和凋亡及心肌坏死对心脏发挥保护作用[25]。Yu等[26]研究发现,芦荟大黄素能够减轻心肌梗死及心肌凋亡;徐瑞明等[27]实验研究发现,大黄素能够减轻脓毒症大鼠心肌损伤,减少脓毒症大鼠心肌组织炎症、氧化损伤和细胞凋亡。研究证实,大黄素减轻脓毒症大鼠心肌损伤的作用可能是通过抑制炎症介质的产生以及激活心肌细胞线粒体膜ATP敏感性K+通道来对抗细胞凋亡而实现的[28]。Wei等[29]研究显示,大黄素能够通过抑制Akt、NF-κB活性,减少半胱氨酸蛋白酶-3(Caspase-3)、半胱氨酸蛋白酶-9(Caspase-9),抑制线粒体依赖凋亡途径。研究表明,大黄酸可减少IL-6、白细胞介素-1β(IL-1β)和TNF-α等促炎细胞因子的生成,同时抑制NF-κB和核苷酸结合寡聚化结构域样受体家族含pyrin结构域蛋白3(NLRP3)炎性因子途径,显著减少免疫细胞迁移而发挥强大的抗炎作用[30-31]。大黄酸已被证明可抑制活性氧的产生,在过氧化氢(H2O2)诱导的人脐静脉内皮细胞中,大黄酸以剂量依赖性的方式显著减少细胞中BH3结构域凋亡诱导蛋白(BID)、Caspase-3、半胱氨酸蛋白酶-8(Caspase-8)和Caspase-9的mRNA表达,减少细胞内活性氧产生,从而逆转H2O2引起的细胞损伤[32-33]。由此可以推测,三黄泻心汤在治疗脓毒症心功能障碍方面,可能主要通过这些有效成分发挥调控炎症反应、氧化应激、细胞凋亡等的重要治疗作用。
本研究发现,三黄泻心汤治疗脓毒症心功能障碍的潜在作用靶点集中在MAPK3、TNF、IL-1β、MMP9等。蛋白互作网络分析结果发现其核心靶点为MAPK3、TNF、ALB。TNF-α、IL-1β是脓毒症发生时重要的促炎因子,其主要是由单核细胞和巨噬细胞产生,具有抑制心肌功能的作用[34-36]。TNF-α作为凋亡的启动介质,通过激活线粒体膜上促凋亡因子(Bax)促凋亡蛋白家族,导致心肌细胞凋亡[37]。IL-1β可浓度依赖性抑制心肌收缩,与TNF-α协同在低浓度即可抑制心肌收缩,同时可诱导一氧化氮等因子产生[38-39]。诱导型一氧化氮合成酶编码诱导型一氧化氮抑制线粒体功能,引起氧化应激、心肌组织代谢性缺氧,收缩功能障碍[40]。一氧化氮合成酶参与心肌梗死、心力衰竭等心肌损伤[41]。MAPK家族蛋白可被上游激酶磷酸化,从而活化下游因子,发挥调节细胞增殖、分化及死亡的作用[42]。其中MAPK3已被证明在心肌细胞凋亡中起保护作用[43]。Tomita等[44]研究发现,内毒素显著增加心脏成纤维细胞中TNF-α和MMP9的表达,广谱MMP抑制剂治疗可减轻脓毒症期间的心脏纤维化和心功能不全等,可见心肌细胞纤维化所致的心脏重构也是脓毒症心功能障碍发病环节之一。综上所述,三黄泻心汤通过调控相关靶点来治疗脓毒症心功能障碍,这些靶点主要涉及炎症反应、心肌凋亡、纤维化等调控。
从GO功能富集分析和KEGG通路富集分析结果可见,三黄泻心汤治疗脓毒症心功能障碍涉及的生物过程主要有信号转导、RNA聚合酶Ⅱ启动子转录的正调控、凋亡过程、蛋白磷酸化、炎症反应、凋亡过程的负调控等,其中靶点主要富集在PI3K/Akt信号通路、TNF信号通路、MAPK信号通路及HIF-1信号通路等。PI3K/Akt信号通路是机体重要信号通路,磷酸化过程中产生转导蛋白,可调节心肌细胞生物活性[45]。以往研究表明,PI3K/Akt能够抑制线粒体凋亡,降低Bax活性,从而减少细胞凋亡,改善病情[46]。PI3K是其信号通路的起始因子,可被多种生长因子激活,在质膜上产生第二信使分子肌醇三磷酸,并与细胞内含有PH结构域的信号蛋白Akt和3-磷酸肌醇依赖性蛋白激酶1结合,促进Akt的磷酸化激活[47]。Akt是PI3K下游信号通路中的重要蛋白,被PI3K激活后,能磷酸化激活其下游雷帕霉素靶蛋白(mTOR),参与细胞生长、存活的调节[48]。其可直接作用于自噬相关基因(Atg)调节自噬体的形成[49]。MAPK信号通路是细胞增殖、应激、炎症、分化、转化、凋亡等信号转导通路的共同交会通路之一[50]。研究发现,TNF信号通路与炎症、细胞凋亡密切相关[51]。综上所述,三黄泻心汤通过调控这些信号通路对脓毒症心功能障碍发挥抗炎、调控细胞凋亡和自噬及减轻氧化应激损伤等潜在治疗作用。
综上所述,基于网络药理学研究结果显示,三黄泻心汤中大黄酸、大黄素、黄芩素、大黄酚、芦荟大黄素等有效成分可能通过TNF、MAPK1、MAPK8、IL-1β、MMP9、MYC、STAT3、ICAM1等关键靶点,调控PI3K/Akt通路、TNF通路、MAPK通路及HIF-1通路等,发挥抗炎、抑制心肌细胞凋亡、调控自噬、减轻氧化应激损伤等作用,为三黄泻心汤治疗脓毒症心功能障碍的进一步临床和基础研究提供了依据和新的思路。
