骨折挫伤胶囊中黄曲霉毒素的测定
2023-05-07罗定强
丁 琳,刘 新,龚 宇,吴 芳,戴 涌,罗定强
陕西省食品药品检验研究院,西安 710065
骨折挫伤胶囊现收载于2020年版《中国药典》一部;处方主要由猪骨、炒黄瓜子、煅自然铜、红花、大黄、当归、醋乳香、醋没药、血竭、土鳖虫组成;具有舒筋活络、消肿散瘀、接骨止痛的作用,用于治疗跌打损伤、扭腰岔气、筋伤骨折属于瘀血阻络者[1]。
在2021年作为国家抽验品种前,该品种于2013年曾作为国家抽验品种,并有多个单位及学者对其进行过质量评价,其中主要包括整体质量评价的研究[2-3],大黄、乳香、血竭、红花、挥发油等主要成分的含量测定[4-12],溶出度和临床应用方面的研究[13-16],还有重金属元素的检测和非法染色剂添加等安全性研究[17-20]。
骨折挫伤胶囊除猪骨外,均以生药粉投料,并且含有动物类药材土鳖虫,土鳖虫富含挥发油、蛋白质,易受黄曲霉毒素污染[21]。按照2020年版《中国药典》四部通则真菌毒素测定指导原则项下说明:“处方中含有易污染的药材以及生粉投料的中成药品种应注意相关真菌毒素的检测”[22-23]。黄曲霉毒素是二氢呋喃香豆素的衍生物,主要是由黄曲霉寄生曲霉产生的次生代谢产物,是霉菌毒素中毒性最大、对人类健康危害极为突出的一类霉菌毒素,它的危害性在于对人及动物肝脏组织有破坏作用,严重时可导致肝癌甚至死亡。其中以B1毒性最大,其毒性和致癌性也最强,远远高于氰化物、砷化物和有机农药的毒性。2020年版《中国药典》对部分中药饮片中黄曲霉毒素限量做出明确规定,但迄今未有标准对中成药中的黄曲霉毒素作出限度要求。目前尚无骨折挫伤胶囊中黄曲霉毒素研究的报道,有必要关注骨折挫伤胶囊中黄曲霉毒素的污染情况,以保证其用药安全。
1 仪器与试药
1.1 仪器
2695高效液相色谱仪、Waters 2475荧光检测器均购自美国Waters公司;KRC光化学柱后衍生器(青岛普瑞邦生物工程有限公司);BS224S电子分析天平(德国Sartorius公司);AUegra X-30离心机(美国Backman公司);KQ-500DE超声仪(昆山市超声仪器有限公司);Aflatoxin B1、B2、G1、G2免疫亲和柱[月旭科技(上海)股份有限公司]。
1.2 试药
甲醇(色谱纯)、乙腈(色谱纯),均购自Honeywell公司;高纯水由四川优普超纯科技有限公司UPH-11-10T超纯水机制备;甲醇、氯化钠、磷酸二氢钾、磷酸氢二钠均为分析纯,购自天津市科密欧化学试剂有限公司;吐温 20(化学纯);氯化钾(分析纯)购自国药集团化学试剂有限公司;自制纯化水;黄曲霉毒素混合对照品溶液(批号为61001-202006,含B11.04 μg·mL-1、B20.38 μg·mL-1、 G11.08 μg·mL-1、G20.38 μg·mL-1,中国食品药品检定研究院);骨折挫伤胶囊138批,购自a、b、c、d、e、f、g、h共8个企业;土鳖虫3批(自行购买1批,其余2批由厂家b、c提供)。
2 方法与结果
2.1 色谱条件
色谱柱为Persuit 5 C18色谱柱(250 mm×4.6 mm,5 μm);流动相:甲醇-乙腈-水(27∶12∶61)(A)-甲醇(B)梯度洗脱(洗脱梯度详见表1);流速为0.8 mL·min-1;检测器为荧光检测器;激发波长λex=360 nm,发射波长λem=450 nm;柱温为30 ℃;进样体积为10 μL。
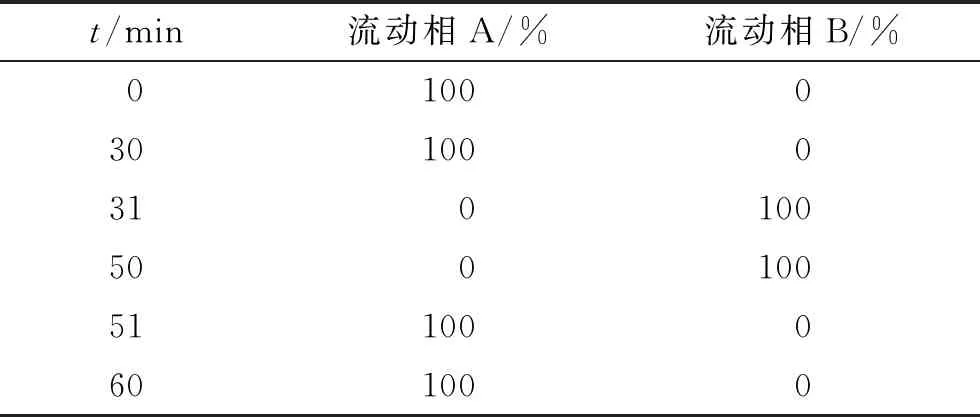
表1 洗脱梯度程序
2.2 溶液的制备
2.2.1对照品储备液的制备 精密量取黄曲霉毒素混合对照品溶液1 mL,置于100 mL量瓶中,用甲醇稀释至刻度,摇匀,作为对照品储备液。
2.2.2标准曲线的制备 精密量取对照品储备液0.5、1、2、3、4、5 mL分别置于10 mL量瓶中,用甲醇稀释至刻度,作为系列质量浓度的对照品溶液。见表2。
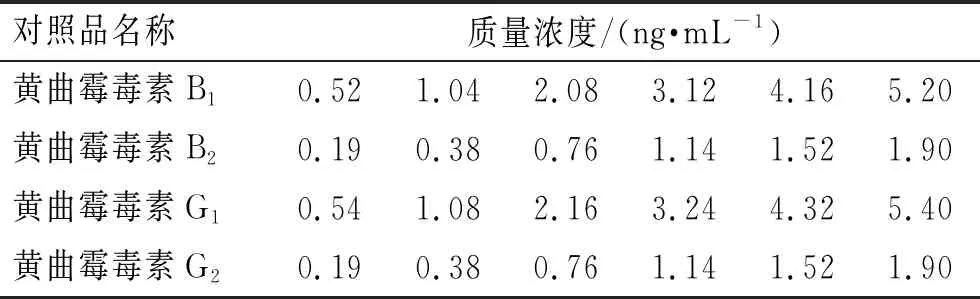
表2 标准曲线质量浓度
2.2.3供试品溶液的制备 取供试品约15 g,精密称定,置于具塞锥形瓶中,加入氯化钠3 g,精密加入体积分数为70%的甲醇溶液75 mL,超声处理(功率为500 W,频率为40 kHz)45 min,离心5 min(转速为4 000 r·min-1),精密量取上清液15 mL,置于50 mL量瓶中,用水稀释至刻度,摇匀,离心10 min(转速为4 000 r·min-1),精密量取上清液20 mL,通过免疫亲合柱,流速为3 mL·min-1,用10 mL·L-1吐温-20的磷酸盐缓冲溶液(10 mL·L-1吐温-20的磷酸盐缓冲溶液的制备:称取氯化钠8.0 g、磷酸氢二钠1.2 g、磷酸二氢钾0.2 g、氯化钾0.2 g,用900 mL水溶解,用盐酸调节pH值至7.4±0.1,加水稀释至1 000 mL,得磷酸盐缓冲溶液。取10 mL吐温-20,加入磷酸盐缓冲溶液稀释至1 000 mL[24-25])20 mL洗脱,再用水20 mL洗脱,使空气进入柱子,将水挤出柱子,再用适量甲醇洗脱,收集洗脱液,置于2 mL量瓶中,并用甲醇稀释至刻度,摇匀,即得。
2.2.4阴性样品溶液的制备 选择在黄曲霉毒素出峰位置处无干扰的阴性样品,按2.2.3项下方法制备阴性样品溶液。
2.3 系统适用性实验
按上述色谱条件将标准曲线项下的对照品溶液、供试品溶液、阴性样品溶液分别进样10 μL。色谱见图1。结果显示,阴性样品色谱峰无干扰,对照品、供试品各峰间分离度良好。
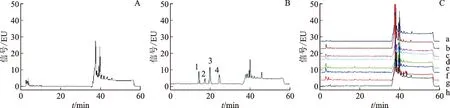
注:A.阴性样品色谱图;B.对照品色谱图;C.供试品色谱图;a.a企业供试品色谱图;b.b企业供试品色谱图;c.c企业供试品色谱图;d.d企业供试品色谱图;e.e企业供试品色谱图;f.f企业供试品色谱图;g.g企业供试品色谱图;h.h企业供试品色谱图;1.黄曲霉毒素G2;2.黄曲霉毒素G1;3.黄曲霉毒素B2;4.黄曲霉毒素B1。
2.4 线性关系考察
将2.2.2项下系列质量浓度对照品溶液分别进样10 μL,收集色谱图,以质量浓度为横坐标、峰面积响应值为纵坐标,绘制标准曲线,结果见表3。

表3 黄曲霉毒素B1、B2、G1、G2线性回归结果
2.5 精密度实验
精密量取2.2.2项下对照品溶液(黄曲霉毒素B1、B2、G1、G2质量浓度分别为0.28、0.76、2.16、0.76 ng·mL-1)10 μL,按上述色谱条件重复测定6次,计算黄曲霉毒素B1、B2、G1、G2峰面积的RSD值分别为0.51%、0.39%、1.16%、0.43%,表明方法精密度良好。
2.6 黄曲霉毒素B1、G1重复性实验
取本品(批号20200601,e企业)15 g,精密称定,按2.2.3项下方法平行制备6份供试品溶液,测定峰面积,计算含量。结果显示,黄曲霉毒素B1、G1含量的RSD值分别为2.25%、2.60%,表明样品重复性良好。
2.7 回收率实验
取阴性样品(批号200904,a企业)15 g,精密称定,分别置于编号为1~9的具塞锥形瓶中;分别精密量取上述对照品储备液2、3、4 mL各3份,分别加入编号为1~9的样品中,按上述供试品制备方法制备供试品溶液,按拟定色谱条件测定含量,计算回收率。结果表明,本方法回收率结果满意。结果详见表4。
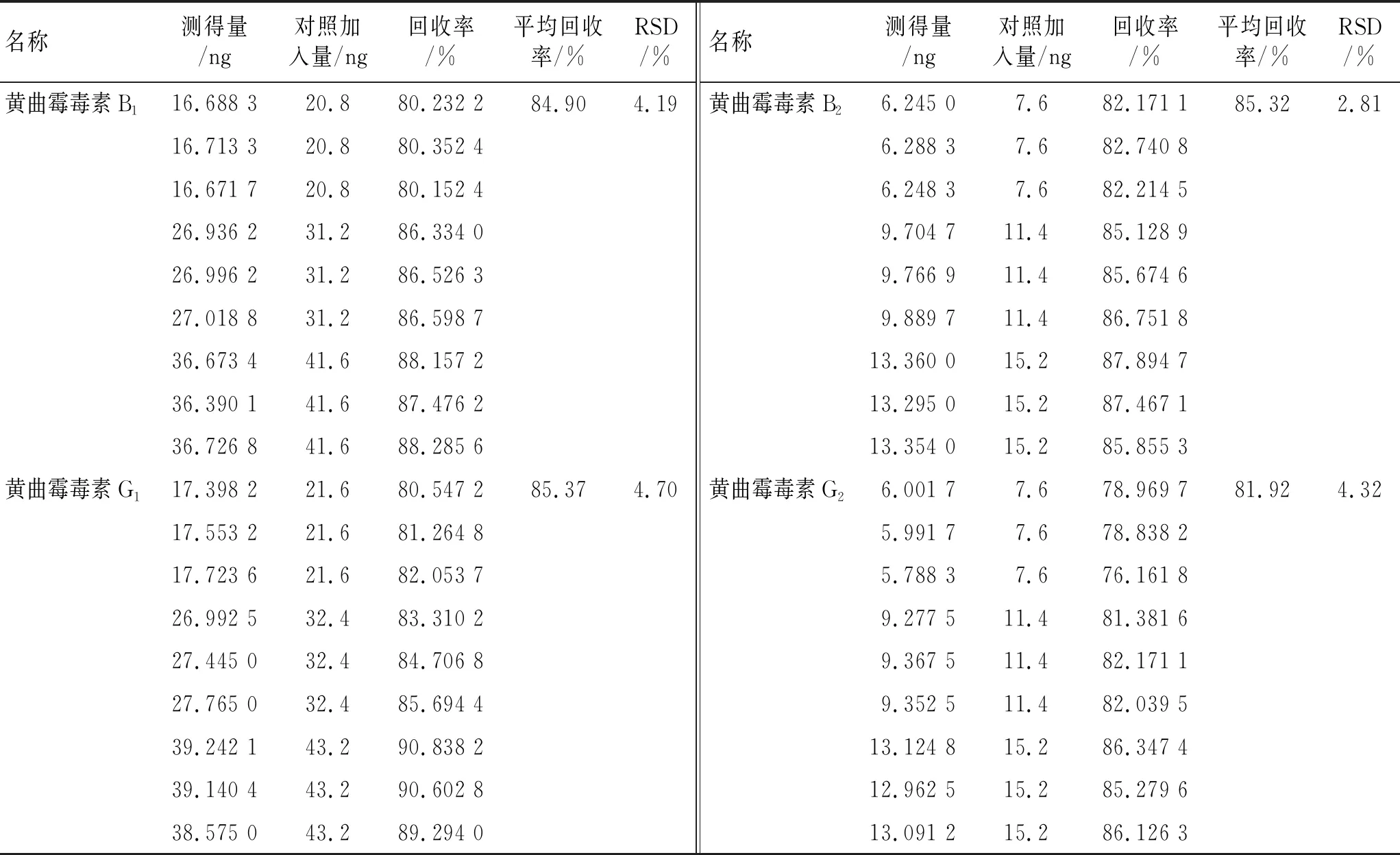
表4 黄曲霉毒素B1、B2、G1、G2回收率实验结果
2.8 方法检出限
取阴性样品(批号200904,a企业)15 g,精密称定,置于具塞锥形瓶中,再精密加入2.2.2项下的对照品溶液(黄曲霉毒素B1:3.12 ng·mL-1、B2:1.14 ng·mL-1、G1:3.24 ng·mL-1、G2:1.14 ng·mL-1)2 mL,按2.2.3项下方法制备检出限溶液。黄曲霉毒素B1、B2、G1、G2检出限分别为0.42、0.16、0.43、0.16 μg·kg-1,均符合要求。
2.9 样品测定结果
对138批骨折挫伤胶囊和3批土鳖虫饮片进行含量测定。7批骨折挫伤胶囊检出黄曲霉毒素B1、G1,但均未超出限度,其余检品均未检出黄曲霉毒素。另外2批土鳖虫药材检出黄曲霉毒素B1、G1,其中1批超出限度要求。结果见表5。
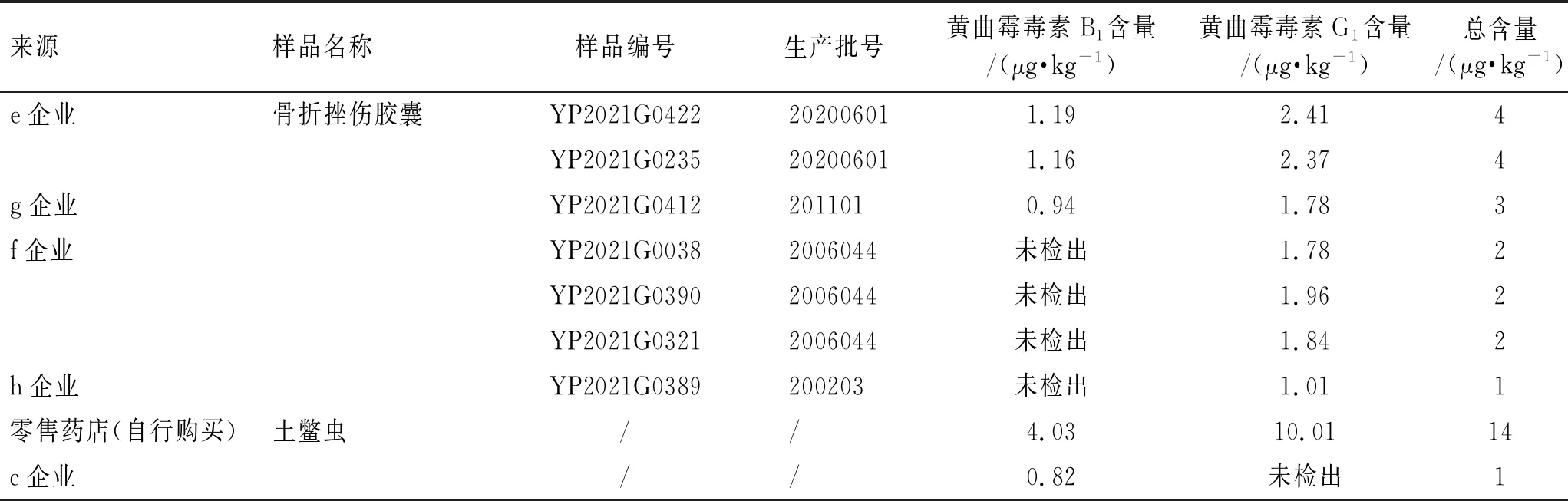
表5 骨折挫伤胶囊中黄曲霉毒素含量测定结果
2.10 拟定限度及结果
2020年版《中国药典》黄曲霉毒素限量要求:“每1 000g含黄曲霉毒素B1不得过5 μg,含黄曲霉毒素G2、黄曲霉毒素G1、黄曲霉毒素B2和黄曲霉毒素B1的总量不得过10 μg”。根据此要求拟定骨折挫伤胶囊限度同《中国药典》2020年版四部要求。由以上结果可得,所有样品中黄曲霉毒素含量均小于规定限度,符合要求。
3 讨论
3.1 色谱条件的考察
流动相分别用甲醇-乙腈-水(27∶12∶61)、甲醇-乙腈-水(27∶12∶61)(A)-甲醇(B)梯度洗脱,结果发现,当流动相用等度洗脱时供试品溶液在适当时间内未完全出峰,造成对随后供试品色谱图的干扰,而用梯度洗脱时,供试品可在适当时间内全部出峰,避免干扰,因此色谱条件选择梯度洗脱程序。结果见图2。
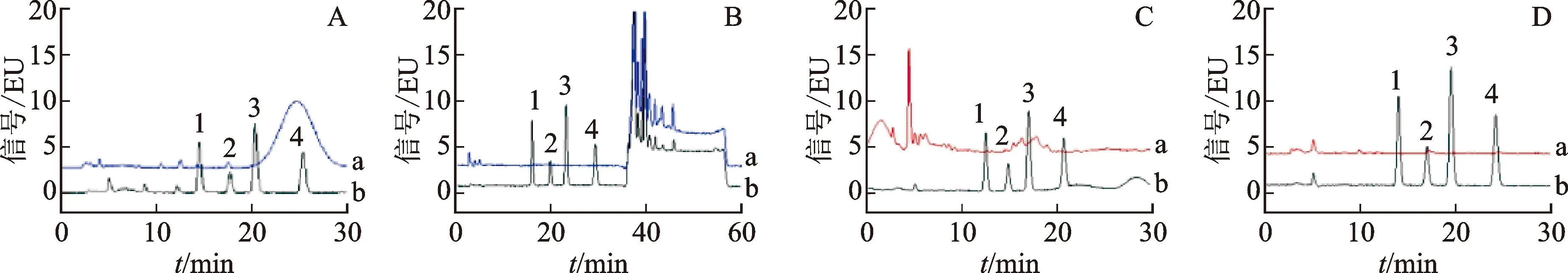
注:A.等度洗脱色谱图;B.梯度洗脱色谱图;C.水洗脱色谱图;D.10 mL·L-1吐温-20的磷酸盐缓冲溶液-水洗脱色谱图;a.供试品色谱图;b.对照品色谱图;1.黄曲霉毒素G2;2.黄曲霉毒素G1;3.黄曲霉毒素B2;4.黄曲霉毒素B1。
3.2 免疫亲和柱洗脱条件的考察
分别用水20 mL、10 mL·L-1吐温-20的磷酸盐缓冲溶液10 mL和水10 mL进行洗脱,结果显示,用20 mL水进行洗脱时对测定结果有干扰,改用10 mL·L-1吐温-20的磷酸盐缓冲溶液10 mL和水10 mL进行洗脱时对测定结果无干扰。因此免疫亲和柱洗脱剂选用10 mL·L-1吐温-20的磷酸盐缓冲溶液-水。结果见图2。
4 结论
通过对138批骨折挫伤胶囊检测发现,部分检品中虽存在黄曲霉毒素B1和G1,但均符合要求,可确定所有样品中的黄曲霉毒素对人体不会造成威胁。
根据2020年版《中国药典》和以往检验检测经验对处方进行分析,推测黄曲霉毒素可能是由土鳖虫引入的。通过检测3批土鳖虫结果发现,自行购买的土鳖虫中黄曲霉毒素超出了国家标准的限度要求。该结果为样品中黄曲霉毒素的来源提供了数据支持。另外,以上结果表明黄曲霉毒素B1、G1在饮片和样品中存在较多,而黄曲霉毒素B1的毒性和致癌性最强。由此可见,控制中药饮片中的黄曲霉毒素是保证用药安全的关键。因此,有关企业应加强对中药材质量、加工与储存、成药生产工艺及存放条件等一系列环节的重视,以更好地控制样品中黄曲霉毒素的含量。
理论上,企业使用检验合格的原料生产中成药,其产品中的黄曲霉毒素限量应符合要求,从而可以有效改善中成药的安全性问题。但本实验发现部分样品中黄曲霉毒素污染情况不容乐观,建议企业或检验检测机构等相关部门可开展含高风险品种的中成药筛查工作,掌握中成药高危品种黄曲霉毒素的含量情况,采取相应措施保障中成药的临床用药安全。
