超声异常胎儿产前诊断及妊娠结局的研究
2023-04-08韩咏梅程翠云
韩咏梅 程翠云
产前超声检查作为筛查胎儿畸形的常用方法,现已得到临床广泛应用,经超声检查能够有效鉴别诊断异常胎儿,若胎儿为轻度畸形,可严重影响家庭生活质量,同时也会对家庭经济造成严重负担;若畸形情况严重,则会危及胎儿生命安全[1,2]。因此,尽早明确胎儿畸形情况,对指导临床治疗、改善妊娠结局、提高优生优育率等具有重要作用。在胎儿超声软指标检查中可见其微小结构变化情况,通常在染色体正常或异常胎儿中均可发生,但前者发生率更高。目前,异常胎儿诊断以羊水穿刺结果作为“金标准”,对选择性的染色体核型进行有效分析利于降低胎儿出生缺陷率,从而提高新生儿出生质量[3,4]。现阶段,产前诊断的重要方法为染色体核型分析,但该方法检测时间较长,同时受到显微镜分辨率、实验室显带技术等因素影响,极易出现未知染色体异常、亚显微异常等现象,影响判断结果,从而导致误诊或漏诊[5]。CMA 是近年发展起来的分子生物学检测方法,其特点是分辨率高、检测速度快、检测通量高,可分辨出100 KB 以上的染色体片段变异。由于该基因芯片检测不需要进行细胞培养,因此其适用于细胞培养较难成功的检测样本,或者有明显症状但常规核型分析未检出异常的样本。CMA技术包括基于微阵列的比较基因组杂交(array-based Comparative Genomic Hibridization,aCGH)技术和单核苷酸多态性微阵列技术,能够在全基因组水平进行检测染色体不平衡的CNVs,且较染色体核型分析具有更高的分辨率和敏感度,目前广泛应用于胎儿异常的产前诊断[6]。鉴于此,本研究分析超声异常胎儿产前诊断及妊娠结局,现报告如下。
1 资料与方法
1.1 一般资料 选择2019 年11 月~2021 年10 月于本院行产前超声检查且发现异常妊娠的产妇265 例作为研究对象,年龄22~45 岁,平均年龄(31.58±2.37)岁;孕周18~34 周,平均孕周(22.63±1.74)周。本研究获本院伦理委员会批准。
1.2 纳入及排除标准 纳入标准:常规产前超声异常妊娠产妇;单胎妊娠;产妇及家属签署同意书。排除标准:妊娠前或妊娠期间存在其他系统恶性肿瘤;凝血及造血功能障碍;产检资料缺乏;免疫系统疾病;既往存在不良妊娠史,或存在家族异常妊娠史;精神疾病或意识障碍,无法配合完成本次研究者。
1.3 方法①超声检查:使用超声诊断仪(西门子公司)筛查胎儿发育系统,具体包括颈后皮肤增厚、脉络丛囊肿、肠管强回声、心室强回声光点、单脐动脉、肾盂扩张、轻度侧脑室增宽、鼻骨短及胎儿结构畸形等,并仔细观察胎儿发育异常的超声检查结果。②羊膜腔穿刺术:在无菌环境中应用超声做引导采集25~30 ml 羊水进行检测,其中取20 ml 行染色体核型分析,另5~10 ml 行CMA 检测。③染色体核型分析:对抽取的羊水样本行离心处理,以3500 r/min 速度离心10 min,离心半径为10 cm,获得上层清液,将离心后的沉淀物质制备为细胞悬液,随后将其接种于羊水培养基上,待培养7 d 后观察培养基上细胞生长情况,但在此基础上需及时更换培养基中液体,再经低渗、消化、固定等操作制备为细胞悬液,再行制片、G 显带染色,明确每个标本显带选择清晰、形态适中的核型行进一步分析。④CMA:严格按照Affymetrix Cyto Scan 750K芯片(55 万CNV 探针和20 万SNP 探针)的标准操作流程进行检测:基因组DNA 酶切、连接、聚合酶链式反应(PCR)扩增、纯化、片段化、标记,芯片杂交、洗涤及扫描。数据结果采用Chromosome Analysis Suite (ChAS 3.1)软件进行分析,CNV 的报告阈值为200 KB 缺失、500 KB 重复。对CMA 检出的CNV 结果判读,主要参考常用国际公共数据库,如基因组变异数据库(DGV)、美国国家生物技术信息中心(NCBI)临床突变数据库(Clinvar)、剂量敏感判断数据库(ClinGen)、拷贝数变异数据库(Decipher)等公共数据库及本实验室内部数据库进行数据分析,将CNVs 分为致病性、疑似致病性、VOUS、可能良性及良性。
1.4 观察指标①分析超声异常胎儿的染色体核型分析结果;②分析超声异常胎儿的CMA 结果;③分析超声异常胎儿的妊娠结局。
2 结果
2.1 超声异常胎儿的染色体核型分析结果 265 例超声异常胎儿中,行染色体核型分析的胎儿205 例,共检出染色体异常29 例,检出率为14.15%(29/205)。包括染色体数目异常21 例,占比为72.41%(21/29);结构异常8 例,占比为27.59%(8/29)。见表1。

表1 21 例染色体数目异常胎儿的超声表现
2.2 超声异常胎儿的CMA 结果 265 例超声异常胎儿中共检出CMA 异常56 例,检出率为21.13%(56/265),包括染色体核型分析中检出的染色体数目异常21 例,另发现致病性CNVs 9 例,占16.07%(9/56),VOUS 26 例,占46.43%(26/56)。见表2。
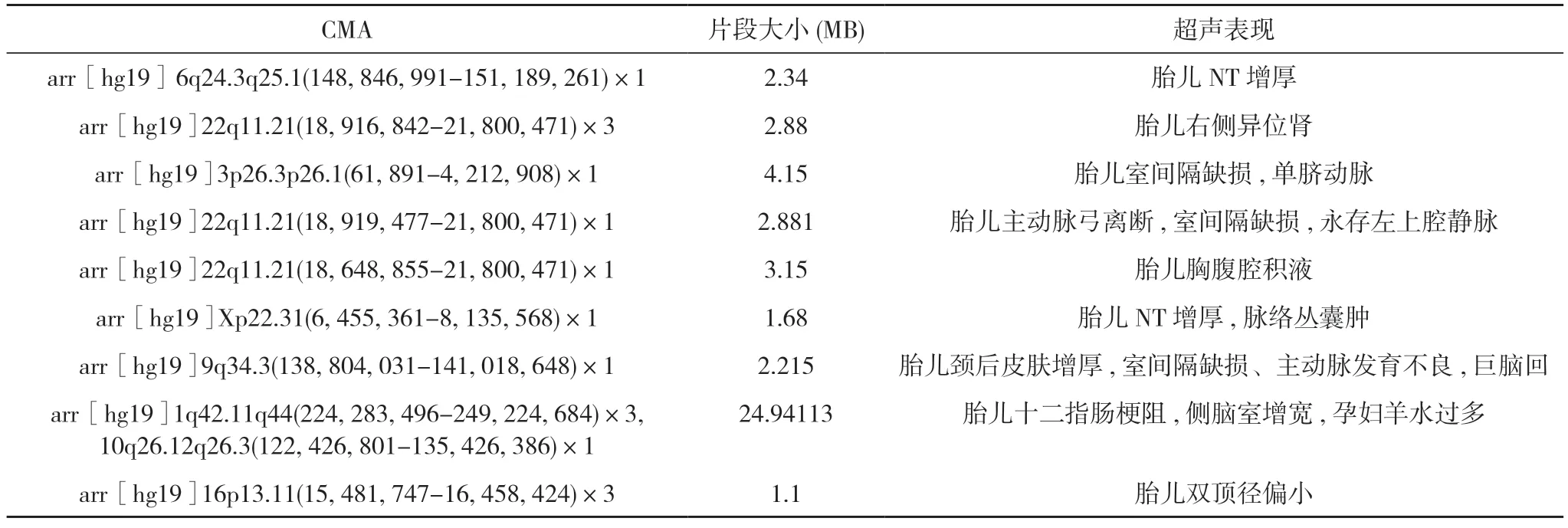
表2 CMA 异常胎儿的超声表现
2.3 超声异常胎儿的妊娠结局分析 所有超声异常胎儿均接受电话随访,明确阳性30 例,占11.32%(30/265),引产36 例,流产或因死胎引产12 例。
3 讨论
产前细胞遗传学检查的首选为染色体核型分析,通过该分析能够检出染色体非整倍体性异常及大片段的染色体结构异常等信息[7]。相关研究显示[8,9],常规的染色体核型分析与胎儿脑部发育、语言发育迟缓、生长发育迟缓等多种症状间联系密切。
传统的染色体核型分析需要经过细胞培养、制片、染色等复杂手段,且其分辨率一般为5~10 MB。但是很多遗传疾病可能是由<5 MB 的“亚显微结构异常”导致,常规核型分析技术难以发现。并且染色体培养的过程较困难,存在一定的细胞培养失败几率,给后期的分析和发报告带来困难,且孕周>26 周,羊水中胎儿脱落细胞老化,则不能行核型分析。基因芯片检测是近年发展起来的分子生物学检测方法,其特点是分辨率高、检测速度快、检测通量高,可分辨出>100 KB的染色体片段变异。由于该基因芯片检测不需要进行细胞培养,因此其适用于细胞培养较难成功的检测样本,或者有明显症状但常规核型分析未检出异常的样本。基因芯片技术除了能检出非整倍体异常,还可在全基因组范围内检测核型分析难以发现的微缺失和微重复、部分嵌合体、杂合性缺失/ 单亲二倍体等,一次性同步检测多种与出生缺陷相关的基因组异常[10]。但目前基因芯片无法分析染色体的结构变异。
本研究结果显示,265 例超声异常胎儿中,行染色体核型分析的胎儿205 例,共检出染色体异常29 例,检出率为14.15%(29/205)。包括染色体数目异常21 例,占比为72.41%(21/29);结构异常8 例,占比为27.59%(8/29)。265 例超声异常胎儿中共检出CMA 异常56 例,检出率为21.13%(56/265),包括染色体核型分析中检出的染色体数目异常21 例,另发现致病性CNVs 9 例,占16.07%(9/56),VOUS 26 例,占46.43%(26/56)。所有超声异常胎儿均接受电话随访,明确阳性30 例,占11.32%(30/265),引产36 例,流产或因死胎引产12 例。分析其原因可知超声异常通常提示染色体异常,且缺乏特异性,作为产前诊断的有效指征,该项检查可明显提升染色体异常检出率[11]。另在分子生物学技术与常规染色体核型分析等共同作用下,可有效提高产前遗传学异常检出率,有助于减少缺陷胎儿出生率[12,13]。此外,为了减少宫内感染导致的超声异常现象的发生,要求产妇于孕前行相关感染检测,一旦明确感染情况,则需立刻给予对症治疗[14,15]。
综上所述,产前超声检查能够有效检出胎儿异常,且其与染色体异常等因素间存在密切联系,在临床应用中需结合染色体核型分析与基因芯片检测,以提高胎儿发育异常检出率,从而改善妊娠结局,提高新生儿出生质量,并为临床遗传咨询等提供可靠信息。
