信迪利单抗联合射频消融治疗Ⅱa 期肝癌临床研究*
2023-03-30付彦爽陈晓丽付彦青
付彦爽,陈晓丽,付彦青
(1.河北省衡水市第三人民医院,河北 衡水 053000;2.河北省衡水市第六人民医院,河北 衡水 053000)
肝癌在我国常见恶性肿瘤中位列第4,肿瘤致死病因中位列第2,具有发病隐匿、恶性程度高、病死率高等特点,其中肝细胞癌占85%~90%[1-2]。早期肝癌患者的主要治疗方法有肝切除、射频消融(RFA)和原位肝移植,其中RFA 是将肿瘤组织加热至60 ℃以上,使其蛋白质变性、磷脂双层分子结构破坏,从而促进肿瘤细胞死亡[3-4]。但RFA 对直径超过3 cm 的肿瘤组织效果有限,这是由于大肝癌常临近大血管,在RFA 治疗中血流会出现明显的“热沉效应”,导致疗效降低,WANG 等[5]认为,多次RFA 治疗或联合其他治疗方案可保证疗效。免疫检查点抑制剂是通过阻断抑制剂检查点与配体之间的作用,解除免疫抑制,激活免疫细胞,从而产生抗肿瘤作用[6],其对肝癌有明显疗效。目前,信迪利单抗联合RFA 的疗效还未在Ⅱa 期肝癌中得到证实,本研究中对此进行了探讨。现报道如下。
1 资料与方法
1.1 一般资料
纳入标准:符合原发性肝癌诊断标准[7],并经实验室生化指标、超声影像学或组织病理学确诊;病理分期为Ⅱa 期;年龄18~75 岁。本研究经衡水市医院医学伦理委员会批准,患者及其家属签署知情同意书。
排除标准:原发性肝癌转移;接受过肝癌手术、化学药物治疗;合并严重心、脑、肾等重要器官疾病;认知功能障碍;对本研究中拟用药物有禁忌或过敏;拒绝接受本研究方案。
病例选择与分组:选取衡水市第三人民医院2020年6 月至2021 年12 月收治的Ⅱa 期肝癌患者102 例,按随机数字表法分为对照组和观察组,各51例。两组患者一般资料比较,差异无统计学意义(P >0.05),具有可比性。详见表1。
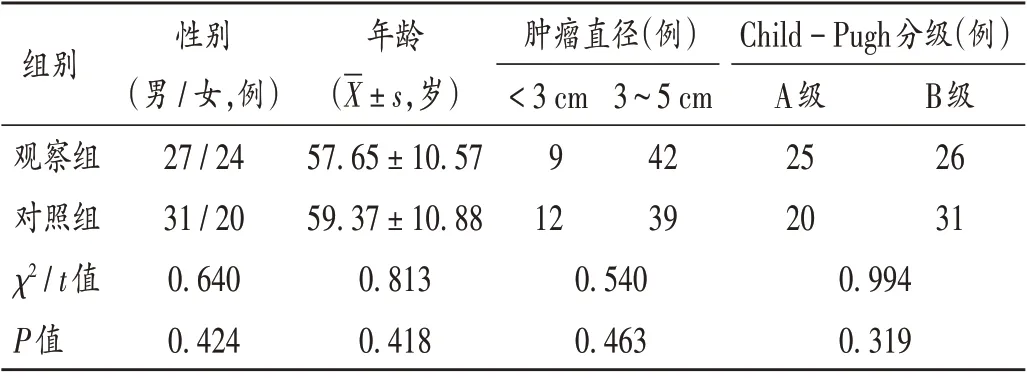
表1 两组患者一般资料比较(n=51)Tab.1 Comparison of the patients' general data between the two groups(n=51)
1.2 方法
两组患者均予RFA治疗,治疗前12 h禁食禁饮,静脉麻醉后,在彩色超声引导下行穿刺。根据肿瘤大小确定消融布针及点数。治疗初始功率为50 W,间隔1 min 升高10~100 W,阻抗明显上升、输出功率自动降至10 W以下则该点位结束。尽量达到0.5 cm 的周围正常肝组织完全热凝坏死。结束出针时通过针道凝血,以免针道出血或肿瘤种植。治疗结束后30 min 造影,观察射频消融区,确定消融完全后结束治疗。观察组患者加用信迪利单抗注射液(信达生物制药<苏州>有限公司,国药准字S20180016,规格为每瓶100 mL∶100 mg)200 mg 静脉输注。以3 周为1 个治疗周期,每6 周评估1 次疗效。两组患者均治疗6个月。
1.3 观察指标与疗效判定标准
免疫功能:采用流式细胞仪检测T 淋巴细胞CD4+,CD8+,计算CD4+/CD8+并检测CD4+CD25+FOXP3+Treg。
肿瘤标志物:采集治疗前后患者空腹静脉血,采用放射免疫分析法检测甲胎蛋白(AFP)、糖类抗原199(CA199)、细胞角蛋白19片段抗原21-1(CYFRA21-1)水平。
生活质量:采用健康调查简表(SF-36)[8]评估,包括躯体功能、躯体角色、身体疼痛、总健康状况、生命力、社会功能、情绪角色和心理健康,各领域条目之和为粗分,采用极差变换法换算为百分制,分值越高表明生活质量越好。
疗效判定[9]:完全缓解(CR),肿瘤病灶完全消失,至少维持1个月;部分缓解(PR),病灶缩小50%,至少维持1个月;病变稳定(SD),病灶缩小不超过50%,增大不超过25%,且无新肿瘤病灶出现;病变进展(PD),病灶无缩小,或增大超过25%,或有新肿瘤病灶出现。客观缓解(OR)=CR+PR,疾病控制(DC)=CR+PR+SD。
药品不良反应:根据常见药品不良反应事件评价标准4.0 版本(CTCAE v 4.0)评价患者白细胞减少、乏力、皮疹、转氨酶升高、甲状腺功能减退等发生情况。
1.4 统计学处理
2 结果
结果见表2至表6。

表2 两组患者临床疗效比较[例(%),n=51]Tab.2 Comparison of clinical efficacy between the two groups[case(%),n=51]
表3 两组患者免疫功能指标比较(±s,n=51)Tab.3 Comparison of immune function indexes between the two groups(±s,n=51)
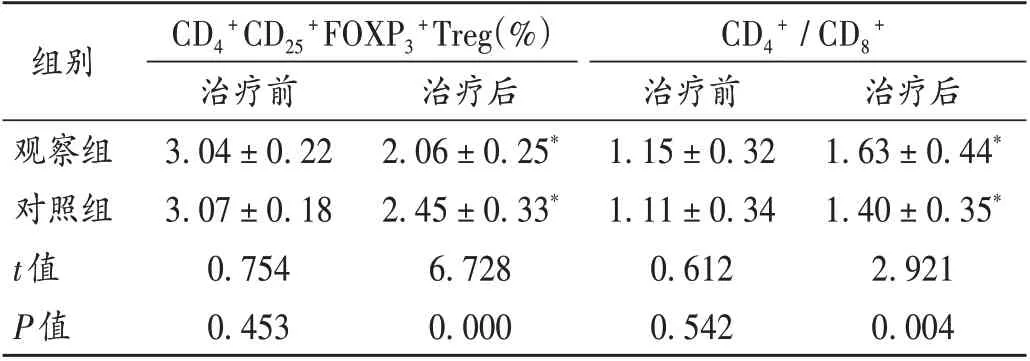
表3 两组患者免疫功能指标比较(±s,n=51)Tab.3 Comparison of immune function indexes between the two groups(±s,n=51)
注:与本组治疗前比较,*P <0.05。表4和表5同。Note:Compared with those before treatment,*P < 0.05 (for Tab.3-5).
+组别观察组对照组t值P值CD4+CD25+FOXP3+Treg(%)CD4+ /CD8治疗后1.63±0.44*1.40±0.35*2.921 0.004治疗前3.04±0.22 3.07±0.18 0.754 0.453治疗后2.06±0.25*2.45±0.33*6.728 0.000治疗前1.15±0.32 1.11±0.34 0.612 0.542
表4 两组患者肿瘤标志物水平比较(±s,n=51)Tab.4 Comparison of tumor marker levels between the two groups(±s,n=51)
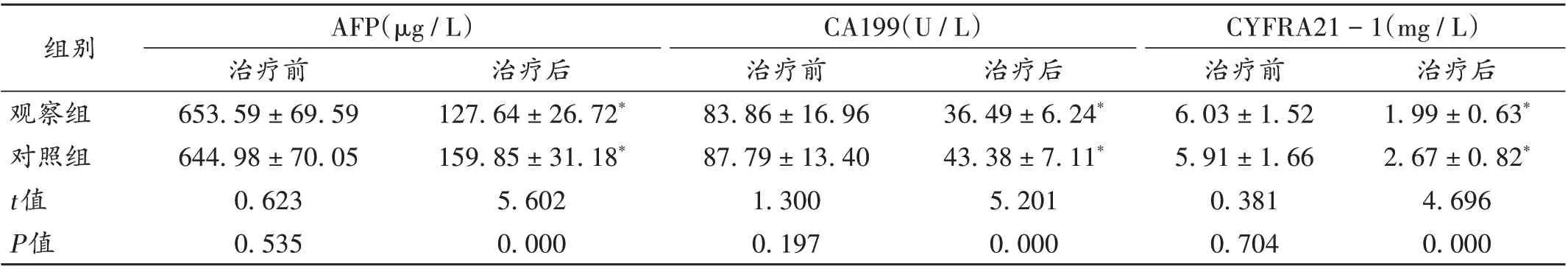
表4 两组患者肿瘤标志物水平比较(±s,n=51)Tab.4 Comparison of tumor marker levels between the two groups(±s,n=51)
组别观察组对照组t值P值AFP(µg/L)治疗前653.59±69.59 644.98±70.05 0.623 0.535治疗后127.64±26.72*159.85±31.18*5.602 0.000 CA199(U/L)治疗前83.86±16.96 87.79±13.40 1.300 0.197治疗后36.49±6.24*43.38±7.11*5.201 0.000 CYFRA21-1(mg/L)治疗前6.03±1.52 5.91±1.66 0.381 0.704治疗后1.99±0.63*2.67±0.82*4.696 0.000
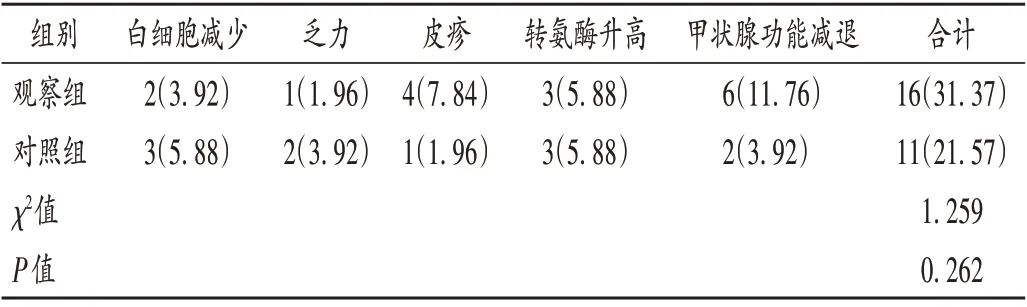
表6 两组患者不良反应发生情况比较[例(%),n=51]Tab.6 Comparison of the incidence of adverse drug reactions between the two groups[case(%),n=51]
表5 两组患者生活质量评分比较(±s,分,n=51)Tab.5 Comparison of quality of life scores between the two groups(±s,point,n=51)
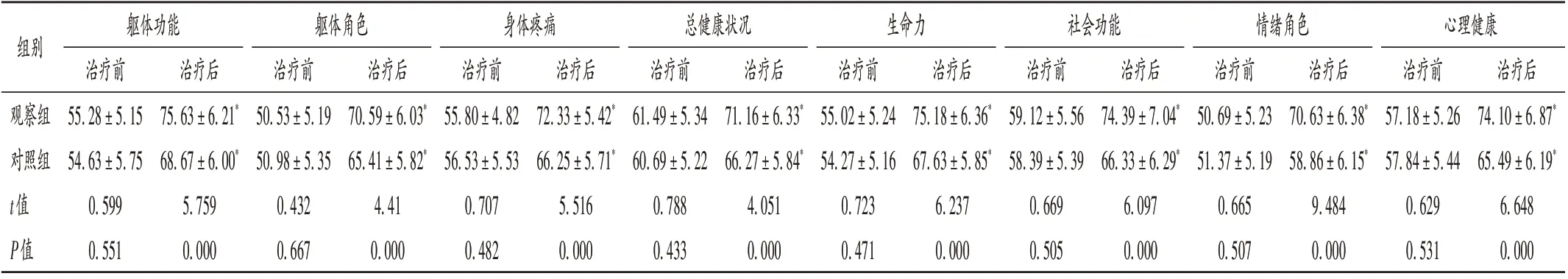
表5 两组患者生活质量评分比较(±s,分,n=51)Tab.5 Comparison of quality of life scores between the two groups(±s,point,n=51)
组别躯体功能治疗前55.28±5.15 54.63±5.75 0.599 0.551治疗后75.63±6.21*68.67±6.00*5.759 0.000躯体角色治疗前50.53±5.19 50.98±5.35 0.432 0.667治疗后70.59±6.03*65.41±5.82*4.41 0.000身体疼痛治疗前55.80±4.82 56.53±5.53 0.707 0.482治疗后72.33±5.42*66.25±5.71*5.516 0.000总健康状况治疗前61.49±5.34 60.69±5.22 0.788 0.433治疗后71.16±6.33*66.27±5.84*4.051 0.000生命力治疗前55.02±5.24 54.27±5.16 0.723 0.471治疗后75.18±6.36*67.63±5.85*6.237 0.000社会功能治疗前59.12±5.56 58.39±5.39 0.669 0.505治疗后74.39±7.04*66.33±6.29*6.097 0.000情绪角色治疗前50.69±5.23 51.37±5.19 0.665 0.507治疗后70.63±6.38*58.86±6.15*9.484 0.000观察组对照组t值P值心理健康治疗前57.18±5.26 57.84±5.44 0.629 0.531治疗后74.10±6.87*65.49±6.19*6.648 0.000
3 讨论
RFA 治疗是一种经皮微创手术,其利用高频率的射频电流杀死病灶区的肿瘤细胞,但其疗效欠佳,因此,为提高疗效仍需进一步杀灭体内的肿瘤细胞[10]。随免疫治疗被用于临床,以阻断免疫检查点蛋白程序性细胞死亡受体-1(PD-1)为靶点的免疫抑制剂疗效也逐渐被认可,信迪利单抗属靶向PD-1 单克隆抗体,其可与PD - 1 配体产生竞争作用,与PD - 1 进行竞争性结合,从而重新激活淋巴细胞的抗肿瘤作用,进而达到治疗肿瘤的目的[11-12]。本研究结果显示,观察组客观缓解率和疾病控制率均优于对照组,提示联合治疗可提高Ⅱa期肝癌临床疗效。
Treg会影响肿瘤细胞的免疫逃逸和导致免疫耐受,与多种肿瘤的发生和进展密切相关,在肿瘤患者的外周血和肿瘤组织中呈高表达[13];肿瘤产生免疫耐受的重要机制是肿瘤诱导的CD4+CD25+Treg 细胞增多,FOXP3 是叉头翼状螺旋转录因子家族的一员,在肿瘤逃逸中发挥重要作用,是Treg 发育过程中的重要因子,因此CD4+CD25+FOXP3+Treg 可用于评估肿瘤的进展情况[14]。CD4+/ CD8+可反映机体细胞免疫功能,数值越低表明恶性肿瘤发生风险越高[15]。本研究结果显示,观察组治疗后CD4+/ CD8+明显高于对照组,CD4+CD25+FOXP3+Treg 水平明显低于对照组,提示联合治疗可改善患者免疫功能,与何斯怡等[16]的研究结果一致。AFP 属胎儿肝脏合成糖蛋白,其水平升高一般可见于肝癌、胃癌等恶性肿瘤机体,是肝癌诊断的标志物之一;CA199 为糖类蛋白肿瘤标志物,在肝癌中呈高表达[17];CYFRA21- 1 是细胞角蛋白19 可溶性片段之一,在癌变细胞中,细胞角蛋白可促进CYFRA21-1 表达,从而参与肿瘤细胞的增殖、转移等[18]。本研究结果显示,观察组患者治疗后的AFP,CA199,CYFRA21- 1水平均明显低于对照组,提示联合治疗可降低患者血清肿瘤标志物水平,原因为信迪利单抗可通过激活机体免疫功能,使T 淋巴细胞恢复抗肿瘤效应,降低肿瘤标志物水平[19]。两组不良反应发生率无明显差异,提示信迪利单抗联合RFA 治疗方案具有一定安全性。本研究中发生的不良反应多为1 级和2 级,短期停药或减少剂量均可缓解,不良反应可控。信迪利单抗的不良反应涉及血液、肝、胆等,这与信迪利单抗作用的免疫系统相关[20]。生活质量可反映患者最直接的感受,现已成为评估肿瘤治疗效果的重要组成部分[21]。观察组患者治疗后的SF - 36 各领域生活质量评分均明显高于对照组,提示信迪利单抗联合RFA 治疗可提升患者的生活质量。
综上所述,信迪利单抗联合RFA 治疗Ⅱa 期肝癌疗效较好,可有效改善免疫功能(如CD4+/ CD8+,CD4+CD25+FOXP3+Treg 水平)和肿瘤标志物水平,提升患者的生活质量。
