降脂颗粒联合生活方式干预治疗湿热蕴结型非酒精性脂肪性肝病的临床观察
2023-03-26舒祥兵赵燕婷杨志新
舒祥兵,赵燕婷,杨志新
上海市宝山区中西医结合医院(上海 201999)
非酒精性脂肪性肝病(non-alcoholic fatty liver disease,NAFLD)是一种除外酒精、病毒、药物等其他病理因素引起的以肝细胞脂质堆积和大泡性脂肪变性为主的病理综合征[1]。随着肥胖和代谢综合征在世界范围内的流行,NAFLD的发病率逐年上升,目前已经取代病毒性肝炎成为最常见的慢性肝脏疾病[2]。我国成人NAFLD的发病率约为30%,部分患者会进展为肝纤维化/肝硬化、肝细胞肝癌等终末期肝病,此外,NAFLD与心血管疾病、慢性肾脏疾病、结肠癌、代谢性肿瘤等疾病的发生密切相关[3-4]。本病的发病机制尚不十分明确,越来越流行的“多重打击”学说认为胆汁酸代谢紊乱与肠道菌群、氧化应激、铁超载等多重因素共同促进了NAFLD的进展[5]。遗憾的是目前尚未有明确有效的治疗药物,生活方式干预是针对NAFLD的基础治疗手段[6]。
上海中医药大学附属龙华医院脾胃病研究所季光教授团队前期通过流行病学调查和数据挖据技术,认为湿热蕴结是NAFLD的主要证候,并研发了具有清热利湿作用的中药复方降脂颗粒,对NAFLD安全有效[7]。前期动物研究[8]发现,降脂颗粒能调节模型小鼠的胆汁酸代谢。因此,我们采用降脂颗粒联合生活方式干预治疗湿热蕴结型NAFLD,并观察其对胆汁酸代谢的影响。现将结果报道如下。
1 资料与方法
1.1 病例选择
1.1.1 诊断标准 NAFLD的诊断符合《非酒精性脂肪性肝病防治指南(2018年更新版)》[9]中的有关标准。中医湿热蕴结证的诊断参照《非酒精性脂肪性肝病中西医结合诊疗共识意见(2017年)》[10]中的有关内容:主症包括右胁肋部胀痛、周身困重、脘腹胀满或疼痛、大便黏腻不爽、舌红、舌苔黄腻,次症包括身目发黄、小便色黄、口中黏滞、口干口苦、脉弦滑或濡数,符合主症1项,次症2项即可诊断。
1.1.2 纳入标准 ①符合上述疾病及中医证候诊断标准;②年龄18~65岁;③体质量指数(BMI)在20~30 kg·m-2之间;④入组前1个月未服用过降脂、保肝、降糖等对NAFLD有治疗作用的药物;⑤自愿参加本研究,并签订知情同意书。
1.1.3 排除标准 ①合并病毒性肝炎、自身免疫性肝病、酒精性肝病、遗传性肝病者;②肝功能显著异常,丙氨酸转氨酶(ALT)或天冬氨酸转氨酶(AST)≥正常上限值1.5倍者;③血清肌酐≥正常上限值者;④糖尿病患者;⑤需要服用他汀类、贝特类等降脂药物者;⑥合并严重的心、脑、肾、内分泌、血液以及代谢系统疾病者;⑦有本研究涉及药物(或同类药物)过敏史者;⑧研究者认为存在不适合作为研究对象的其他因素者。
1.1.4 脱落与剔除标准 ①试验期间出现严重不良反应或事件,无法继续进行试验者;②依从性差,未按既定方案进行治疗者;③不符合纳入标准,误纳入者;④疾病加重或者出现其他严重疾病,需要进行相关治疗者;⑤失访,或其他任何原因导致试验资料不全,影响疗效及安全性判定者。
1.2 一般资料 本研究共收集90例病例,均为2021年5月至2022年4月上海市宝山区中西医结合医院老年病科和健康管理中心诊治的湿热蕴结型NAFLD患者,采用随机数字表法分为2组,每组45例。本研究经上海市宝山区中西医结合医院医学伦理委员会批准(批件号:202014)。
1.3 治疗方法
1.3.1 对照组 采用单纯生活方式干预进行治疗,包括饮食结构的调整(限热卡饮食,适当增加膳食纤维摄入,减少高热量和高饱和脂肪酸食物的摄入)和坚持有氧运动(每周至少3次,30 min/次)。连续治疗16周。
1.3.2 治疗组 在单纯生活方式干预的基础上加用降脂颗粒。药物组成:绞股蓝15 g,虎杖15 g,丹参9 g,茵陈9 g,荷叶6 g。1剂/d,由上海市宝山区中西医结合医院中药房加工成水煎剂,分装成2袋,100 mL/袋,早晚餐后各服1袋。连续治疗16周。
市政府发布《上海市取水许可和水资源费征收管理实施办法》,明确市取水总量控制指标控制管理。《上海市地面沉降管理条例》的出台,进一步强化了地下水管理。市水务局印发《上海市取水设施现场核验规定》《上海市取水口标识管理规定》《关于上海市实施建设项目水资源论证分类管理通知》《上海市工业区块规划水资源论证管理办法(试行)》,编制完成《上海市取水许可审批手册》,有效促进取水管理工作有章可循。
1.4 观察项目与方法
1.4.1 一般情况 分别于治疗前后测量所有患者的身高、体质量,并据此计算BMI。
1.4.2 肝脏超声疗效 治疗前后所有患者均行肝脏超声检查,并于治疗后参照《非酒精性脂肪性肝病中医诊疗专家共识意见(2017)》[11]中的有关内容判定肝脏超声疗效。①痊愈:无脂肪肝声像;②显效:脂肪肝等级下降2级;③有效:脂肪肝等级下降1级;④无效:脂肪肝等级无变化或更严重。
1.4.3 中医证候积分 治疗前后,参照文献[10]中的有关内容,采用计分法评价患者的中医证候。主症按正常、轻度、中度、重度分别计为0、2、4、6分,次症按正常、轻度、中度、重度分别计为0、1、2、3分,主症、次症内容见“1.1.1”项下。
1.4.4 实验室指标 治疗前后检测所有患者的血脂相关指标[(总胆固醇(TC)、三酰甘油(TG)、高密度脂蛋白胆固醇(HDL-C)、低密度脂蛋白胆固醇(LDL-C)],以及尿液、血清胆汁酸代谢相关指标。胆汁酸代谢相关指标包括总胆汁酸(TBA)、胆汁酸代谢亚型[胆酸(CA)、甘氨胆酸(GCA)、猪胆酸(HCA)、熊去氧胆酸(UDCA)、甘氨熊去氧胆酸(GUDCA)、甘氨鹅去氧胆酸(GCDCA)、鹅去氧胆酸(CDCA)、α-鼠胆酸(α-MCA)、甘氨猪胆酸(GHCA)、牛磺胆酸(TCA)、脱氧胆酸(DCA)、石胆酸(LCA)、甘氨脱氧胆酸(GDCA)、甘氨石胆酸(GLCA)、牛磺-β-鼠胆酸(T-β-MCA)]。
1.4.5 安全性评价 观察并记录试验期间两组患者不良反应的发生情况。
2 结果
2.1 试验完成情况及一般资料比较 试验期间,治疗组脱落2例(1例因不能完成疗程主动退出,1例因不能按时随访主动退出),对照组脱落4例(3例因不能按时随访主动退出,1例失访),最终完成试验者84例,其中治疗组43例、对照组41例。两组性别、年龄、身高、体质量、BMI比较,差异无统计学意义(P>0.05),具有可比性。见表1。
表1 两组一般资料比较(±s)
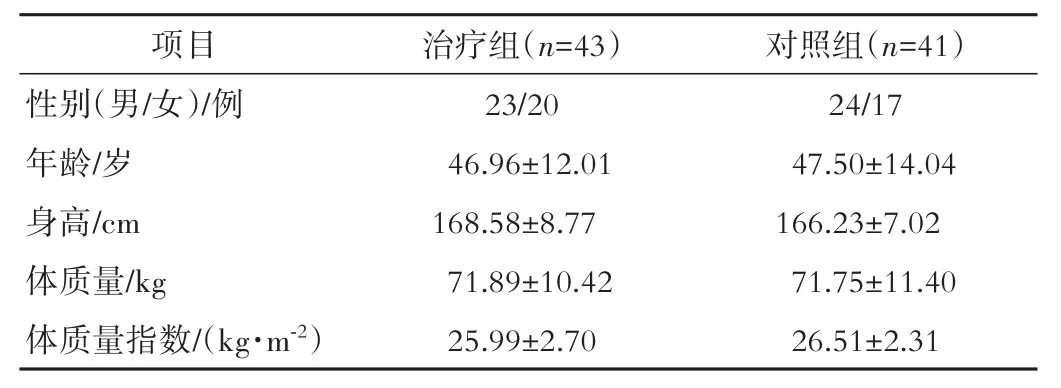
表1 两组一般资料比较(±s)
项目性别(男/女)/例年龄/岁身高/cm体质量/kg体质量指数/(kg·m-2)治疗组(n=43)23/20 46.96±12.01 168.58±8.77 71.89±10.42 25.99±2.70对照组(n=41)24/17 47.50±14.04 166.23±7.02 71.75±11.40 26.51±2.31
2.2 肝脏超声疗效比较 治疗组、对照组肝脏超声总有效率分别为62.8%、36.6%;两组肝脏超声疗效比较,治疗组优于对照组(P<0.05)。见表2。
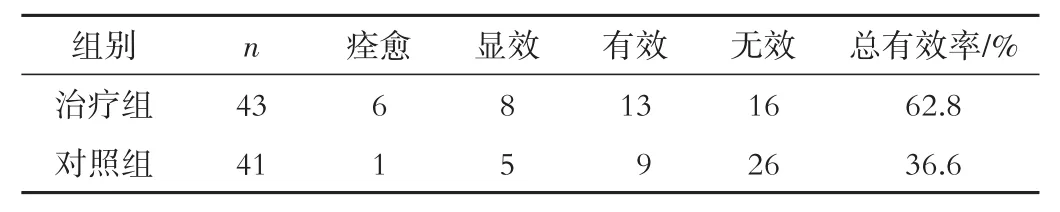
表2 两组肝脏超声疗效比较(例)
2.3 中医证候积分、体质量、BMI变化情况 治疗前后组内比较,治疗组中医证候积分减少,体质量、体质量指数降低(P<0.05),对照组仅中医证候积分减少(P<0.05)。组间治疗后比较,治疗组中医证候积分少于对照组,体质量指数低于对照组(P<0.05)。见表3。
表3 两组中医证候积分、体质量、体质量指数变化情况比较(±s)
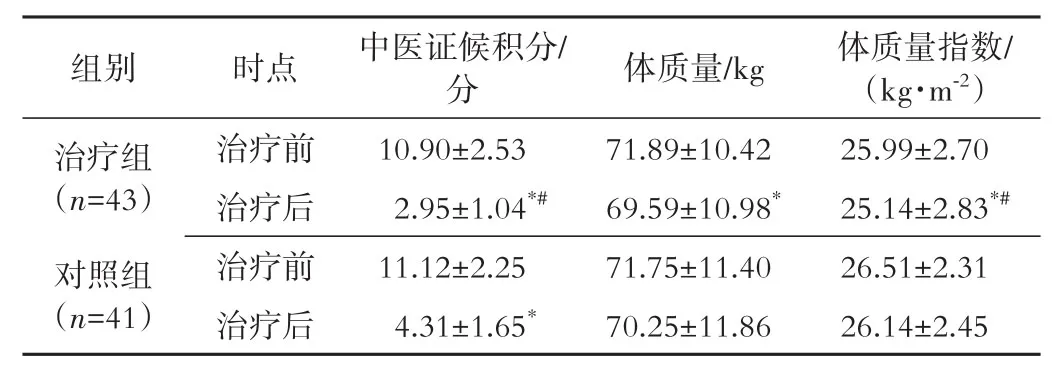
表3 两组中医证候积分、体质量、体质量指数变化情况比较(±s)
注:与本组治疗前比较,*P<0.05;与对照组治疗后比较,#P<0.05。
组别治疗组(n=43)对照组(n=41)时点治疗前治疗后治疗前治疗后中医证候积分/分10.90±2.53 2.95±1.04*#11.12±2.25 4.31±1.65*体质量/kg 71.89±10.42 69.59±10.98*71.75±11.40 70.25±11.86体质量指数/(kg·m-2)25.99±2.70 25.14±2.83*#26.51±2.31 26.14±2.45
2.4 实验室相关指标变化情况
2.4.1 血脂相关指标 治疗前后组内比较,治疗组血清TC、TG水平降低(P<0.05),对照组血清TG水平降低(P<0.05)。组间治疗后比较,血清TC、TG、HDL-C、LDL-C水平差异无统计学意义(P>0.05)。见表4。
表4 两组血脂相关指标水平变化情况比较(±s,mmol·L-1)
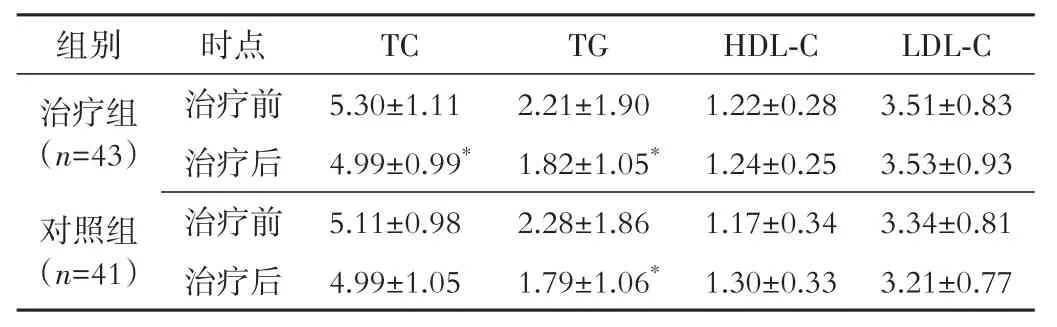
表4 两组血脂相关指标水平变化情况比较(±s,mmol·L-1)
注:TC为总胆固醇,TG为三酰甘油,HDL⁃C为高密度脂蛋白胆固醇,LDL⁃C为低密度脂蛋白胆固醇。与本组治疗前比较,*P<0.05。
LDL-C 3.51±0.83 3.53±0.93 3.34±0.81 3.21±0.77组别治疗组(n=43)对照组(n=41)时点治疗前治疗后治疗前治疗后TC 5.30±1.11 4.99±0.99*5.11±0.98 4.99±1.05 TG 2.21±1.90 1.82±1.05*2.28±1.86 1.79±1.06*HDL-C 1.22±0.28 1.24±0.25 1.17±0.34 1.30±0.33
2.4.2 胆汁酸代谢相关指标 (1)血清。治疗前后组内比较,两组血清TBA水平均降低(P<0.05)。组间治疗后比较,治疗组血清TBA水平低于对照组(P<0.05)。进一步分析两组血清胆汁酸亚型。治疗前后组内比较,治疗组血清初级胆汁酸部分指标(CA、GCA、HCA、UDCA、GUDCA、GCDCA、CDCA)和次级胆汁酸部分指标(DCA、GDCA)水平降低(P<0.05),对照组血清初级胆汁酸部分指标(CA、GCA、UDCA、GCDCA、CDCA)和次级胆汁酸部分指标(DCA、GDCA)水平降低(P<0.05)。组间治疗后比较,治疗组初级胆汁酸部分指标(CA、HCA、UDCA、GUDCA、GCDCA)和次级胆汁酸部分指标(DCA、GDCA)水平低于对照组(P<0.05)。见表5。
表5 两组血清胆汁酸代谢相关指标水平变化情况比较(±s,μg·L-1)
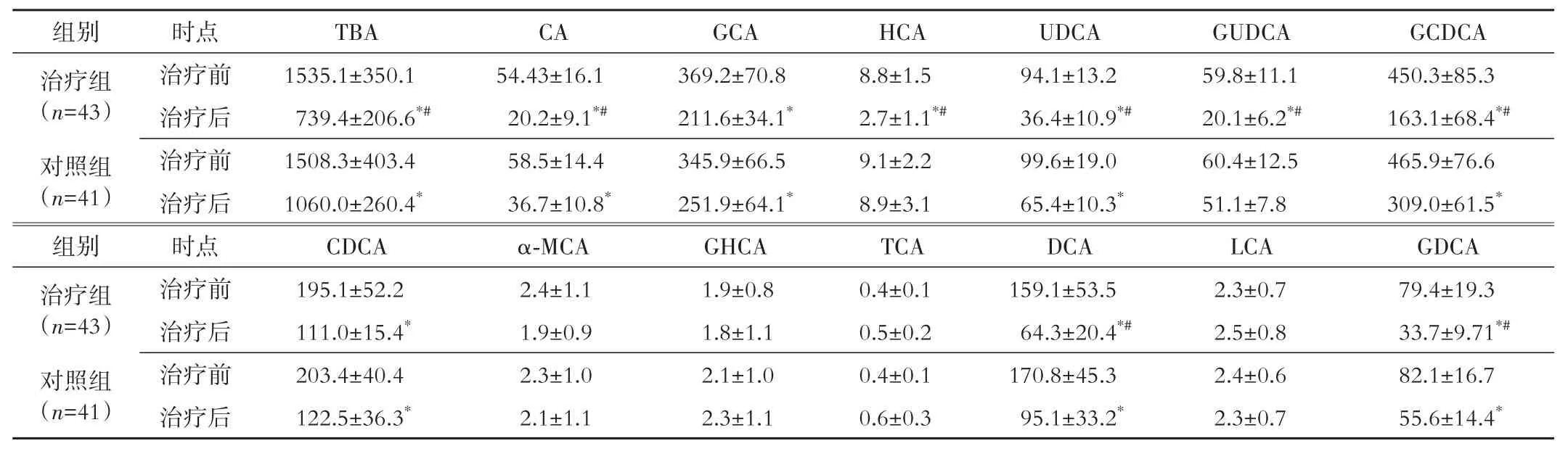
表5 两组血清胆汁酸代谢相关指标水平变化情况比较(±s,μg·L-1)
注:TBA为总胆汁酸,CA为胆酸,GCA为甘氨胆酸,HCA为猪胆酸,UDCA为熊去氧胆酸,GUDCA为甘氨熊去氧胆酸,GCDCA为甘氨鹅去氧胆酸,CDCA为鹅去氧胆酸,α⁃MCA为α⁃鼠胆酸,GHCA为甘氨猪胆酸,TCA为牛磺胆酸,DCA为脱氧胆酸,LCA为石胆酸,GDCA为甘氨脱氧胆酸。与本组治疗前比较,*P<0.05;与对照组治疗后比较,#P<0.05。
GCDCA 450.3±85.3 163.1±68.4*#465.9±76.6 309.0±61.5*GDCA 79.4±19.3 33.7±9.71*#82.1±16.7 55.6±14.4*组别治疗组(n=43)对照组(n=41)组别治疗组(n=43)对照组(n=41)时点治疗前治疗后治疗前治疗后时点治疗前治疗后治疗前治疗后TBA 1535.1±350.1 739.4±206.6*#1508.3±403.4 1060.0±260.4*CDCA 195.1±52.2 111.0±15.4*203.4±40.4 122.5±36.3*CA 54.43±16.1 20.2±9.1*#58.5±14.4 36.7±10.8*α-MCA 2.4±1.1 1.9±0.9 2.3±1.0 2.1±1.1 GCA 369.2±70.8 211.6±34.1*345.9±66.5 251.9±64.1*GHCA 1.9±0.8 1.8±1.1 2.1±1.0 2.3±1.1 HCA 8.8±1.5 2.7±1.1*#9.1±2.2 8.9±3.1 TCA 0.4±0.1 0.5±0.2 0.4±0.1 0.6±0.3 UDCA 94.1±13.2 36.4±10.9*#99.6±19.0 65.4±10.3*DCA 159.1±53.5 64.3±20.4*#170.8±45.3 95.1±33.2*GUDCA 59.8±11.1 20.1±6.2*#60.4±12.5 51.1±7.8 LCA 2.3±0.7 2.5±0.8 2.4±0.6 2.3±0.7
(2)尿液。治疗前后组内比较,治疗组尿液TBA水平升高(P<0.05),对照组尿液TBA水平无明显变化(P>0.05);组间治疗后比较,治疗组尿液TBA水平高于对照组(P<0.05)。进一步分析两组尿液胆汁酸亚型。治疗前后组内比较,治疗组尿液初级胆汁酸部分指标(CA、α-MCA、T-β-MCA、CDCA、UDCA)和次级胆汁酸部分指标(DCA、GDCA)水平升高(P<0.05),对照组尿液初级胆汁酸部分指标(CA、α-MCA、T-β-MCA、CDCA)和次级胆汁酸部分指标(DCA、GDCA)水平升高(P<0.05)。组间治疗后比较,治疗组尿液初级胆汁酸部分指标(CA、T-β-MCA、CDCA、UDCA)和次级胆汁酸部分指标(DCA、GDCA)水平高于对照组(P<0.05)。见表6。
表6 两组尿液胆汁酸代谢相关指标水平变化情况(±s,μg·L-1)
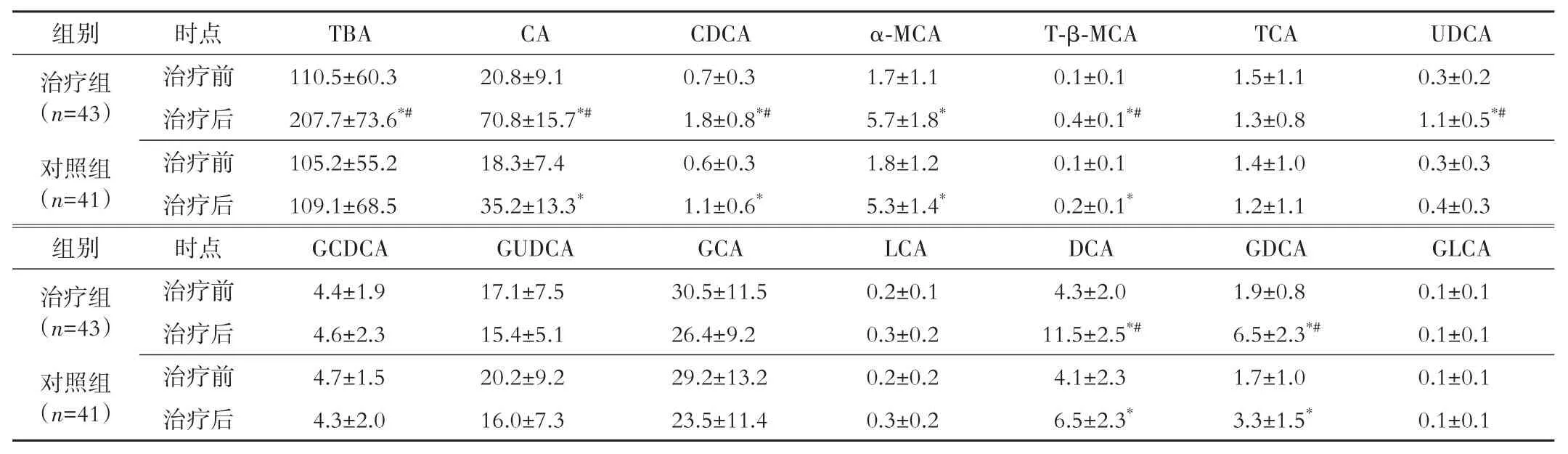
表6 两组尿液胆汁酸代谢相关指标水平变化情况(±s,μg·L-1)
注:TBA为总胆汁酸,CA为胆酸,CDCA为鹅去氧胆酸,α⁃MCA为α⁃鼠胆酸,T⁃β⁃MCA为牛磺β⁃鼠胆酸,TCA为牛磺胆酸,UDCA为熊去氧胆酸,GCDCA为甘氨鹅去氧胆酸,GUDCA为甘氨熊去氧胆酸,GCA为甘氨胆酸,LCA为石胆酸,DCA为脱氧胆酸,GDCA为甘氨脱氧胆酸,GLCA为甘氨石胆酸。与本组治疗前比较,*P<0.05;与对照组治疗后比较,#P<0.05。
UDCA 0.3±0.2 1.1±0.5*#0.3±0.3 0.4±0.3 GLCA 0.1±0.1 0.1±0.1 0.1±0.1 0.1±0.1组别治疗组(n=43)对照组(n=41)组别治疗组(n=43)对照组(n=41)时点治疗前治疗后治疗前治疗后时点治疗前治疗后治疗前治疗后TBA 110.5±60.3 207.7±73.6*#105.2±55.2 109.1±68.5 GCDCA 4.4±1.9 4.6±2.3 4.7±1.5 4.3±2.0 CA 20.8±9.1 70.8±15.7*#18.3±7.4 35.2±13.3*GUDCA 17.1±7.5 15.4±5.1 20.2±9.2 16.0±7.3 CDCA 0.7±0.3 1.8±0.8*#0.6±0.3 1.1±0.6*GCA 30.5±11.5 26.4±9.2 29.2±13.2 23.5±11.4 α-MCA 1.7±1.1 5.7±1.8*1.8±1.2 5.3±1.4*LCA 0.2±0.1 0.3±0.2 0.2±0.2 0.3±0.2 T-β-MCA 0.1±0.1 0.4±0.1*#0.1±0.1 0.2±0.1*DCA 4.3±2.0 11.5±2.5*#4.1±2.3 6.5±2.3*TCA 1.5±1.1 1.3±0.8 1.4±1.0 1.2±1.1 GDCA 1.9±0.8 6.5±2.3*#1.7±1.0 3.3±1.5*
2.5 安全性评价 试验期间,治疗组出现大便溏稀2例,轻微胃部不适1例,不良反应发生率为6.66%;对照组出现轻度疲劳2例,轻微胃部不适1例,轻微头晕1例,不良反应发生率为8.88%。上述均为轻微不良反应。两组不良反应发生率比较,差异无统计学意义(P>0.05)。
3 讨论
NAFLD是一种由肝细胞脂肪变性引起的慢性疾病,其发病机制尚未完全阐明,随着研究的深入,“多重打击”假说逐渐被业内认可。该假说认为,多重损害共同影响NAFLD的发生和发展,如肠道菌群失调、胆汁酸代谢失衡[12]。胆汁酸的代谢过程相对复杂,肝脏内初级胆汁酸由胆固醇氧化而来,其中约5%的肝脏胆汁酸直接进入外周循环系统,通过肾脏以尿液的形式排出体外,约95%的肝脏胆汁酸进入肠道以促进食物的消化和吸收,在肠道微生物和胆盐水解酶等的作用下初级胆汁酸转化成次级胆汁酸,再通过“肠肝循环”的重吸收回肝脏,少数以粪便的形式排出体外[13]。越来越多的证据表明,胆汁酸代谢除了能够调节脂类的消化和吸收以外,还会影响机体系统性炎症和糖脂代谢[14]。NAFLD患者血清和肝脏中的初级和次级胆汁酸水平明显高于正常健康人群[15-16],且部分胆汁酸代谢指标(GCDCA、TCDCA、GUDCA)与NAFLD的严重程度呈正相关[17-18]。随着疾病的进展,单纯性脂肪肝和脂肪性肝炎患者的粪便初级胆汁酸水平逐渐上升,次级胆汁酸水平逐渐下降[19],但关于NAFLD患者尿液胆汁酸代谢水平的研究较少[20],文献质量也不高,有待进一步研究。因此,调节胆汁酸代谢是NAFLD治疗的潜在靶点,近年来靶向胆汁酸代谢的临床药物研究逐步展开,如奥贝胆酸[21]。
上海中医药大学附属龙华医院脾胃病研究所季光教授团队通过长期研究和临床实践[22],研发出中药复方降脂颗粒(由绞股蓝15 g、虎杖15 g、丹参9 g、茵陈9 g、荷叶6 g组成),治疗NAFLD疗效满意。本研究采用降脂颗粒联合生活方式干预治疗湿热蕴结型NAFLD,观察其临床疗效及对胆汁酸代谢的影响。
本研究结果显示,治疗组肝脏超声疗效优于对照组(P<0.05),其能更好地改善患者的临床症状、降低血清TC、TG水平(P<0.05)。在血清胆汁酸代谢相关指标方面,经治疗,治疗组血清TBA、初级胆汁酸部分指标(CA、GCA、HCA、UDCA、GUDCA、GCDCA、CDCA)和次级胆汁酸部分指标(DCA、GDCA)水平降低(P<0.05),且血清TBA、初级胆汁酸部分指标(CA、HCA、UDCA、GUDCA、GCDCA)和次级胆汁酸部分指标(DCA、GDCA)水平低于对照组治疗后水平(P<0.05);在尿液胆汁酸代谢相关指标方面,经治疗,治疗组尿液TBA、初级胆汁酸部分指标(CA、αMCA、TβMCA、CDCA、UDCA)和次级胆汁酸部分指标(DCA、GDCA)水平升高(P<0.05),且尿液 TBA、初级胆汁酸部分指标(CA、TβMCA、CDCA、UDCA)和次级胆汁酸部分指标(DCA、GDCA)水平高于对照组治疗后水平(P<0.05)。
本研究结果提示,降脂颗粒联合生活方式干预治疗湿热蕴结型NAFLD疗效满意,可有效改善患者的临床症状,调节血脂水平,其机制可能与降低血清胆汁酸水平,促进胆汁酸从尿液排泄,进而维持胆汁酸代谢稳态有关。
