HPLC法测定人血浆中万古霉素的血药浓度
2023-03-24杨杰李兰林
杨杰,李兰林
万古霉素(vancomycin)是一种三环糖肽类抗生素,对革兰阳性球菌抗菌作用强,特别是目前临床上较棘手的严重耐药金黄色葡萄球菌和表皮葡萄球菌所致的感染有较好的疗效[1]。万古霉素于1958年被批准用于临床,因其在严重感染中具有重要地位,因此,万古霉素曾被誉为“人类对付难治性耐药菌株的最后一道防线”,通常在其他抗菌药物无效时才应用[2]。其主要的给药方式是静脉给药,90%以上由肾脏排泄,万古霉素的抑菌机制之一是通过其七肽骨架与细菌细胞壁糖蛋白合成启动子——胞壁酰五肽的末端二肽片段D-Ala-D-Lac形成5个氢键抑制细菌细胞壁的生长,导致细胞凋亡[3]。随着万古霉素的大量使用,不良反应时有发生。万古霉素服用量较大,肾功能不全或老年患者更易发生耳肾毒性,因此,需要通过监测万古霉素的血药浓度实现个体化给药方案,提高MRSA等革兰阳性球菌感染的治愈率,减少药物不良反应[4-5]。
目前国内外对万古霉素的血药浓度监测多采用免疫检测法、微生物法及高效液相色谱法(HPLC)等。免疫检测法试剂盒较昂贵,需集中标本后检测,专属性较差,测量结果偏高,且FPID购置仪器费用较高,受专用试剂供应限制,因此,限制了其在临床应用[6-7]。微生物检测法是利用抗菌药物在琼脂培养基内的扩散作用,比较标准品与供试品两者对接种的试验菌产生抑菌圈的大小,以检测供试品效价的一种测试方法。微生物法因步骤繁琐、耗时长而较少使用[8]。HPLC测定万古霉素血药浓度多采用内标法,但内标法操作步骤较繁琐,同时由于内标物的不稳定性,检测过程中需不断地配制内标。本实验通过建立了一种外标法定量测定血清中万古霉素浓度的HPLC,该法简便、准确、快速,适用于万古霉素血药浓度的监测和药动学研究。现报道如下。
1 实验材料
1.1 试剂 乙腈(色谱纯,天津市科密欧化学试剂有限公司生产,批号:20140101);磷酸二氢钾(分析纯,广东光华科技股份有限公司生产,批号:20111129);三氯醋酸(分析纯,湖南汇虹试剂有限公司生产,批号:20140623);磷酸(色谱纯,上海士锋生物科技有限公司生产,批号:T13200-500);灭菌注射用水(安徽双鹤药业有限责任公司生产,批号:k17062107);万古霉素标准品(中国药品生物制品检定所生产,批号:130338-200303)。
1.2 仪器与设备 HITACHI高效液相色谱仪(日立高新技术公司生产);AJXDC-10氮气吹扫仪(上海净信实业发展有限公司生产);FA114A电子天平(万分之一,上海海康电子仪器厂生产);雷磁PHS-3C型pH计(上海仪电科学仪器股份有限公司生产);TDL-80-2B低速台式离心机(上海安亭科学仪器生产);HMS-350涡旋震荡器(天津市威仪科技发展有限公司生产);Lenovo微型计算机(新圆梦F2028,北京联想有限公司生产);微量进样器MC20 μl(上海安亭微量进样器厂生产)。
2 实验方法选择
2.1 流动相的考察 本实验结合彭芳辰等[9]、林玉仙等[10]文献,分别考察了如下流动相的分离效果:16%甲醇:84%磷酸二氢钾(pH 3.2);91%邻苯二甲酸氢钾:9%乙腈;91%磷酸二氢钾:9%乙腈(pH 3.2)。最终选择流动相为91%磷酸二氢钾:9%乙腈(pH 3.22)。峰型良好,且无杂质峰干扰。色谱图见图1-3。
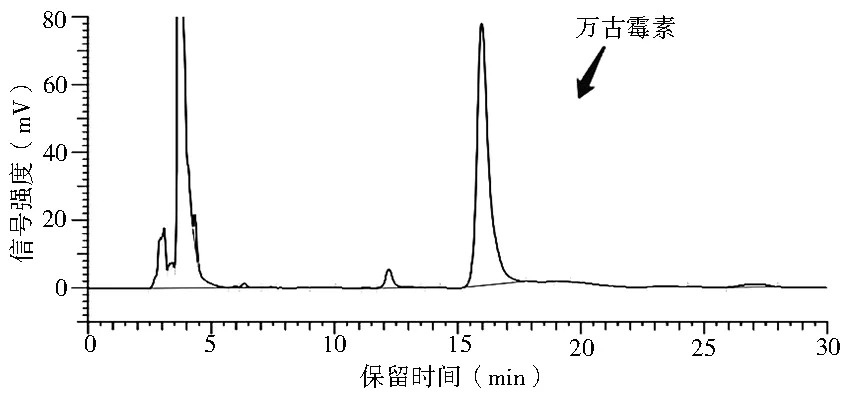
图1 16%甲醇:84%磷酸二氢钾(pH 3.2)
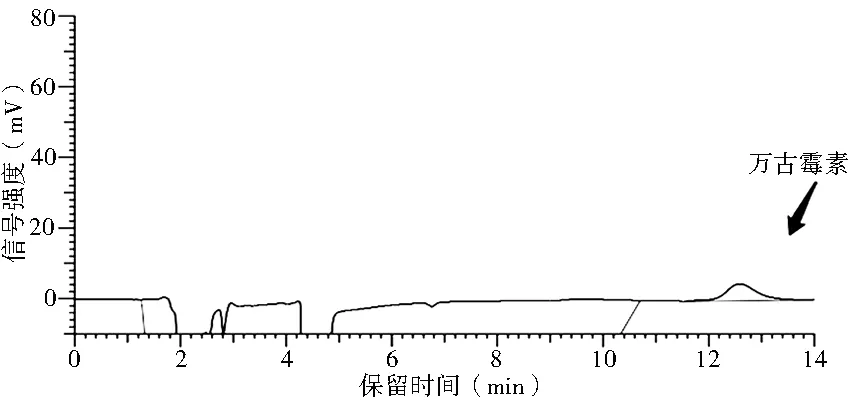
图2 91%邻苯二甲酸氢钾:9%乙腈(pH 3.2)
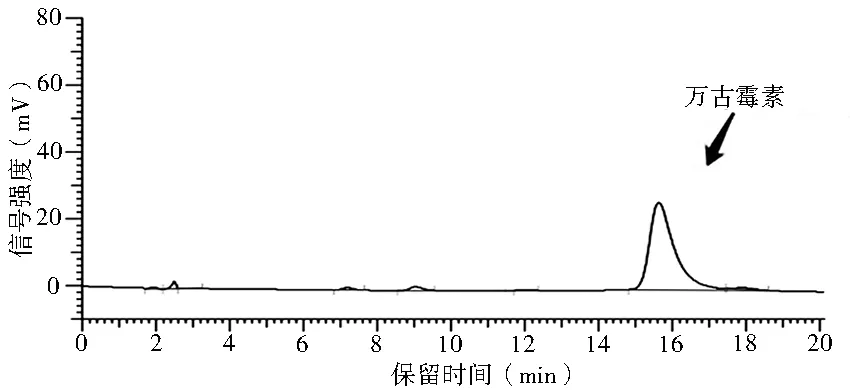
图3 91%磷酸二氢钾:9%乙腈(pH 3.2)
2.2 外标法的选择 目前国内文献报道中多为内标法测定万古霉素血药浓度,而去甲万古霉素、维生素B等内标物是临床常用药物,若患者同时使用万古霉素和内标物质,内标物质可能作为内源性杂质干扰检测结果,不能准确计算万古霉素血药浓度,因此本实验采取更简便的外标法检测。
2.3 血样预处理的选择 万古霉素的提取方案有多种,国外多采用固相提取和在线提取,在线提取对仪器要求较高,蛋白沉淀法的沉淀机理是降低水的介电常数,导致具有表面水层的生物大分子脱水,互相聚集,最后析出。使用较多的有机溶剂有乙醇、甲醇及乙腈等。低温可保持生物大分子活性,同时降低溶解度,提高提取效率。蛋白沉淀-HPLC快速简便经济,取样量少[11-12]。本实验采用10%三氯醋酸对样品进行蛋白沉淀,得到良好的分离条件,因此确定为本实验血样处理方案,见图4。
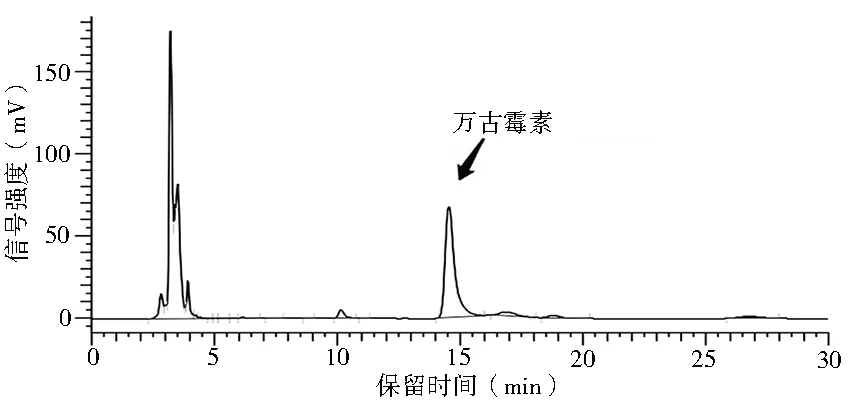
图4 三氯醋酸处理
3 实验操作方法
3.1 血浆的来源 采集健康体检者的静脉血,离心后,取上层清液用于制备空白血浆,备用。采集给予万古霉素治疗患者的静脉血,离心后,取上层清液备用,作为患者血浆样品。
3.2 色谱条件 色谱柱Agilent TC-C185 μm(150 mm×4.6 mm);流动相9%乙腈-91%磷酸二氢钾(pH 3.2);流速1.0 ml/min;柱温25 ℃;检测波长236 nm;进样量20 μl;采集时间30 min。
3.3 万古霉素对照品溶液 精密称取万古霉素对照品56.3 mg于50 ml量瓶中,用注射灭菌用水溶解定容至刻度线,配制成浓度为1 126 mg/L的万古霉素对照品储备液,置于冰箱4 ℃冷藏保存备用。
3.4 血浆样品的处理 将患者血样以3 500 r/min离心5 min后,吸取上层血清150 μl于离心管中,10%三氯醋酸40 μl,漩涡震荡3 min,13 000 r/min离心12 min后,取上清液20 μl进样,在上述色谱条件下测定,记录万古霉素的峰面积。
4 方法学验证
4.1 标准曲线与线性范围 取空白血浆100 μl置于试管中,精密量取不同质量浓度、相同体积的万古霉素对照品稀释储备液50 μl,混匀,制备成浓度分别为4.69、9.38、18.76、37.52、75.04、300.16 mg/L的系列标准血浆样品,按“血浆样品的处理”项下方法操作测定,经HPLC分析,记录色谱图,测定结果见表1。以万古霉素进样浓度(mg/L)为横坐标(X),峰面积(A)为纵坐标(Y),绘制标准曲线。计算回归方程为Y=10 526X+10 533,r=0.9998。结果表明,绿原酸在4.69~300.16 mg/L范围内有良好的线性关系,见图5。
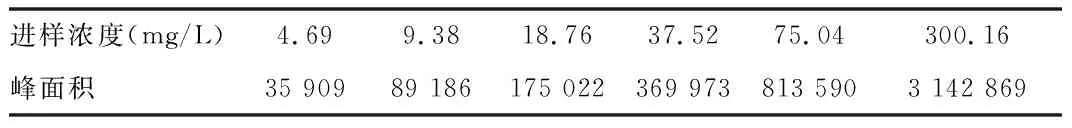
表1 万古霉素进样浓度与峰面积关系 (n=6)
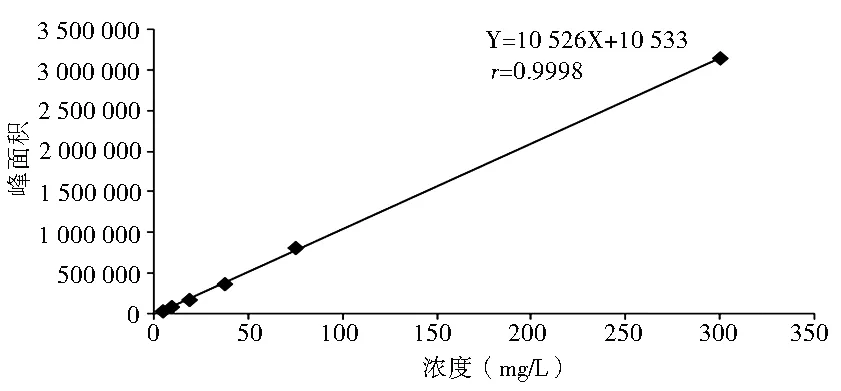
图5 标准曲线
4.2 方法的专属性 分别取空白血浆和含药血浆样品,每个浓度各配制5份,按“血浆样品的处理”项下进行处理,测得色谱图,见图6、图7。
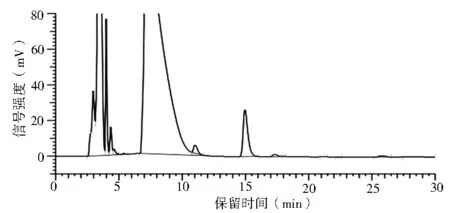
图6 空白血浆
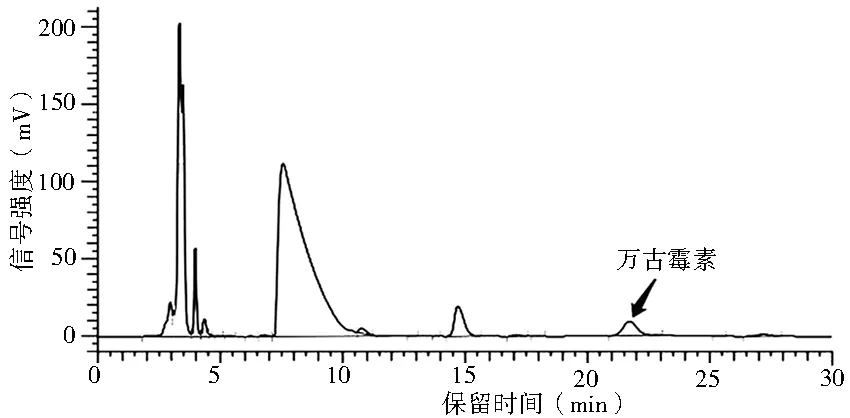
图7 含药血浆
4.3 相对回收率实验 取空白血浆,加入已知浓度的万古霉素对照品,配制成浓度分别为9.38、37.52、150.08 mg/L的血浆样品各5份,按“血浆样品的处理”项下进行处理,测得回收率。精密度用相对标准差RSD(RSD=SD/平均值×100%)表示,提取回收率用测得平均浓度/实际浓度×100%表示。结果见表2,提取回收率分别为107.02%、91.18%、106.56%。
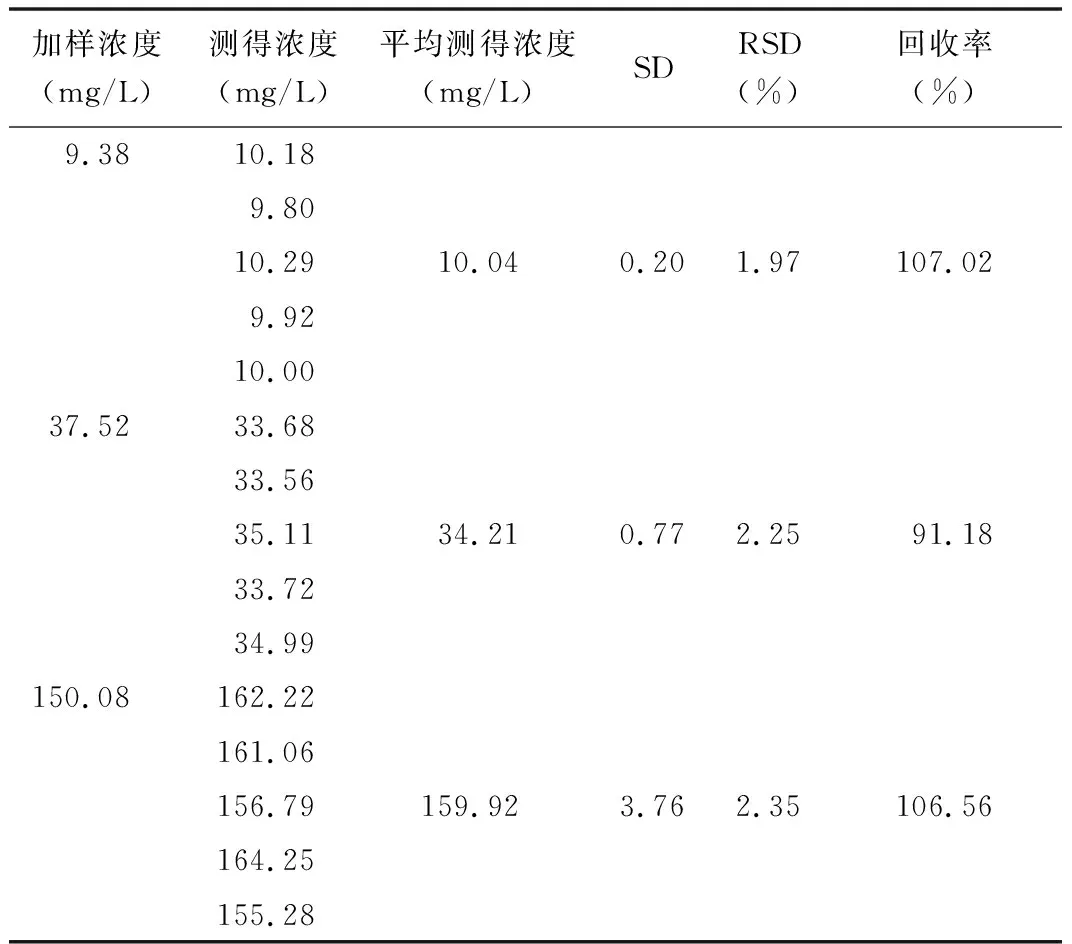
表2 提取回收率实验结果
4.4 精密度实验 配制9.38、37.52、150.08 mg/L的万古霉素血浆样品各5份,作为一批精密度样品,按“血浆样品的处理”项下进行处理,测得峰面积。以1 d内每个浓度5个样品测得的万古霉素浓度计算日内精密度,每天制备上述浓度血样各5份连续测定3 d,得日间精密度,见表3。
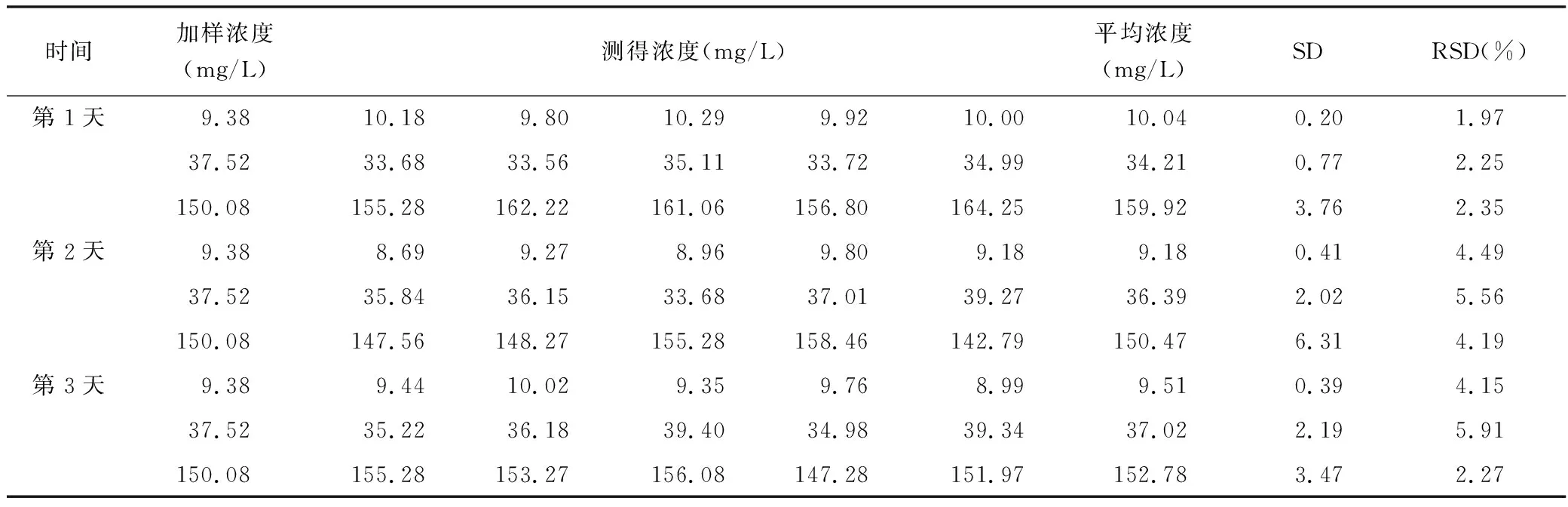
表3 万古霉素批内、批间精密度 (n=5)
4.5 稳定性实验 将万古霉素的低、中、高浓度的血浆样品避光放置在4 ℃的冰箱中冷冻0、24、48 h,样品经不同条件保存后按“血浆样品的处理”项下操作进行稳定性考察,结果显示见表4,精密度达到要求,但随着时间的延长,万古霉素会降解。
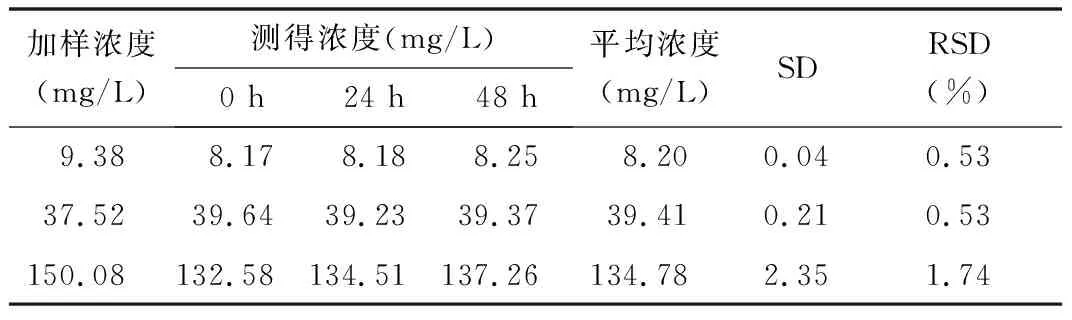
表4 万古霉素稳定性考察 (n=5)
5 讨 论
本实验建立的HPLC法测定人血清中万古霉素的血药浓度,在4.69~300.16 mg/L范围内线性关系良好;方法回收率均>90%,精密度实验、稳定性实验等的RSD也在规定范围内,符合《中国药典》中生物样品测定的要求。本方法具有灵敏、准确、测定成本低、操作简便等优点,适用于人血清中万古霉素血药浓度监测,有利于患者个性化治疗的安全实施,为临床用药剂量和给药方案调整提供重要参考依据。
利益冲突:所有作者声明无利益冲突。
