tRNA-ValAAC-5 促进肝癌细胞增殖和迁移作用机制研究
2023-03-18陈卜钰云虹渝
石 慧,谭 琰,陈卜钰,云虹渝,杨 彦
(1.海南医学院第一附属医院消化内科, 海南 海口 570000;2.海南医学院第一附属医院肝胆外科, 海南 海口 570000)
肝癌是常见的恶性肿瘤之一,其发病率和死亡率每年以大约3%的速度增长。80%肝癌的组织学类型是肝细胞癌 (hepatocellular carcinoma, HCC)。目前,肝癌的早期诊断困难,无明显症状,初治即为中晚期肝癌,没有有效的治疗手段,死亡率逐年增高[1-3]。因此,发现新的肝癌特异性靶标分子对HCC 的治疗,提高患者生存率具有重要意义。
tsRNA 是tRNA 衍生的一种新型调节性小非编码RNA,参与多种生理和病理过程[4,5]。tsRNA通常长度为18~40 个核苷酸,由前体tRNA 或成熟tRNA 产生。tsRNA 可分为3 个不同的类别,包括:前体tRNA 衍生的小RNA,其以3'末端的poly U 残基特征(3'U tRF);成熟的tRNA 衍生的片段(tRF),常分为3 种亚型(5'tRF、3'tRF 和inter tRF);tRNA半分子(tRH)。tsRNA 参与了肿瘤的发生和发展,研究发现tsRNA 在胃癌[6]和胆管癌[7]中表达失调;tRNA-ValAAC-5 来源的tRF-17 能够靶向凝血酶敏感蛋白(Thrombospondin-1, THBS1)抑制TGF-β 1/smad3 信号的活化,从而抑制乳腺癌的增殖和侵袭转移[8]。Zhu 等[9]的研究提示tRNA-ValTAC-3、tRNA-GlyTCC-5、tRNA-ValAAC-5 和tRNAGluCTC-5 在肝癌患者血浆外泌体表达显著升高,并可以作为肝癌新的诊断标志物;但未见tsRNA 参与肝癌进程的相关报道。
本研究通过检测不同肝癌胞株及人永生化细胞株中tRNA-ValAAC-5 的表达差异,通过特异性性抑制剂干预tRNA-ValAAC-5 生物作用,研究tRNA-ValAAC-5 的表达对肝癌细胞增殖及侵袭转移的影响,为治疗肝癌提供新的思路。
1 材料与方法
1.1 实验材料
人 正 常 细 胞 肝 细 胞 系(THLE2,THLE3)和HCC 细 胞 株(Hep3B, HuH7, SNU398, Hep3G2)均由上海冠导生物工程有限公司提供,由本实验室保存。tRNA-ValAAC-5 检测引物及tRNA-ValAAC-5-inhibitor/tRNA-NC 由上海生物工程有限公司合成;EntransterTM-R4000 转染试剂由北京英格恩生物科技有限公司提供;鼠抗人p21、MMP2、MMP9 抗体,GAPDH 抗体和HRP 标记二抗购自美国CST 公司;RNA 提取,反转录试剂盒,qPCR 检测试剂盒购自中国大连Takara 分公司;BCA 蛋白浓度测定、ECL 化学发光试剂盒、CCK-8 试剂盒(细胞增殖及毒性检测试剂盒)购自北京索莱宝科技有限公司;培养液RPIM 1640 和胎牛血清(FBS)购自美国GIBCO 公司。普通光学显微镜、数码显微摄影系统购自日本Olympus 公司;Varioskan LUX 多功能酶标仪购自赛默飞世尔科技;蛋白质印迹法电泳和电转仪器、ABI-7300 PCR 仪购自美国 Bio-Rad 公司。
1.2 实验方法
1.2.1 细胞培养及分组 人肝永生化细胞系(THLE2,THLE3)和HCC 细 胞 株(Hep3B, HuH7,SNU398, Hep3G2)由本实验室保存;细胞置于37 ℃水浴解冻,离心收取细胞,10%FBS 的RPIM 1640 培养液重悬、5%CO2、37 ℃温箱中培养,每24 h换液,细胞呈单层贴壁生长,待细胞长满后,0.25%胰蛋白酶消化传代培养。细胞传代至24 孔板中,细胞长至30%~40%时进行细胞转染。依照试剂盒操作说明使用EntransterTM-R4000 进行转染,Hep3B, Hep3G2 细胞分别转染50 pmol tRNA-ValAAC-5-inhibitor /tRNA-NC,分别命名为inhibitor组 和NC 组。转 染24 h 后,Real-time PCR 检 测 对tRNA-ValAAC-5 的干预作用。
1.2.2 Real-time PCR 检 测tRNA-ValAAC-5 的 表达 按试剂说明书提取细胞总RNA,经测定A260/A280 在1.8~2.0 之间。按说明书进行逆转录获得cDNA,20 μL 逆转录反应体系包括:MMLV (200 U/μL) 0.2 μL, RT primer (1 μmol/L) 1.2 μL,dNTP(10 mmol/L) 0.75 μL, 5×RTBuffer 4 μL,RT primer (5’GTCGTATCCAGTGCAGGGTC CGAGGTATTCGCACTGGATACGACAGGCG AA-3’)。反应条件:37 ℃,30 min;85 ℃,10 min。
Real-time PCR 反应体系为20 μL,包括:cDNA模 板1 μL,上 下 游 引 物(10 μmol/L)各0.5 μL,SYBR GREEN Master Mix 10 μL,同时设阴性对照。引 物:forward-tRNA-ValAAC-5(5’-GAGGACGTTTCCGTAGTGTAGTGG-3’), reversetRNA-ValAAC-5(5-CCAGTGCAGGGTCCGAGGTA-3’);forward-U6 (5-CTCGCTTCGGCAGCACA-3)、reverse-U6 (5-AACGCTTCACGAATTTGCGT-3);反应条件为:95 ℃ 15 s,62 ℃ 40 s,72 ℃ 3 min,40 个循环。实验设3 个复孔,反应结束后计算机自动分析出定量结果。
1.2.3 细胞增殖能力检测 传代培养Hep3B,Hep3G2 细胞转染tRNA-ValAAC-5-inhibitor/tRNA-NC 后细胞24 h,收集细胞计数,96 孔板每孔接种5 000 个细胞,接种后的24、48、72、96 h 除去细胞培养上清,按照CCK-8 检测试剂盒说明书操作,于570 nm 处酶标仪读取吸光度(A 值),并绘制生长曲线。1.2.4 Transwell 法检测细胞侵袭能力变化Hep3B, Hep3G2 细胞传代培养,细胞贴壁过夜,转染tRNA-ValAAC-5-inhibitor/tRNA-NC 后24 h,收集细胞计数,按照每孔2×105个细胞平铺于Transwell 小室(有基质胶)。24 h 后取出Transwell 小室,用棉签擦去上室内的细胞和基质胶,将小室置于0.1%结晶紫染色,显微镜进行观察统计小室底部的细胞数,并拍照。
1.2.5 蛋白质印迹法检测p21、MMP2、MMP9 蛋白表达 Hep3B, Hep3G2 细胞传代培养, tRNA-ValAAC-5-inhibitor/tRNA-NC 转染后48 h 收集细胞,预冷PBS 洗2 遍,置于冰上,加入400 μL NP-40 裂解液后重悬细胞,冰上放置30 min 后,4 ℃离心机,12 000 r/min 10min,取上清液,BCA 蛋白定量试剂盒法检测蛋白浓度。水煮制备样品后,上样(每孔20 μg 蛋白),依次10% SDS-聚丙烯酰胺凝胶电泳分离、转膜、5%脱脂奶粉封闭、p21、MMP2、MMP9一抗(1∶2 000) 4 ℃摇床孵育过夜,漂洗,二抗(1∶5 000)孵育30 min,漂洗后,ECL 显影并拍照,灰度扫描检测蛋白表达。
1.3 统计学处理
所有数据采用SPSS 22.0 进行统计学分析。所有计量资料以(±s)表示,符合正态分布的两组均值间比较采用t检验。检验水准α=0.05 (双尾),P<0.05 为差异有统计学意义。
2 结果
2.1 tRNA-ValAAC-5 在HCC 细胞中的表达量高于正常细胞肝癌细胞系
HCC 细 胞 株(Hep3B, HuH7, SNU398,Hep3G2)和人正常细胞肝癌细胞(THLE2,THLE3)分别传代培养,收取6 孔板内对数生长期细胞检测tRNA-ValAAC-5 的表达。通Real-time PCR结果显示:以THLE2 细胞tRNA-ValAAC-5 的表达量为标准(1.000±0.003), THLE3、Hep3B、 HuH7、SNU398、Hep3G2 细胞中tRNA-ValAAC-5 的表达相对表达量为1.005±0.014、2.799±0.171、1.884±0.080、1.363±0.054、2.185±0.117;与THLE2 细胞相比,Hep3B、HuH7、SNU398、Hep3G2 细胞表达显著 升 高,差 异 有 统 计 学 意 义(n=3),P<0.05。Hep3B 和Hep3G2 细胞,其相对表达量分别为THLE2 细 胞 的2.80 倍 和2.18 倍,后 续 选 择Hep3B 和Hep3G2 细胞用于实验(图1)。表明tRNA-ValAAC-5 在肿瘤细胞中高表达可能对增殖、侵袭转移等恶行表型发挥关键作用。因此,使用tRNA-ValAAC-5-inhibitor/tRNA-NC 分别转染Hep3B, Hep3G2 细胞干预tRNA-ValAAC-5,24h 后收集细胞检测得到与NC 组相比,inhibitor 组tRNA-ValAAC-5 表达显著降低(表1),表明转染成功,tRNA-ValAAC-5-inhibitor 干预有效。
表1 Hep3B、Hep3G2细胞tRNA-ValAAC-5的表达 (n=3,±s)Tab 1 Expression of tRNA ValAAC-5 in Hep3B and Hep3G2 cells (n=3,±s)

表1 Hep3B、Hep3G2细胞tRNA-ValAAC-5的表达 (n=3,±s)Tab 1 Expression of tRNA ValAAC-5 in Hep3B and Hep3G2 cells (n=3,±s)
注:与NC 组相比,**P<0.01。
组别HuH7 1.03±0.04 0.29±0.02**27.45<0.001 NC inhibitor t P tRNA-ValAAC-5 Hep3B 1.04±0.02 0.32±0.03**36.52<0.001
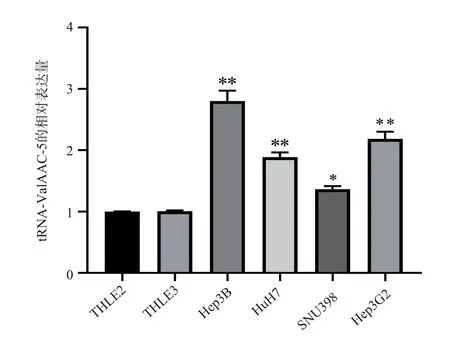
图1 不同肝癌细胞系tRNA-ValAAC-5 的表达(n=3)Fig 1 Expression of tRNA ValAAC-5 in different hepatoma cell lines (n=3)
2.2 tRNA-ValAAC-5 对HCC 增 殖 的 影 响
Hep3B 和Hep3G2 细胞分别传代培养于6 孔板中,转染tRNA-ValAAC-5-inhibitor/tRNA-NC 24 h后收集细胞平铺于96 孔板中,CCK-8 法检测细胞增殖情况,结果见表2。得到转染inhibitor 组Hep3B 和HuH7 细胞增殖受到显著抑制,P<0.01。表明tRNA-ValAAC-5 在HCC 细胞中高表达能有效促进细胞增殖。
表2 tRNA-ValAAC-5 对HCC 细胞Hep3B 和Hep3G2 增强的影响(±s)Tab 2 Effect of tRNAValAAC-5 on the proliferation of Hep3B and Hep3G2 cells in HCC(±s)
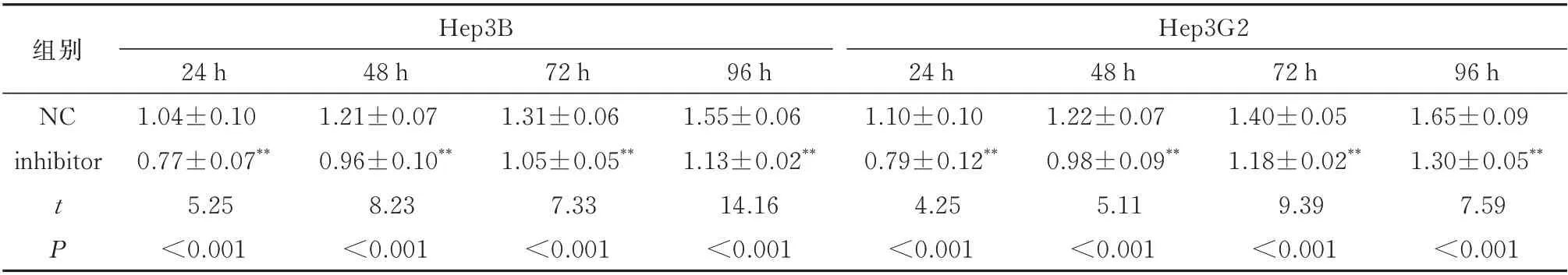
表2 tRNA-ValAAC-5 对HCC 细胞Hep3B 和Hep3G2 增强的影响(±s)Tab 2 Effect of tRNAValAAC-5 on the proliferation of Hep3B and Hep3G2 cells in HCC(±s)
注:与NC 组相比,**P<0.01。
组别Hep3B Hep3G2 96 h 1.65±0.09 1.30±0.05**7.59<0.001 48 h 1.21±0.07 0.96±0.10**8.23<0.001 48 h 1.22±0.07 0.98±0.09**5.11<0.001 72 h 1.40±0.05 1.18±0.02**9.39<0.001 NC inhibitor 72 h 1.31±0.06 1.05±0.05**7.33<0.001 24 h 1.04±0.10 0.77±0.07**5.25<0.001 96 h 1.55±0.06 1.13±0.02**14.16<0.001 24 h 1.10±0.10 0.79±0.12**4.25<0.001 t P
2.3 tRNA-ValAAC-5 对HCC 侵袭转移的影响
Hep3B 和Hep3G2 细胞分别传代培养于6 孔板中,转染tRNA-ValAAC-5-inhibitor/tRNA-NC 24h后收集细胞,Transwell 小室法检测对细胞侵袭转移能力的影响(图2);得到结果见表3。与转染NC 组相比,inhibitor 转染Hep3B 和HuH7 细胞侵袭转移能力减弱,差异均有统计学意义(P<0.001)。表明tRNA-ValAAC-5 在HCC 细胞中高表达促进细胞侵袭和转移。
表3 两组转染对Hep3B 和Hep3G2 细胞侵袭转移能力影响(n=5, ±s)Tab 3 Effect of tRNA ValAAC-5 on Hep3B and Hep3G2 cell invasion and metastasis(n=5, ±s)

表3 两组转染对Hep3B 和Hep3G2 细胞侵袭转移能力影响(n=5, ±s)Tab 3 Effect of tRNA ValAAC-5 on Hep3B and Hep3G2 cell invasion and metastasis(n=5, ±s)
注:与NC 组相比,**P<0.01。
HuH7 153.2±8.8 59.8±3.8**21.85<0.001组别NC inhibitor t P Hep3B 145.0±15.7 44.8±2.78**14.01<0.001
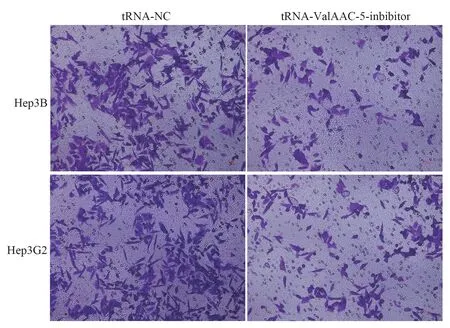
图2 tRNA-ValAAC-5 抑制剂抑制细胞侵袭转移(结晶紫染色,×200)Fig 2 tRNA ValAAC-5 inhibitor inhibits cell invasion and metastasis (crystal violet staining, ×200)
2.4 tRNA - ValAAC - 5 表 达 对p21、MMP2 和MMP9 表达的影响
Hep3B 和Hep3G2 细胞分别传代培养于6 孔板中,转染tRNA-ValAAC-5-inhibitor/tRNA-NC 48 h后收集细胞,Western blot 法检测Hep3B 细胞和Hep3G2 中p21、MMP2 和MMP9 的表达(表4)。得到 与NC 组 相 比, inhibitor 组Hep3B(图3)和Hep3G2(图4)细胞p21 表达升高,MMP2 和MMP9的表达均降低,差异有统计学意义(t=8.96、12.80、4.652,P<0.01)、(t=15.17、22.36、12.61,P<0.01)。表明tRNA-ValAAC-5 在HCC 细胞中高表达可以参与调控p21、MMP2 和MMP9 的表达。
表4 两组转染对Hep3B 和Hep3G2 细胞p21、MMP2 和MMP9 的表达影响(n=5, ±s)Tab 4 Effect of tRNA ValAAC-5 on the expression of p21, MMP2 and MMP9 in Hep3B and Hep3G2 cells(n=5, ±s)
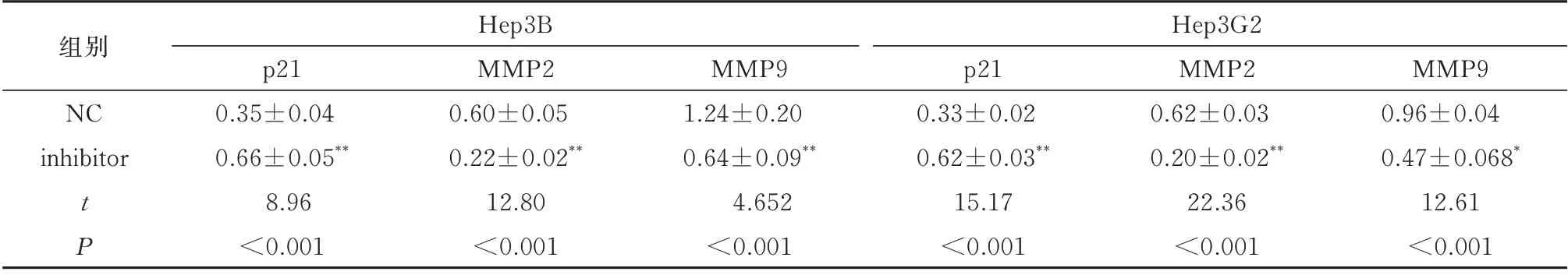
表4 两组转染对Hep3B 和Hep3G2 细胞p21、MMP2 和MMP9 的表达影响(n=5, ±s)Tab 4 Effect of tRNA ValAAC-5 on the expression of p21, MMP2 and MMP9 in Hep3B and Hep3G2 cells(n=5, ±s)
与NC 组相比,*P<0.05,**P<0.01。
组别Hep3B Hep3G2 MMP9 0.96±0.04 0.47±0.068*12.61<0.001 MMP2 0.62±0.03 0.20±0.02**22.36<0.001 tP MMP9 1.24±0.20 0.64±0.09**4.652<0.001 p21 0.35±0.04 0.66±0.05**8.96<0.001 MMP2 0.60±0.05 0.22±0.02**12.80<0.001 p21 0.33±0.02 0.62±0.03**15.17<0.001 NC inhibitor
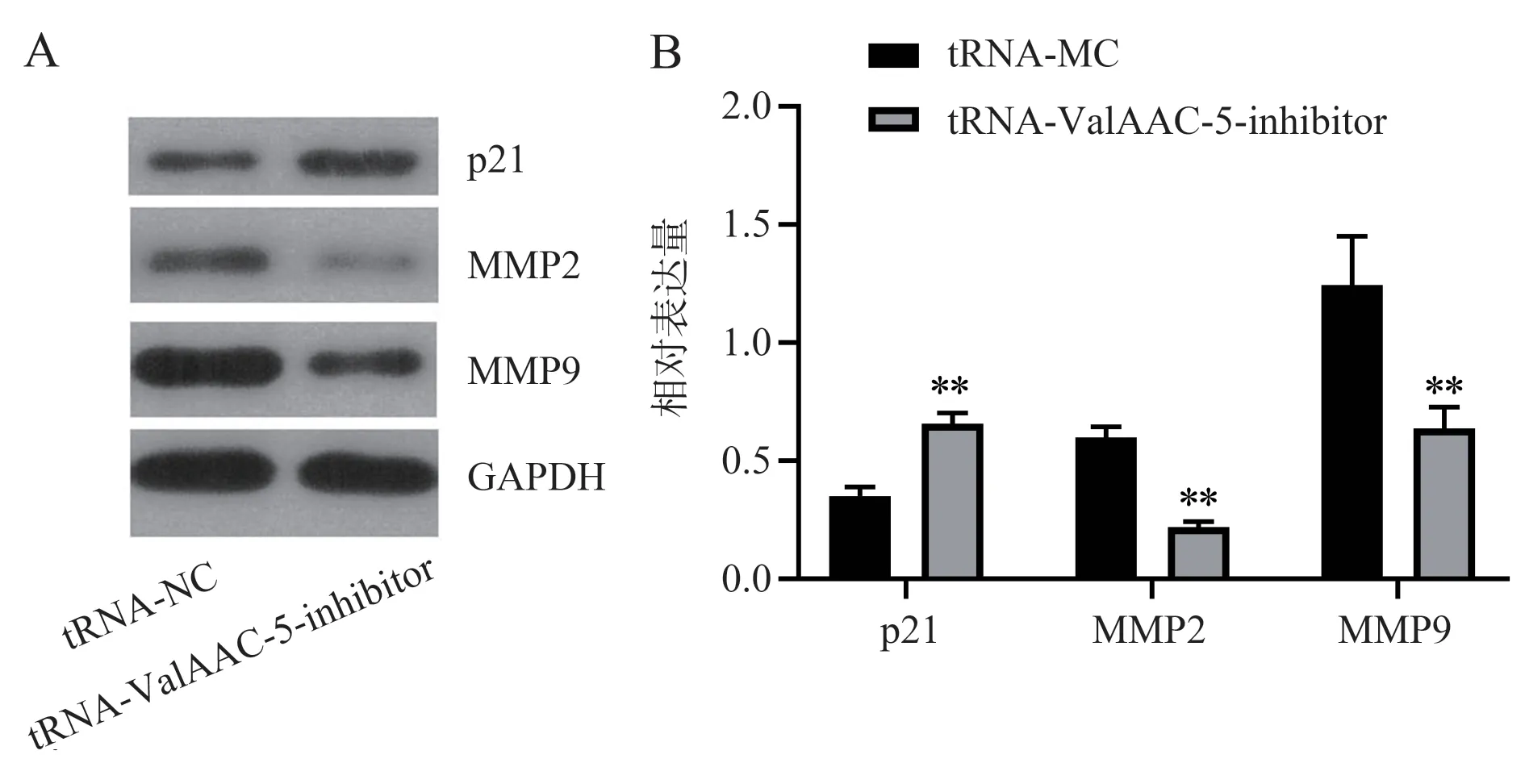
图3 tRNA-ValAAC-5 抑制剂对Hep3B 细胞p21、MMP2 和MMP9 表达影响(n=3)Fig 3 Effect of tRNA ValAAC-5 inhibitor on the expression of p21, MMP2 and MMP9 in Hep3B cells (n=3)
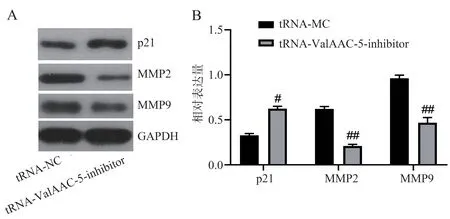
图4 tRNA-ValAAC-5 抑制剂对Hep3G2 细胞p21、MMP2和MMP9 表达影响(n=3)Fig 4 Effect of tRNA ValAAC-5 inhibitor on the expression of p21, MMP2 and MMP9 in Hep3G2 cells (n=3)
3 讨论
由于肝细胞癌发病隐匿,导致患者确诊时多数已是中晚期,基本失去了手术治疗、肝移植的机会。探索肝癌生长,转移的新机制对肝癌的早期诊断与治疗具有积极意义。小RNA 在调控肝癌进展中发挥关键作用。tsRNAs 被认为是一种新型的、潜在的非编码RNA(ncRNAs),它参与多种细胞过程,并在癌症进展中发挥重要作用[5,10]。本研究中,我们通过检测不同HCC 细胞中tRNA-ValAAC-5 表达,并干扰其在Hep3B 和Hep3G2 的表达,发现其在HCC 中高表达促进细胞增殖和侵袭转移,并调控p21、MMP2 和MMP9 的表达。
tsRNA 以前被认为是tRNA 的随机降解产物,没有生物学作用。但近年来将归类为一类重要的功能性小非编码RNA;能够以microRNA 的方式发挥特定的生物学作用。如tsRNA 参与RNA 干扰,调节目标mRNA 的稳定性,改变胚胎转录级联调控,作为父本表观遗传因子介导代谢疾病遗传;作为蛋白结合因子,tsRNA 与细胞色素C 互作调控细胞凋亡等[11-13]。相关报道指出乳腺癌患者癌组织样本 中tsRNA-26576 高 表 达[14],tsRNA-26576 抑 制MDA-MB-231 细胞细胞凋亡的同时,能促进细胞增殖和迁移;mRNA 测序结果显示,在MDA-MB-231细胞中提供tsRNA-26576 抑制剂后,包括FAT4 和SPEN 在内的几个抑癌基因表达升高。因此,tsRNA-26576 可以作为乳腺癌的潜在临床治疗靶点和预测标记。转录因子Runt-特相关的转录因子1(RUNX1)是乳腺上皮中的抑癌基因,RUNX1 下调节与乳腺癌的启动和进展相关;研究者发现tsRNA(ts-19、ts-29、ts-46 和ts-112),它 们 能 有 效 抑 制RUNX1 的 生 物 学 作 用;ts-112 和RUNX1 在 正 常 样乳腺上皮和乳腺癌中表达负相关,Ts-112 促肿瘤相关活性和RUNX1 的肿瘤抑制活性一致。在侵略性乳腺癌细胞MCF10CA1a 中抑制ts-112 可显著减少增殖,ts-112 在正常上皮MCF10A 细胞的异位表达显著增加增殖。这些发现支持了ts-112 的致癌潜力[15]。慢性淋巴细胞白血病(CLL)患者是白血病最主要的类型,研究者调查了CLL 样本和健康对照中tRNA 的tRF-5 片段的表达水平,发现tRF-5 在CLL 中与正常对照相比降低了5 倍[16]。本研究发现肝癌细胞中tRNA-ValAAC-5 表达量显著高于正常对照细胞,其中Hep3B 和Hep3G2 表达最高,这可能与不同来源的肿瘤细胞恶性程度有关。此外通过使用inhibitor 干预tRNA-ValAAC-5 发挥作用,得到tRNA-ValAAC-5 在肝癌中高表达发挥促癌作用,能够有效促进细胞增殖,侵袭和转移。这也与前期文献[9]报道的肝癌患者外泌体中tRNA-ValAAC-5升高,并作为肝癌早期诊断指标具有一致性。基于肝癌细胞中tRNA-ValAAC-5 的表达,提示我们tRNA-ValAAC-5 除促进肝癌细胞自身的增殖,侵袭和转移外,亦可能通过远端调控肿瘤的微环境,加速肝癌的全身性转移。
细胞周期负调控因子p21 能够有效抑制细胞周期G1-S 期的转化,p21 作为重要的抑癌基因,p21 表达升高抑制细胞增殖[17,18]。MMPs 在肿瘤间质中表达水平与肿瘤的侵袭转移密切相关,TIMP3 结合具有酶活性MMPs 并抑制MMPs 降解ECM[19]。本研究结果显示,在抑制tRNA-ValAAC-5 表达的基础上,p21 的表达显著升高,MMP2 和MMP9 的表达降低;提示tRNA-ValAAC-5 调控肝癌细胞增殖可能调控细胞周期有关,并通过影响MMP2 和MMP9 的表达调控细胞侵袭和转移。
综上所述,肝癌细胞中tRNA-ValAAC-5 表达沉默后,细胞增殖,侵袭和转移能力受到抑制;tRNA-ValAAC-5 可 能 通 过 调 控p21、MMP2 和MMP9 的表达影响细胞周期和细胞的转移。本研究存在一定的不足之处,只进行了体外细胞实验,没有证实tRNA-ValAAC-5 的直接作用靶点;接下来将通过动物实验探讨tRNA-ValAAC-5 体内肝癌生长的影响及tRNA-ValAAC-5 发挥作用的具体机制;以期进一步阐明肝癌发生,发展的机制,为肝癌的治疗提供新途径。
作者贡献度说明:
石慧:参与实验,收集整理数据及撰写论文;杨彦:课题设计和论文校审;其余作者:谭琰、陈卜钰、云虹渝:参与实验及管理报账。
所有作者声明不存在利益冲突关系。
