Cu@PtCu催化薄膜的构筑及氧还原催化性能研究
2023-03-14邓晓婷李振溱姚启文尹绍峰谢志勇梁伊丽
邓晓婷,李振溱,姚启文,尹绍峰,谢志勇,梁伊丽,刘 峰
(1.邵阳学院食品与化学工程学院,邵阳 422000;2.中南大学粉末冶金研究院,长沙 410083;3.广东氢发新材料科技有限公司,佛山 528000;4.昆明贵金属研究所铂金属综合利用先进技术国家重点实验室,昆明 650106)
0 引 言
质子交换膜燃料电池(proton exchange membrane fuel cell, PEMFC)是直接将化学能转化为电能的一种装置,可实现真正意义上的零污染和零排放[1-2],相对于现阶段广泛使用的锂离子电池,其具有加氢时间短,续航里程长等优点。膜电极(membrane electrode assembly, MEA)是燃料电池的核心部件,目前燃料电池膜电极的制备方法如下:首先配制催化剂浆料,然后直接将浆料涂布或转印到质子膜上得到催化剂/质子交换膜组件(catalyst coated membrane, CCM),最后将气体扩散层与CCM贴合得到MEA[3-4]。该工艺下燃料电池催化剂必须是易分散的粉体材料,由于催化层采用“浆料喷涂”的工艺进行加工,难以实现电化学反应和传质动力学的精确协同。
静电纺丝可利用高压电场力抗争溶液表面张力而实现纺丝,通过调控纺丝前驱体溶液、针型、纺丝环境(如温度、湿度、电场及磁场)等参数进行中空纳米管、多孔纳米纤维等纳米结构材料的大规模制备[5]。碳纳米纤维(carbon nanofibers, CNF)和碳纳米管(carbon nanotubes, CNT)等一维碳材料具有长程取向性以及良好的导电性、耐高温、耐腐蚀等性能,它们相互搭连形成三维网状结构,为气、液的传输提供了通道。利用静电纺丝获得长程连续超薄纳米纤维膜,再通过一定的碳化处理工艺得到炭膜,该炭膜能保留原纤维长程连续性,同时具有良好的导电性能,可用作催化剂载体材料。将催化剂附着在载体纤维膜上,做成催化剂膜,可直接将催化剂膜与质子交换膜贴合成CCM。
质子交换膜燃料电池的成本、稳定性问题限制了其商用推广,其中阴极铂基催化剂的活性和耐久性的提高是其主要的挑战。为此,很多研究者开辟不同的方法,发展了非贵金属催化剂、合金化和核壳结构等催化剂[6-7]。其中合金化是一种有效的方法,它不仅可以减少昂贵的铂载量,也可通过其他金属改变催化剂表面的原子的核外电子密度从而增加其活性[8-9]。
Pt基催化剂的合金化能提高催化剂的活性,同时一维的纤维能相互搭连成三维的网络结构,作为催化剂载体有利于气、液、电的传输[10]。本研究通过静电纺丝法制备特定结构的CNF膜,选用脉冲电沉积的手段将具有还原性且能与Pt形成合金结构的Cu纳米晶负载在碳膜上。研究Cu微晶在碳膜上沉积分布生长调控工艺,然后用置换法制得Cu@PtCu/CNF催化薄膜,并对其形貌、结构和氧还原性能进行研究,表现出较好的氧还原活性及稳定性。
1 实 验
1.1 实验原料
聚丙烯腈(PAN)MW=90 000, N,N-二甲基甲酰胺(DMF),五水硫酸铜和氯铂酸(H2PtCl6·6H2O)购自阿拉丁。纯铜片来自大冶铜铸铜业,商业JM 20% Pt/C(JM20)购自美国Johnson-matthey公司。
1.2 材料制备
1.2.1 碳纳米纤维膜的制备
取1.5 g PAN和13.5 g DMF在35 ℃的水浴中搅拌4 h,使其彻底溶解得到分散均匀的前驱体液,然后将前驱体液装入针头内径为(0.41±0.02) mm的注射器中,将注射器安装在静电纺丝机上,设备工作参数设定为:推进速度为0.4 mL·min-1、针头与滚筒间距离为15 cm、工作电压为20 kV、湿度40%、温度35 ℃。将纺好的PAN膜平整的放置在玻璃板上,四面用夹子固定,放入220 ℃烘箱中预氧化6 h后,再将其转至惰性气氛保护的高温炉中,以3 ℃·min-1的升温速率升温至1 600 ℃,并保温2 h,然后随炉冷却至室温,取出得到碳膜。
1.2.2 脉冲电沉积制备Cu纳米晶/CNF膜
工作电极的夹具如图1所示,脉冲电沉积时采用三电极体系,工作电极的电沉积面积为20 mm×25 mm。电极夹具及电解槽接线,在0.1 mol·L-1H2SO4和2 mmol·L-1CuSO4电解液中,1.0 V电压下预极化120 s,去除表面杂质。操作流程为:工作电极在CuSO4溶液中浸泡10 min,电化学氧化(使疏水性的CNF膜亲水,溶液浸透到膜内),然后进行脉冲电沉积。控制反向脉冲氧化电流密度15 mA·cm-2,脉冲导通时间Ton=100 μs和关断时间Toff=500 μs,平均电流密度-8.33 mA·cm-2,峰电流密度-50 mA·cm-2,脉冲沉积时间20 s。电沉积结束后迅速将膜转入无水乙醇中浸泡10 min(乙醇能使铜表面钝化,避免后续操作中被空气持续氧化),取出用去离子水冲洗干净,在50 ℃真空干燥箱中干燥。阴阳极上的反应式分别为:
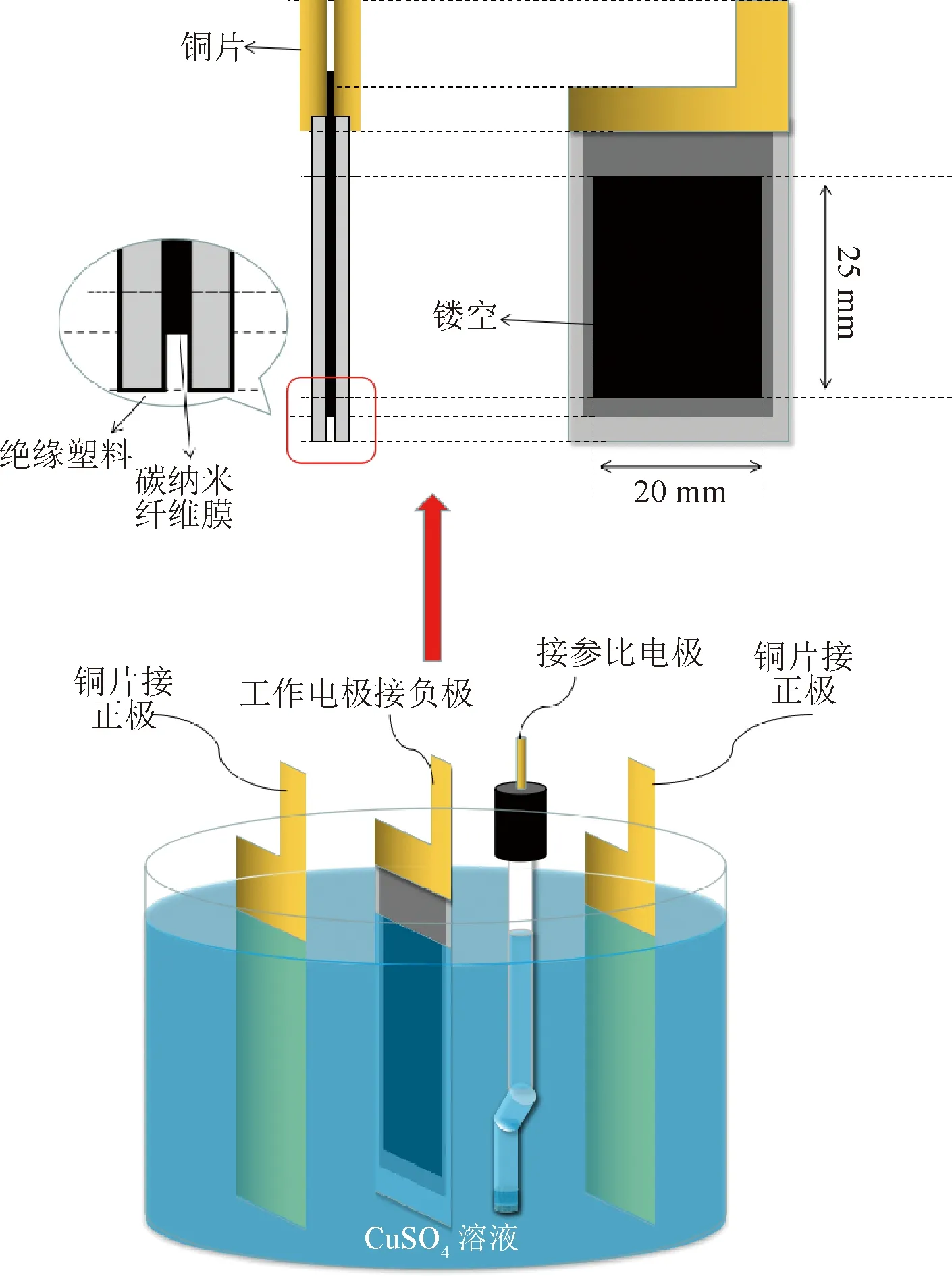
图1 三电极系统示意图
阴极:Cu2++2e-→Cu
阳极:Cu-2e-→Cu2+
(1)
(2)
1.2.3 原位化学置换制备Cu@PtCu/CNF催化薄膜
将Cu纳米晶/CNF膜浸入0.25 mg·mL-1氯铂酸(H2PtCl6)溶液中,用浓硝酸和10% KOH调节pH值分别为2、4、6(分别命名为P1、P2和P3),分别进行1 h的置换反应,通过三电极体系测试开路电压曲线,监测表面的化学反应,去离子水冲洗干净后放入真空干燥,得到Cu@PtCu/CNF催化薄膜。
1.3 材料结构和形貌表征
碳材料的石墨化程度、缺陷情况采用拉曼光谱(LabRAM HR800)进行分析;催化剂样品材料的晶格参数和结构采用 X 射线衍射衍射仪(XRD,Bruker Advance D8)进行测试,选取Cu Kα靶,扫描范围10°~80°,扫描速度为5 (°)·min-1;利用透射电子显微镜(TEM, JEM-2100F)和扫描电子显微镜(SEM, JEOL JSM-7600F)分析微观结构;化学状态和元素含量用X射线光电子能谱(XPS, ESCALAB250X)表征;电阻率测试采用苏州晶格电子有限公司四探针电阻率测试仪(ST2258C)。
1.4 催化氧还原电化学性能表征
循环伏安(cyclic voltammetry, CV)试验在0.1 mol/L HClO4溶液中进行,温度为25 ℃。测试时,电解池中装上新配制的0.1 mol/L HClO4,稳定通入高纯氮气25 min,脱除溶液中氧气。测试采用三电极体系, 工作电极采用玻碳电极负载催化剂,对电极为1 cm×1 cm的Pt箔,参比电极为饱和甘汞电极,本文中的电极电位均转换为可逆氢电极电位(RHE)。催化剂薄膜的制备方法:称取2 mg催化剂,加入900 μL 20%的异丙醇水溶液和100 μL 5% nafion溶液,40 ℃以下超声60 min。用移液枪汲取10 μL上述混合液(铂载量约20~80 μg·cm-2)滴到玻碳电极上,阴凉避光自然干燥。扫描范围为0.05~1.20 V,扫描速度10 mV·s-1。线性扫描伏安(LSV)测试条件:20 mV·s-1,旋转速度1 600 r/min。电化学活性比表面积(ECSA)、质量比活性(MA)和面积比活性(SA)评价催化剂的催化活性。其计算如下:
ECSA=QCu/(420×mPt)
(3)
式中:QCu为欠电位铜电化学剥离过程中从0.35 V到0.80 V积分得到的电量,420 μC·cm-2为假定Pt表面单层Cu的电荷密度。
(4)
(5)
(6)
式(4)为Koutecky-Levich极限电流方程公式,其中j为实测电流密度,取0.9 V时的实测电流值进行动力学校正,jl为极限扩散电流密度,jk为动力学电流,mPt为Pt载量[11]。
为了评估电催化剂的稳定性,在0.1 mol/L HClO4溶液中,用三电极体系以扫描速率为100 mV·s-1,电位扫描范围为0.6~1.1 V,进行5 000个周期的CV测试。每隔一定的周期计算ECSA,稳定性通过ECSAn/ECSA0比值的值来评估,其中n为周期数,ECSA0为初始电化学活性比表面积。
2 结果与讨论
2.1 物相分析
分别在pH值为2、4、6置换液中制备的Cu@PtCu/CNF催化薄膜的SEM照片和XRD图谱如图2和图3所示。根据SEM测试中进行的EDS面扫结果和XRD图谱的Debye-Scherrer公式计算得到的晶粒尺寸统计于表1。SEM结果显示随着pH值的升高,纤维表面的纳米颗粒晶粒逐渐增大,从图2(d)光学照片可以看出,CNF膜具有较好的柔韧性。EDS元素分析发现pH值的升高会使Pt载量降低、Cu含量上升,CuPt原子比增大。XRD图谱和标准PDF卡片的比对发现,P1和P2的衍射峰与Pt的标准卡片特征峰的2θ值相比发生正移,特征峰接近PtCu合金标准卡片的特征峰位置,说明形成了合金结构。P2的偏移量更大,根据Vegard定律[7]计算得到P2的合金结构中固溶组分的Cu和Pt的原子比约为3∶2,小于EDS中测得的83.8∶16.2,说明Pt原子与Cu形成合金结构在Cu核外部形成了富Pt壳层[12]。XPS的全谱分析显示P2表层Cu和Pt的原子比为64∶36,与XRD检测的比例相近。因此,推测置换反应的过程为:Pt离子在Cu的还原下依附于Cu纳米晶表面形核,在此过程中部分Cu与Pt形成富Pt的壳结构,而没有完全消耗的Cu纳米晶在内部形成核的结构,最终形成Cu@PtCu结构。
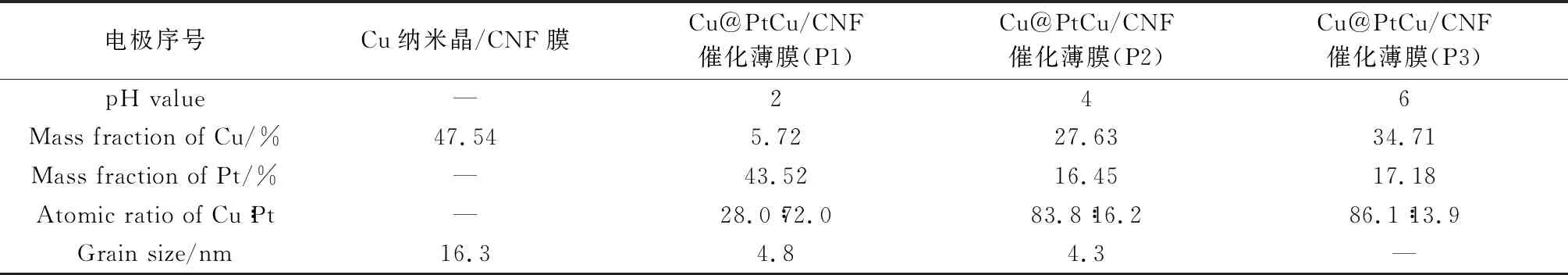
表1 CNF催化薄膜EDS面扫元素统计及XRD晶粒度统计

图2 不同pH值氯铂酸置换液制备的Cu@PtCu/CNF催化薄膜的SEM照片
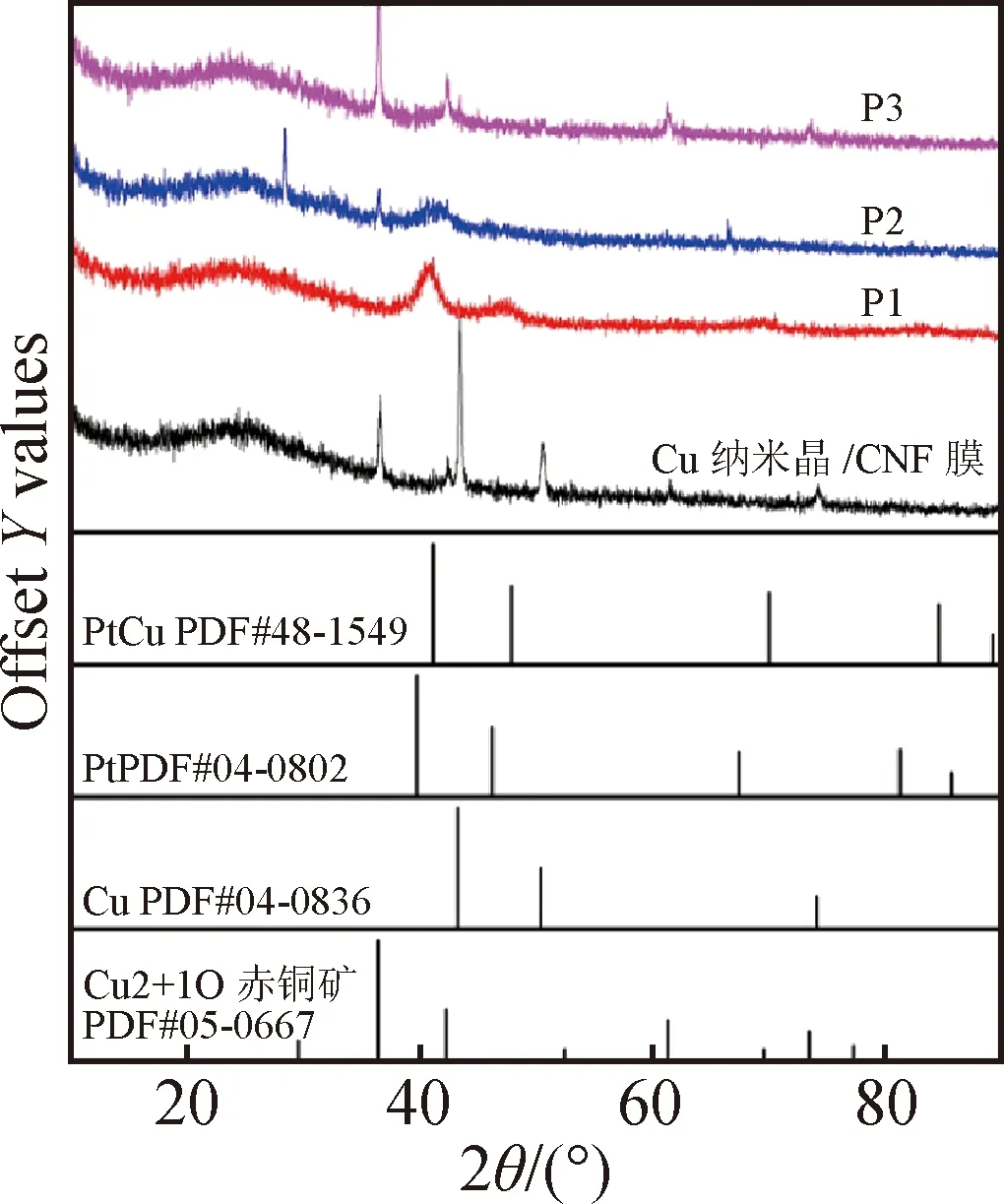
图3 不同pH值氯铂酸置换液制备的Cu@PtCu/CNF催化薄膜的XRD图谱
根据布拉格定律,2θ值的正移表明Cu的加入使Pt的晶格发生收缩,Pt受到相应的拉应力,有利于催化剂活性正向调控[10]。制备的Cu纳米晶/CNF膜不仅有Cu晶体的特征衍射峰,还存在其氧化物——赤铜矿物相的衍射峰,说明在制备Cu纳米晶/CNF膜后进行的钝化和干燥处理使Cu纳米晶表面存在着氧化层。在pH=2的置换液中制备的Cu@PtCu/CNF催化薄膜的Cu晶体和赤铜矿物相的特征衍射峰消失,而pH值增加至4时出现了赤铜矿物相的衍射峰,在pH值为6时铜晶体和赤铜矿的衍射峰同时出现。结果说明,较低的pH值有利于溶解Cu纳米晶表面的氧化层,使内部具有还原性的金属Cu暴露,从而加速Pt的还原及Cu@PtCu结构的形成,但过低的pH值会使Cu的溶解过快,从而导致CuPt合金原子比例的下降,不利于合金壳层中Cu成分的保留(EDS分析中显示pH值降低,Cu含量下降,CuPt原子比例下降)。
为了解Cu@PtCu/CNF催化薄膜的活性物质的金属原子的化学状态以及表面电子的电子云分布和能级结构,对获得的XPS的Pt 4f和Cu 2p区曲线进行分峰拟合处理,如图4所示。图中的结合能已通过C 1s峰的参考峰(284.8 eV)校正。图4显示所制备的P1(71.72 eV)和P2(71.54 eV)样品的Pt 4f7/2相对于JM20(71.95 eV)向结合能小的方向偏移,而P2的Cu 2p3/2峰(935.0 eV)相对于P1的Cu 2p3/2峰(932.5 eV)向结合能大的方向移动,结合能的变化说明了电子的得失,这说明由于壳层的Pt和Cu形成了合金结构,活性物质表面的电子结构发生改变,Cu的表面电子部分转移至Pt表面,可提髙氧还原的起峰电位,抑制Pt的氧化,从而有利于催化剂催化活性的正向调控。其中P2的Pt 4f7/2负向偏移值更大,表明更多的电子从Cu转移到Pt,使Pt的d带中心更低[13],对OH的吸附最弱,有利于氧还原(oxygen reduction, ORR)过程中的中间产物的脱附,说明其Cu合金成分含量对催化活性有更好的调控,可以预测其催化活性更好[14]。Pt 4f区的4f7/2和4f5/2峰为Pt的三种价态发出的特征峰的叠加,对其做分峰处理,能得到Pt元素的价态分布,其中约71.4和74.8 eV位置的峰为0价Pt(Pt(0))所激发;约72.4和75.8 eV位置的峰为2价Pt(Pt(II),物质包括PtO和Pt(OH)2)所激发;约75.2和78.6 eV位置的峰为4价Pt(Pt(IV))所激发。对三种价态得到的峰进行面积积分可以统计其价态比例,将拟合后的面积进行统计,计算结果列于表2中,值得注意的是Pt的0价的比例的增加有利于催化活性的增加。表2显示随着pH值的增加,Pt(0)比例降低,说明较低的pH值能使Pt还原得更彻底。当pH值升至6时,Pt(0)比例只占16.72%,Pt在膜上没有得到有效的还原,这是因为在该pH值时,Cu晶体表面的氧化物没有去除(XRD和XPS分析中已论述),具有还原性的Cu无法充分暴露,导致Pt在膜表面只有少量被还原,大部分是以离子形式吸附在膜的表面。
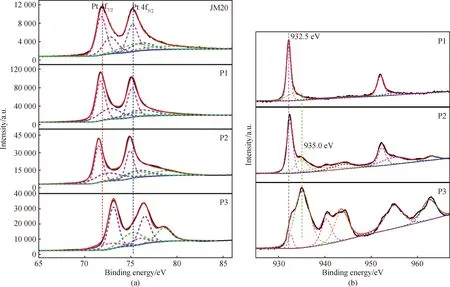
图4 JM20和P1、P2、P3的XPS图谱中(a)Pt 4f和(b)Cu 2p曲线

表2 XPS图中Pt 4f区的拟合数据统计表
2.2 电化学分析
Cu@PtCu/CNF催化薄膜P1、P2和P3在0.1 mol/L HClO4和N2饱和条件下, 0.05~1.2 V测试循环伏安曲线如图5所示。为了比较,商业催化剂JM20以同样的方式测试。P1(0.788 V)、P2(0.809 V)和P3(0.785 V)的氧化物还原峰相对于纯Pt催化剂JM20(0.766 V)均有所正移,P2的正移值最多(43 mV)。氧化物还原峰的正移表明中间产物OH-在催化界面上的结合力较弱,有利于其脱附(这与XPS中的分析相一致),从而提高催化活性。

图5 JM20、P1、P2和P3的循环伏安(CV)曲线
根据循环伏安曲线,计算 0.075~0.4 V的氢原子吸附区电量积分,P1有较高的氢吸附电量积分面积,而P2、P3的积分面积依次递减,这主要由Pt载量依次递减导致。耦合等离子体原子发射光谱(ICP-AES)测试结果显示:P1中Pt含量(质量分数)41.0%,Cu含量(质量分数)5.93%;P2中含Pt 14.5%,Cu 30.7%;P3中含Pt 6.1%,Cu 45.5%;JM20 含Pt 19.2%。进一步计算0.075~0.4 V电化学活性面积(ECSA)(见表3),结果显示P1的电化学活性面积高于P2,但其XRD统计的颗粒大小(4.8 nm)大于P2(4.3 nm),这可能是P1的Cu含量较低(P1的Cu含量为5.93%,P2的为30.7%),晶粒表面的Pt原子能占据更大的面积,使其ECSA高于P2。JM20的ECSA高于P1、P2和P3,这与JM20的活性纳米金属颗粒直径(2.3 nm)较小有关。

表3 催化剂的电化学性能
在0.1 mol/L HClO4,O2饱和条件下,以20 mV·s-1扫速测试Cu@PtCu/CNF催化薄膜P1、P2和P3线性伏安曲线(见图6)。P1和P2的起始还原电位和半波电位均高于JM20,说明与JM20相比,P1、P2更容易催化氧还原。同时,P1、P2和P3的起始还原电位和半波电位依次降低,这是由于这三种催化剂中起活性主导作用的Pt含量依次降低。P1(0.057 A·mg-1)、P3(0.043 A·mg-1)的质量比活性均小于JM20(0.080 A·mg-1),而P1、P3的面积比活性与JM20相当,这说明Cu加入后生成的合金化结构能起到增加面积比活性的作用。值得注意的是,在pH=4下置换反应得到的Cu@PtCu/CNF催化薄膜P2,其质量比活性是JM20的1.125倍,面积比活性相对于P1和P3有较大提升,是JM20的2.4倍,说明合适比例的Cu和Pt合金结构更有利于活性的提高。
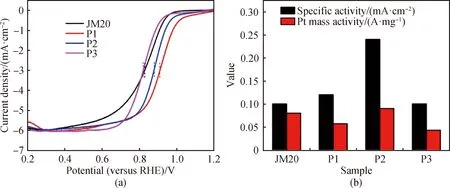
图6 JM20、P1、P2和P3的(a)的氧还原(ORR)极化曲线(1 600 r/min),(b)面积比活性(SA)和Pt的质量比活性(Pt MA)的条形统计图
图6(a)显示P1和P2的起始还原电位和半波电位高于JM20的,说明P1、P2相比于JM20氧更容易还原,同时P1、P2和P3的起始还原电位和半波电位均依次降低,这是由于这三种催化剂中起活性主导作用的Pt含量依次降低。为更好地进行活性比较,归一化后进行横向比较,如图6(b)所示,P1(0.057 A/mg)、P3(0.043 A/mg)的质量比活性均小于JM20(0.080 A/mg),这是因为P1、P3的活性金属纳米颗粒的粒径较大,导致其活性表面积相对减小,而P3的质量比活性比P1更小,是因为pH=3下Pt的还原不充分(XPS分析已给出,其中0价的Pt更有利于氧还原)。值得注意的是,P1、P3的面积比活性与JM20相当,这说明Cu加入后生成的合金化结构能起到增加面积比活性的作用。值得注意的是,不同于P1、P3,P2的活性金属纳米颗粒虽然比JM20大,且其电化学活性表面积也比JM20小,但其质量比活性高于JM20,是JM20的1.125倍,这是因为其Cu和Pt的比例适中,合金结构起到了活性正向调控作用。同时P2的面积比活性相对于P1和P3有较大提升,是JM20的2.4倍。
为更深入地了解制备的合金催化剂的氧还原的电子转移过程,选取比较有代表性的P2进行电子转移数(n)计算,通过Koutecky-Levich方程(K-L方程)计算处理P2在不同转速下的LSV曲线,即可得到其在氧还原中的电子转移数(n)。图7中以ω-1/2为横坐标,J-1为纵坐标作图(ω为电极旋转速度,J为电流)。根据斜率计算转移电子数,将在0.825、0.85、0.875、0.9和0.925 V时的斜率代入K-L方程得到的电子转移数均接近4,这说明反应大致为4电子过程,产物主要是水。
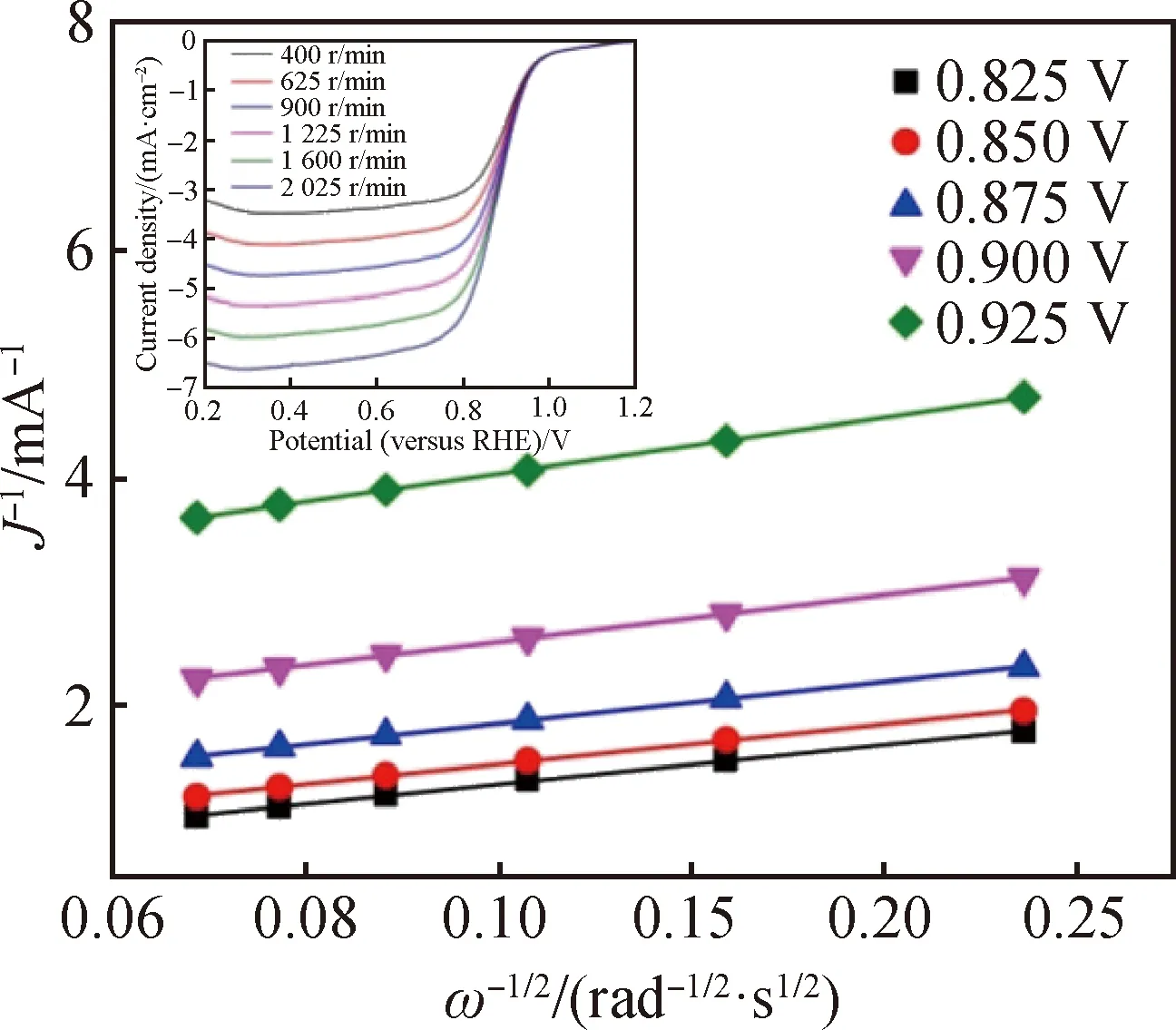
图7 P2在不同电压下的Koutecky-Levich曲线及不同转速下的LSV曲线
通过5 000循环的稳定性试验(ADT)研究自制催化剂的电化学耐久性。JM20、P1、P2和P3催化剂计算统计的电化学活性表面积(ECSA)下降趋势如图8(a)所示。并将稳定性测试前后测试的循环伏安曲线列于图8(b)、图8(d)、图8(f)和图8(h)中,测试的1 600 r/min的线性伏安曲线列于图8(c)、图8(e)、图8(g)和图8(i)中。图8(a)显示P3的电化学活性表面积在1 000个循环期间下降较快,这是由于它的Pt还原不充分,大量的高价态的Pt在循环伏安的正向扫描中发生溶解,在负向扫描时被吸附还原长大,从而使颗粒越长越大,ECSA下降较快,同时因为制备过程中由于Cu表面的氧化层的阻碍,还有大量的Cu没有与Pt形成合金结构,在循环过程中铜表面的氧化层逐渐被氧化和还原,反映在5 000个循环后测试的循环伏安曲线出现了Cu晶体氧化还原峰。此外,在经历了5 000个循环后,氧还原曲线的半波电位下降(322 mV)严重。在5 000个循环后,P1的ECSA下降较慢,但其半波电位下降(63 mV)较多,而P2的半波电位只下降了9 mV,说明P2的壳层Cu的含量较适宜,可能起到了稳定性的正向调控作用,能缓解活性金属纳米颗粒的溶解和生长,同时高炭化温度制备的CNF能更好地抗电化学氧化,阻止颗粒的脱落长大。综上分析发现,以pH=4作为置换反应条件能得到最佳活性和稳定性的催化剂。

图8 (a)JM20、P2、P3和P4在5 000个循环的稳定性测试中的相对稳定性(ECSAn/ECSA0)的变化;JM20、P2、P3和P4稳定性测试前后的循环伏安曲线(b),(d),(f),(h)和1 600 r/min下的氧还原(ORR)曲线(c),(e),(g),(i)
3 结 论
采用静电纺丝技术制备了氮掺杂碳纳米纤维,通过改善热处理等过程,制备出了高导电性碳纳米纤维膜。为得到利于后续的原位置换Pt的Cu纳米晶/碳纳米纤维膜,进行了电沉积实验的探索。发现在反向脉冲氧化电流密度15 mA·cm-2,置换pH值为4的条件下,纤维膜不会遭受损坏,得到的Cu晶体粒径较小,且能在纤维膜内均匀分布,制备的Cu@PtCu/碳纳米纤维催化薄膜有最好的催化性能。
