表皮生长因子受体-酪氨酸激酶抑制剂靶向治疗联合CT引导下射频消融术对中晚期非小细胞肺癌患者的治疗效果
2023-03-14汪波李婷
汪波,李婷
鞍山市肿瘤医院肿瘤内科,辽宁 鞍山 114036
肺癌是起源于肺部支气管黏膜或腺体的恶性肿瘤,临床表现复杂,其中非小细胞肺癌占所有肺癌的80%[1]。随着肺癌筛查水平的进步,非小细胞肺癌可在早期被发现。对于早期肺癌患者,手术治愈率和5年生存率均可达80%[2],中晚期非小细胞肺癌患者一般无法进行手术治疗,多采用生物靶向治疗,其中以吉非替尼为主的表皮生长因子受体-酪氨酸激酶抑制剂(epidermal growth factor receptor-tyrosine kinase inhibitor,EGFR-TKI)成为一线治疗药物。而对于没有相应靶点的患者需考虑化疗,化疗虽然延长了患者的生存期,但由于化疗药物会导致患者产生恶心呕吐、骨髓抑制等一系列不良反应,严重降低了患者的生活质量[3]。近年来射频消融术在临床中广泛应用,该技术通过电磁波产生的热能杀死肿瘤细胞,具有安全、微创、并发症少、可重复性好的特点,但对于中晚期非小细胞肺癌患者,射频消融术能否替代手术还缺乏研究论证[4]。本研究探讨EGFR-TKI靶向治疗联合CT引导下射频消融术对中晚期非小细胞肺癌患者的治疗效果,现报道如下。
1 资料与方法
1.1 一般资料
收集2020年1月至2022年1月鞍山市肿瘤医院收治的中晚期非小细胞肺癌患者的病历资料。纳入标准:①符合《中华医学会肺癌临床诊疗指南(2018版)》[5]中非小细胞肺癌的诊断标准;②年龄为40~60岁;③既往未接受过手术、化疗及靶向治疗;④语言表达能力、精神正常;⑤TNM分期为Ⅲ~Ⅳ期。排除标准:①伴有严重咯血或胸腔积液;②对本研究使用的药物过敏;③合并肺部感染性疾病、血液系统疾病、急性心脑血管事件;④混合细胞性肝癌;⑤近期有外伤史及大手术史;⑥合并严重免疫系统疾病;⑦合并其他恶性肿瘤。依据纳入和排除标准,本研究共纳入80例患者。根据治疗方法的不同将患者分为对照组和观察组,每组40例,对照组患者采用CT引导下射频消融术联合化疗,观察组患者采用CT引导下射频消融术联合EGFR-TKI靶向治疗。对照组中,男25例,女15例;体重指数16~26 kg/m2,平均(22.35±2.25)kg/m2;肿瘤直径2~6 cm,平均(4.01±0.23)cm;病理类型:鳞状细胞癌12例,腺癌28例。观察组中,男23例,女 17例;体重指数 17~25 kg/m2,平均(22.31±2.20)kg/m2;肿瘤直径2~6 cm,平均(4.03±0.20)cm;病理类型:鳞状细胞癌14例,腺癌26例。两组患者的性别、体重指数、肿瘤直径、病理类型比较,差异均无统计学意义(P>0.05),具有可比性。本研究经医院伦理委员会审批通过,所有患者均知情同意。
1.2 治疗方法
两组患者均采用常规预防呕吐治疗,如控制饮食、调节输液速率等,均给予吸氧、化痰平喘、维持电解质和酸碱平衡以及营养支持等常规治疗。
对照组患者采用CT引导下射频消融术联合化疗。射频消融术:根据患者的CT和彩超检查结果选择穿刺点和穿刺角度,使用利多卡因局部麻醉,应用RITA 1500射频发射器,功率设为250 W,发射频率设为460 kHz,消融温度90℃,每次15 min,肿瘤直径<4 cm者需消融2次,肿瘤直径≥4 cm者需消融3~5次,总次数应在5次及以下,退针时需电凝止血。术后化疗:第1天,白蛋白紫杉醇150 mg/m2,静脉滴注;第2~4天,顺铂注射液30 mg/m2,静脉滴注。21天为1个周期,共治疗4个周期。
观察组患者采用CT引导下射频消融术联合EGFR-TKI靶向治疗,射频消融方法同对照组。术后1周口服吉非替尼,每次0.25 g,每天1次,共治疗4周。
1.3 观察指标和评价标准
1.3.1 特异症状采用欧洲癌症研究与治疗组织生命质量测定量表(European Organization for Research and Treatment of Cancer quality of life questionnaire core 30,EORTC QLQ-C30)[6]评价治疗前后两组患者的特异症状,包括疼痛、腹泻、疲劳、睡眠障碍、便秘、恶心呕吐6个维度,采用5级评分法,评分越高表明特异症状越严重。
1.3.2 肿瘤标志物水平分别于治疗前后采集两组患者的空腹静脉血5 ml,3000 r/min离心10 min,离心半径14 cm,采用化学发光法检测血清癌胚抗原(carcinoembryonic antigen,CEA)、糖类抗原125(carbohydrate antigen 125,CA125)、神经元特异性烯醇化酶(neuron specific enolase,NSE)水平。
1.3.3 免疫功能指标血清采集方法同1.3.2,应用流式细胞仪检测治疗前后两组患者的T淋巴细胞亚群(CD3+、CD4+)水平,计算CD4+/CD8+。
1.3.4 不良反应比较两组患者的不良反应发生情况,包括脱发、皮疹、恶心呕吐、白细胞减少。
1.4 统计学方法
采用SPSS 22.0软件对数据进行统计分析,计量资料以均数±标准差(±s)表示,组间比较采用t检验;计数资料以例数和率(%)表示,组间比较采用χ2检验。以P<0.05为差异有统计学意义。
2 结果
2.1 特异症状的比较
治疗前,两组患者疼痛、腹泻、疲劳、睡眠障碍、便秘、恶心呕吐评分比较,差异均无统计学意义(P>0.05);治疗后,两组患者疼痛、腹泻、疲劳、睡眠障碍、便秘、恶心呕吐评分均低于本组治疗前,观察组患者疼痛、腹泻、疲劳、睡眠障碍、便秘、恶心呕吐评分均低于对照组,差异均有统计学意义(P<0.05)。(表1)

表1 治疗前后两组患者EORTC QLQ-30评分的比较
2.2 肿瘤标志物水平的比较
治疗前,两组患者血清CEA、CA125、NSE水平比较,差异均无统计学意义(P>0.05);治疗后,两组患者血清CEA、CA125、NSE水平均低于本组治疗前,观察组患者血清CEA、CA125、NSE水平均低于对照组,差异均有统计学意义(P<0.05)。(表2)
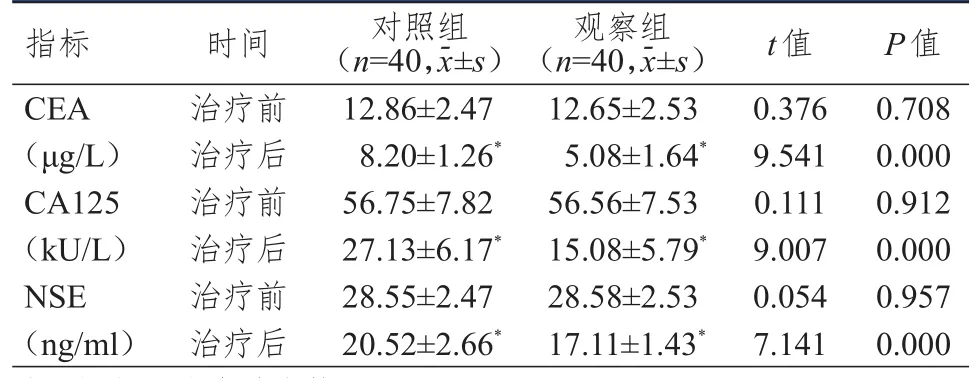
表2 治疗前后两组患者肿瘤标志物水平的比较
2.3 免疫功能指标的比较
治疗前,两组患者CD3+、CD4+水平及CD4+/CD8+比较,差异均无统计学意义(P>0.05);治疗后,两组患者CD3+、CD4+水平及CD4+/CD8+均高于本组治疗前,观察组患者CD3+、CD4+水平及CD4+/CD8+均高于对照组,差异均有统计学意义(P<0.05)。(表3)
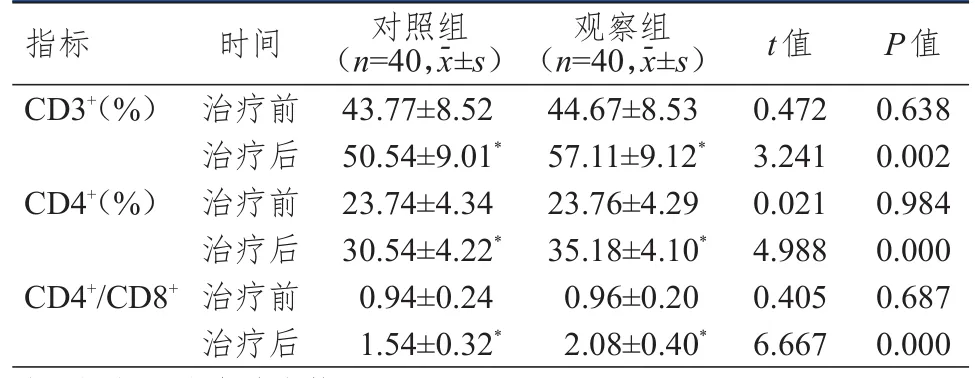
表3 治疗前后两组患者免疫功能指标的比较
2.4 不良反应发生情况的比较
观察组患者的不良反应总发生率为7.50%(3/40),明显低于对照组患者的37.50%(15/40),差异有统计学意义(χ2=10.323,P=0.001)。(表4)

表4 两组患者的不良反应发生情况[ n(%)]
3 讨论
肺癌早期诊断率较低,病死率较高,手术是治疗肺癌的主要方式,早期肺癌患者术后5年生存率为70%,而中晚期患者则不足50%,死亡原因多为远处转移和复发[7]。靶向治疗具有定位准确、针对性强的特点,可使肿瘤细胞特异性死亡,但其存在一定的劣势:仅适用于部分患者、会产生肿瘤细胞耐药以及价格昂贵等。临床中也可采用化疗治疗肿瘤,但会导致患者出现一系列不良反应。既往有研究表明,肺癌患者在确诊后45%合并抑郁,35%合并焦虑,而化疗会加重患者心理问题的严重程度[8]。目前晚期非小细胞肺癌的一线化疗方案是以铂类为基础的两药联合化疗,铂类药物属于高致吐性药物,具有神经毒性,且会损伤脏器功能,对患者造成痛苦,甚至会引起焦虑抑郁情绪,进而导致生理和心理状态的恶性循环,在一定程度上影响治疗效果。因此,寻找一种安全有效的治疗方法对改善非小细胞肺癌患者的预后非常重要。
射频消融术是近年来新兴的晚期肿瘤的治疗方法,其原理是将电磁波作用于肿瘤组织并杀死肿瘤细胞[9]。人体是由多种有机物质和无机物质组成的复杂结构,主要靠离子移动传导电流,在高频振荡下,离子沿电力线方向快速移动,离子相互摩擦与其他微粒相撞产生生物热作用。肿瘤细胞在高温状态下迅速脱水,导致DNA断裂、肿瘤凝固坏死,而且肿瘤细胞散热能力较差,对高热敏感,因此,高热可杀死肿瘤细胞[10]。当射频线流经人体组织时,细胞内的正离子和负离子与其他分子和离子摩擦升温,导致细胞水分蒸发以致无菌性坏死,进而达到治疗效果[11]。吉非替尼是一种表皮生长因子受体抑制剂,其通过将肿瘤细胞阻滞于G1期,减少肿瘤组织新生血管生成,从而抑制肿瘤细胞生长和转移,可作为肺癌治疗的靶点[12]。本研究结果显示,治疗后观察组患者疼痛、腹泻、疲劳、睡眠障碍、便秘、恶心呕吐评分及血清CEA、CA125、NSE水平均低于对照组,CD3+、CD4+水平及CD4+/CD8+均高于对照组,表明EGFR-TKI靶向治疗联合CT引导下射频消融术可有效改善中晚期非小细胞肺癌患者的临床症状和免疫功能,降低肿瘤标志物水平。有效的肿瘤标志物能够早于影像学发现病情变化,其在肿瘤诊断和预后评估中发挥着重要作用。CEA是一类酸性糖蛋白,在肺癌中呈高表达;CA125能够反映肿瘤近期变化情况;NSE主要存在于神经组织和神经内分泌组织中,可用于小细胞肺癌和非小细胞肺癌的鉴别诊断[13-14]。T淋巴细胞源于骨髓淋巴样干细胞,是免疫应答的主要参与者,在免疫调节、杀伤靶细胞方面具有重要作用。CD3+T细胞是成熟的T淋巴细胞,其升高表明患者的免疫功能较好,CD4+T细胞具有直接杀伤肿瘤细胞和免疫记忆功能,CD8+T细胞能够识别内源性抗原肽,抑制细胞免疫反应和抗体形成[15]。吉非替尼可通过增加巨噬细胞功能,促进脾淋巴细胞增殖,诱导白细胞介素和肿瘤相关细胞因子表达,提高机体免疫力[16]。此外,吉非替尼具有针对肺癌的特异性靶点,可特异性结合致癌位点,诱发肿瘤细胞凋亡,且不影响正常细胞的增殖,也不影响机体的免疫功能[17]。射频消融术和吉非替尼联合可发挥协同作用,从多方面提升抗肿瘤效果,提高患者的生活质量。本研究结果还显示,观察组患者的不良反应总发生率为7.50%,明显低于对照组患者的37.50%,差异有统计学意义(P<0.01)。说明EGFR-TKI靶向治疗联合CT引导下射频消融术治疗中晚期非小细胞肺癌具有较好的安全性。但本研究纳入的样本量较少且来源单一,缺乏多地区、大规模研究,需在今后继续开展大样本、多地区以及多方面观察治疗效果的深入研究。
综上所述,EGFR-TKI靶向治疗联合CT引导下射频消融术可有效改善中晚期非小细胞肺癌患者的临床症状和免疫功能,降低肿瘤标志物水平,安全性较高,疗效确切。
