废磷酸铁锂电池回收制备磷酸锂*
2023-03-01何佰玫郑明宇王建波陈海焱
鲁 琦,何佰玫,郑明宇,王建波,陈海焱
(1.西南科技大学 环境与资源学院,四川 绵阳 621000;2.固体废物处理与资源化教育部重点实验室,四川 绵阳 621000)
0 引言
随着世界各国对环境和能源问题的重视,以锂离子电池为主的动力电池市场迎来了爆发式增长,锂离子电池在电动汽车、固定储能领域中的应用越来越广泛[1-3]。而锂离子动力电池的寿命有限,一般为4~5 年,磷酸铁锂电池的退役高峰期即将到来[4]。根据国际能源署的预测,到2030年,全球电动汽车数量将达到1.45亿辆[5],预计到2025年报废动力电池将达到136万t。
虽然动力锂电池是一种绿色能源,但是其中仍含有许多有害物质(如有机结合剂、导电剂和碳酸酯电解液等),会污染土壤和地下水,并释放有害气体,对环境和人类健康构成严重威胁[6-7]。废动力锂电池中还含有大量有价金属元素,如锂、镍、铜和铝等,其含量比矿石中的高[8]。吴西顺等[9]的研究指出,锂资源和产业供应链仍是全球关注的热点,世界对锂资源的开发和应用极为重视。因此,对于报废量越来越大的磷酸铁锂电池,若进行合理的回收再利用,不仅可以减少其对环境产生的不利影响,还能节约宝贵的矿产资源,减少能源浪费,并带来一定的经济效益。
目前,废磷酸铁锂电池的回收工艺可分为火法回收和湿法回收。火法回收[10]是将电池拆卸和破碎后经高温焚烧,使电极材料中的金属元素转变为稳定的金属氧化物,再进行分离回收。此工艺流程短且无废水产生,但是操作环境不友好,能耗高,得到的产品纯度低,尚处于实验室研究阶段。湿法回收[11]是废磷酸铁锂电池资源化回收中运用较为成熟的工艺,主要是以酸浸富集金属Li为核心,配合不同的除杂工艺对LiFePO4进行回收,该方法回收率高,分离效果良好。
废电极材料的浸出可采用无机酸和一些有机酸进行溶解。LI等[12]采用硫酸-过氧化氢体系选择性浸出锂,约96.85%的锂从废LiFePO4电池中浸出;ZHANG等[13]以盐酸、硫酸和盐酸羟胺为浸出剂,研究发现钴和锂的浸出率高于99%。近年来,将磷酸作为浸出剂成为了研究热点,在此体系下,锂浸出率较高,且无杂质离子带入,后续除杂压力小[14-16]。目前采用湿法回收废磷酸铁锂电池的研究较多,其工艺流程为:废磷酸铁锂电池经预处理后进入以酸浸为核心的工艺环节,得到锂富集液;然后采用化学沉淀或萃取等方法进行除杂,再进一步回收有价金属锂[17-19]。其中:沉淀法操作简单,金属分离效果好,适用范围广,实用价值高[20-21];萃取法回收率高,能耗低,但是有机溶剂对环境的危害较大[22]。
目前的废磷酸铁锂电池回收工艺需消耗大量的化学试剂,成本高,废水排放量大,对环境产生了极大危害[23-24],故开展废磷酸铁锂电池的绿色高效回收研究很有必要。本文针对废磷酸铁锂电池开发了一种高效的短流程回收工艺,旨在提高其回收效率、缩短工艺流程、降低能耗及成本,为废磷酸铁锂电池的资源化回收研究提供理论参考。为了减小后续资源化回收过程中的除杂压力,采用磷酸浸出废磷酸铁锂电池粉末,得到锂富集液;对比萃取法和水解法净化锂富集液的除杂效果,以除杂效率和锂损失率为评价指标,确定最佳除杂条件;随后通过蒸发浓缩法,从净化的锂富集液中提取磷酸锂。本研究明确了以磷酸二辛酯(P-204)作为萃取剂在磷酸体系下的影响规律,可为P-204在有色金属有机萃取除杂研究中的应用提供参考。
1 实验
1.1 原料、试剂及设备
原料:经磷酸-过氧化氢体系酸浸废磷酸铁锂电池所得的锂富集液。
试剂:磷酸、过氧化氢、P-204、磺化煤油、氢氧化锂,均为分析纯。
设备:恒温磁力搅拌器、破碎机、电热恒温干燥箱、循环水多用真空泵、电感耦合等离子体发射光谱仪(ICP-OES)、X射线衍射仪(XRD)和扫描电子显微镜(SEM)等。
1.2 实验方法
1.2.1 废磷酸铁锂电池预处理
经放电处理后的废磷酸铁锂电池采用多功能粉碎机(9FQ-30型)破碎,通过0.075、0.125、0.250、0.300、0.500、1.000 mm的标准分样筛将破碎后的物料筛分成6个粒级,分析各粒级物料中不同有价金属元素的富集规律,以选择合适粒度的浸出原料,再采用磷酸-过氧化氢体系浸出获得锂富集液。每次实验称取5 g粒度<0.300 mm的废磷酸铁锂电池正负极混合粉末,置于500 mL的烧杯中,加入250 mL浓度为1 mol/L的H3PO4溶液和50 mL质量分数为1.7% 的H2O2溶液,设置恒温磁力搅拌器的转速为200 r/min,整体混合后于75 ℃恒温水浴锅中浸出,整个实验过程持续45 min。
1.2.2 废磷酸铁锂电池锂富集液净化实验
以磷酸-过氧化氢体系浸出废磷酸铁锂电池粉末获得的锂富集液为研究对象,分别采用P-204-磺化煤油溶液体系萃取和氢氧化锂水解进行净化除杂实验。P-204-磺化煤油溶液体系萃取是将有机相和料液混合装在分液漏斗中,在设定的温度下萃取一定时间,萃取结束后静置分相,排出萃余液进行收集测试;氢氧化锂水解则是使用LiOH溶液调节锂富集液的pH,在一定的温度下反应至陈化时间即趁热过滤。
采用ICP-OES测试净化后的锂富集液中主要金属离子的浓度,对比分析两种除杂方式得到的锂富集液中杂质离子的浓度,计算除杂率和锂损失率,考查不同影响因素对铜、铁、铝杂质去除率的影响,以确定最佳的除杂条件。
1.2.3 磷酸锂的制备与表征分析
将最佳除杂条件下净化后的锂富集液在磁力加热搅拌器上于150 ℃下蒸发处理1.5 h得到产品,再蒸发浓缩制得磷酸锂产品,分别采用XRD和SEM对磷酸锂进行物相和表面形貌分析。
2 结果与讨论
2.1 废磷酸铁锂电池的破碎及筛分
失活后的废磷酸铁锂电池经过拆卸、破碎和筛分后得到的物料如图1所示,各粒级物料质量分数见表1。

图1 破碎筛分废磷酸铁锂电池实验物料Fig.1 Materials to be fed to crushing and screening testing of waste lithium iron phosphate battery

表1 各粒级物料分布Table 1 Material distribution of each size fraction
由图1、表1可知,当废磷酸铁锂电池破碎产物粒径<0.300 mm 时,物料呈黑灰色,并伴有少量金属颗粒,该粒级物料最多,占废磷酸铁锂电池总质量的63.344%。
罗丽萍等[25]通过研究攀枝花地区煤矸石中金属元素的浸出行为发现,粒径对煤矸石中金属元素的浸出有影响,且不同粒径间具有较大的差异。为了尽可能提高目的金属元素Li的回收率,进一步表征分级后不同粒级下的物料成分及含量,再选取合适粒级的磷酸铁锂粉末浸出[26]。
采用HNO3-HClO4体系对不同粒级物料进行消解处理,通过ICP-OES测试得到主要金属元素的质量分数(见表2)。由表2可知,Al和Cu在>0.300 mm粒级中的质量分数很高,在>0.500 mm粒级时分别达19.566%和22.020%,这是因为>0.300 mm粒级破碎产物主要以磷酸铁锂电池的隔膜和外壳为主(见图1)。Fe和Li在<0.300 mm粒级中的质量分数相对较高,在0.250~0.300 mm粒级中分别占19.420%和19.560%,而Al和Cu的质量分数较低,据计算,电池中74.94%的锂富集在该粒级。因此,为了得到较多的废磷酸铁锂电池正负极物料,同时又减少杂质金属的引入,选择粒径<0.300 mm 的破碎粉末为后续酸浸的实验样品。

表2 不同粒级下主要金属元素的质量分数 单位:%Table 2 Contents of major metal elements with different particle sizes Unit:%
分别采用XRD和ICP-OES对粒径<0.300 mm的废磷酸铁锂电池粉末进行物相和成分分析,结果见图2、表3。从图2可以看出,样品中的主要成分是LiFePO4,还有部分铜箔和铝箔。表3与表2的分析结果吻合,试样中主要含有锂和铁,还有部分的铜和铝。

图2 粒径<0.300 mm样品的XRD图Fig.2 XRD picture of sample with particle size of less than 0.300 mm

表3 粒径<0.300 mm样品中的主要金属元素及质量分数Table 3 Major metals and their contents in samples with particle size of minus 0.300 mm
2.2 废磷酸铁锂电池锂富集液净化实验
2.2.1 萃取实验
2.2.1.1 P-204质量分数对杂质去除率的影响
在萃取体系中,P-204质量分数对杂质去除的影响规律如图3所示。由图3可知,料液中铜和铁的去除率达到100%,随着P-204质量分数的升高,其对铝的去除效果增强,但是锂的损失率也显著升高。提高萃取组分中P-204的质量分数时,萃取剂的萃取能力增强,但是锂的损失率也随之升高。综合考虑P-204成本、杂质去除率以及锂的损失率,确定P-204与磺化煤油的最佳质量比为1∶9。

图3 P-204质量分数对杂质去除率的影响Fig.3 Effect of P-204 content on removal rate of impurities
2.2.1.2 皂化率对杂质去除率的影响
在萃取体系中,皂化率对杂质去除率的影响规律如图4所示。由图4可知:随着皂化率的升高,金属被共萃取进有机相的比例增大,溶液中Fe、Al、Cu的去除率逐渐升高;当皂化率为70%时,料液中Fe和Cu的去除率均达到100%,Al的去除率为81.039%,但是锂的损失率较高(69.763%);当皂化率高于70%时,既影响萃取过程的分相, 又降低了萃余液中金属杂质的去除率。综合考虑,确定皂化率为70%。

图4 皂化率对杂质去除率的影响Fig.4 Effect of saponification rate on removal rate of impurities
2.2.1.3 油水相比对杂质去除率的影响
油水相比对杂质去除率的影响规律如图5所示。由图5可知:当油水相比为1∶1时,Cu和Fe的去除率达到100%;继续增大油水相比,各杂质离子的萃取率变化缓慢, 甚至出现下降。随着油水相比的增大,料液中Fe的去除率基本保持100%不变,Cu和Al的去除率先降低后升高,锂的损失率先升高后降低再升高,这是因为油水相比过大会使体系的黏度增大,影响分相效果和分相速度,同时也会造成萃取剂的浪费。综合考虑,油水相比为1∶1时最佳,此时Fe、Cu的去除率为100%,Al的去除率为83%。
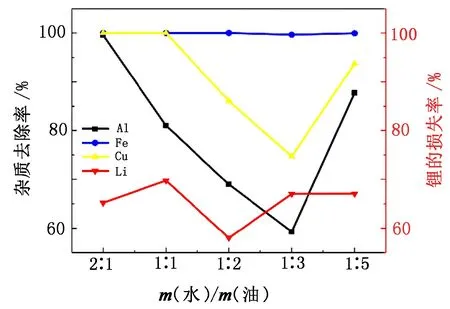
图5 油水相比对杂质去除率的影响Fig.5 Effect of oil-water ratio on impurity removal rate
2.2.1.4 水相pH对杂质去除率的影响
萃取剂P-204对不同金属离子的萃取能力受料液pH的影响较大,杂质去除率随pH的变化规律如图6所示。由图6可知:随着水相pH的增大,3种杂质的去除率均升高;当水相pH为3时,Fe和Cu的去除率达到100%,Al的去除率比pH为2时明显升高,锂的损失率降低。在该体系中实际存在两个反应相互制约:①主反应,nNaR+Men+→MeRn+nNa+;②副反应:Men++nHR→MeRn+nH+(HR为P-204,Men+为水相中的金属离子,MeRn为金属离子与P-204形成的萃合物)[26]。溶液pH增大,有利于反应向右进行,杂质的去除率变化不大,而水相中锂损失严重。综合考虑,保持水相pH为3时最佳。

图6 水相pH对杂质去除率的影响Fig.6 Effect of pH in water phase on removal rate of impurities
2.2.1.5 萃取时间对杂质去除率的影响
萃取时间对杂质去除率的影响规律见图7。
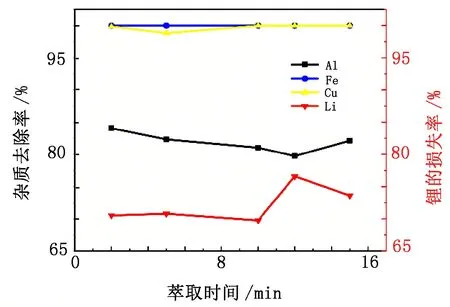
图7 萃取时间对杂质去除率的影响Fig.7 Effect of extraction time on removal rate of impurities
由图7可知:水相和有机相的萃取平衡取决于传质速度,传质速度越快所需萃取时间越短;随着萃取时间的增加,两相的接触时长增加,3种杂质的去除率呈升高趋势;当萃取时间为10 min时,Cu和Fe的去除率达到100%,Al的去除率也能保持在80%以上;但若继续延长萃取时间,金属杂质离子留在萃余液中的量反而增加,导致杂质去除率降低,锂的损失量增加。综合考虑,萃取时间为10 min时最佳。
在此条件下,虽然杂质去除率较高,但是锂的损失率也高,达到了69.763%,P-204净化除杂的效果不好。因此,本文还采用了化学沉淀法探究水解净化对锂富集液中杂质去除效率和锂的损失率的影响。
2.2.2 水解实验
2.2.2.1 溶液pH对杂质去除率的影响
采用LiOH调节溶液的pH,水解反应时间为30 min,对比研究了溶液pH为5、6、7、8、9时的除杂效果,结果如图8所示。由图8可知:不同溶液pH下,铜、铁和铝的去除效果均较好,在溶液pH为6时,3种杂质的去除率均在95%以上;随着溶液pH的继续升高,3种杂质的去除效果均得到提升,但是锂的损失率也逐渐升高。综合考虑,溶液pH=6为最佳。

图8 溶液pH对杂质去除率的影响Fig.8 Effect of pH in solution on removal rate of impurities
2.2.2.2 温度对杂质去除率的影响
采用LiOH调节溶液的pH为6,水解反应时间为30 min,对比研究了20(室温)、30、40、50、60、70 ℃下的除杂效果,结果如图9所示。
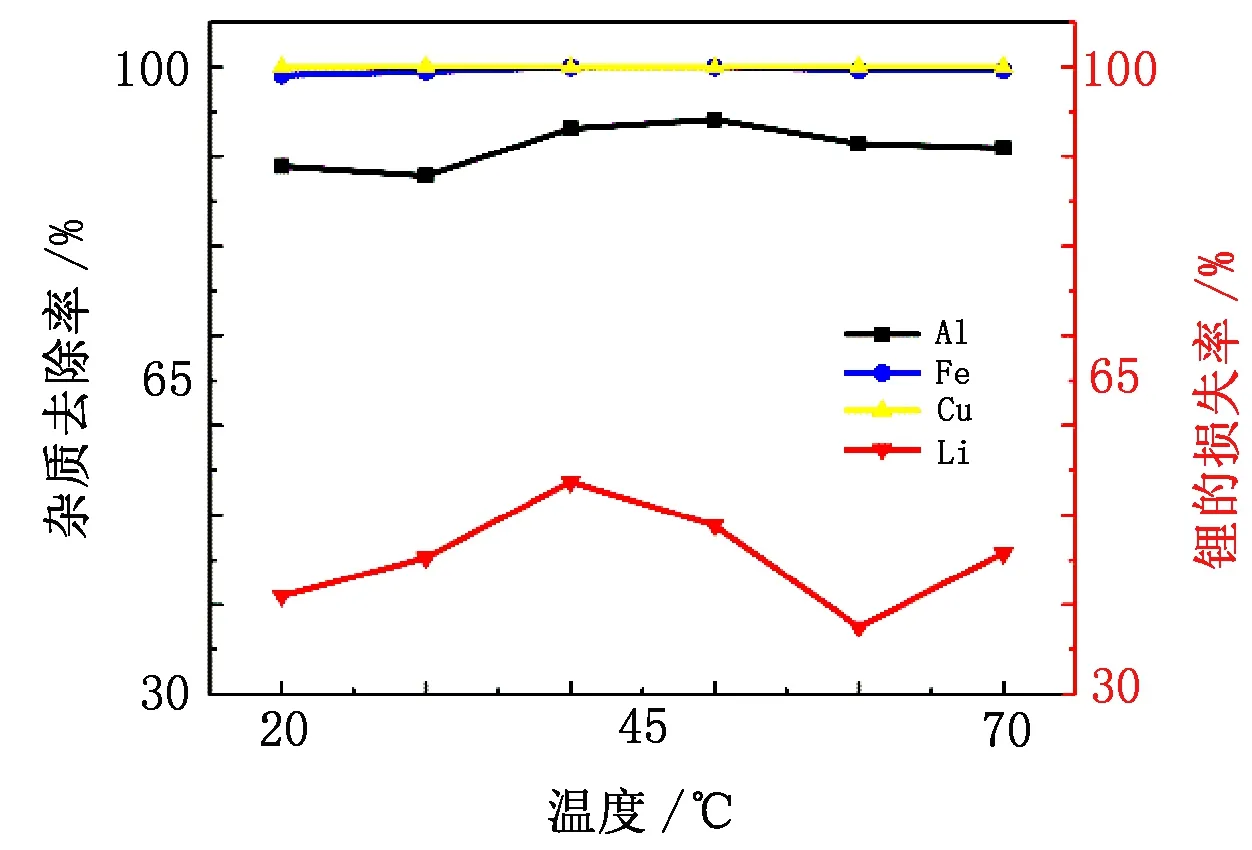
图9 温度对杂质去除率的影响Fig.9 Effect of temperature on removal rate of impurities
由图9可知:不同温度下,铜、铁、铝的去除效果均较好,温度为20 ℃时,3种杂质的去除率均高于88%;随着温度的升高,3种杂质的去除效果均得到提升,但是锂的损失率也逐渐升高;当温度为60 ℃时,3种杂质的去除率均高于90%,继续升温对杂质的去除效果无明显影响,但是会造成锂的损失率升高,原因可能是高温加快了沉淀,导致锂的夹带损失严重。考虑到操作的经济性,选择20 ℃为最佳反应温度。
2.3 磷酸锂的制备
通过对比萃取和水解除杂实验结果发现,两种净化处理对杂质铜、铁、铝的去除率接近,但是萃取实验中锂的损失率较高,综合考虑选择水解法对锂富集液进行净化除杂。即在pH=6,反应温度为20 ℃,使用0.1 g/mL的LiOH水解除杂30 min时,效果最好,此时杂质Al、Fe和Cu的去除率分别为100%、100%和82.61%,Li的损失率为53.54%。锂富集液经过水解净化除杂后,溶液中主要成分是Li+、PO43-,杂质Cu、Fe、Al的含量得到了有效控制。随后将净化溶液在150 ℃下蒸发1.5 h,得到白色固体粉末磷酸锂,经计算,锂的回收率高于45%。
利用XRD对所得磷酸锂粉末进行物相分析,结果如图10所示。物相结果显示峰型尖锐,无杂峰存在,图10中的衍射峰位置强度与标准卡片(JSPDS 71-1528)一致,说明产物为晶相纯净的磷酸锂。利用SEM分析磷酸锂的形貌,结果如图 11 所示。从图11 可以看出,颗粒粒径分布均匀,形成了规整的片状颗粒结晶,磷酸锂粉体的整体分散性好,大颗粒较少。
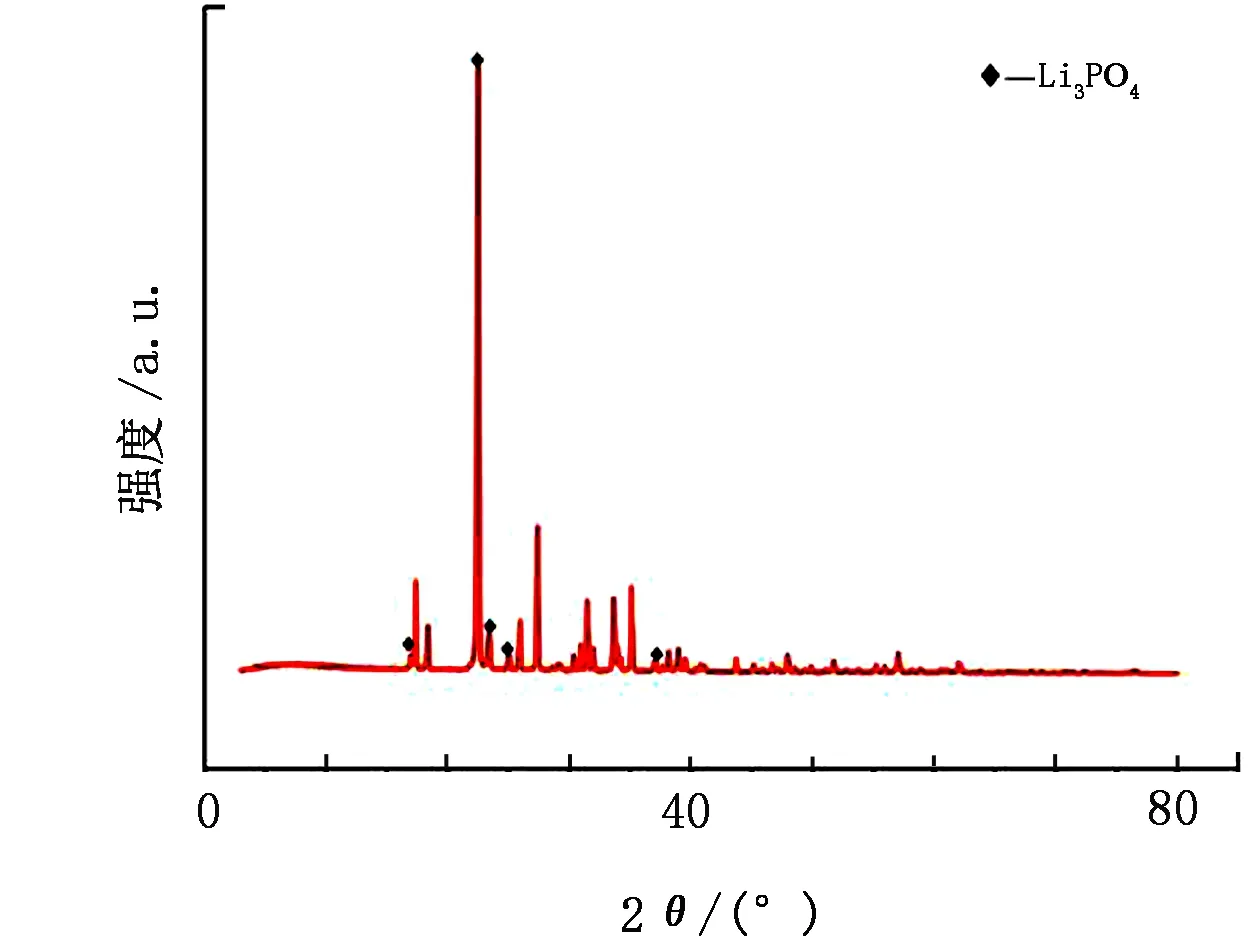
图10 磷酸锂的XRD图Fig.10 XRD diagram of lithium phosphate

图11 磷酸锂的SEM图Fig.11 SEM image of lithium phosphate
3 结论
a.废磷酸铁锂电池经破碎筛分后,大部分物料集中在<0.300 mm粒级,占63.346%。该部分物料的主要成分为LiFePO4,还有少量的铜箔和铝箔,电池中74.94%的锂富集在该粒级,因此选择<0.300 mm粒级物料进行磷酸-过氧化氢体系浸出,然后除杂净化回收有价金属元素Li。
b.通过萃取和水解对锂富集液进行净化除杂实验,综合考虑杂质铜、铁和铝的去除率以及锂的损失率,采用水解除杂的效果更好。在最佳的净化除杂条件(pH=6、反应温度为20 ℃)下,采用质量浓度为0.1 g/mL的LiOH水解除杂30 min,杂质Al、Fe和Cu的去除率分别为100%、100%和82.61%,Li的损失率为53.54%。该净化液经蒸发浓缩制得磷酸锂粉末,粉体颗粒呈规整的片状结构,后续可尝试将其用于生产彩色荧光粉、特种玻璃、光盘材料等。
c.对于废磷酸铁锂电池,采用H3PO4-H2O2体系浸出—LiOH水解除杂—蒸发浓缩工艺制得磷酸锂,该工艺流程短,化学试剂消耗少,成本低,锂回收率高于45%。
