两步沉淀耦合H2O2氧化深度处理高浓度含氰废水
2023-02-28徐文彬张艳华
徐文彬 ,周 凯 ,张艳华 ,何 龙 ,杨 林
(1.广东省危险废液资源化与深度处理技术研发企业重点实验室,广东深圳 518057;2.东江环保股份有限公司,广东深圳 518057)
氰化电镀是电镀行业常用的镀种之一,主要用于镀锌、镀镉、镀铜、镀金、镀银等〔1-3〕。氰化电镀过程中产生的含氰废水具有如下特点:一是氰化物浓度高,每升废水中的总氰质量可达几十克;二是废水成分复杂,废水中除含有剧毒游离氰外,还有与金属离子络合形成的铜氰、锌氰、铁氰等金属氰化络合物,这些物质进入水体后会对水环境造成严重污染。为消除高浓度含氰废水造成的环境污染,必须采用合适的处理工艺,使其达到国家排放标准。
国内针对高浓度电镀含氰废水的无害化处理方法主要有络合沉淀法〔4-6〕和化学氧化法〔7-8〕。络合沉淀法常用硫酸亚铁作为沉淀剂,与含氰废水中氰化物络合形成Fe4[Fe(CN)6]3沉淀,达到去除氰化物的目的,但该方法无法直接将总氰处理至排放标准要求。常规化学氧化剂如次氯酸钠、二氧化氯、臭氧等,无法破坏废水中的铁氰络合离子;有研究〔9-10〕表明,紫外光照射能催化氧化铁氰化物,但处理条件苛刻,难以应用于生产中。因此,如何高效、稳定地处理铁氰等金属络合物是深度处理高浓度电镀含氰废水的关键。
针对公司收运的电镀含氰废水中铁氰络合物浓度高的特点,本研究采用硫酸亚铁与氯化锌两步沉淀耦合H2O2氧化的深度处理技术对高浓度含氰废水进行处理,总氰及主要重金属离子浓度可达到国家相关废水排放标准。该技术处理效果好、工艺简单,具有良好的经济效益和环境效益。
1 实验部分
1.1 材料与仪器
废水取自广东某电镀厂高浓度含氰废水,主要成分见表1。

表1 含氰废水主要成分Table 1 Main components of cyanide-containing wastewater
试剂:氢氧化钠(AR)、浓硫酸(AR)、七水硫酸亚铁(AR)、氯化锌(AR),双氧水(质量分数30%)。
仪器:雷磁pHS-30型pH计、IKA RW 20数显搅拌器、HZ2001C型分析天平、自制尾气吸收装置。
1.2 实验方法
1.2.1 两步沉淀处理
取300 mL高浓度含氰废水,加入质量分数为30%的氢氧化钠或硫酸调节废水pH后,再加入一定量质量分数为40%的硫酸亚铁溶液,室温下搅拌反应40 min,静置,过滤去除沉渣;取滤液加入氯化锌进一步沉淀,加入质量分数为10%的氢氧化钠或硫酸调节反应液pH,在室温下搅拌反应40 min,固液分离。对两步沉淀过程中的溶液取样分析,测定总氰、游离氰及铜、铬、锌离子的含量,并计算总氰、游离氰去除率。该步工艺的主要沉淀反应见式(1)~式(6)。
1.2.2 H2O2深度处理
取300 mL经两步沉淀处理后的含氰废水,加入质量分数为10%的氢氧化钠调节废水pH,待pH稳定后,加入一定量H2O2进行深度氧化处理;室温下反应40 min后,静置,取上清液分析检测总氰含量,并计算总氰去除率。H2O2深度氧化反应见式(7)和式(8)。
两步沉淀耦合H2O2氧化深度处理工艺流程如图1所示。

图1 工艺流程Fig. 1 Process flow
1.3 分析方法
高浓度总氰、游离氰采用银容量法检测,低浓度总氰、游离氰采用异烟酸-吡唑啉酮分光光度法(HJ 484—2009)检测;重金属离子含量采用ICP检测(HJ 776—2015)。
2 结果与讨论
2.1 硫酸亚铁投加量对其沉淀处理含氰废水的影响
取7份300 mL高浓度含氰废水,调节废水pH=8,按式(1)~式(4)计算硫酸亚铁的理论投加量为56.2 g,按不同投加质量比(实际投加量/理论投加量)加入硫酸亚铁,常温下搅拌反应40 min后,取样测定总氰、游离氰及铜、铬、锌离子的含量。硫酸亚铁投加量对含氰废水处理效果的影响见图2。

图2 硫酸亚铁投加量对含氰废水处理效果的影响Fig. 2 Effect of FeSO4 dosage on treatment of cyanide-containing wastewater
由图2可以看出,加入硫酸亚铁对废水中总氰及游离氰的去除效果很明显,硫酸亚铁投加量越大,总氰和游离氰的去除率也随之增大。当硫酸亚铁实际投加量与理论量之比达到1.5时,废水中总氰和游离氰的去除率分别达到99.9%和99.8%,总氰和游离氰质量浓度分别降至57.4 mg/L和4.6 mg/L;继续增大硫酸亚铁投加量,总氰去除率变化不大。综合考虑,选择硫酸亚铁投加量为理论投加量的1.5倍。
从图2也可以看出,硫酸亚铁对废水中重金属离子也具有较好的处理效果,原因可能是CN-具有强配位络合能力,废水中的重金属离子大多以重金属氰化络 合 物 的 形态存在,如[Zn(CN)4]2-、[Cu(CN)4]2-、[Cr(CN)6]3-等,重金属氰化络合物可以和加入的Fe2+发生沉淀反应。随着硫酸亚铁投加量增大,溶液中Fe2+浓度随之增大,促使沉淀反应向正向进行,废水中氰化物和铜、铬、锌等重金属离子含量降低。当硫酸亚铁实际投加量与理论投加量之比为1.5时,废水中铜、铬、锌离子质量浓度可分别降低至0.1、0.31、0.27 mg/L。
2.2 pH对硫酸亚铁沉淀处理含氰废水的影响
取300 mL含氰废水,按实际量/理论量=1.5的比例投加硫酸亚铁,分别用质量分数为30%的氢氧化钠和硫酸调节废水pH为6~11,搅拌反应40 min后,取样测定总氰、游离氰及铜、铬、锌离子含量。pH对硫酸亚铁沉淀处理含氰废水效果的影响见图3。

图3 pH对硫酸亚铁处理含氰废水效果的影响Fig. 3 Effect of pH on the treatment of cyanide-containing wastewater by FeSO4
由图3可知,pH对总氰和游离氰去除率影响明显,随pH增大,总氰和游离氰去除率明显下降。pH为11时,总氰和游离氰去除率分别仅为90.4%和86.7%;而pH=8时,总氰和游离氰去除率分别达到99.9%和99.8%。实验检测到反应pH=8、9、10时总氰质量浓度分别为57.4、1 079.4、2 981.2 mg/L,总铁质量浓度分别为41.46、395.47、1 092.17 mg/L。总氰去除率随pH增大而降低的原因可能是部分亚铁氰化铁沉淀在碱性条件下发生水解生成[Fe(CN)6]4-,导致溶液中总氰浓度升高。综合考虑,硫酸亚铁沉淀反应的最适pH为8。
2.3 氯化锌投加量对其沉淀处理含氰废水的影响
按2.1和2.2章节的优化条件对含氰废水进行硫酸亚铁沉淀处理,处理后废水总氰质量浓度为57.4 mg/L,pH为8,总铁质量浓度为41.46 mg/L。取7份300 mL硫酸亚铁沉淀处理后的含氰废水,根据式(5)和式(6)计算氯化锌的理论用量为30.02 mg,按照一定投加质量比(实际投加量/理论投加量)向含氰废水中加入氯化锌,用质量分数为10%的氢氧化钠或硫酸调节废水pH=5,搅拌反应40 min后,取样测定总氰及铁离子含量。氯化锌投加量对其沉淀处理含氰废水效果的影响见图4。
由图4可知,随氯化锌投加量增加,废水中总氰去除率逐渐增大。因为Zn2+浓度增大促进了Zn2+与CN-、[Fe(CN)6]4-的沉淀反应,使得废水中总氰和铁离子含量降低;氯化锌投加量越大,沉淀反应越完全。氯化锌实际投加量与理论量之比增至2时,总氰去除率达到97.5%,处理后废水中总氰质量浓度为1.65 mg/L;此后继续增大氯化锌投加量,总氰去除率和铁离子含量都未发生明显变化,沉淀反应基本达到平衡。综合考虑,最适氯化锌实际投加量与理论投加量之比为2。
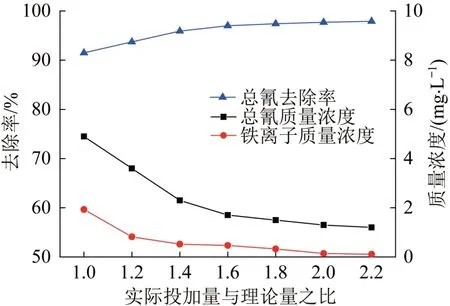
图4 氯化锌投加量对含氰废水处理效果的影响Fig. 4 Effect of ZnCl2 dosage on the treatment of cyanide-containing wastewater
2.4 pH对氯化锌沉淀处理含氰废水的影响
取6份300 mL硫酸亚铁沉淀处理后的含氰废水,加入理论加药量2倍的氯化锌,分别用质量分数为10%的氢氧化钠和硫酸调节溶液pH为5~10,搅拌反应40 min后,取样测定溶液中总氰及铁离子含量。pH对氯化锌沉淀处理含氰废水效果的影响见图5。

图5 pH对氯化锌处理含氰废水效果的影响Fig. 5 Effect of pH on the treatment of cyanide-containing wastewater by ZnCl2
由图5可知,随pH升高,总氰去除率逐渐降低,尤其在碱性条件下,总氰去除率降低更加显著,碱性越强,总氰去除率越低,该沉淀反应受pH影响较大。Zn2[Fe(CN)6]络合沉淀在碱性条件下容易水解,且碱性越强,水解程度越大,废水中总氰浓度因而越高。综合考虑,选择最佳反应pH为6,处理后废水中总氰质量浓度降低至1.65 mg/L。
2.5 H2O2投加量对H2O2氧化处理含氰废水的影响
按上述两步沉淀法的最佳条件对含氰废水进行处理,处理后废水中总氰质量浓度为1.65 mg/L,pH=6。取5份300 mL两步沉淀处理后的含氰废水,根据式(7)和式(8)计算H2O2的理论投加量为2.16 mg,按照一定投加质量比(实际投加量/理论投加量)投加H2O2,调节废水pH=8,搅拌反应40 min后,取样测定溶液中总氰含量。H2O2投加量对H2O2氧化处理含氰废水效果的影响见图6。
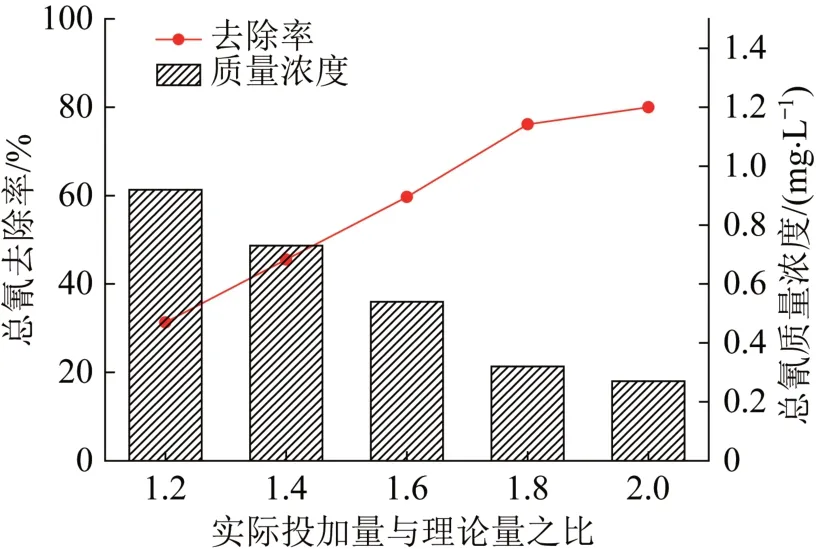
图6 H2O2投加量对含氰废水处理效果的影响Fig. 6 Effect of H2O2 dosage on the treatment of cyanide-containing wastewater
由图6可知,随着H2O2投加量增加,废水总氰去除率逐渐增大。当实际投加量超过理论投加量的1.8倍后,总氰去除率增幅不再显著。在H2O2投加量为理论值的1.8倍时,总氰去除率为76.1%,废水中剩余总氰质量浓度为0.32 mg/L,达到《污水综合排放标准》(GB 8978—1996)一级排放标准,即总氰质量浓度<0.5 mg/L。因此,H2O2最适投加量与理论投加量之比为1.8。
2.6 pH对H2O2氧化处理含氰废水的影响
取6份300 mL两步沉淀处理后的含氰废水,按照理论投加量的1.8倍投加H2O2,用质量分数为10%的氢氧化钠调节废水pH,搅拌反应40 min后,取样测定溶液中总氰含量。pH对H2O2氧化处理含氰废水效果的影响见图7。
由图7可知,当pH≤9时,随着pH升高,废水总氰去除率也逐渐增大;当pH=9时,总氰去除率达到最高,为76.1%,此时废水中剩余总氰质量浓度为0.32 mg/L。当pH>9时,随着pH升高,废水总氰去除率反而逐渐降低,这可能是因为随着反应体系碱性增强(pH>9),H2O2更容易发生水解,导致有效活性氧化物质减少,从而减弱对总氰的去除效果。综合考虑,最适反应pH为9。

图7 pH对H2O2处理含氰废水效果的影响Fig. 7 Effect of pH on the treatment of cyanide-containing wastewater by H2O2
2.7 多批次处理稳定性
取5批次高浓度含氰废水,投加1.5倍理论投加量的硫酸亚铁,调节pH=8,搅拌反应40 min;取第一步沉淀处理后废水,继续投加2倍理论投加量的氯化锌,调节pH=6,搅拌反应40 min;取经第二步沉淀处理后废水,调节废水pH=9,加入1.8倍理论投加量的H2O2,氧化反应40 min。分析检测各批次出水水质,并考察出水总氰处理效果的稳定性,结果见图8。
由图8可知,采用优化的两步沉淀耦合H2O2氧化工艺深度处理高浓度含氰废水后,出水总盐含量降低,废水总氰质量浓度可稳定降低至0.5 mg/L以下,总氰去除率接近100%,总铬质量浓度低于0.5 mg/L,总铜质量浓度低于0.3 mg/L,总锌质量浓度低于1 mg/L,说明处理后的出水总氰和重金属离子均能稳定达标。

图8 两步沉淀耦合H2O2氧化深度处理高浓度含氰废水稳定性Fig. 8 Stability of two-step precipitation coupled with H2O2 oxidation for advanced treatment of high concentration cyanide-containing wastewater
2.8 经济效益
该工艺的实际运行成本为804.44元/t,其中电费为2.1元/t,人工费为4.1元/t,药剂费为269.32元/t(费用明细见表2),滤泥处理费为528.92元/t(处理1 t含氰废水产生406.86 kg滤泥,含水率61.14%)。目前此类高浓度电镀含氰废水(总氰质量浓度超过20 g/L)收运费用约3 000~5 000元/t。按此工艺处理,具有可观的经济效益。

表2 水处理药剂成本Table 2 The chemical cost of water treatment
3 结论
(1)两步沉淀耦合H2O2氧化深度处理高浓度含铁氰化物废水效果良好,工艺稳定,出水总氰和铜、铬、锌等重金属离子浓度均达到国家《污水综合排放标准》(GB 8978—1996)一级排放标准要求。
(2)室温下应用两步沉淀法的最优工艺参数为:硫酸亚铁实际投加量与理论投加量之比为1.5,反应pH=8;氯化锌实际投加量与理论投加量之比为2,反应pH=6。
(3)应用H2O2氧化深度处理经两步沉淀处理后的含氰废水的最优工艺参数为:H2O2实际投加量与理论投加量之比为1.8,反应pH=9。