水中微塑料污染及转化去除的研究进展
2023-02-27马惠芳闫桂焕王文语
杨 敏,王 莹,陈 蕾,马惠芳,闫桂焕,王文语*
(1.齐鲁工业大学(山东省科学院),环境科学与工程学院,济南 250353;2.齐鲁工业大学(山东省科学院),山东省科学院生态研究所,济南 250013)
0 前言
塑料制品被广泛应用,但由于塑料垃圾回收率低和管理不当等问题,导致其不可避免地进入水生环境,通过物理、光照和生物降解的方式被分解成微塑料。微塑料是指颗粒粒径小于5 mm的塑料,其作为1种新兴污染物已成为目前亟待解决的环境问题[1]。
微塑料的研究最早可追溯到20世纪70年代,早期研究主要集中于海洋环境中,目前可遍及河流、湖泊以及整个水体环境[2]。张子琪等[3]对中国各种水环境中微塑料的污染情况进行了综述分析,现阶段我国对不同水环境中微塑料污染情况的研究比较分散,且对微塑料在不同水域中的迁移赋存很少报道,提出未来研究应加强对微塑料各个迁移环节的连续式研究,将微塑料的研究扩展至整个水循环系统。微塑料的体积小、比表面积大、疏水性强,易吸附许多疏水性有机污染物、重金属等形成复合污染物,被水生生物摄食后可威胁其生命和发育,一旦通过食物链被人体摄入,对人类的健康会造成潜在的风险[4]。Dong等[5]通过全面综述动物在环境中接触微塑料的途径,表明微塑料可以通过水、食物、呼吸甚至皮肤进入动物体内,通过肺部和消化道进入血液循环,并最终在各种组织中积累,通过食物链的方式对人体健康造成潜在危害。面对水中微塑料污染的严峻现状,从微塑料污染与控制的角度,对微塑料的污染特征、迁移转化机制、构效关系及去除机理等方面有待深入论述,为微塑料污染防治理论和去除技术提供参考。
1 水环境中微塑料的污染特征
微塑料在种类、形状、来源和分布上具有多样性,其不仅可以直接进入水环境,而且能够在水体中迁移转化。在迁移转化过程中会释放出有机单体和有毒添加剂,对生态系统造成了严重的危害,进而威胁人体健康。
1.1 微塑料的来源和分布
微塑料按来源可分为初生微塑料和次生微塑料两大类[6]。初生微塑料最主要的来源之一是个人洗护产品中的塑料微珠和清洁产品中的磨砂颗粒,在使用后会随生活废水排入到污水处理系统,由于其粒径小、密度低等不易从污水中分离去除,而随尾水排放到水环境中[7]。此外,初生微塑料也存在于工业原料中,因工业生产过程中管控不严而排放到环境中[8]。次生微塑料一般指大片塑料因自然风化、紫外辐射和物理磨损等物理、化学以及生物降解的作用,所形成的微小塑料颗粒。这类微塑料主要因塑料产品在使用后的不当丢弃,经物理磨损、降解等过程进入环境[9],已成为环境中微塑料的主要来源[10]。
微塑料已广泛存在于世界各地的河流、湖泊等水环境中,主要聚合物类型包括聚乙烯(PE)、聚丙烯(PP)、聚氯乙烯(PVC)、聚苯乙烯(PS)、聚对苯二甲酸乙二醇酯(PET)等[11]。PE主要应用于薄膜、包装、电线电缆、管道等材料的制作, 以及汽车、建筑等领域[12-13];PP广泛应用于服装、医疗器械、汽车零件、输送管道、化工容器等生产,也用于食品、药品的包装[14-15];PVC曾是世界上产量最大的通用塑料,广泛应用于建筑材料、发泡材料、密封材料、工业制品、日用品、人造革等领域[16];PS主要用于包装容器、日用品及电子电器三大行业[15,17];PET最早应用于合成纤维,而后广泛应用于薄膜、工程塑料和聚酯瓶等[18]。微塑料在形状上可分为纤维状、泡沫状、薄膜状和碎片状,其中纤维状微塑料主要来源是衣物的洗涤过程[17],泡沫状微塑料则主要来自隔热材料以及设施包装,薄膜状和碎片状微塑料主要由大塑料碎片和农用薄膜破碎形成。表1汇总了世界部分地区地表水环境中微塑料的分布情况,但由于微塑料的分布受到人口密度、季节、水文特征和微塑料本身性质等诸多因素的影响[19],同时对微塑料的定量和定性仍没有统一、标准化的方法,所以表中的结果仅可作为认识世界部分地区地表水环境中微塑料污染情况的参考。
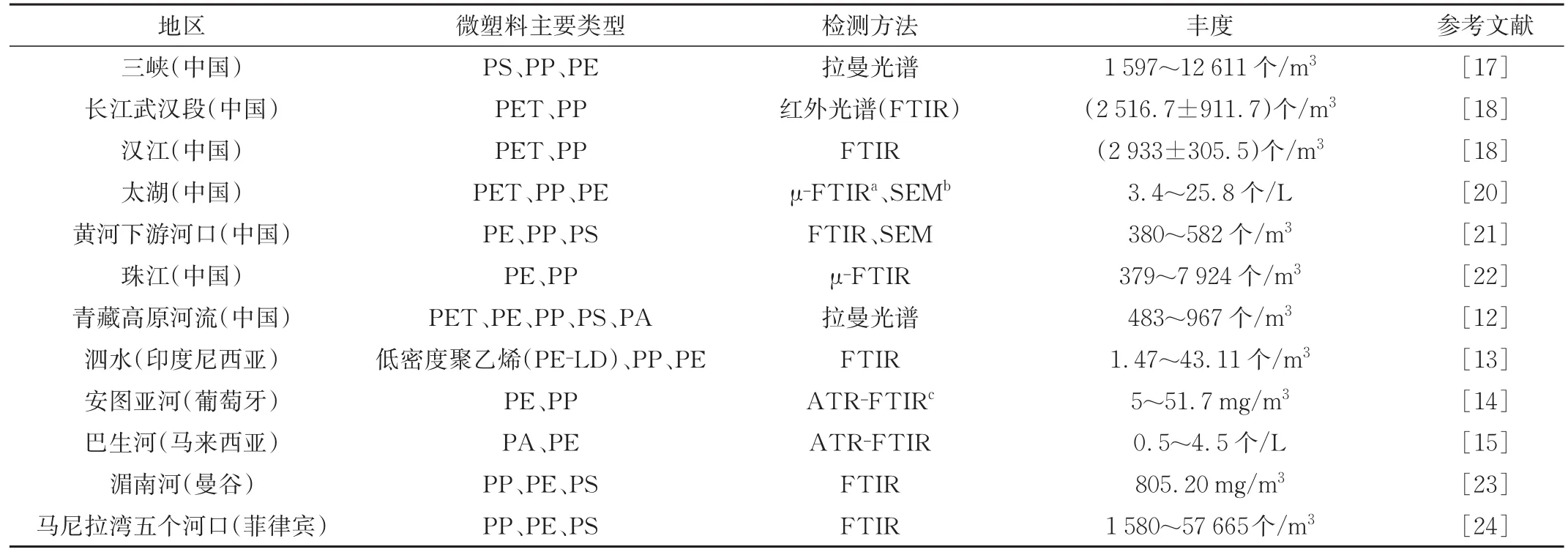
表1 世界部分地区地表水环境中的微塑料分布现状Tab.1 Status of microplastics distribution in surface water environment in some regions of the world
1.2 微塑料的迁移转化过程
大部分微塑料的密度较小,由于水流湍急且不易沉积,多会漂浮在水面,在风力、洋流、海啸等外力作用下,沿水流向下游迁移到海洋环境或封闭的湖泊中[25]。漂浮在水体表面的微塑料碎片容易受到紫外线和可见光诱导的氧化降解作用,引起微塑料表面官能团发生变化,进而改变其化学特性。Bandow等[26]研究发现老化后的微塑料表面会形成许多含氧官能团,包括C=O、C—O和·OH等,含氧官能团能够增加微塑料与有机污染物之间的亲水性,使得亲水性有机物更容易吸附在微塑料表面。Lapointe等[27]对原始和风化的微塑料进行研究,并对风化微塑料做了表征,在风化的PE微球上出现了新的官能团,如羟基、芳烃、羧基和乙烯基,羟基和羧酸基团的形成主要与紫外线照射有关,而乙烯基的形成归因于光氧化和天然有机物的吸附。此外,老化后的微塑料结晶度显著降低,表面官能团会发生一定的变化,导致对水体中重金属的吸附能力增强[28]。Mao等[29]研究了PS在紫外线照射下老化后对重金属的吸附性能,结果表明老化可以显著增加PS对重金属的吸附。
密度较大的微塑料会在重力的作用下沉降在河流、湖泊的底部或悬浮在深层水体中,沉积在底部的微塑料会和淤泥掺杂在一起,不易随水流迁移[30]。太湖和三峡水库的沉积物中检测到大量微塑料,其主要类型是密度均大于水的PS和PET[25],表明密度较大的微塑料大部分会迁移至底部。此外,漂浮的微塑料碎片会由于微生物在其表面定居和聚集,从而导致微塑料的密度增加而下沉至水底。
另外,通过食物链的传递是微塑料的1个重要迁移途径。早期研究表明,海洋中的鱼类、甲壳类动物、浮游动物等能够摄入微塑料[31],使微塑料从海洋的表层或底部迁移至生物体内,随后通过食物链进入到更高营养级的生物体内。然而,被水生生物摄入的微塑料,只有少部分通过消化系统进入其他组织滞留在体内,大部分会排出体外,再次进入到水环境中[32]。微塑料在水环境中迁移的同时也会受到微生物降解作用的影响,微生物首先分泌胞外聚合物,通过分解酶将大颗粒的塑料分解转化为小分子的中间产物(单体、低聚物或二聚物),而后这些中间产物作为微生物的碳源被进一步矿化为二氧化碳、水或甲烷[33]。
综上所述,微塑料无论是在老化、沉积还是在微生物的降解过程中,都很容易浸出各种有毒有害的物质,通过自然途径或通过生物摄食对水体环境造成严重的污染,对生物甚至人类产生潜在危害。此外,老化后的微塑料吸附其他有机污染物和重金属后形成复合污染物。这种复合污染物由于重力作用可能沉积在水底,和沉积物掺杂在一起,对水体产生持久性的污染,同时也可能发生远距离迁移,在一定程度上增加了污染范围,对生态系统造成严重的威胁。
1.3 微塑料的危害
水环境中的微塑料严重威胁着水生生物的生长活动和生命健康,并对生态系统造成潜在的风险。以下从物理、化学和表面微生物3个方面阐述微塑料对水生生物的危害,并进一步论述了微塑料对人体健康的潜在威胁。
1.3.1 微塑料对水生生物的危害
(1) 物理危害
一些水生生物在摄食时会误食微塑料颗粒,由于它们无法区别食物和微塑料颗粒,在咀嚼过程中会对颌骨造成损害[34],同时进入到生物体内的一部分微塑料颗粒相对坚硬,会直接划伤肠道等器官和其他组织,其他颗粒也会由于长期的摩擦造成器官和组织的损伤[35]。另外,微塑料颗粒在被鱼类等生物摄入后会造成消化道的堵塞,食物和微塑料颗粒在消化系统中积累,使其产生1种虚假的饱腹感,从而减少进食导致营养的缺乏[36]。
(2) 化学危害
微塑料对水生生物的化学危害是其主要的潜在危害,漂浮的微塑料能吸附持久性有机物、重金属和抗生素等许多污染物形成复合污染物[37],其更难降解、毒性更强,被水生生物摄食后对生态环境和人体健康会造成更大的威胁。持久性有机物比较稳定,被疏水性的微塑料吸附后形成复合污染物会增强它们在环境中的潜在毒性,一旦被水生生物摄入,会造成内分泌失调、基因突变和癌变等,进而危害到整个水生生态系统[2]。Rochman等[38]研究发现低密度PE吸附多环芳烃和多氯联苯后投喂给青鳉鱼会产生联合毒性效应,青鳉鱼出现糖原耗竭和细胞坏死等肝脏损伤。微塑料对重金属有很高的亲和力,二者的协同作用增加了重金属的毒性[39]。Lu等[40]通过研究微塑料对斑马鱼组织中镉积累的影响,并探讨微塑料和镉联合暴露引起的慢性毒性作用,基于对组织病理学观察和功能基因表达等综合分析,结果表明微塑料增强了镉对斑马鱼的毒性,并且联合暴露引起了斑马鱼组织的氧化损伤和炎症。抗生素是一类备受关注的新兴污染物,其被微塑料吸附后对生态系统造成潜在风险[41]。Han等[42]通过研究贻贝中土霉素、氟苯尼考和磺胺甲恶唑在PS共存的情况下的免疫毒性作用,发现微塑料会加剧抗生素的积累,微塑料和抗生素的共同暴露会引起活性氧、F-肌动蛋白细胞骨架和细胞活力的改变。
塑料产品中一般都会掺杂增塑剂、热稳定剂和着色剂等各种添加剂,一旦浸出到水环境中,会扰乱水生生物体的内分泌系统、造成生殖毒性并影响生长发育[43],通过食物链传递后会威胁整个生态系统,而处于食物链顶端的人类将会是最终的受害者。常用的添加剂有溴化阻燃剂、双酚A、壬基酚和邻苯二甲酸酯等。多溴联苯醚和六溴环十二烷是塑料工业中最常见的溴化阻燃剂。Sun等[44]研究证明微塑料被生物摄入后,其中的添加剂多溴联苯醚会浸出到生物体组织中,从而导致化学物质暴露增加。Jang等[45]调查了栖息在PS泡沫塑料中的贻贝积累六溴环十二烷的特征,发现贻贝中六溴环十二烷含量高达5 160 ng/g脂重,而且贻贝内部存在PS泡沫塑料颗粒,表明微塑料的摄入是六溴环十二烷进入贻贝的重要途径。双酚A常用作聚合物的抗氧化剂和增塑剂,被生物所接触后可影响其生长发育,甚至有致畸、致癌作用[46]。Chen等[47]通过研究在纳米塑料存在与不存在的情况下斑马鱼中双酚A的生物蓄积潜力,发现纳米塑料的存在导致斑马鱼头部和内脏的双酚A吸收量明显增加2.2倍和2.6倍,双酚A和纳米塑料都能引起中枢神经系统中髓鞘碱性蛋白/基因的上调,同时对乙酰胆碱酯酶的活性有明显的抑制作用。壬基酚作为1种内分泌干扰物,常用于生产塑料的抗氧化剂和增塑剂,在被水生生物群降解后,很容易浸入到周围环境中,即便浓度很低,也极具危害性[48]。Browne等[49]研究发现微塑料能将壬基酚和菲转移到沙蚕的肠道组织中,引起一些生物效应,并且会使体腔细胞去除病原菌的能力降低60 %以上,损害生物体的生理功能。邻苯二甲酸酯作为1种内分泌干扰物是1种常见的增塑剂,主要用于PVC的生产。由于邻苯二甲酸酯不与塑料聚合物共价结合,在制造、使用和处置过程中很容易渗入到环境中[16],对神经系统和生殖系统造成潜在威胁,尤其对婴幼儿的影响较大。Mathieu-Denoncourt等[50]研究发现邻苯二甲酸二甲酯和邻苯二甲酸二环己酯可增加蝌蚪的畸形率,并上调细胞应激相关信使核糖核酸水平。
(3) 表面微生物的危害
微塑料的物理、化学性质稳定,可为水体中的微生物提供适宜的栖息环境。各种微生物(包括致病菌)会附着在微塑料的表面,使微塑料成为致病菌的载体,随着微塑料在水体中的迁移发生扩散,导致疾病的传播[51]。附着在微塑料表面的致病菌往往不止1种,不同的菌种基因重组会产生新型物种,新型物种的出现易对水生生物的生存造成更加严重的威胁[52]。此外,微塑料上的基因重组可能产生耐药菌,从而加速耐药菌的迁移及其携带的抗性基因在环境中的泛滥[53]。另外,微生物附着在微塑料表面迁移至其他生态系统将导致物种入侵,给生态系统造成更大的威胁。Goldstein等[54]研究发现漂浮流入北太平洋珊瑚礁生态系统的塑料垃圾附着病原体,从而导致珊瑚骨骼侵蚀带疾病。因此,微生物随微塑料的迁移将导致一系列多样且复杂的生态效应,进而危害水生生态系统的健康。
1.3.2 微塑料对人体健康的潜在危害
海产品是人类饮食中的1个重要部分,而海产品中存在的微塑料会以食物链的方式进入人体,微塑料进入人体肠道系统会构成向身体其他部位扩散的严重风险,表2总结了微塑料在毒理学角度对人体的一些潜在危害。
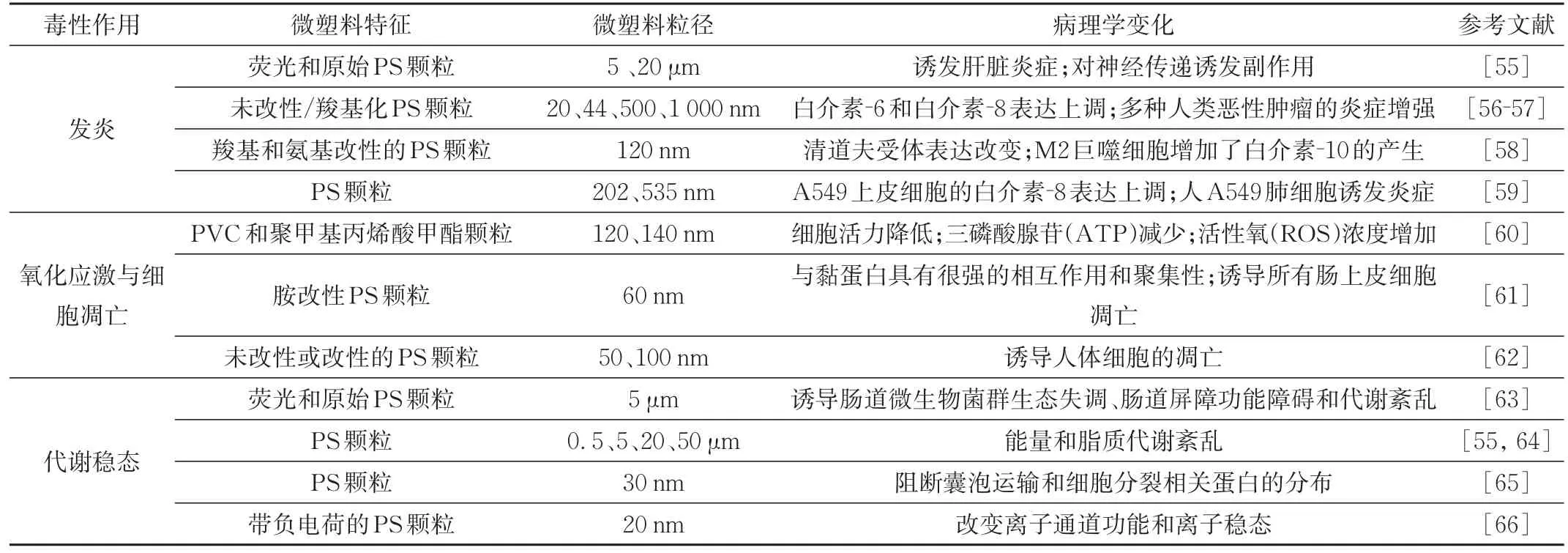
表2 微塑料对人体健康的潜在危害Tab.2 Potential human health hazards of microplastics
2 水环境中微塑料的去除
鉴于微塑料对生态系统以及人体健康的严重影响,减少甚至消除水环境中的微塑料污染是现阶段亟须解决的问题。针对水环境中微塑料的去除,本文以物理、化学和生物处理方法为指导,主要对混凝、高级氧化和膜生物反应器技术进行了论述。
2.1 混凝
混凝法主要是利用各种混凝剂改变溶解和悬浮固体的物理状态,使其通过沉淀去除的1种净水技术[67],对微塑料的去除机制如图1所示。电荷中和是混凝去除微塑料的主要机制之一,投加混凝剂后,微塑料的表面电荷会被中和,静电排斥力会降低到最小,由于沉淀作用,微塑料聚集在一起形成大尺寸的絮状物[68]。此外,吸附架桥在混凝中也发挥着重要作用,聚合物在静电引力、范德华力和化学键的作用下,通过活性位点与未达到完全脱稳的微塑料连接,发挥吸附架桥效应[69]。当混凝剂的投加量足够大时会产生网捕卷扫作用,金属盐混凝剂产生的絮凝氢氧化物具有巨大的网状表面结构和一定的静电黏附能力,在沉积物生成过程中,微塑料颗粒被网捕在沉积物中并迅速被沉积物卷扫[70]。混凝法具有成本低,可升级等优点,在去除微塑料方面表现出了良好的性能,但因其混凝剂种类和混凝条件的限制,混凝法对微塑料的去除效果差异较大,因此通过优化混凝工艺提高去除效率显得尤为重要。Rajala等[71]研究了混凝沉淀对二级废水处理厂流出基质中微塑料的去除,对于尺寸为1 μm的PS微塑料,氯化铁对其去除率达到99.4 %,而聚合氯化铝对其去除率为98.2 %。Ma等[72]使用传统铁基混凝剂对PE颗粒的去除率低于15 %,但聚丙烯酰胺的投加显著提高了PE的去除效率,特别是阴离子聚丙烯酰胺与高剂量的铁基盐结合,能够增加絮体的密度,使更多的PE颗粒被铁基絮体吸附和捕获,去除率高达90.9 %。Pivokonsky等[73]调查了污水处理厂原水和经过处理后水中的微塑料浓度,发现混凝沉淀工艺对尺寸在1~5 μm的微塑料去除率达到62 %,比深床过滤和活性炭过滤工艺去除效果好。
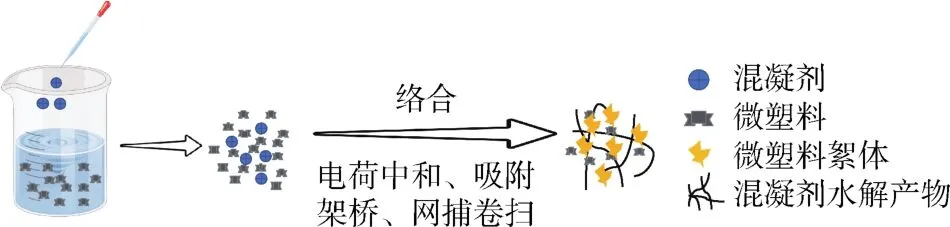
图1 混凝法去除微塑料示意图Fig.1 Schematic diagram of microplastic removal by coagulation
混凝法在去除微塑料过程中会受到混凝剂的类型、混凝条件等因素的影响。铁盐和铝盐是常用的两类混凝剂,研究证明,铝基混凝剂比铁基混凝剂去除PE的效果更佳[74],而且聚丙烯酰胺作为1种助凝剂对去除效率的影响较大。微塑料粒径大小也会影响混凝沉淀效率,对于小尺寸微塑料,颗粒越大(>10 μm),去除效率越好[75]。溶液pH值对混凝剂的水解和混凝效率也有重要影响,碱性条件对聚合氯化铝的水解具有促进作用,因此在碱性条件下微塑料的去除效率高于酸性条件[76]。此外,溶液中阴离子也会影响混凝的效率,Cl-对微塑料的去除效率影响不大,而SO42-和CO32-分别有抑制和促进作用[68]。
2.2 高级氧化
2.2.1 光催化
光催化降解微塑料是1个氧化还原过程,其中光催化剂在光照作用下,内部低能量区中的电子获得能量被激发,跃迁后,催化剂内形成光生电子和光生空穴,光生电子和氧气反应生成超氧化物自由基,光生空穴和水分子反应生成羟基自由基,这些活性氧化物进一步与微塑料反应,导致聚合物链断裂,甚至完全矿化为水和二氧化碳[77],其降解机制如图2所示。光催化作为1种去除污染物的绿色技术,具有成本低、环境友好等优点,但是催化剂再生困难、缺乏选择性和微塑料降解效率较低等缺点会限制其规模化的应用。二氧化钛和氧化锌是常见的2种光催化剂,二氧化钛催化剂对紫外光响应明显,而氧化锌催化剂对可见光更有活性。Nabi等[78]研究了在紫外光照射下,二氧化钛纳米颗粒薄膜对微塑料的有效降解和完全矿化,通过用Triton X-100制成的二氧化钛纳米颗粒薄膜观察到不同尺寸的PE和PS显著的光催化和矿化,空穴、羟基自由基和超氧自由基在其光降解过程中起着重要作用,而空穴是反应中的主导活性物种。由于紫外光响应的光催化剂具有吸收范围较窄和光能利用率低等弊端,因此发明了可见光响应的催化剂。Uheida等[79]通过可见光照射固定在玻璃纤维基材上的氧化锌纳米棒,实现悬浮在水中的PP微塑料球形颗粒的光催化降解,从氧化锌纳米棒光激发产生的羟基自由基引发了聚合物链的降解,生成了PP烷基自由基,烷基自由基与氧气反应形成超氧自由基,然后从另一个聚合物链中抽取1个氢原子形成过氧化氢,过氧化氢通过O—O键的裂解分裂成2个自由氧和羟基自由基,这些活性物质参与了PP微塑料的光降解,2周后平均颗粒体积减小了65 %,而且光降解副产物也是无毒的分子。
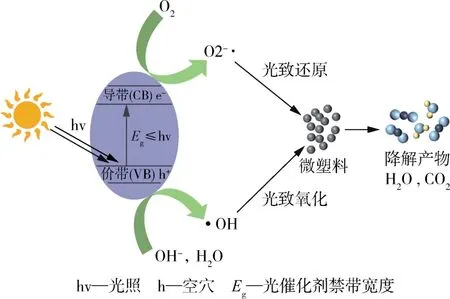
图2 光催化降解微塑料示意图Fig.2 Schematic diagram of photocatalytic degradation of microplastics
光催化降解微塑料的过程会受到微塑料的大小形状、溶液pH、温度等因素的影响。微塑料的尺寸越小,与光催化剂之间的接触面积就越大,因此降解效率会更高,而薄膜状微塑料会导致降解效率降低[80]。酸性条件会刺激H+融入反应体系,促进光催化剂与微塑料之间的相互作用;而碱性溶液中库仑斥力会致使微塑料难以降解[80-81]。低温会导致一些微塑料颗粒的表面破碎,增加其表面积,从而增加与光催化剂之间的相互作用[81]。
2.2.2 过氧化物氧化
过氧化物氧化通常采用催化剂活化过硫酸盐或过氧化氢(芬顿氧化),产生具有强氧化性的硫酸根自由基或羟基自由基等来降解和矿化微塑料(图3)。过氧化物氧化能在较短时间内得到较高的微塑料降解率,降解产物同时可作为藻类生长的碳源[82],但降解微塑料的研究大多处于实验室研究阶段,对污染水体的处理能力有限,在今后的研究中,建议设计1种简单、高效的组合反应器,供实际应用。Kang等[82]研究了磁性螺旋状碳纳米管降解化妆品中微塑料的应用,由于氮掺杂、对锰氧化物的包覆和稳定的螺旋结构,致使磁性螺旋状碳纳米管可以产生更多的活性位点,通过活化过氧一硫酸盐产生硫酸根自由基和羟基自由基降解微塑料,其降解效率高于传统金属催化剂以及其它碳纳米材料。Liu等[83]研究了通过热活化过硫酸盐对40~50 μm PE和PS微塑料的处理,经30 d催化氧化后,几乎所有微塑料的粒径均小于 30 μm,80.1 %的 PS 和 97.4 %的PE均小于20 μm。Hu等[84]开发了1种水热耦合芬顿系统用于降解超高分子量PE微塑料,由于水热水解、富含质子的环境和大量羟基自由基产生的协同作用,微塑料经历了碳链断裂和羰基形成的显著变化,仅仅在12 h内就实现了75.6 %的矿化效率。Miao等[85]提出了1种基于TiO2/石墨(TiO2/C)阴极的类电芬顿技术,用于降解水中典型的PVC微塑料。PVC微塑料直接从TiO2/C阴极获得电子,在加热条件下通过阴极还原引发脱氯反应,同时羟基自由基使PVC主链氧化和断裂形成有机中间体,进一步被降解为低分子量的醇、羧酸和酯,最终部分被矿化为水和二氧化碳,此过程也间接促进了PVC微塑料的进一步脱氯。在100 ℃下进行恒电位电解6 h后,PVC微塑料去除率达到56 %,脱氯效率为75 %。该体系通过三电子转移过程在TiO2/C阴极上发生氧还原反应产生H2O2并原位活化产生羟基自由基,避免了H2O2的使用,降低了操作成本。
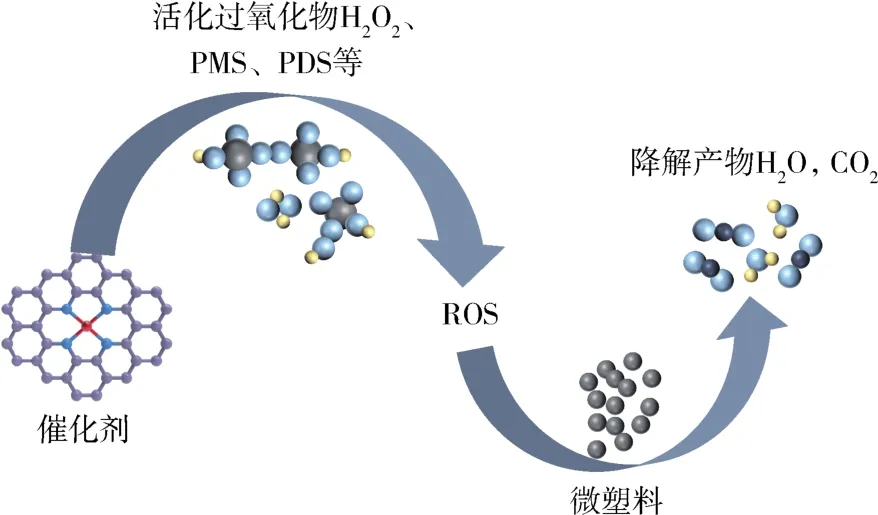
图3 过氧化物氧化降解微塑料示意图Fig.3 Schematic diagram of peroxide oxidative degradation of microplastics
过氧化物氧化降解微塑料的过程受到温度和pH的影响较大。高温条件在微塑料降解过程中至关重要,不仅能使密集的大分子展开,还能加速自由基的产生,从而显著增强分解过程[86]。在降解过程中存在最适的pH范围,偏高和偏低的pH会影响高级氧化反应的能力,如在芬顿反应中,较高的pH会抑制羟基自由基的生成,并且会形成氢氧化铁沉淀,极大地降低了系统的氧化能力[87]。
2.3 膜生物反应器技术
膜生物反应器技术是将膜分离和传统活性污泥法相结合的污水处理方法[88],在微塑料的处理过程中,生物反应器首先将污水中的微塑料进行生物降解,然后通过膜分离混合液,由于膜的过滤作用,微塑料被浓缩在污泥中,其机制如图4所示。膜生物处理系统中膜的孔径一般是0.1 μm,对微塑料的去除效率是目前所有处理技术中最高的,但是运行费用和膜成本太高,使其不适合在我国现行的污水处理厂中推广使用。Talvitie等[89]研究了芬兰图尔库污水处理厂中微塑料的去除,发现膜生物反应器对微塑料的去除效率高达99.9 %。Lares等[90]采用传统活性污泥工艺和中试规模的膜生物反应器去除污水处理厂中的微塑料,发现膜生物反应器对微塑料的去除效率可达99.4 %,比传统活性污泥工艺要高。与混凝和光催化技术相比,膜生物处理的性能不受微塑料的大小和形状的影响,对微塑料的去除非常有效且相对稳定,但是在处理过程中微塑料会造成膜污染,大部分微米级微塑料造成的膜污染可以通过物理清洗的方式减缓,而纳米级的小尺寸微塑料会造成膜的不可逆污染,降低膜的使用寿命[91]。为了保证膜的长期运行,有效控制膜污染显得尤为重要。近年来,许多基于生物技术的膜污染控制策略被开发,相比传统的物理和化学方法,生物方法更有效、更温和、更环保,因此也越来越被广泛采用。研究证明,基于微生物群体感应理论的群体猝灭是1种具有良好前景的膜污染控制技术[92]。此外,通过添加生物絮凝剂也能实现对膜污染的有效控制,与添加化学絮凝剂相比而言,生物絮凝剂对环境更加友好[93]。
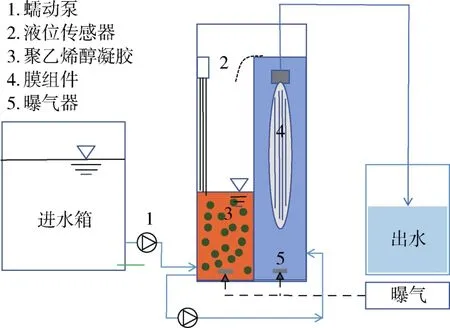
图4 膜生物处理微塑料示意图[91]Fig.4 Schematic diagram of membrane biological treatment of microplastics[91]
3 结语
目前,水环境中微塑料污染问题已引起全球重视,尤其COVID-19的持续蔓延,使一次性口罩等塑料垃圾因乱丢乱弃和管控不当而进入水体环境,从而增加了水中微塑料的数量。在已有的微塑料研究成果的基础上,由于微塑料进入大众视野的时间不长,研究还存在许多空白,对于不同水域微塑料的定量和检测仍没有形成统一的标准,而且对微塑料复合污染物迁移转化过程的研究相对较少。此外,微塑料的去除技术目前存在许多局限性,比如已有的去除技术大部分处于实验室规模研究阶段,主要集中于毫米级或微米级较大粒径微塑料的研究,而且去除技术较为单一,仍存在成本高,难以大规模推广使用以及去除效果不稳定等问题。基于此,本文通过分析微塑料的污染特征,进一步阐述了微塑料的迁移转化过程,并以混凝、高级氧化和膜生物反应器技术为例,对微塑料的去除作用机制进行了综述。结合当前微塑料的研究现状,后续研究可从以下方面进行深入和拓展:(1)构建统一、标准的微塑料检测体系和分析方法,以及进行长期、系统的监测调查,以便获得更具代表性的微塑料分布现状,从而评估地表水中微塑料的环境风险;(2)加强微塑料复合污染物的迁移转化以及风险评估的研究,构建一套微塑料复合污染物的去除及风险评价方法体系,以便更加精确定量地解决微塑料的污染问题;(3)建议将不同的微塑料去除技术组合联用,加强对微塑料去除技术的实际工程应用研究,以提高微塑料去除的效果及稳定性,同时降低成本;且对具有更高丰度和生物毒性的纳米级微塑料,仍需展开深入研究。
