氧气微纳米气泡曝气异位修复渗滤液污染地下水效果研究
2023-02-24刘志彬詹良通范占煌元妙新
白 梅,刘志彬,詹良通,范占煌,元妙新,刘 朱
氧气微纳米气泡曝气异位修复渗滤液污染地下水效果研究
白 梅1,刘志彬1,詹良通2,范占煌3,元妙新3,刘 朱1
(1. 东南大学江苏省城市地下工程与环境安全重点实验室,南京 211189;2. 浙江大学软弱土与环境土工教育部重点实验室,杭州 310050;3. 中节能大地(杭州)环境修复有限公司,杭州 310020)
针对城市固废填埋场场地地下水污染的修复难题,提出氧气微纳米气泡(OMNB)曝气异位修复渗滤液污染地下水的方法.为研究该方法的效果,首先对渗滤液污染地下水开展OMNB曝气与氧气常规(OCB)曝气室内试验,通过对比两种曝气的传质效率、曝气前后水样的微生物活性和污染物浓度的变化研究了OMNB曝气的污染物去除效率,之后对OMNB曝气前后的水样进行紫外-可见光光谱(UV-VIS)、同步荧光光谱(SFS)和三维荧光光谱(3D-EEM)分析研究OMNB曝气前后水样中溶解性有机物(DOM)种类及浓度的变化.试验结果表明:OMNB曝气与OCB曝气的体积传质系数分别为0.265s-1和0.005s-1.在曝气后第30d时,OMNB曝气与OCB曝气处理的水样的脱氢酶活性(DHA)分别提高了151%和84%,OMNB曝气处理水样的五日生化需氧量(BOD5)、化学需氧量(COD)和氨氮的去除率分别约为95%、50%和10%.OMNB曝气后,水样中DOM聚合度增加,芳香性、疏水性降低,水样中类蛋白物质和可溶性微生物产物的浓度显著降低.OMNB曝气在增强水样微生物降解作用的同时可以发挥一定的化学氧化作用.OMNB曝气是一种可行的渗滤液污染地下水抽出处理方法.
城市固废填埋场;地下水污染;微纳米气泡曝气;生物修复;化学氧化
中国目前大约有1600余座城市固体废物卫生填埋场和两万余座简易填埋场,其中普遍存在渗滤液渗漏污染土壤和地下水的风险,城市固体废物卫生填埋场附近的地下水水质综合等级“非常差”[1].且我国70%固废填埋场分布在中东部地区[1-3],这些地区第四系地层以细粒土层为主,土颗粒吸附性强,土层透水/气性较弱,渗滤液渗漏导致的土壤和地下水复合污染的净化修复难度非常大,抽出处理是该类场地中地下水处理最有效且经济的方法之一.
城市固废填埋场渗滤液污染地下水的典型污染物包含有机物、无机盐、重金属和异型生物质化合物四大类,与矿业、石油、化工等工业污水不同,其主要污染物(生化需氧量、化学需氧量和氨氮等)具有可降解、可转化的特征,所以此类地下水常通过曝气刺激好氧细菌生长降解有机污染物的生物修复法进行修复[4-5].在传统曝气中,气泡的粒径为毫米级别(常规气泡),极易从水中溢出,且其较低的传质效率显著降低了曝气中的气体利用率.近年来,微纳米气泡(MNB)曝气受到了大家的广泛关注.MNB曝气中,气泡粒径主要集中在50nm~200μm,气泡在水中停留时长、传质效率和气体的利用率分别是常规气泡的2000倍[6]、50倍和10倍[7].
目前,有关空气或氧气微纳米气泡(OMNB)曝气增强微生物降解作用的研究非常有限.Jenkins等[8]通过室内模型试验研究了OMNB曝气增强假单胞菌活性降解对位二甲苯的效果.Xiao等[9]研究了MNB曝气生物膜系统对葡萄糖与氯化铵合成的污染液的污染物降解情况,发现MNB曝气能够显著增强好氧生物膜的生长,提高膜系统的微生物活性,实现更高的有机污染物去除效率.刘春等[10]对比研究了空气微气泡曝气与空气常规曝气生物膜系统对氯化铵和磷酸二氢钾合成污染液的污染物降解效果,发现微气泡曝气的污染物去除效果显著高于常规曝气的去除效果.但是以上的研究均是针对污染物种类和微生物种群单一的试验室配制污水进行的,实验室模拟污水与填埋场渗滤液污染地下水相比,在污染物种类及微生物丰度等方面差异巨大,因此有必要对抽出的渗滤液污染地下水开展MNB曝气试验,研究MNB曝气异位修复渗滤液污染地下水效果.
本文对不同污染物浓度的渗滤液污染地下水开展OMNB曝气与氧气常规(OCB)曝气室内试验.一方面,通过对比OMNB与OCB曝气后水样中氧气传质、脱氢酶活性(DHA)、五日生化需氧量(BOD5)、化学需氧量(COD)和氨氮的浓度变化研究OMNB曝气降解渗滤液污染地下水的效果;另一方面,通过紫外-可见光光谱(UV-VIS)、同步荧光光谱(SFS)和三维荧光光谱(3D-EEM)分析OMNB曝气前后水样中可溶性有机物(DOM)种类及浓度的变化.
1 试验材料与方法
1.1 试验材料
试验渗滤液取自浙江省温州市的卧旗山填埋场,渗滤液的pH值为9.07,总溶解性固体(TDS)浓度为1.963×10-6mg/L,BOD5值为1775mg/L,COD值为6075mg/L,氨氮浓度为2463mg/L及总氮浓度为4998mg/L.渗滤液收集在棕色的玻璃样品瓶中,并在4℃的冰箱中冷藏保存.试验中使用的水为蒸馏水,COD、氨氮和DHA等测量使用的药品均为分析纯级.
试验中不同污染物浓度的地下水是用蒸馏水稀释渗滤液制得的,渗滤液被稀释10、15、20、25、30和35倍制备的污染地下水水样分别命名为S10、S15、S20、S25、S30和S35.各水样的BOD5、COD和氨氮浓度如表1所示.
表1 水样的BOD5、COD和氨氮浓度
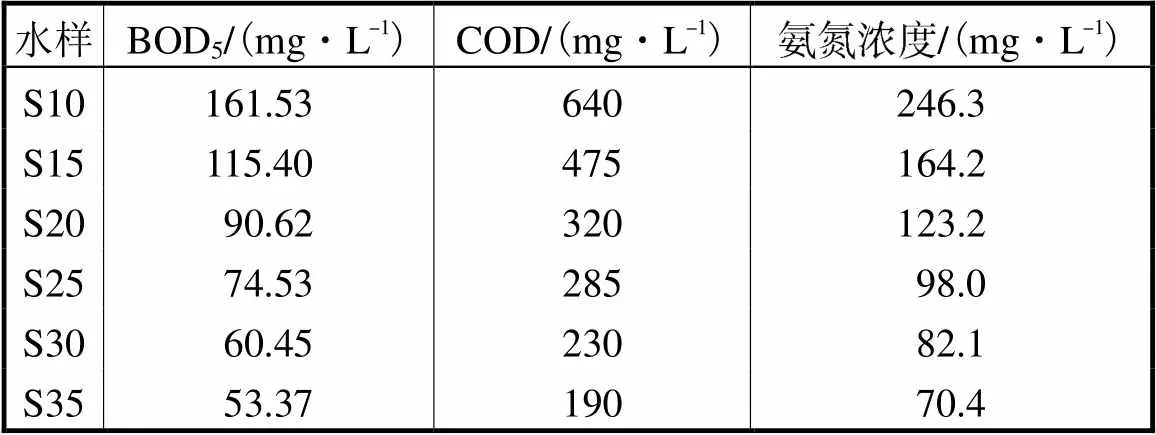
Tab.1 BOD5, COD and ammonia nitrogen concentration of water samples
1.2 试验方法
为对比研究OMNB曝气去除渗滤液污染地下水有机污染物的效果,在对所有水样进行OMNB曝气的同时对水样S10、S25及S35进行OCB曝气.OMNB曝气试验装置如图1所示[11],曝气模型柱是内径260mm、高650mm有机玻璃圆柱桶.在曝气模型柱中装20L水样,设定MNB发生器(XZCP-K-1.1,云南夏之春环保科技有限公司)的进水量为20L/min,出水量为20L/min,进气量为1.8L/min,之后启动MNB发生器进行OMNB曝气.OCB曝气中,在氧气瓶上连接内径3mm的气管,气管的一端放置在装有20L水样的曝气模型柱中,设置氧气瓶的出气量为1.8L/min进行OCB曝气.OMNB曝气与OCB曝气均持续5min,曝气过程中使用溶解氧测量仪(YSI ProSolo)连续测量水样的溶解氧(DO)值.曝气结束后所有水样均被收集在锥形瓶中,并在避光20℃恒温环境中分别放置3、5、10、15、20、30d,之后测定水样的DHA、BOD5、COD和氨氮浓度,并对水样进行UV-VIS、SFS及3D-EEM分析.
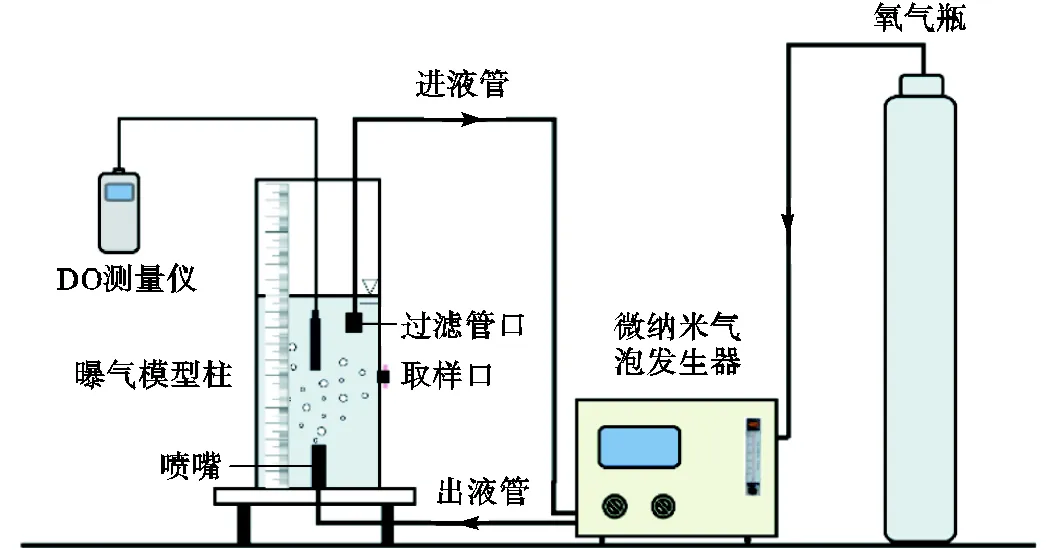
图1 OMNB曝气试验装置
使用DO测量仪(YSI ProSolo)与250mL的棕色BOD瓶,根据《水质五日生化需氧量(BOD5)的测定稀释与接种法》[12]测定BOD5;使用量程范围为20~1500mg/L的试剂(HACH,Loveland,CO,USA)和分光光度计(HACH 3900),根据《水质化学需氧量的测定快速消解分光光度法》[13]测定COD;使用测量范围为0.4~50mg/L的试剂(HACH,Loveland,CO,USA)和分光光度计,根据《水质氨氮的测定纳氏试剂分光光度法》[14]测定氨氮浓度.BOD5、COD和氨氮测试采用3个平行样.DHA可以表征曝气前后好氧微生物的活性.本试验中,使用三苯基四氮唑氯化物(TTC)依据活性污泥脱氢酶测定法测量曝气前后水样的DHA[15].在进行UV-VIS、SFS和3D-EEM分析时,所有水样均使用蒸馏水稀释20倍.UV-VIS通过紫外可见分光光度计(Shimadzu,UV3600)扫描,扫描的波长范围为200~600nm,扫描间隔为1nm. SFS采用荧光分光光度计(Shimadzu,RF-5301PC)扫描,扫描范围240~540nm,波长差40nm.3D-EEM采用荧光光谱仪(Edinburgh Instruments,FS5)扫描,激发波长(EM)范围为230~550nm,步长5nm,发射波长(EX)范围为250~650nm,步长1nm.
2 试验结果与分析
2.1 OMNB曝气的氧气传质特征与微生物活性
图2记录了OMNB曝气与OCB曝气过程中水样DO的变化过程.在OMNB曝气的100s内水样的DO值迅速增长并达到峰值39mg/L,之后保持不变;而在OCB曝气中,水样的DO值一直保持相同的速率增加,在曝气结束时达到7mg/L左右.在相同的氧气输入量下,OMNB曝气使更多的气态氧转化为溶解态,显著提高了氧气利用率.使用动态吸收法计算OMNB曝气与OCB曝气过程中的体积传质系数[11]为
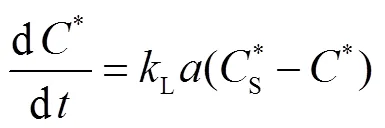
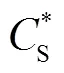
OMNB曝气与OCB曝气前后水样DHA的变化如图3所示,图中0d时水样S25的DHA值即是水样S25曝气前的DHA值.且下文中所有图上所示水样0d时的指标值均是指水样曝气前的值.由图3可知,在OMNB曝气和OCB曝气后第30d时,水样的DHA值从68.2μgTF/pc分别提高到171.3μgTF/pc和125.7μgTF/pc,提高了151%和84%.OMNB曝气后水样的DHA值显著高于OCB曝气的原因是OMNB曝气后水样极高的DO浓度为细胞代谢提供了足够的电子受体[16].OMNB曝气后10d内,水样的DHA值增加缓慢,随着水样中活性微生物不断累积,DHA值在10d后显著提升.即OMNB曝气可以显著提高渗滤液污染地下水的好氧微生物活性.
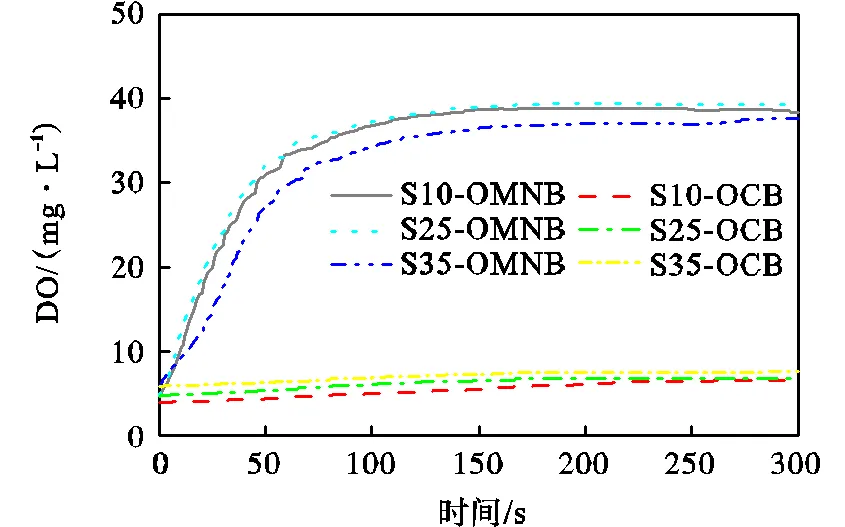
图2 曝气过程中水样DO的变化
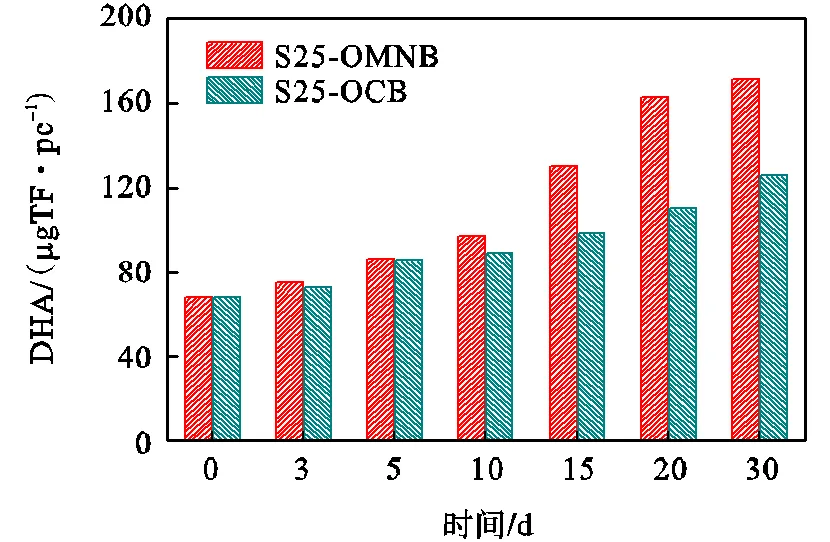
图3 曝气前后水样DHA的变化
2.2 OMNB曝气的污染物去除效果
OMNB曝气和OCB曝气结束后30d内水样BOD5的变化如图4所示.水样S10、S25和S35在OMNB曝气和OCB曝气后,BOD5的值均降低,但是在曝气后第30d时,经OMNB曝气处理水样的BOD5值明显低于OCB曝气处理水样的,说明OMNB曝气的BOD5去除效果优于OCB曝气.如图4所示,在曝气后30d时,经OMNB曝气和OCB曝气的水样BOD5的去除率排序为:S10>S25>S35.由此可知,污水的初始BOD5值越大,OMNB曝气的BOD5去除效果越优于OCB曝气.OMNB曝气后,水样S10、S15和S20的BOD5的值在30d内持续下降,水样S25、S30和S35的BOD5的值约在第5d后保持不变,即BOD5的初始值小于90mg/L的渗滤液污染地下水,OMNB曝气后5d即可达到95%的BOD5去除率;而BOD5的初始值大于100mg/L的渗滤液污染地下水,OMNB曝气后30d才能达到95%的BOD5去除率.表1中各水样的初始BOD5值各不相同,但是在相同的曝气条件(DO值约均为39mg/L)、不同的反应时间下可以达到相同的BOD5去除效果,即OMNB曝气处理渗滤液污染地下水时,BOD5的去除效果与曝气后的反应时间密切相关.
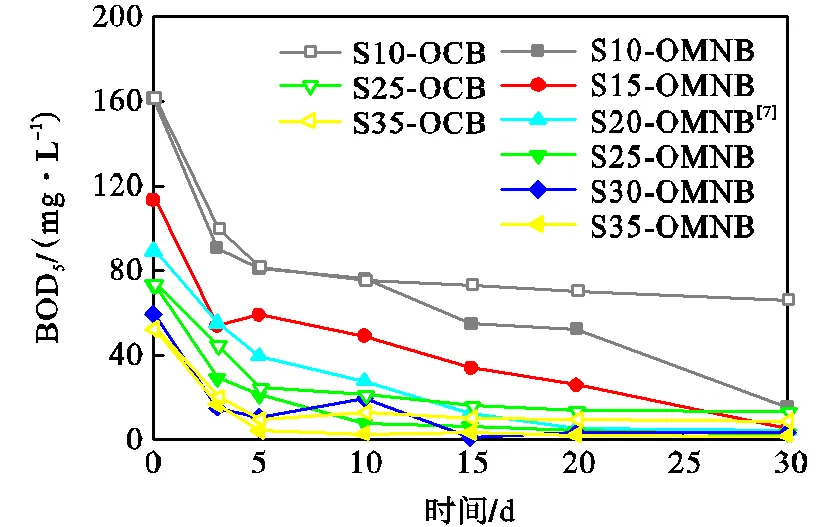
图4 曝气前后水样BOD5的变化
曝气后各水样COD的变化如图5所示.OMNB曝气后水样的COD值明显低于OCB曝气的,且水样初始COD值越高,这种差异越明显.在OMNB曝气后30d时,水样S10、S20和S35的COD去除率分别为60%、50%和40%.即在相同的OMNB曝气条件下,水样的COD初始值越高,在曝气后30d时COD的去除率越大.如图5所示,OMNB曝气后,水样S10、S15和S20的COD值在30d内保持均速下降,而水样S25、S30和S35的COD值则在5d内迅速下降之后几乎保持不变.由此可知,水样的COD初始值越低,COD去除速率越大.
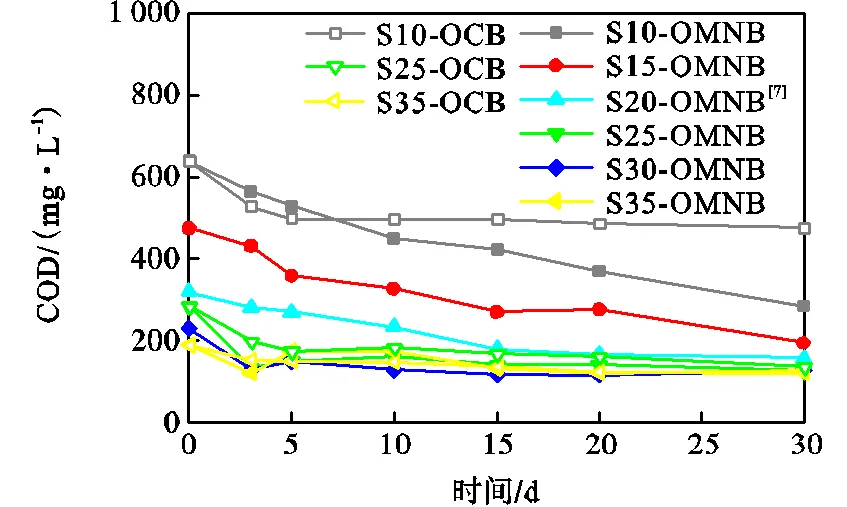
图5 曝气前后水样COD的变化
图6所示为曝气前后各水样氨氮浓度的变化情况.OMNB曝气后水样的氨氮浓度略低于OCB曝气的.OMNB曝气后30d内氨氮浓度先降低后升高.该变化趋势与水样反应过程中C/N的变化有密切关系[17].OMNB曝气后,水样S10、S15和S20的氨氮浓度在5d时达到最低,去除率约18%,在30d时的去除率约10%;水样S25、S30和S35的氨氮浓度在3d达到最低,去除率约25%,30d的去除率约8%.由此可知,通过OMNB曝气去除污水中的氨氮时,曝气结束后5d内的去除效果最为明显.
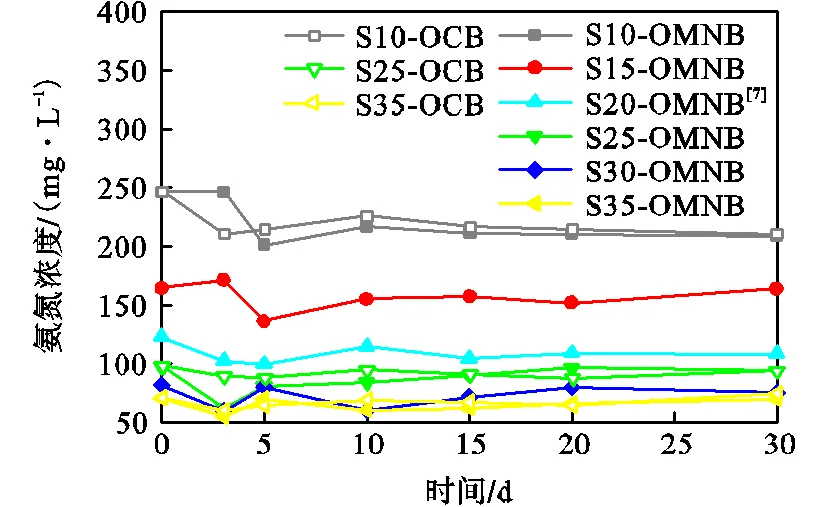
图6 曝气前后水样氨氮浓度的变化
由上述分析可知,与OCB曝气相比,OMNB曝气处理渗滤液污染地下水具有更高的污染物去除率,这是因为OMNB曝气后水样具有更高的好氧微生物活性,污染物通过微生物降解作用被去除.且与OCB曝气相比,OMNB曝气处理高污染物浓度的渗滤液污染地下水具有更高的污染物去除率.在渗滤液污染地下水的抽出处理中使用OMNB曝气去除污染物时,初始污染物浓度较高的水样在曝气后反应时间大于30d,可以达到较好的污染物去除效果,初始污染物浓度较低的污水在5d时可达到稳定的污染物去除效果.
2.3 OMNB曝气后渗滤液污染地下水中溶解性有机物的变化
2.3.1 紫外-可见光光谱
UV-VIS的吸收强度主要与含共轭双键有机物浓度有关,紫外区的吸收强度与水样中有机物的芳香性和复杂化程度有关[17].OMNB曝气前及曝气后30d时水样S10、S20和S35的UV-VIS谱图如图7所示,由于本研究使用渗滤液污染地下水所含有机物种类繁多,所以UV-VIS谱图中没有明显的吸收峰.但是所有水样均在紫外光区(≤400nm)出现了较大的吸光度值,说明水样中有机物具有较大的共振能量,芳香性也较高.OMNB曝气后30d,所有水样在紫外区的吸光度值均下降,说明曝气降低了水样中有机物的分子复杂程度.
在UV-VIS谱图上,特定波长下的吸光度值及其比值通常可以反映DOM的腐殖化程度、团聚及相对分子质量的大小等信息.其中,水样在波长250nm处的吸光度(250)与波长365nm处的吸光度(365)比值(250/365)可以表征DOM的相对分子质量;水样在波长300nm处的吸光度(300)与波长400nm处的吸光度(400)比值(300/400)可以表征DOM的腐殖化、芳香性和相对分子质量[18-19];水样在波长254nm处的吸光度(254)和波长280nm处的吸光度(280)分别可以表征DOM的芳香性和相对疏水性;水样的吸光度曲线在波长239~400nm之间的积分面积()可以表征苯类化合物的变化[20-22].图8所示为水样S10、S20和S35在OMNB曝气前后的250/365、300/400、254、280和值的变化情况.
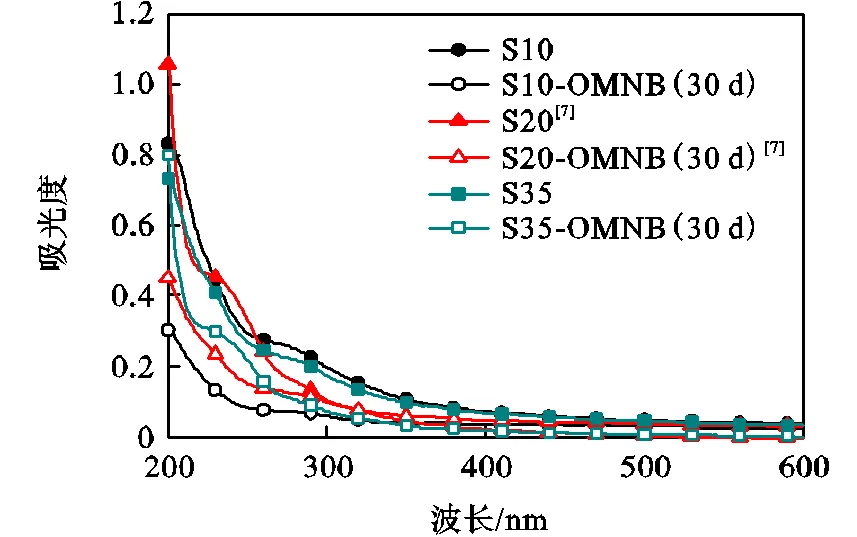
图7 水样的UV-VIS谱图
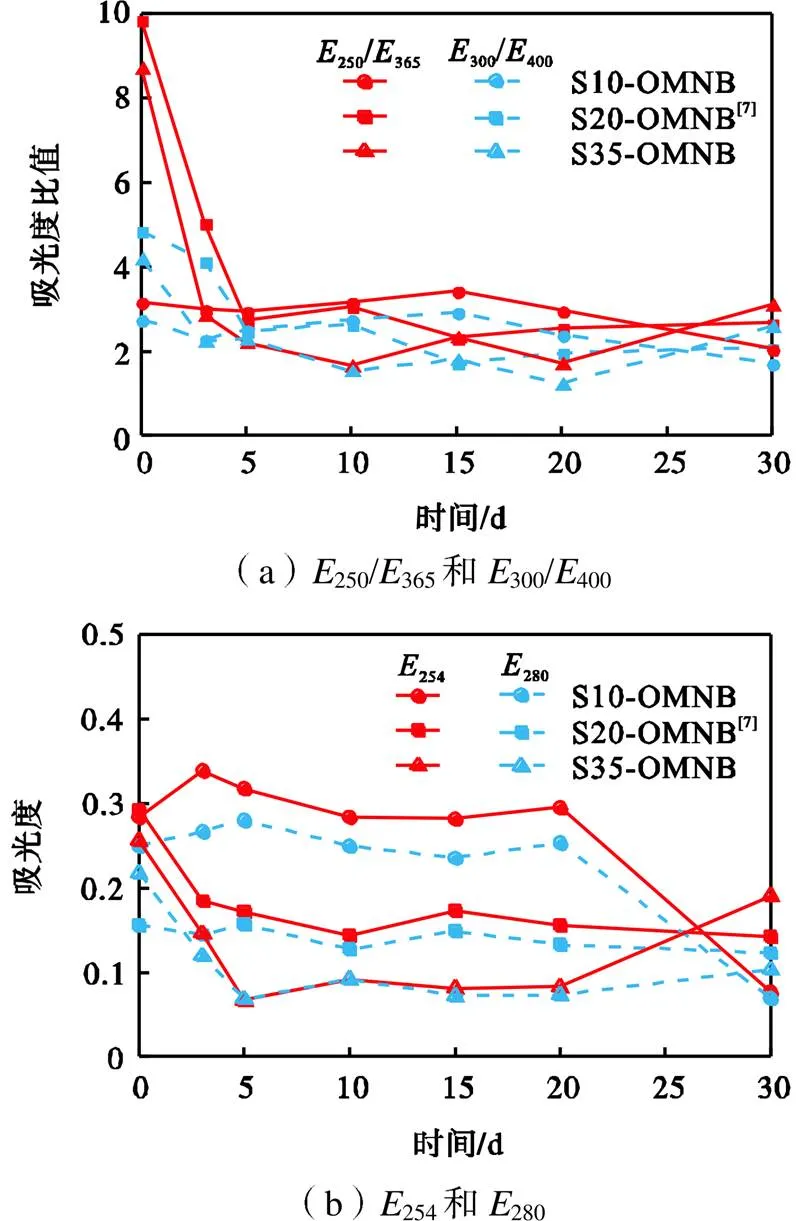
如图8(a)所示,OMNB曝气后,水样S10、S20和S35的250/365及300/400的值均在减少,即曝气后水样中DOM的相对分子质量变大,聚合度增加,说明OMNB曝气增强的微生物降解作用去除了相对分子质量小且结构简单的有机物污染物.水样S20和S35的250/365和300/400值在曝气结束后的5d内变化明显,随后几乎保持不变,该趋势与第2.2节中讨论的BOD5和COD的变化趋势一致.由图8(b)中各水样的254与280值在曝气后降低的现象可知水样中DOM的芳香性和疏水性降低,这说明OMNB曝气可以去除一定的芳香类物质.图8(c)中3个水样的积分面积值均在降低,即苯环化合物被去除.因为芳香族化合物及苯环化合物是难生物降解的,所以曝气后水样中DOM芳香性及苯环化合物的减小可以说明OMNB曝气在发挥增强生物作用的同时可以发挥一定的化学氧化作用.
2.3.2 同步荧光光谱
图9为水样S10、S20和S35曝气前后30d的SFS谱图,如图所示,水样中污染物浓度越小吸光度越小.SFS谱图根据波长可分为3个不同的区域,吸光度在不同波长区域的积分面积表示不同物质的含量[23]:在波长250~300nm之间的积分面积用于表征类蛋白物质的含量,在波长300~380nm之间的积分面积用于表征富里酸类物质的含量,在波长380~550nm之间的积分面积表征腐殖酸类物质的含量.如图9所示OMNB曝气后富里酸类物质及腐殖酸类物质的含量略有减少,因为富里酸类物质与腐殖酸类物质只能在一定程度上通过微生物作用降解.由此可知OMNB曝气增强了地下水的生物降解作用.
2.3.3 三维荧光光谱
3D-EEM谱图可分为5个代表不同的DOM类型的EX/EM区域[24]:Ⅰ区(EX<250nm且EM<330nm)和Ⅱ区(EX<250nm且330<EM<380nm)表征类蛋白物质,易于被微生物利用和降解;Ⅲ区(EX<250nm且EM>380nm)表征富里酸类物质;Ⅳ区(EX>250nm且EM<380nm)表征可溶性微生物产物,易生物降解;Ⅴ区(EX>250nm且EM>380nm)表征难生物降解的类腐殖酸有机物.如图10所示,水样S20的3D-EEM谱图在上述5个区域均有荧光强度,说明水样的DOM包括类蛋白物质、富里酸类物质、可溶性微生物产物及类腐殖酸有机物. 在OMNB曝气后,各区域的荧光强度随着反应时间的延长而变弱,说明各类DOM浓度均减少.根据3D-EEM的定量分析方法计算出OMNB曝气前后地下水水样中各类DOM浓度[24],计算结果如表2所示.
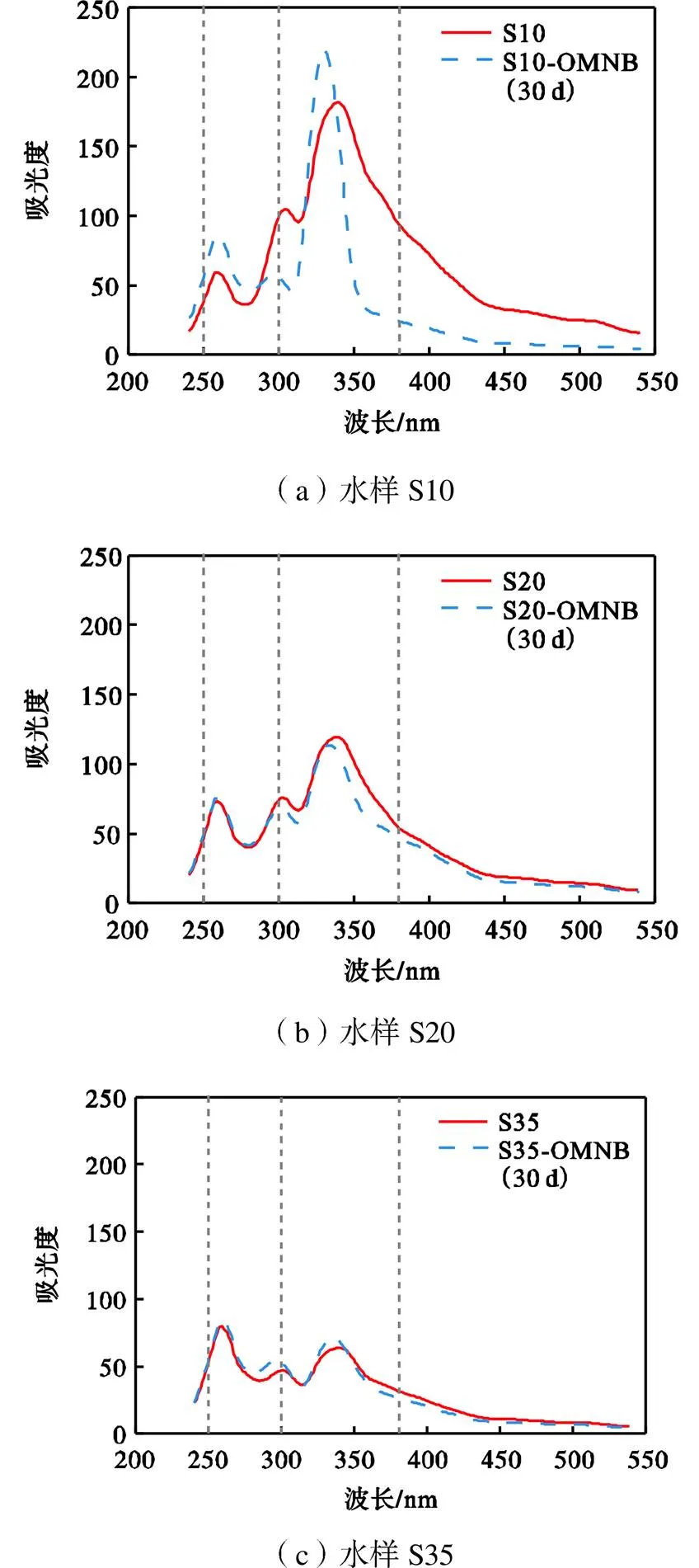
图9 水样的SFS谱图
表2中水样总的荧光强度在激发和发射波长范围内的归一化积分体积随着OMNB曝气后反应时间的增加先增加后减少.DOM浓度的增大可能是在曝气增强的生物及化学氧化作用下,一部分难溶的有机物溶解到了水中;之后水样中DOM浓度的减少是因为DOM被微生物利用并降解.单独分析曝气前后各区域积分体积的变化可知,Ⅰ区、Ⅱ区和Ⅲ区积分体积减小最多代表类蛋白物质及可溶性微生物产物浓度减小得最多,这些可被微生物利用和降解物质浓度的减小说明OMNB曝气显著增强了水样的微生物降解作用.此外,Ⅳ区和Ⅴ区积分体积减小较少代表富里酸类物质和类腐殖酸类物质浓度变化较小,一方面是因为富里酸类物质和类腐殖酸类物质只能在一定程度上通过微生物作用降解,另一方面是水样反应过程中有富里酸类及腐殖酸类物质产生[25-26].
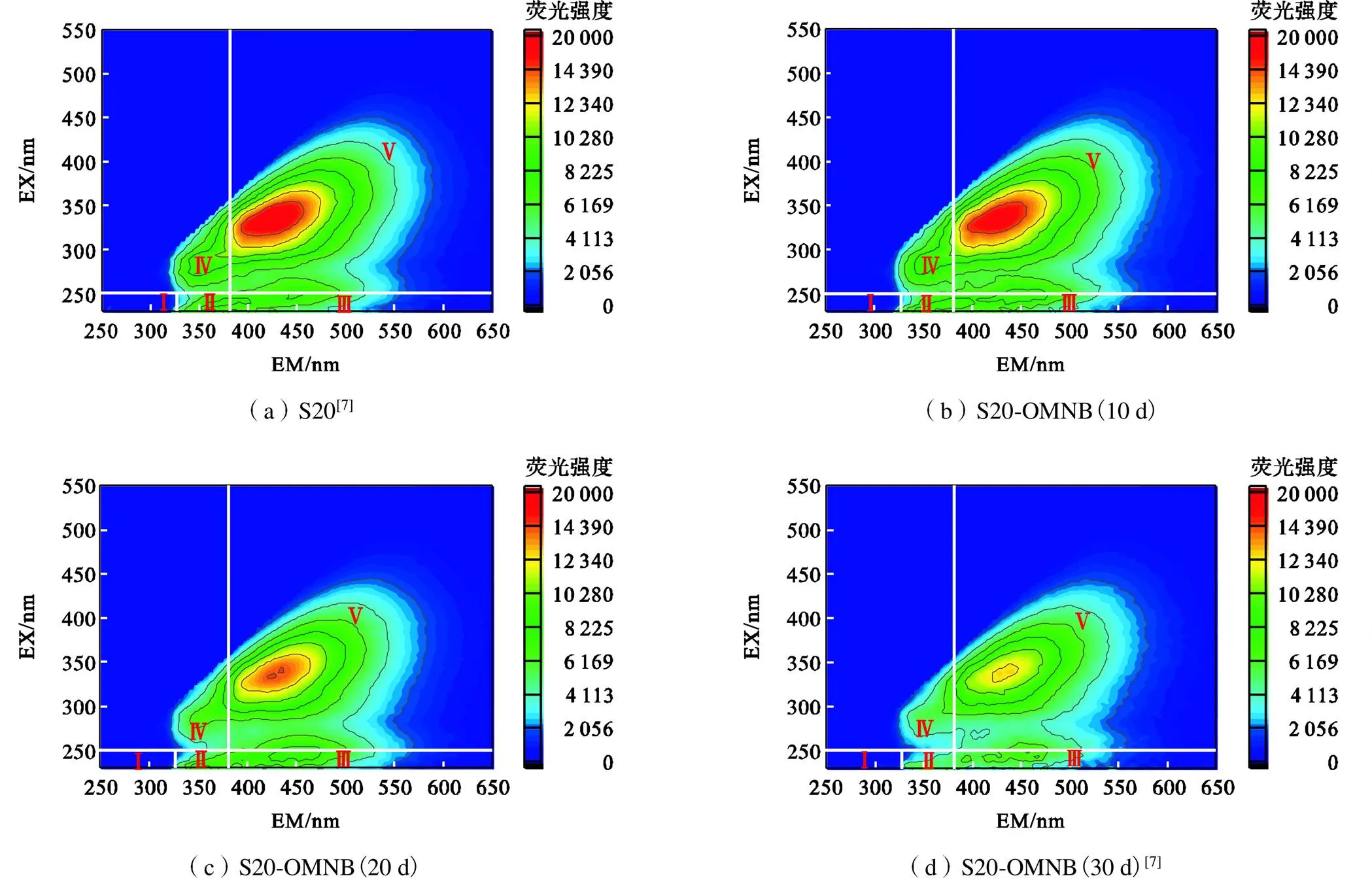
图10 水样S20的3D-EEM谱图
表2 水样S20的3D-EEM各区域的归一化积分体积
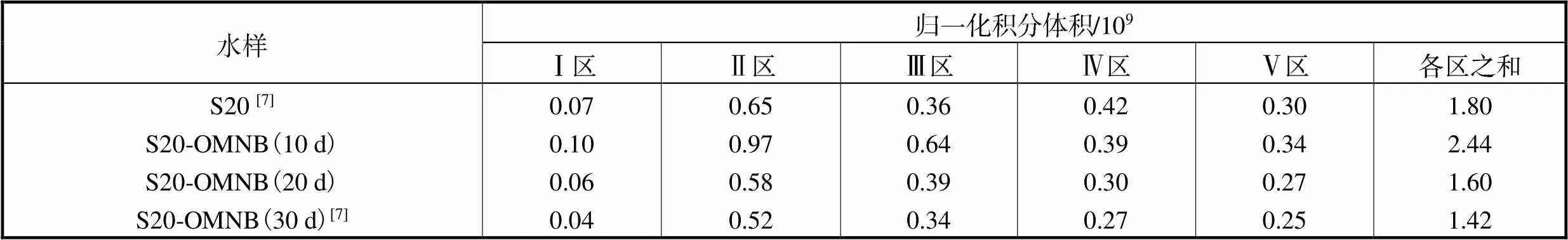
Tab.2 Normalized region-specific 3D-EEM volume of groundwater sample S20
3 结 论
本文对不同污染物浓度的渗滤液污染地下水进行了OMNB曝气与OCB曝气试验,通过对比两种曝气后水样DO、DHA及COD、BOD5和氨氮浓度变化研究了OMNB曝气在渗滤液污染地下水抽出处理中的污染物去除效果;通过水样的UV-VIS、SFS及3D-EEM谱图研究了OMNB曝气前后渗滤液污染地下水水样的DOM种类及浓度变化,得出如下结论:
(1) OMNB曝气后,水样的DO峰值达到38mg/L,曝气后第30d时,水样的DHA值提高了151%,水样的BOD5、COD和氨氮去除率分别约95%、50%和10%.在渗滤液污染地下水的抽出处理中使用OMNB曝气去除有机污染物是一种可行的方法.
(2) OMNB曝气处理渗滤液污染地下水时,有机物浓度较高的地下水在曝气结束后30d可以达到稳定的污染物去除效果,曝气后5d污染物浓度较低的地下水即可达到稳定的污染物去除效果.
(3) OMNB曝气后,渗滤液污染地下水中的DOM聚合度增加,芳香性、疏水性降低,水样中类蛋白物质和可溶性微生物产物的含量显著降低,富里酸类物质及类腐殖酸物质含量略有下降,OMNB曝气在增强水样微生物降解作用的同时发挥了一定的化学氧化作用.
[1] Han Zhiyong,Ma Haining,Shi Guozhong,et al. A review of groundwater contamination near municipal solid waste landfill sites in China[J]. Science of the Total Environment,2016,569:1255-1264.
[2] 陈记文,薛 强,刘 磊,等. 非平衡吸附模型在研究渗滤液对土壤污染影响中的应用[J]. 岩土力学,2006,27(12):2186-2190.
Chen Jiwen,Xue Qiang,Liu Lei,et al. Application of non-equilibrium adsorption model to study of influence of waste landfill leachate on soil pollution[J]. Rock and Soil Mechanics,2006,27(12):2186-2190(in Chinese).
[3] 何小松,余 红,席北斗,等. 填埋垃圾浸提液与地下水污染物组成差异及成因[J]. 环境科学,2014,35(4):1399-1406.
He Xiaosong,Yu Hong,Xi Beidou,et al. Difference of contaminate composition between landfill leachates and groundwater and its reasons[J]. Environmental Science,2014,35(4):1399-1406(in Chinese).
[4] 郑艳梅,李鑫钢,韩玉峰,等. 生物曝气去除MTBE的实验[J]. 天津大学学报,2007,40(12):1495-1499.
Zheng Yanmei,Li Xingang,Han Yufeng,et al. Experiments on MTBE removal using biosparging[J]. Journal of Tianjin University,2007,40(12):1495-1499(in Chinese).
[5] 魏燕杰,季 民,李国一,等. 好氧颗粒污泥SBR处理垃圾渗滤液的污泥理化特性分析[J]. 天津大学学报,2012,45(6):522-528.
Wei Yanjie,Ji Min,Li Guoyi,et al. Physicochemical characteristics of aerobic granular sludge in granular sequencing batch reactor treating landfill leachate[J]. Journal of Tianjin University,2012,45(6):522-528 (in Chinese).
[6] 车 林,金文标,陈洪一,等. 反硝化微生物菌剂提升A2/O工艺TN去除效果[J]. 化工学报,2021,72(增1):467-474.
Che Lin,Jin Wenbiao,Chen Hongyi,et al. Denitrifying microbial agents improving TN removal of A2/O process[J]. CIESC Journal,2021,72(Suppl 1):467-474(in Chinese).
[7] Bai Mei,Liu Zhibin,Zhan Liangtong,et al. A comparative study of removal efficiency of organic contaminant in landfill leachate-contaminated groundwater under micro-nano-bubble and common bubble aeration[J]. Environmental Science and Pollution Research,2022,DOI:10.1007/s11356-022-21805-7.
[8] Jenkins K B,Michelsen D L,Novak J T. Application of oxygen microbubbles for in situ biodegradation of p-xylene-contaminated groundwater in a soil column[J]. Biotechnology Progress,1993,9(4):394-400.
[9] Xiao Wanting,Xu Guoren. Mass transfer of nanobubble aeration and its effect on biofilm growth:Microbial activity and structural properties[J]. Science of the Total Environment,2020,703:134976.
[10] 刘 春,肖太民,张 晶,等. 微气泡曝气对生物膜反应器启动运行性能影响[J]. 中国环境科学,2014,34(12):3093-3098.
Liu Chun,Xiao Taimin,Zhang Jing,et al. Influence of microbubble aeration on start-up and performance of a biofilm reactor[J]. China Environmental Science,2014,34(12):3093-3098(in Chinese).
[11] Bai Mei,Liu Zhibin,Zhang Jinpeng,et al. Prediction and experimental study of mass transfer properties of micronanobubbles[J]. Industrial & Engineering Chemistry Research,2021,60(22):8291-8300.
[12] 中华人民共和国环境保护部. HJ505—2009水质五日生化需氧量(BOD5)的测定稀释与接种法[S]北京:中国环境科学出版社,2009.
Ministry of Environmental Protection of the People’s Republic of China. HJ505—2009 Water Quality—Determination of Biochemical Oxygen Demand after 5 Days(BOD5) for Dilution and Seeding Method[S]. Beijing:China Environmental Science Press,2009(in Chinese).
[13] 中华人民共和国环境保护总局. HJ/T399—2007水质化学需氧量的测定快速消解分光光度法[S]北京:中国环境科学出版社,2008.
Ministry of Environmental Protection of the People’s Republic of China. HJ/T399—2007 Water Quality—Determination of the Chemical Oxygen Demand—Fast Digestion-Spectrophotometric Method[S]. Beijing:China Environmental Science Press,2008(in Chinese).
[14] 中华人民共和国环境保护部. HJ535—2009水质氨氮的测定纳氏试剂分光光度法[S]北京:中国环境科学出版社,2010.
Ministry of Environmental Protection of the People’s Republic of China. HJ535—2009 Water Quality—Determination of Ammonia Nitrogen—Nessler’s Reagent Spectrophotometry[S]. Beijing:China Environmental Science Press,2010(in Chinese).
[15] Wang Sen,Li Zhiwei,Gao Mengchun,et al. Long-term effects of nickel oxide nanoparticles on perform-ance,microbial enzymatic activity,and microbial community of a sequencing batch reactor[J]. Chemosphere,2017,169:387-395.
[16] 梁 贤,任勇翔,杨 垒,等. 异养硝化-好氧反硝化菌YL的脱氮特性[J]. 环境科学,2015,36(5):1749-1756.
Liang Xian,Ren Yongxiang,Yang Lei,et al. Characteristics of nitrogen removal by a heterotrophic nitrification-aerobic denitrification bacterium YL[J]. Environmental Science,2015,36(5):1749-1756(in Chinese).
[17] Tizazoui C,Bouselmi L,Mansouri L,et al. Landfill leachate treatment with ozone and ozone/hydrogen peroxide systems[J]. Journal of Hazardous Materials,2007,140(1/2):316-324.
[18] Peuravuori J,Pihlaja K. Molecular size distribution and spectroscopic properties of aquatic humic substances[J]. Analytica Chimica Acta,1997,337(2):133-149.
[19] Aatinger R,Buckau G,Geyer S,et al. Characterization of groundwater humic substances:Influence of sedimentary organic carbon[J]. Applied Geochemistry,2000,15(1):97-116.
[20] Korshin G V,Li C W,Benjamin M M. Monitoring the properties of natural organic matter through UV spectroscopy:A consistent theory[J]. Water Research,1997,31(7):1787-1795.
[21] Kavurmaci S S,Bekbolet M. Specific UV-VIS absorbance changes of humic acid in the presence of clay particles during photocatalytic oxidation[J]. Desalination and Water Treatment,2014,52(10/11/12):1903-1910.
[22] Guo Xujing,Xi Beidou,Yu Huibin,et al. The structure and origin of dissolved organic matter studied by UV-vis spectroscopy and fluorescence spectroscopy in lake in arid and semi-arid region[J]. Water Science and Technology,2011,63(5):1010-1017.
[23] Chen Wei,Hanibul N,Liu Xiaoyong,et al. FTIR and synchronous fluorescence heterospectral two-dimensional correlation analyses on the binding characteristics of copper onto dissolved organic matter[J]. Environmental Science & Technology,2015,49(4):2052-2058.
[24] Chen Wen,Westerhoff P,Leenheer J A,et al. Fluorescence excitation emission matrix regional integration to quantify spectra for dissolved organic matter[J]. Environmental Science & Technology,2003,37(24):5701-5710.
[25] He Ruo,Tian Baohu,Zhang Qiqi,et al. Effect of Fenton oxidation on biodegradability,biotoxicity and dissolved organic matter distribution of concentrated landfill leachate derived from a membrane process[J]. Waste Management,2015,38:232-239.
[26] Zhuang Haifeng,Hong Xiaoting,Han Hongjun,et al. Effect of pure oxygen fine bubbles on the organic matter removal and bacterial community evolution treating coal gasification wastewater by membrane bioreactor[J]. Bioresource Technology,2016,221:262-269.
Ex-Situ Remediation of Landfill Leachate Contaminated Groundwater by Oxygen Micro-Nano-Bubble Aeration
Bai Mei1,Liu Zhibin1,Zhan Liangtong2,Fan Zhanhuang3,Yuan Miaoxin3,Liu Zhu1
(1. Jiangsu Key Laboratory of Urban Underground Engineering and Environmental Safety,Southeast University,Nanjing 211189,China;2. Key Laboratory of Soft Soils and Geoenvironmental Engineering of Ministry of Education,Zhejiang University,Hangzhou 310050,China;3. CECEP Dadi(Hangzhou)Environmental Remediation Co.,Ltd.,Hangzhou 310020,China)
The remediation of landfill leachate contaminated groundwater is a challenge. Herein,oxygen micro-nano-bubble(OMNB)aeration was used for ex-situ landfill leachate contaminated groundwater remediation,and the contaminant removal efficiency was studied. First,landfill leachate contaminated groundwater samples were treated by OMNB aeration and oxygen common bubble(OCB)aeration,respectively.Then,the mass transfer efficiencies of OMNB and OCB aeration,the concentrations of contaminants and microorganisms activity of the water samples before and after OMNB or OCB aeration were tested to estimate the contaminant removal efficiencies of OMNB aeration. At last,the kinds and concentrations variations of dissolved organic matter (DOM) in groundwater before and after OMNB aeration were characterized by ultraviolet-visible absorption spectrum (UV-VIS),synchronous fluorescence spectroscopy (SFS) and three-dimensional fluorescence excitation-emission matrix (3D-EEM).The test results indicated that the volumetric mass transfer coefficients of OMNB and OCB aeration were 0.265s-1and 0.005s-1,respectively. On the 30th day after aeration,the dehydrogenase activity(DHA) of the water sample treated with OMNB and OCB aeration improved by 151% and 84%,respectively. Furthermore,on the 30th day after OMNB aeration,5-day biochemical oxygen demand,chemical oxygen demand,and ammonia nitrogen removal efficiency were about 95%,50%,and 10%,respectively. OMNB aeration reduced the aromaticity and hydrophobicity,but increased the condensation degree of DOM in a water sample. Additionally,after OMNB aeration,the protein-like and soluble microbial byproduct-like substances in groundwater decreased significantly. OMNB aeration imparts a chemical oxidation effect while enhancing the biodegradation of groundwater. Therefore,OMNB aeration is an effective method for the ex-situ remediation of landfill leachate contaminated groundwater.
municipal solid waste landfill;groundwater pollution;micro-nano-bubble aeration;bioremediation;chemical oxidation
X523
A
0493-2137(2023)01-0018-09
10.11784/tdxbz202111014
2021-11-07;
2022-02-16.
白 梅(1992— ),女,博士研究生,230198270@seu.edu.cn.
刘志彬,seulzb@seu.edu.cn.
国家重点研发计划资助项目(2018YFC1802300);国家自然科学基金资助项目(41877240);东南大学优秀博士学位论文培育基金资助项目(YBPY2154).
Supported by the National Key Research and Development Program of China(No. 2018YFC1802300),the National Natural Science Foundation of China(No. 41877240),the Scientific Research Foundation of Graduate School of Southeast University(No. YBPY2154).
(责任编辑:田 军)
