金黄色葡萄球菌血流感染住院患儿临床特征及危险因素
2023-02-21王红梅邓继岿
施 君,王红梅,邓继岿,
(1.遵义医科大学珠海校区,广东 珠海 519090;2.深圳市儿童医院感染科,广东 深圳 518038)
金黄色葡萄球菌(Staphylococcusaureus,SA)是一种定植于人类皮肤和鼻腔的革兰阳性球菌,可引起多种形式感染[1],如皮肤软组织感染、骨关节感染、泌尿道感染、感染性心内膜炎等,也可导致败血症、脓毒性综合征、脓毒症休克等全身感染[2-3]。金黄色葡萄球菌的血流感染会导致心肌收缩力减弱、心输出量减少和血管通透性增加,使得有效血容量减少和组织灌注不足,机体出现血压降低、微循环障碍和严重感染性休克;内皮细胞损伤,血流速度减慢,血液高凝,微血栓形成增多后导致缺血性器官功能障碍性缺血,血栓形成还可形成栓塞,甚至使化脓性病变扩散形成持续脓肿以及脓毒性休克、器官功能障碍,增加患者的病死率和预后不良的风险[4-5]。有资料显示SA血流感染住院患者病死率可高达20%~30%[6]。
本研究收集SA血流感染住院患儿的临床资料及菌株的抗菌药物药敏试验结果,根据其药敏试验结果及来源分为耐甲氧西林金黄色葡萄球菌(MRSA)组与甲氧西林敏感金黄色葡萄球菌(MSSA)组、医院感染(HA)组与社区感染(CA)组,通过分析其临床特点、耐药情况、预后、转归及其危险因素,为儿童SA血流感染的诊断及临床抗菌药物的合理使用提供参考。
1 对象与方法
1.1 研究对象 收集深圳市儿童医院2014年1月—2019年12月实验室数据库中血培养检出SA的病例,根据患者住院号,通过病历系统搜索患者的临床资料。纳入标准:患者有相应感染的症状或体征且至少一次血培养分离出SA。排除标准:(1)既往有SA血流感染病史;(2)门诊患者;(3)血培养检出SA但无临床表现者;(4)临床资料不完整者。根据感染来源及耐药性分为CA-MRSA组、CA-MSSA组、HA-MRSA组及HA-MSSA组。本研究通过深圳市儿童医院伦理委员会批准(批件2021086号)。
1.2 资料收集 收集患儿的基本信息、临床诊断及治疗等信息,包括患儿的性别、年龄、感染类型、临床症状、药物使用情况、辅助检查及预后情况等,预后情况分为治愈、好转、未愈及死亡。
1.3 相关定义 MRSA标准: 药敏试验结果显示头孢西丁筛选试验阳性或苯唑西林最小抑菌浓度(MIC)≥4 mg/L。HA血流感染诊断标准[7]:患者入院时不存在感染且不处于感染潜伏期,在入院48 h后血培养阳性;或者血培养在入院48 h内为阳性,但患者是从其他医院转入或长期留置导尿管、造瘘管等医疗设备。
1.4 细菌培养与药敏试验 采用BACTECFX自动化血培养系统进行检测。按《全国临床检验操作规程》(第三版)进行操作,剔除污染菌及同一患儿检出的重复菌株。采用法国生物梅里埃公司VITEK 2 Compact全自动细菌鉴定药敏分析仪完成细菌鉴定及药敏试验,参照2018年美国临床和实验室标准化协会(CLSI)抗菌药物敏感性试验标准判读结果。质控菌株为金黄色葡萄球菌ATCC 25923和ATCC 29213,源于美国标准菌种保藏中心。
1.5 统计学方法 应用SPSS 20.0统计软件对数据进行统计学分析,数据进行正态性检验,计数资料采用百分率(%)表示,采用卡方检验进行比较,将有统计学意义的单因素进行多因素logistic回归分析,计算比值比(OR)及95%可信区间(CI)。P≤0.05为差异具有统计学意义。
2 结果
2.1 基本情况 2014年1月—2019年12月深圳市儿童医院共有SA血流感染143例,其中男性92例,女性51例,男女比例为1.8∶1;MARS组50例(34.97%),MSSA组93例(65.03%);HA组73例(51.0%),CA组70例(49.0%)。
2.2 MRSA组与MSSA组比较
2.2.1 临床特征 春夏季和秋冬季的患儿感染人数分别为71例(49.7%)、72例(50.3%),其中MRSA血流感染多见于春夏季(26例,52.0%)。143例患者分布于全院15个科室,其中MRSA感染病例主要来源于重症监护病房[(ICU)11例,22.0%]、骨科(10例,20.0%)、新生儿科(8例,16.0%)。50例MRSA感染病例以病灶性血流感染多见(34例,68.0%),包括皮肤/骨关节软组织感染(16例,32.0%)、肺炎(14例,28.0%)等;93例MSSA感染病例以病灶性血流感染多见(56例,60.2%),包括皮肤/骨关节软组织感染(35例,37.6%)、肺炎(13例,14.0%)等。其中CA-MRSA导致皮肤软组织感染13例(26.0%),肺炎10例(20.0%);HA-MRSA感染导致皮肤软组织感染6例(12.0%),肺炎5例(10.0%)。MRSA组和MSSA组患者的性别、年龄、季节分布、科室分布、临床感染类型、基础疾病及预后情况比较,差异均无统计学意义(均P>0.05)。见表1。

表1 MRSA组与MSSA组血流感染患儿临床特征[例(%)]
2.2.2 MRSA血流感染的危险因素分析 单因素分析结果表明,机械通气、住院时间>7 d、抗菌药物使用时间>7 d、抗菌药物联合使用患者MRSA血流感染率较高,差异均有统计学意义(均P<0.05),见表2。以是否感染MRSA作为因变量,以单因素分析有统计学意义的变量作为自变量,采用多因素logistic回归分析方法分析,结果表明,机械通气[OR=17.320,95%CI(1.576~190.399)]、抗菌药物联合使用[OR=0.580,95%CI(0.359~0.938)]是MRSA血流感染的独立危险因素(均P<0.05)。见表3。
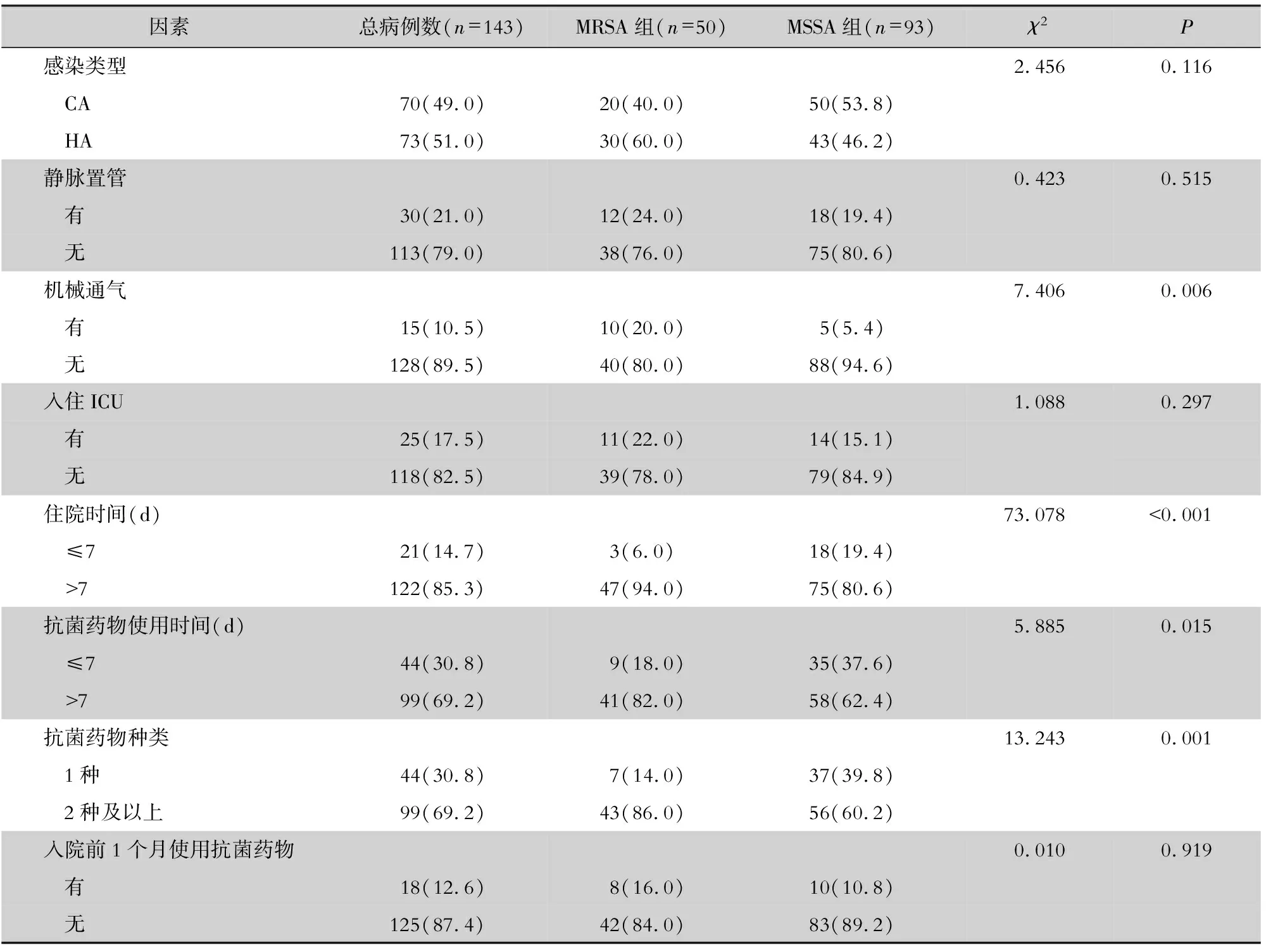
表2 MRSA组血流感染的单因素分析[例(%)]

表3 MRSA血流感染的logistic回归分析
2.3 CA组与HA组比较
2.3.1 临床特征 CA血流感染患儿中合并皮肤/骨关节软组织感染31例(44.3%),高于HA组[20例(27.4%)],两组比较差异有统计学意义(P<0.001)。HA血流感染组基础疾病患有实体瘤、先天性心脏病的比率分别为15.1%、13.7%,均高于CA血流感染组的1.4%(均P<0.05)。HA血流感染组死亡/未愈6例(8.2%),CA血流感染组死亡/未愈4例(5.7%),两组比较差异无统计学意义(P>0.05)。见表4。

表4 HA组与CA组血流感染患儿临床特征[例(%)]
2.3.2 HA血流感染的危险因素分析 单因素分析结果表明,静脉置管、机械通气、入院前1个月使用抗菌药物患者HA血流感染率较高,差异有统计学意义(均P<0.05),见表5。进一步logistic回归分析显示,机械通气[OR=31.466,95%CI(1.434~690.538)]、入院前使用抗菌药物[OR=24.524,95%CI(1.699~353.915)]、住院时间>7 d[OR=1.090,95%CI(1.010~1.176)]、抗菌药物使用时间>7 d[OR=0.910,95%CI(0.842~0.984)]是HA血流感染的独立危险因素(均P<0.05)。见表6。

表5 HA血流感染的单因素分析[例(%)]
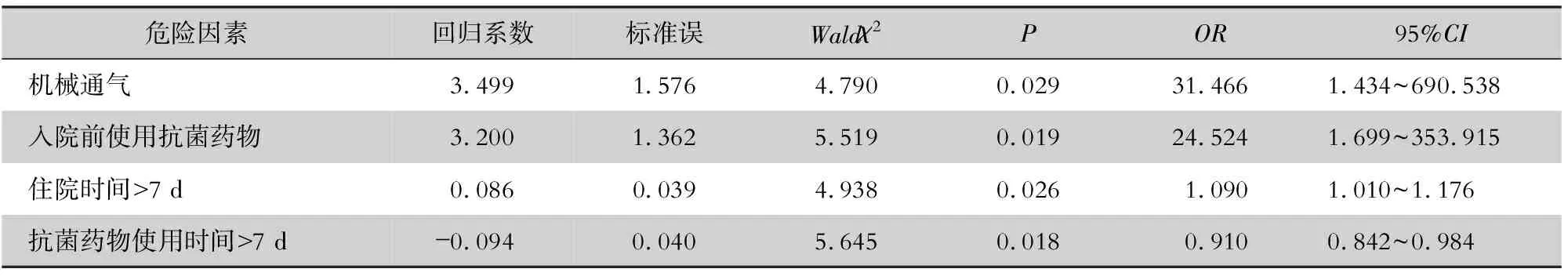
表6 HA血流感染的logistic回归分析

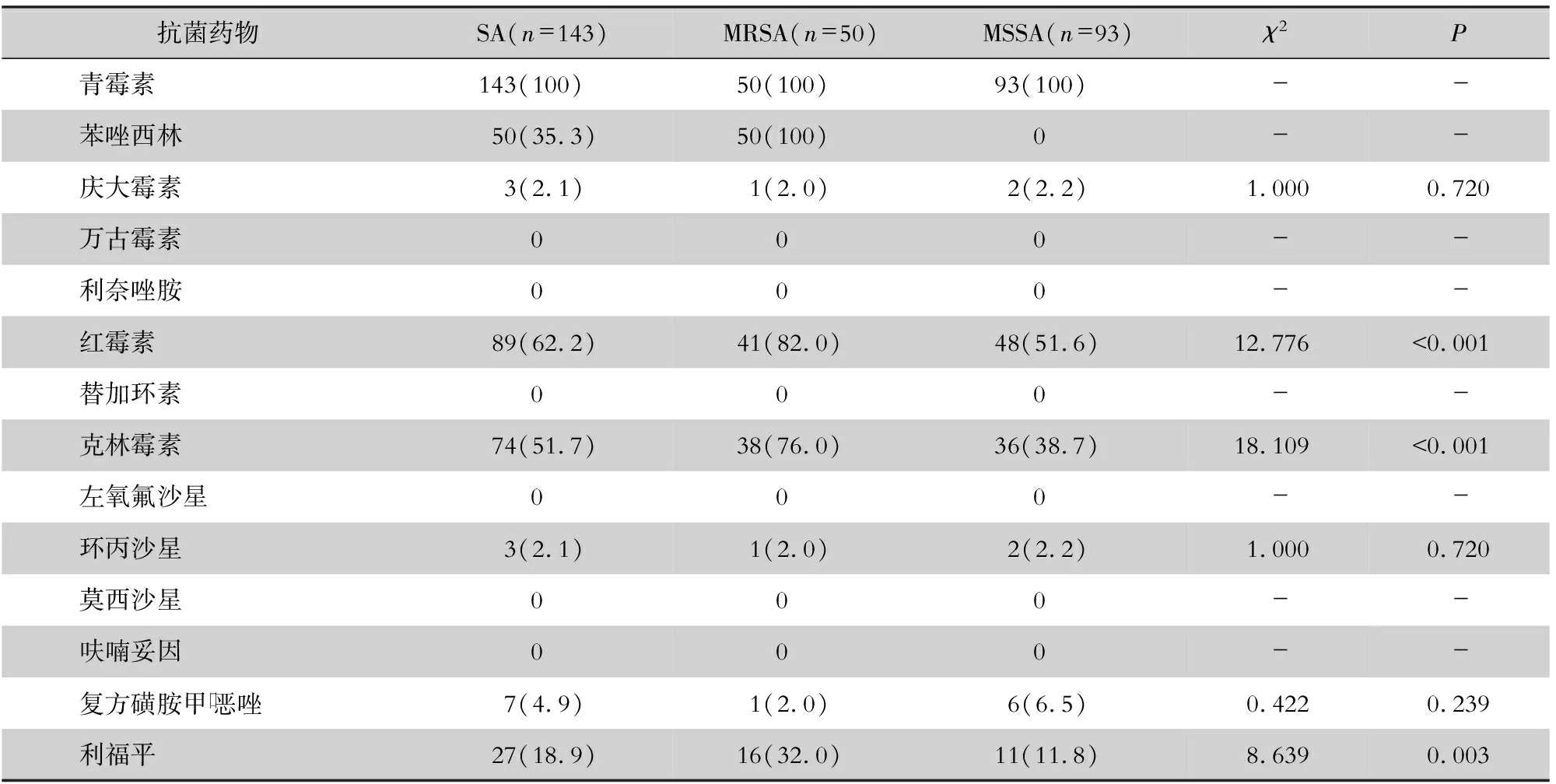
表7 MRSA与MSSA对常用抗菌药物的耐药率比较[株(%)]
2.5 预后不良的相关因素 143例SA血流感染患儿痊愈及好转133例(93.0%),未愈4例(2.8%),死亡6例(4.2%)。单因素分析结果表明,静脉置管、机械通气及入住ICU为SA血流感染患儿预后不良的危险因素(均P<0.05)。见表8。

表8 SA血流感染患儿预后的危险因素分析[例(%)]
3 讨论
SA是医疗机构和社区中最常见的病原菌之一[8],可引起机体多部位的感染。本研究显示,<1岁婴幼儿是SA血流感染的高发人群,与安徽[9]、成都[10]、南京[11]等地区相似,与婴幼儿免疫功能低下有关。临床科室分布上,该院SA血流感染主要来自骨科病区,而成人SA血流感染大都分布在ICU或感染病科[3],可能与不同年龄组疾病谱、SA皮肤携带率有关。本研究143例血培养SA阳性病例中,MRSA占35.0%,低于徐卫华等[9]研究结果,与国内一项多中心研究[12]及温州某医院研究[13]结果相似,高于某些欧洲国家[14-16],推测与标本量大小、地域差异、感染控制医疗实践措施不同有关。
143例患儿中临床表现为病灶性血流感染者90例(62.9%),常见合并化脓性骨髓/关节炎和肺炎,与澳大利亚、新西兰、冰岛、南非相似[4,14,17]。韩国的一项研究[18]表明,CA-MRSA是引起皮肤和软组织感染的主要原因,HA-MRSA主要引起肺炎、脓毒症等。本研究中,CA-MRSA导致皮肤软组织感染比率(26.0%)高于HA-MRSA(12.0%),而HA-MRSA感染导致肺炎的比率(20.0%)高于CA-MRSA(10.0%),与韩国研究结果一致。HA血流感染组中合并基础疾病如实体瘤、先天性心脏病比率高于CA血流感染组,表明这类患儿住院期间发生SA-HA的机会增加,需格外注意医务人员在接触患儿前后的手卫生,发现感染病例后及时隔离治疗,严格消毒和改善病房环境,减少SA在医院中的传播。多因素回归分析显示,住院时间>7 d、入院前使用抗菌药物、使用抗菌药物>7 d是HA血流感染的独立危险因素,对这类患儿更应警惕HA的发生。
最近国内一项多中心研究[12]显示,儿童血培养分离的MRSA对红霉素、克林霉素、四环素、环丙沙星、左氧氟沙星的耐药率均高于MSSA。本研究中MRSA对红霉素、克林霉素、利福平的耐药率分别为82.0%、76.0%、32.0%,均高于MSSA(均P<0.05);而对环丙沙星、左氧氟沙星耐药率与MSSA一样,均较低,考虑与地区差异有关。SA血流感染通常来自皮肤软组织、手术部位、肺部或植入物,包括留置静脉导管等。其治疗基本原则包括确定主要感染部位,清除感染异物(如果存在),引流或排出仅用抗菌药物无法清除的感染源,以及使用敏感的抗菌药物治疗[19]。目前美国传染病学会(IDSA)对MRSA引起的感染治疗优先选择万古霉素,同时建议使用达托霉素与庆大霉素、利福平或利奈唑胺等协同治疗[20]。近几年,部分新的药物如头孢洛林、泰拉万星、达巴万星和特地唑胺被批准用于治疗成人MRSA感染[19],目前儿童应用的经验不多。
部分研究[21-22]发现既往住院病史、抗菌药物使用史、有创性操作、血管内导管的应用是MRSA血流感染的独立危险因素,本研究中也发现机械通气及多种抗菌药物联合使用是MRSA感染的独立危险因素。侵入性操作破坏了人体防御屏障使其更易感染相关病原菌;另外,MRSA的耐药机制主要包括由质粒介导产生大量β-内酰胺酶的获得性耐药以及由耐药基因介导的固有耐药性[23],经验性的广谱抗菌药物、预防性抗菌药物的使用将导致MRSA感染的概率增加。
总之,SA血流感染多出现在<1岁患儿中,男性居多,病灶性血流感染常见。临床治疗中应根据病原学及药敏试验结果,区别对待MRSA及MSSA,针对性地制定合理的治疗方案。
利益冲突:所有作者均声明不存在利益冲突。
