连番止泻微丸制剂工艺及含量测定方法研究
2023-02-20黄德浩黄丽何文涛贺妙兰叶红斌刘永黄源林胡辉宋吉明
黄德浩,黄丽,何文涛,贺妙兰,叶红斌,刘永,黄源林,胡辉,宋吉明
(1.惠州市九惠制药股份有限公司,广东惠州 516007;2.安徽大学,安徽合肥 230039)
连番止泻方是南方医科大学陈宝田教授的临床验方,具有清热解毒、燥湿止泻的功效,由黄连、黄芩、白芍、广藿香、番石榴叶、茯苓组成,常用于治疗由人体轮状病毒引起的急性腹泻[1]。轮状病毒多发于儿童,全球每年约20万婴幼儿因轮状病毒感染而死亡[2]。连番止泻已上市产品为胶囊剂,存在吞咽不便、用药量不准确等问题,因此,拟改剂型为颗粒剂;为解决颗粒剂存在味苦难以下咽的问题,本文将主要成分制成微丸中间体,便于后续研究包衣和混悬颗粒制剂[3-4],并建立HPLC-双波长检测法同时测定微丸中盐酸小檗碱、黄芩苷、白芍苷含量的方法[5-8],为新剂型质量控制提供参考。
1 材料
1.1 仪器与设备
Mini-250C 螺杆挤出滚圆机(深圳信宜特科技有限公司);YK-160D 快速搅拌制粒机(丹东市制药机械有限公司);101A-2 电热鼓风干燥箱(上海实验仪器厂有限公司);LC-20A 高效液相色谱仪(日本岛津公司);MSE3.6P-0CE-DM 型百万分之一天平、CPA225D 型十万分之一天平[赛多利斯科学仪器(北京)有限公司];TH-350型超声波清洗器(济宁天华超声电子仪器有限公司)。
1.2 试剂与试药
盐酸小檗碱对照品(批号:110713-202015,质量分数85.90%)、黄芩苷对照品(批号:110715-202122,质量分数94.20%)、芍药苷对照品(批号:110736-202044,质量分数96.80%)均购自中国食品药品检定研究院;连番止泻干膏粉(批号:20220401,惠州市九惠制药股份有限公司自制);微晶纤维素MCC(上海麦克林生化科技有限公司);交联羧甲基纤维素钠(陕西唐尧生物科技有限公司);滑石粉(上海麦克林生化科技有限公司);聚维酮K30(博爱新开源医疗科技集团股份有限公司);甲醇(北京伊诺凯科技有限公司);纯化水(自制);色谱乙腈(上海星可高纯溶剂有限公司);其他试剂为分析纯。
2 方法与结果
2.1 连番止泻微丸处方工艺研究
2.1.1 微丸的制备工艺 取连番止泻提取物干膏粉末和微晶纤维素等辅料适量分别过80 目筛,混匀,加水制软材;按照实验设计的挤出转速、滚圆转速和滚圆时间,经挤出机筛板挤出,将所得条状物放滚圆机滚圆,取出微丸,于60 ℃烘干,筛出16~30目的微丸进行分析评价。
2.1.2 评价指标 收率(f):f=W1/W0×100%,W0为微丸质量,W1为过筛微丸质量。圆整度:取过筛微丸,置平板,缓慢抬起平板一侧,测量微丸开始滚动时倾斜平面与水平面所形成的夹角,即为平面临界角(Φ),其值越小,圆整度越好。综合评价指标(Y):Y=f-2Φ,f为收率,Y值越高,对应工艺条件越优[9]。
2.1.3 赋形剂的筛选 微晶纤维素(MCC)是一种成球促进剂,由MCC 制得的微丸粒度均匀、表面圆整光滑、堆密度大,对于丸芯的形成和圆整度起关键性作用[10-11]。单独使用MCC 做赋形剂,所得微丸脆碎度较高,故考虑加入其他赋形剂合用。通过预实验表明微晶纤维素与交联羧甲基淀粉钠和乳糖的质量比为4∶1∶3 时,制得的微丸圆整均匀,硬度适中,成丸性好,收率也高。
2.1.4 载药量的考察 研究表明,采用挤出滚圆法制备微丸的载药量为20%~50%时,利于成丸[12]。本试验分别考察了20%、30%、40%、50% 4种载药量制备的微丸圆整度及收率,并观察制备过程及外观。结果显示,载药量越小越易成丸,最终选择连番止泻微丸的载药量为20%。
2.1.5 润湿剂种类及用量的考察 润湿剂的种类和用量在挤出滚圆法制备微丸过程中具有关键性作用[13]。若药物有一定黏性,应使用合适浓度的乙醇作为润湿剂[14-16]。连番止泻提取物干膏粉的黏性适中,考察水、不同浓度的乙醇作为润湿剂。依据“捏之成团,松之不散”的标准[17],结果表明,以水作为润湿剂制软材进行比较顺利,且微丸圆整度较好,综合经济成本考虑,最终选择以水为润湿剂进行微丸的制备。
2.1.6 微丸成型工艺优化 影响制丸工艺主要因素为挤出转速、滚圆转速、滚圆时间。本研究选用三因素三水平按L9(34)设计正交试验作为工艺条件的优化筛选,因素水平见表1,处方为:连番止泻干膏粉∶微晶纤维素∶交联羧甲基纤维素钠∶乳糖=2∶4∶1∶3(质量比),黏合剂为水。由表2 结果可知,3 个因素对微丸性质影响的主次因素顺序为B>A>C,因素B(滚圆转速)对微丸质量影响具有统计学意义(P<0.05)。从正交结果分析表表3,最优工艺条件为A2B3C1,即:挤出转速为40 r/min,滚圆转速为200 r/min,滚圆时间为90 min。

表1 正交试验因素水平表Table 1 Factors and levels of orthogonal test
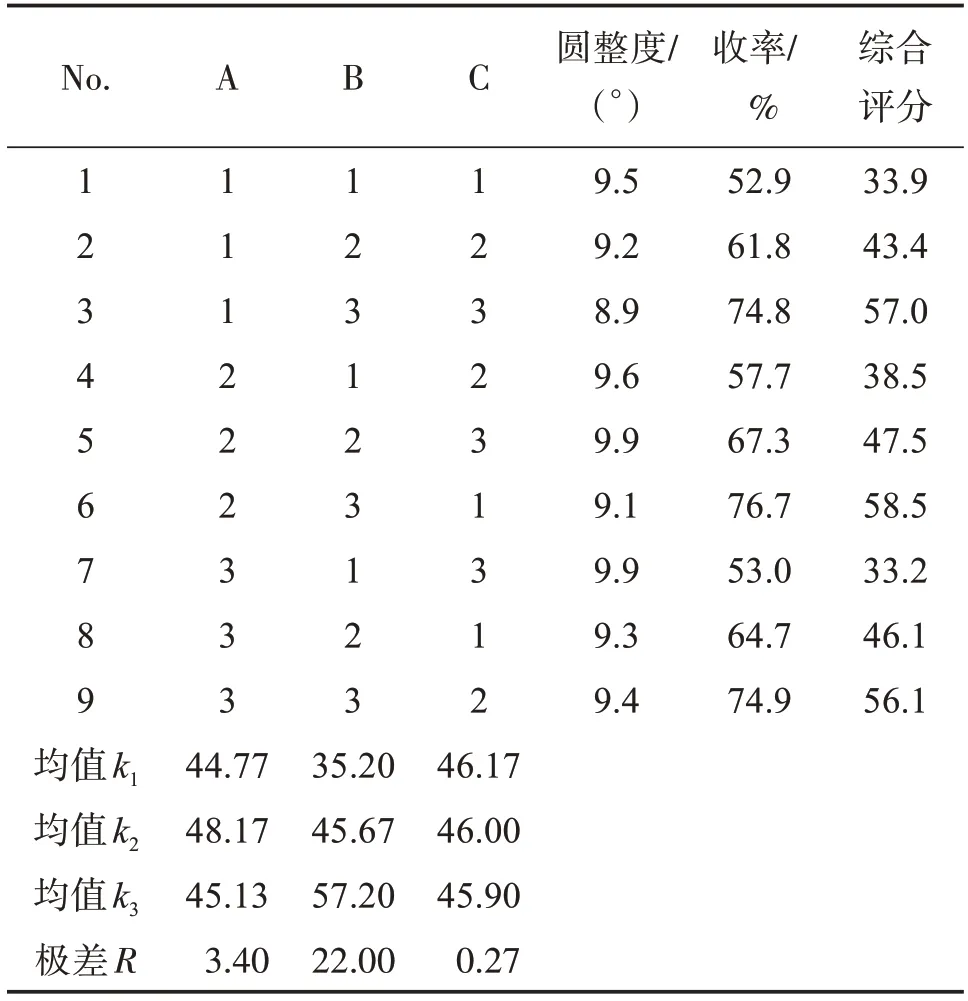
表2 正交试验结果分析Table 2 Results of orthogonal test
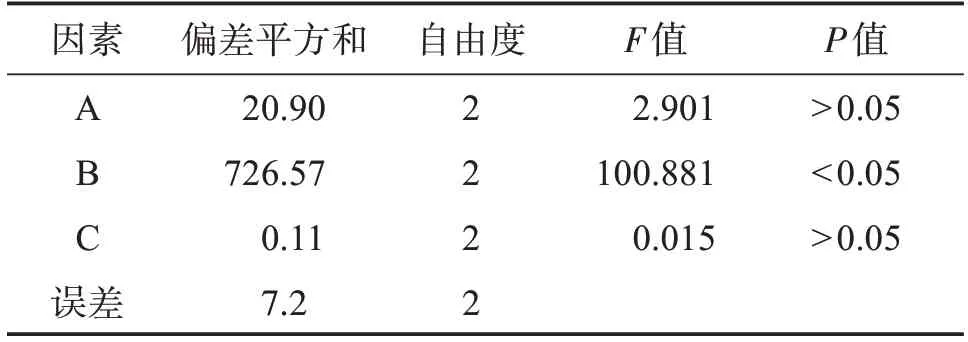
表3 正交试验方差分析结果Table 3 Variance analysis of orthogonal test
2.1.7 工艺验证试验 对处方和工艺考察确定的最优工艺进行验证(n=3)。进行粉体学性质的测定,结果均符合要求,说明工艺稳定,重现性良好,见表4。

表4 3批微丸质量评价结果Table 4 Quality evaluation of 3 batches of pellets
2.2 连番止泻微丸含量测定方法的建立
2.2.1 色谱条件 色谱柱:Hypersil GOLDTMC18色谱柱(250 mm×4.6 mm,5 μm);流动相:乙腈(A)-0.1%磷酸水(B),梯度洗脱(0~3 min,15.5%~15.5%A;3~10 min,15.5%~28%A;10~25 min,28%~28%A;25~30 min,28%~40%A);流速:1.0 mL/min;柱温:30 ℃;检测波长:230 nm(芍药苷),280 nm(黄芩苷、盐酸小檗碱);进样量:10 μL。
2.2.2 对照品储备液的制备 精密称取盐酸小檗碱对照品10.640 mg、黄芩苷对照品10.764 mg 和芍药苷对照品10.661 mg 适量,分别置于10 mL 量瓶中,用甲醇溶解并稀释至刻度,摇匀,分别制成质量浓度为0.914、1.014、1.032 mg/mL 的盐酸小檗碱、黄芩苷、芍药苷单一对照品储备液。
2.2.3 混合对照品溶液的制备 取“2.2.2”项下对照品储备液,精密量取适量,置20 mL 量瓶中,用甲醇稀释至刻度,摇匀,得到含0.045 70 mg/mL盐酸小檗碱、0.020 28 mg/mL 黄芩苷、0.020 64 mg/mL 芍药苷的混合对照品溶液。
2.2.4 供试品溶液的制备 取供试品,研细,精密称取0.1 g,置25 mL 量瓶中,加50%甲醇适量,超声30 min(300 W,50 kHz),取出,放冷,50%甲醇定容,摇匀,0.45 μm微孔滤膜滤过,即得。
2.2.5 阴性对照溶液的制备 按处方制备缺黄连阴性样品、缺黄芩阴性样品、缺白芍阴性样品,按照“2.2.4”项下方法前处理,得各阴性对照溶液。
2.2.6 专属性试验 分别取混合对照品溶液、供试品溶液和各阴性对照溶液各10 μL,注入高效液相色谱仪。按“2.2.1”项色谱条件测定。结果显示阴性对照无干扰,见图1。
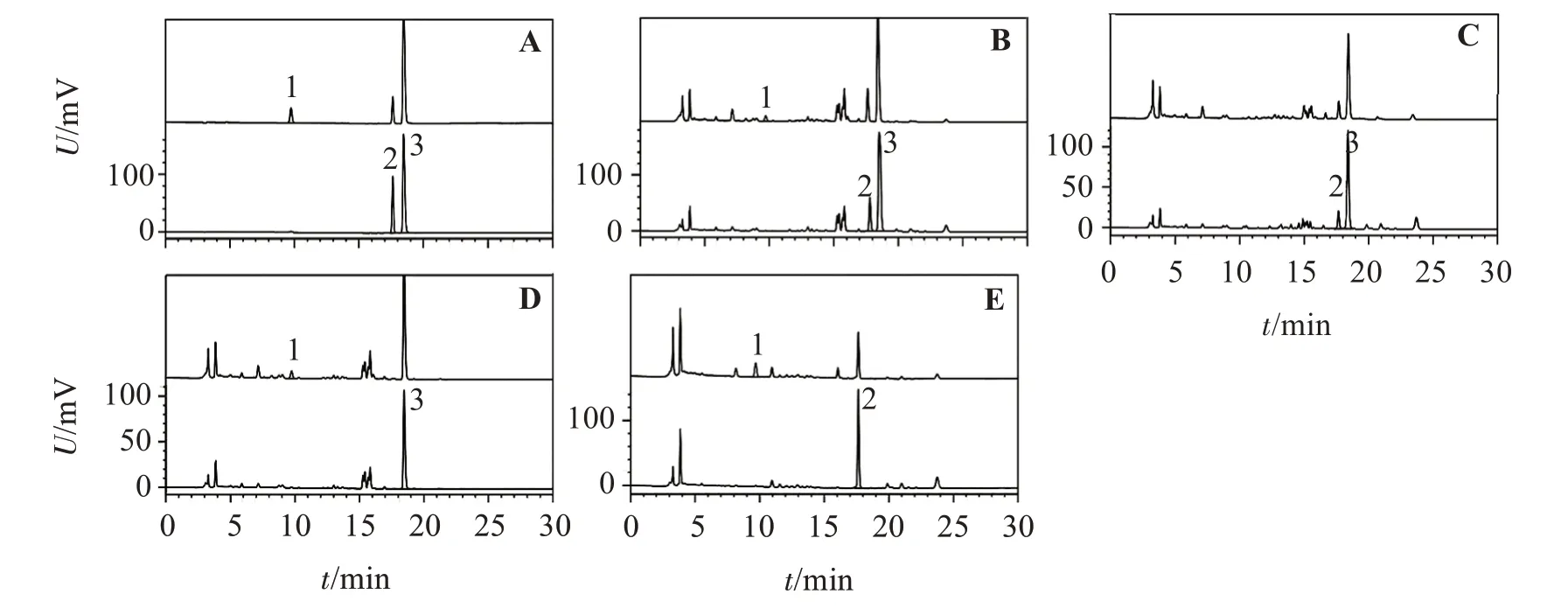
图1 混合对照品(A)、连番止泻微丸(B)、缺白芍阴性样品(C)、缺黄芩阴性样品(D)和缺黄连阴性样品(E)的HPLC色谱图Figure 1 HPLC Chromatograms of mixed reference substances (A),Lianfan Zhixie Pellets (B),sample without Paeonia lactiflora(C),sample without Scutellaria baicalensis(D),and sample without Rhizoma coptidis(E)
2.2.7 线性关系考察 取“2.2.2”项下单独对照品储备液,精密量取适量,置25 mL 量瓶中,用甲醇稀释至刻度,摇匀,得到含0.109 7 mg/mL 盐酸小檗碱、0.040 6 mg/mL 黄芩苷、0.041 3 mg/mL 芍药苷的混合对照品溶液。精密吸取1.0、2.0、4.0、6.0、8.0 mL,分别用甲醇定容至10 mL,摇匀即得系列线性工作溶液。按“2.2.1”项下方法测定,以各对照品质量浓度(x,µg/mL)为横坐标、峰面积(A)为纵坐标,绘制标准曲线,得到盐酸小檗碱、黄芩苷和芍药苷的线性回归方程分别为:A小檗碱=36 665x-3 305.6(r=0.999 9);A黄芩苷=39 129x-1 773.6(r=0.999 9);A芍药苷=14 321x-255.5(r=0.999 8),表明盐酸小檗碱、黄芩苷、芍药苷质量浓度分别在10.968~109.680 μg/mL、4.056~40.560 μg/mL、4.128~41.279 μg/mL 范围内呈良好的线性关系。
2.2.8 精密度试验 取“2.2.3”项下对照品溶液,按“2.2.1”项下色谱条件连续6次进样10 μL,计算峰面积RSD 值。结果盐酸小檗碱、黄芩苷、芍药苷峰面积RSD 值分别为1.61%、1.83%、1.53%,表明仪器精密度良好。
2.2.9 重复性试验 取同一批次连番止泻微丸样品6 份,按“2.2.4”项下方法制备供试品溶液。按“2.2.1”项分别进样10 μL,计算6份供试品溶液中盐酸小檗碱、黄芩苷、芍药苷的平均质量分数。结果显示,6 份供试品溶液中盐酸小檗碱、黄芩苷、芍药苷的平均质量分数分别为10.87、4.62、1.58 mg/g,RSD 值分别为0.38%、1.04%、1.44%,表明方法重复性良好。
2.2.10 稳定性试验 分别精密吸取同一供试品溶液,在配制后0、2、4、8、12、24 h 于同一色谱条件下分别进样10 μL,计算峰面积相对标准偏差。结果盐酸小檗碱、黄芩苷、芍药苷峰面积值的RSD 分别为1.03%、1.74%、1.10%,表明供试品溶液在24 h 内稳定。
2.2.11 加样回收率试验 将“2.2.2”项下的对照品储备液适量,单独配制成质量浓度为0.457 0 mg/mL盐酸小檗碱对照品溶液、0.202 8 mg/mL黄芩苷对照品溶液、0.103 2 mg/mL芍药苷对照品溶液。取已测定含量的连番止泻微丸0.05 g,精密称定,置25 mL量瓶,称取6份,分别按表5所示加入盐酸小檗碱、黄芩苷、芍药苷对照品溶液适量,按“2.2.4”项方法制备供试品溶液,按“2.2.1”项色谱条件分别进样10 μL,计算盐酸小檗碱、黄芩苷、芍药苷的加样回收率。结果见表5。盐酸小檗碱、黄芩苷、芍药苷的平均回收率分别为98.35%、97.90%、98.01%;RSD 分别为1.38%、1.60%、1.18%(n=6),表明方法准确度良好。
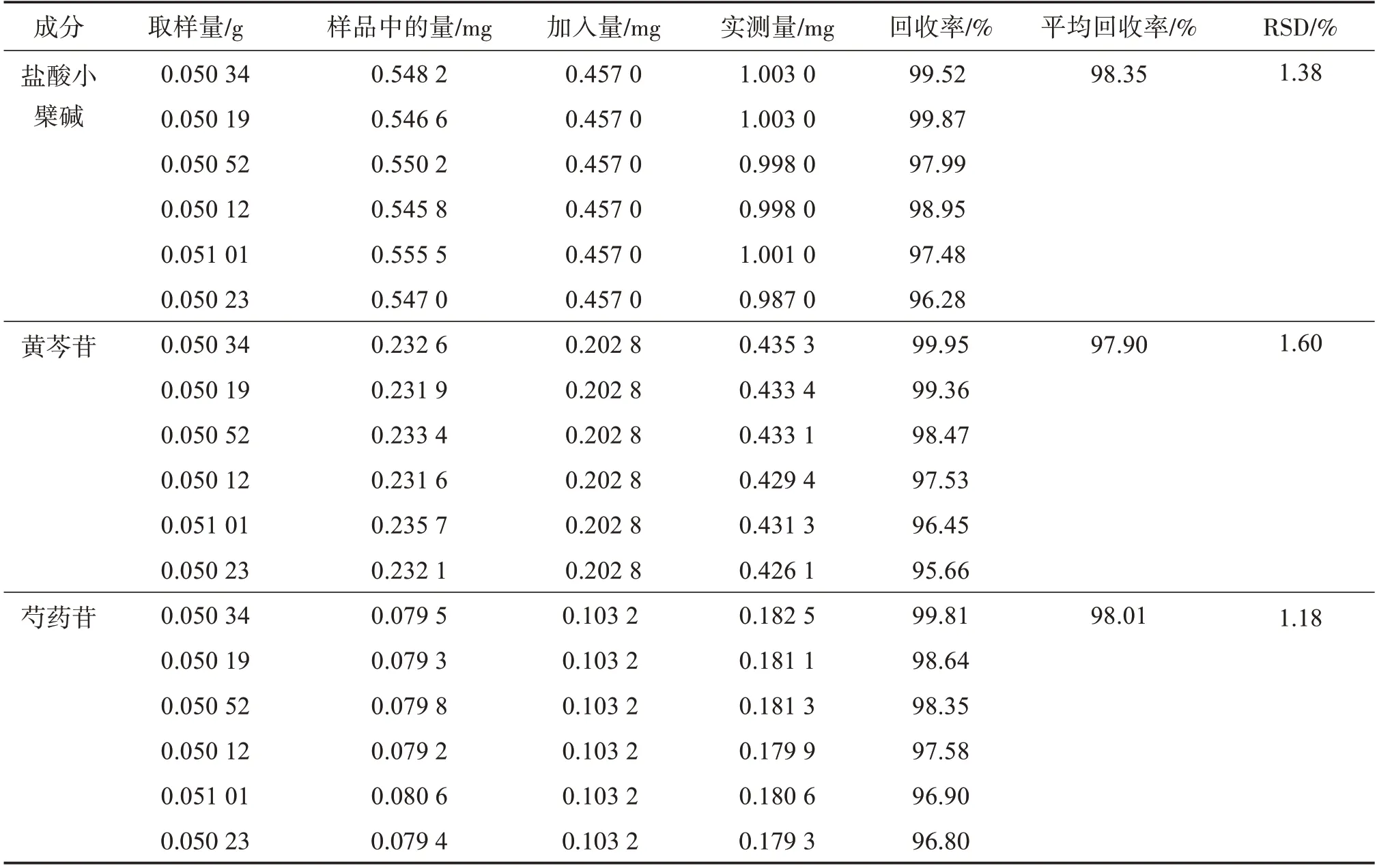
表5 盐酸小檗碱、黄芩苷、芍药苷的加样回收试验结果Table 5 The recoveries of berberine hydrochloride,baicalin and paeoniflorin
2.2.12 耐用性试验 分别精密吸取同一份供试品溶液10 µL,按“2.2.1”项色谱条件考察Hypersil GOLDTTMC18(250 mm×4.6 µm,5 µm)、JADE-PAK RS-C18(250 mm×4.6 µm,5 µm)、Inertsil ODS-SP C18(250 mm×4.6µm,5µm)3 种色谱柱下,盐酸小檗碱、黄芩苷、芍药苷含量测定结果受影响的程度,结果显示图谱中各色谱峰除保留时间有点差别外,理论塔板数和拖尾因子均理想,表明使用不同的色谱柱对检测结果没有影响,见表6。

表6 耐用性试验结果Table 6 Durability test results w/(mg·g-1)
3 讨论
实验中微丸的粉体学性质可以用得率、圆整度、脆碎度、堆密度等多个指标来考察,但在整个处方和工艺因素的选择过程中,微丸堆密度、脆碎度两指标均无显著性差别,而脆碎度除对工艺因素略有影响外,处方考察中变化不大,故本文选取得率和圆整度的综合评分作为评价微丸成型性的主要指标来优化处方。
本文考察得到制备连番止泻微丸的最终优化处方为:连番止泻干膏粉∶微晶纤维素∶交联羧甲基纤维素钠∶乳糖=2∶4∶1∶3(质量比),黏合剂为水,挤出转速为40 r/min,滚圆转速为200 r/min,滚圆时间为90 min。但微丸质量受制备过程影响较大,本文试验条件所限,试验量较小,如投入生产,还需综合考虑滚圆过程中,微丸与微丸之间的挤压碰撞等因素。
中药复方化学成分十分复杂,选择能够反映该中药主要药效的有效成分作为指标对其进行控制,可化繁为简,较好地达到控制药品质量的目的。本文以连番止泻微丸中的君药黄连,臣药黄芩和芍药中主要有效成分盐酸小檗碱、黄芩苷及芍药苷作为指标性成分。根据紫外检测,芍药苷的最大吸收波长为230 nm,黄芩苷和盐酸小檗碱的最大吸收波长为280 nm,故选择230 nm 检测芍药苷、280 nm 检测黄芩苷和盐酸小檗碱。试验过程中,盐酸小檗碱与黄芩苷的保留时间相近,改良流动相后,确定以乙腈-0.1%磷酸水梯度洗脱对连番止泻微丸中盐酸小檗碱、芍药苷和白芍苷分离效果较好。本文建立的检测方法专属性良好、精密度和准确度高,为后续快速准确检测连番止泻微丸的指标性成分提供了实验依据。
